

2. 新疆医科大学 护理学院,新疆 乌鲁木齐 830011;
3. 新疆维吾尔自治区药物研究所,新疆 乌鲁木齐 830004
2. College of Nursing, Xinjiang Medical University, Urumqi 830011, China;
3. Xinjiang Uygur Autonomous Region Institute of Materia Medica, Urumqi 830004, China
肝纤维化(hepatic fibrosis,HF)是一种慢性的瘢痕形成与修复过程,是发病率和死亡率都很高的世界医学难题。HF的特点是细胞外基质过度沉积,晚期HF可诊断为肝硬化,并最终可能发展为肝衰竭,甚至肝细胞癌[1]。目前公认肝星状细胞(hepatic stellate cell,HSC)的活化是HF进展过程中的关键事件[2]。在HF进程中,HSC激活成肌成纤维细胞是瘢痕形成的关键环节[3-4]。中医具有治疗复杂疾病及相关疾病的功效,肉苁蓉(Cistanche)是著名的名贵补益类中药,具有抗炎、抗病毒、抗氧化、免疫调节等作用。课题组前期研究证实,肉苁蓉苯乙醇苷类化合物具有良好的保肝护肝作用,且其能引起Fas诱导的HSC凋亡[5]。本研究旨在探讨肉苁蓉苯乙醇总苷(phenylethanol glycosides from cistanche tubuiosa,CPhGs)脂质体对HSC凋亡的影响及其分子机制,通过靶向载药系统转运药物,来克服一些药物半衰期短、无法到达靶器官,或到达了但无法在其周围形成有效药物浓度等缺点,最大程度发挥药物疗效,达到长效、靶向及减轻药物副作用等目的,期望能寻求更多的可以应用于临床治疗HF的靶向药物治疗途径,为HF的治疗提供理论基础。
1 材料与方法 1.1 材料 1.1.1 细胞株大鼠HSC-T6细胞株,购自上海中乔新舟生物科技有限公司,货号:ZQ0780。
1.1.2 药物与试剂用薄膜分散二次包封法制备pPB修饰的肉苁蓉总苷靶向脂质体,其粒径为212.7 nm,电位35~50 mV,包封率(38.46±7.85)%,由本实验室保存。胎牛血清(美国Gibco公司);DMEM高糖培养基(美国Hyclone公司);MTT(美国Sigma公司);Annexin V-FITC细胞凋亡检测试剂盒(美国BD公司);TRIzol Reagent(Life technologies);RevertAid First Strand cDNA Synthesis Kit、RIPA裂解液(赛默飞公司);SYBR Premix Ex TaqTM Ⅱ(TaKaRa公司);蛋白定量试剂盒(Biomiga公司);重组大鼠血小板衍生生长因子BB(recombinant rat platelet-derived growth factor BB,rrPDGF-BB) (R & D公司);抗β-actin、JNK、p-JNK多克隆抗体(北京博奥森生物科技有限公司)。
1.1.3 仪器超净工作台、全波长自动酶联免疫反应检验测试仪(美国Thermo Scientific公司);CK-40型荧光倒置显微镜(日本Olympus公司);低温离心机(美国Sigma公司);Western blot电泳装置及转膜装置(美国Bio-Rad公司);QuantStudio 6 Flex型实时荧光定量PCR仪(美国ABI公司)。
1.2 方法 1.2.1 细胞培养与传代HSC-T6在含有100 kU·L-1青霉素、100 mg·L-1链霉素和10%胎牛血清的高糖DMEM细胞培养液,于37℃、5% CO2培养箱中培养。细胞隔日换液,待生长融合至80%~90%时,使用0.25%胰蛋白酶消化收集细胞,按1:2进行传代培养,所有实验采用对数生长期细胞。
1.2.2 细胞分组实验分为Normal组、rrPDGF-BB组、rrPDGF-BB+CPhGs脂质体(29.45、14.72、7.36 mg·L-1)组。各组细胞均培养24 h后,收集细胞进行后续实验。
1.2.3 MTT法检测细胞增殖HSC-T6以5 000个/孔密度接种至96孔板,待细胞贴壁后进行分组干预,每组设3个复孔。分别培养24、48、72 h,向每孔加入10 μL MTT溶液,培养箱内37℃培养4 h后,弃去MTT溶液,再向各孔加入100 μL DMSO,置于摇床室温摇动10 min,待结晶充分溶解后,于酶标仪492 nm波长处测定吸光度。
1.2.4 流式细胞术检测细胞凋亡取生长状态良好的对数生长期细胞,经胰酶消化后接种于6孔板,每孔细胞数为1×105个,24 h后按相应浓度加药,继续培养48 h后,每孔加入500 μL胰酶消化细胞,加完全培养液终止消化,吹打混匀移至15 mL离心管,PBS冲洗细胞,1 000 r·min-1离心5 min。弃上清,加PBS冲洗细胞2次,用AnnexinV-FITC/PI细胞凋亡双染试剂标记后,用流式细胞仪检测细胞凋亡。
1.2.5 实时荧光定量PCR检测α-SMA、Collagen Ⅰ、Collagen Ⅲ mRNA的表达TRIzol试剂盒提取HSC-T6总RNA,经纯度及完整性鉴定后反转录反应生成cDNA。按照实时荧光定量PCR试剂盒说明书建立PCR反应体系,使用实时荧光定量PCR检测仪进行检测。PCR热循环参数为:95℃预变性30 s,95℃变性5 s,60℃退火30 s,72℃延伸45 s,共40个循环。结果分析以β-actin为内参基因,确定每个样本、每个基因扩增的循环阈值(CT),按照2-△△CT计算目的基因的相对表达量,所用引物序列见Tab 1。
| Gene | Primer sequence |
| α-SMA | F:5′-GCGTGGCTATTCCTTCGTGACTAC-3′ |
| R:5′-CCATCAGGCAGTTCGTAGCTCTTC-3′ | |
| CollagenⅠ | F:5′-AACGCTATTGCCTGATGGACAGTC-3′ |
| R:5′-CGCTGAGTCAAGGATGACGAAGAG-3′ | |
| Collagen Ⅲ | F:5′-GACACGCTGGTGCTCAAGGAC-3′ |
| R:5′-GTTCGCCTGAAGGACCTCGTTG-3′ | |
| β-actin | F:5′-AGCGAGCATCCCCCAAAGTT-3′ |
| R:5′-GGGCACGAAGGCTCATCATT-3′ |
收集细胞,RIPA细胞裂解液提取各组细胞总蛋白,BCA法测定蛋白浓度,取相同质量的蛋白上样,经SDS-PAGE凝胶电泳转移至硝酸纤维素膜,5%的脱脂奶粉室温封闭1 h,p-JNK、JNK一抗(1:5 000稀释)4℃摇床孵育过夜,TBST漂洗3次,二抗(1:5 000)室温孵育1 h,TBST漂洗3次后,化学发光显影试剂盒(ECL)曝光显影。利用图像分析软件Image J对条带进行灰度值的测定,计算分析各组蛋白相对表达量,以p-JNK与JNK条带信号强度的比值表示p-JNK蛋白表达水平。
1.3 统计学分析采用SPSS 17.0软件进行统计学分析,计量资料以x±s表示,多组间比较采用单因素方差分析,多组样本两两比较采用LSD法。
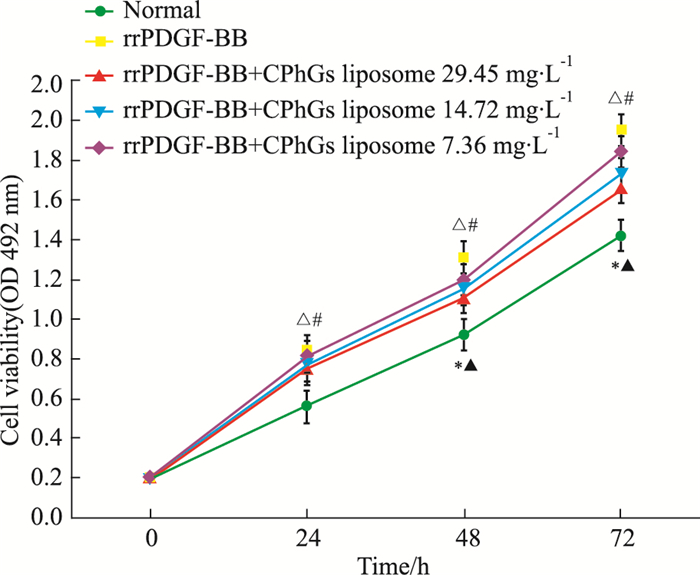
2 结果 2.1 CPhGs脂质体对rrPDGF-BB刺激的HSC-T6增殖的影响Fig 1的MTT结果显示,在24 h时,与Normal组比较,rrPDGF-BB组OD值明显增加(P < 0.05);与rrPDGF-BB组比较,除CPhGs脂质体7.36 mg·L-1组外,其余CPhGs脂质体不同浓度组OD值均明显下降(P < 0.05);与CPhGs脂质体7.36 mg·L-1组相比,CPhGs脂质体29.45 mg·L-1组OD值明显降低(P < 0.05)。在48、72 h时,与Normal组比较,rrPDGF-BB组和CPhGs脂质体不同浓度组OD值均明显增加(P < 0.05);与rrPDGF-BB组比较,CPhGs脂质体不同浓度组OD值明显下降(P < 0.05);与CPhGs脂质体7.36 mg·L-1组比较,CPhGs脂质体(14.72、29.45 mg·L-1)组OD值明显下降(P < 0.05);与CPhGs脂质体14.72 mg·L-1组比较,CPhGs脂质体29.45 mg·L-1组OD值明显下降(P < 0.05)。结果提示,随着药物浓度增大和干预时间的延长,CPhGs脂质体各剂量组抑制HSC-T6增殖的作用呈现明显的剂量-效应关系。
|
| Fig 1 Effect of CPhGs liposome with different doses on rrPDGF-BB induced HSC-T6 proliferation (x±s, n=3) *P < 0.05 vs normal group; #P < 0.05 vs rrPDGF-BB group; △P < 0.05 vs rrPDGF-BB+CPhGs liposome 7.36 mg·L-1 group; ▲P < 0.05 vs rrPDGF-BB+CPhGs liposome 14.72 mg·L-1 group |
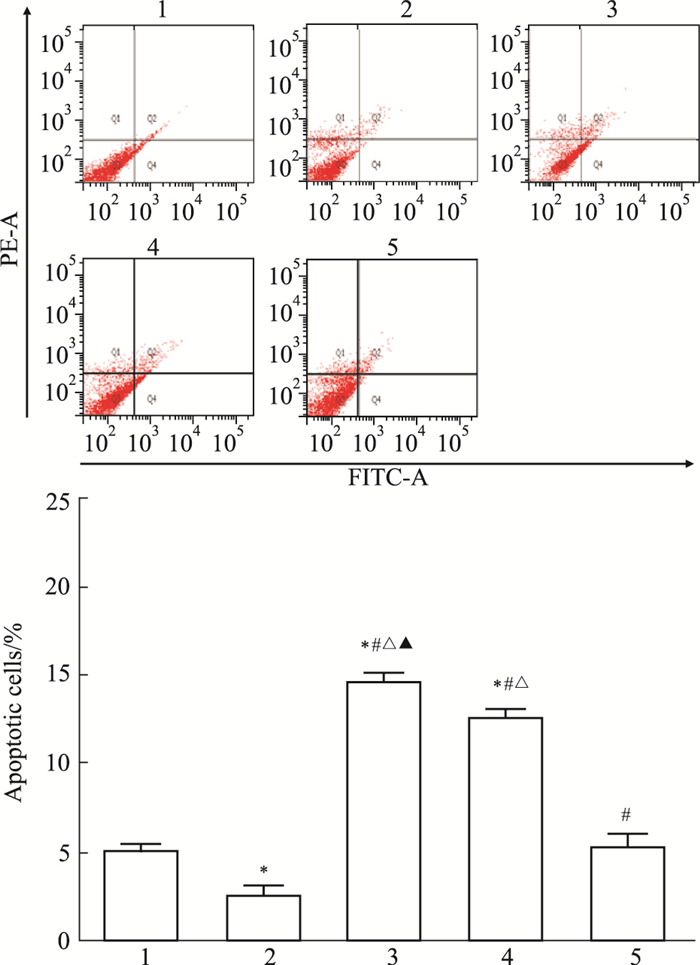
如Fig 2所示,与Normal组相比,rrPDGF-BB组凋亡率下降(P < 0.05);与rrPDGF-BB组相比,CPhGs脂质体不同浓度组凋亡率均明显上升(P < 0.05);与CPhGs脂质体7.36 mg·L-1组比较,CPhGs脂质体(14.72、29.45 mg·L-1)组凋亡率明显上升(P < 0.05);与CPhGs脂质体14.72 mg·L-1组比较,CPhGs脂质体29.45 mg·L-1组凋亡率明显增高(P < 0.05)。结果显示,随着CPhGs脂质体药物浓度的升高,HSC-T6凋亡率也逐渐增高,CPhGs脂质体各剂量组间呈现剂量-效应关系。
|
| Fig 2 Detection of apoptotic rate by flow cytometry (x±s, n=3) 1:Normal; 2:rrPDGF-BB; 3:rrPDGF-BB+CPhGs liposome 29.45 mg·L-1; 4:rrPDGF-BB+CPhGs liposome 14.72 mg·L-1; 5:rrPDGF-BB+CPhGs liposome 7.36 mg·L-1. *P < 0.05 vs normal group; #P < 0.05 vs rrPDGF-BB group; △P < 0.05 vs rrPDGF-BB+CPhGs liposome 7.36 mg·L-1 group; ▲P < 0.05 vs rrPDGF-BB+CPhGs liposome 14.72 mg·L-1 group |
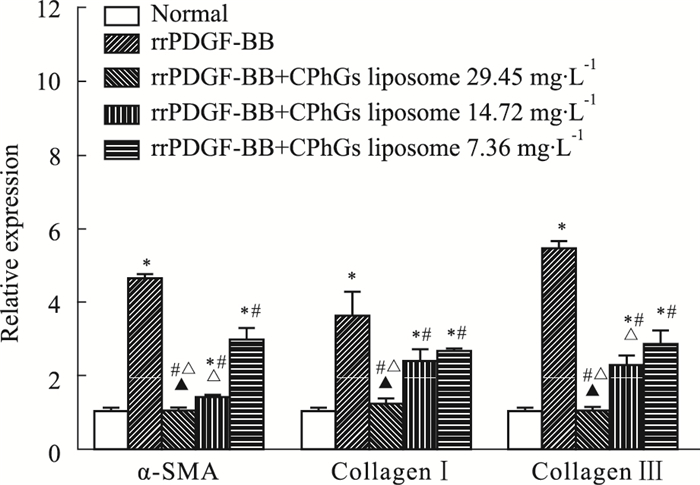
如Fig 3所示,与Normal组比较,α-SMA、CollagenⅠ、Collagen Ⅲ mRNA在rrPDGF-BB组表达明显增加(P < 0.05);与rrPDGF-BB组比较,α-SMA、CollagenⅠ、Collagen Ⅲ mRNA在CPhGs脂质体不同浓度组表达均下降(P < 0.05);CPhGs脂质体各剂量组间比较,可见随CPhGs脂质体浓度增大,α-SMA、CollagenⅠ、Collagen Ⅲ mRNA表达明显下降,差异具有统计学意义(P < 0.05),其中以CPhGs脂质体29.45 mg·L-1组抑制效果最明显。
|
| Fig 3 Effect of CPhGs liposome with different doses on rrPDGF-BB induced HSC-T6 mRNA expression of α-SMA, Collagen Ⅰ and Collagen Ⅲ(x±s, n=3) *P < 0.05 vs normal group; #P < 0.05 vs rrPDGF-BB group; △P < 0.05 vs rrPDGF-BB+CPhGs liposome 7.36 mg·L-1 group; ▲P < 0.05 vs rrPDGF-BB+CPhGs liposome 14.72 mg·L-1 group |
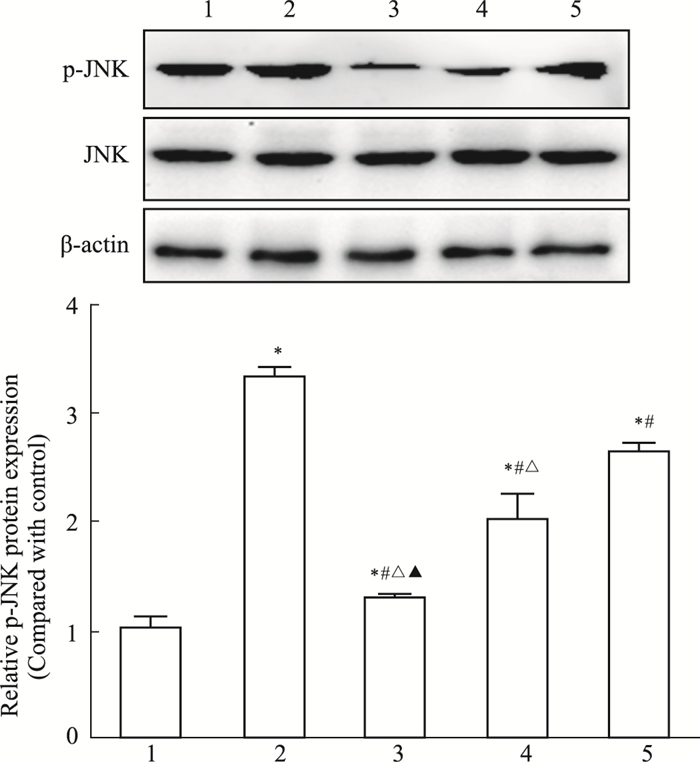
如Fig 4所示,与Normal组比较,p-JNK蛋白在rrPDGF-BB和CPhGs脂质体不同浓度组表达明显增加(P < 0.05);与rrPDGF-BB组比较,p-JNK蛋白在CPhGs脂质体不同浓度组表达下降(P < 0.05);CPhGs脂质体各剂量组间比较,p-JNK蛋白随CPhGs脂质体干预剂量增加表达明显下降,呈现剂量-效应关系(P < 0.05),其中以29.45 mg·L-1组效果最明显。
|
| Fig 4 Effect of CPhGs liposome with different doses on rrPDGF-BB induced HSC-T6 protein expression of p-JNK (x±s, n=3) 1:Normal; 2:rrPDGF-BB; 3:rrPDGF-BB+CPhGs liposome 29.45 mg·L-1; 4:rrPDGF-BB+CPhGs liposome 14.72 mg·L-1; 5:rrPDGF-BB+CPhGs liposome 7.36 mg·L-1. *P < 0.05 vs normal group; #P < 0.05 vs rrPDGF-BB group; △P < 0.05 vs rrPDGF-BB+CPhGs liposome 7.36 mg·L-1 group; ▲P < 0.05 vs rrPDGF-BB+CPhGs liposome 14.72 mg·L-1 group |
在慢性肝病中,HSC的反复激活导致HF,其特征是广泛的瘢痕形成和干扰肝脏正常结构与功能[6]。目前,抗HF的主要策略是抑制HSC活化、增殖、收缩,诱导HSC凋亡。HSC的活化是HF的主要过程[7],HF主要是由于细胞外基质过度沉积所致,而活化的肝HSC是细胞外基质的主要来源。肝损伤后,HSC经历一个复杂的从静止状态向肌成纤维细胞转换或激活过程,α-SMA是HSC活化的标志物,α-SMA在肌成纤维细胞分化中起作用。α-SMA降低了收缩力和Collagen Ⅰ合成,并抑制伤口收缩。Collagen Ⅰ和α-SMA被认为是HF中诱导HSC活化的标志物,可以减少α-SMA的含量,促进HSC凋亡,逆转HF进程。宋阳等[8]的研究结果证实,其研究的药物可明显抑制HSC的增殖,促进其凋亡,并使α-SMA蛋白表达明显降低,以此降低细胞外基质的沉积,从而起到逆转HF的作用。由淑萍等[9]研究表明,肉苁蓉苯乙醇总苷可以抑制rrPDGF-BB诱导的HSC增殖。上述研究结果提示,抑制HSC的激活和增殖,促进HSC凋亡已成为阻止HF发生、发展的关键事件。最近的临床实验证据也提示,HF具有可逆性的[10]。HF的逆转与HSC的凋亡有着密切关联。HF逆转期,活化的HSC数量减少主要依靠细胞凋亡,而不是活化状态细胞向静止状态转化。细胞凋亡是细胞的主动“自杀”过程,与坏死不同,细胞凋亡发生于HF的产生和发展过程中。HSC凋亡在HF发展过程中不仅起着主动作用,而且贯穿整个纤维化形成的过程。本研究用不同浓度的CPhGs脂质体药物作用于HSC-T6 48 h后,用流式细胞仪检测细胞凋亡,结果显示,与Normal组相比,rrPDGF-BB组凋亡率下降,CPhGs脂质体(29.45、14.72 mg·L-1)组凋亡率上升,与rrPDGF-BB组相比,CPhGs脂质体不同浓度组凋亡率均明显上升,且CPhGs脂质体不同浓度组相比,差异具有统计学意义。实验结果表明,CPhGs脂质体可诱导HSC-T6的凋亡,且凋亡程度与CPhGs脂质体浓度存在联系,CPhGs脂质体各剂量组间表现出明显的剂量-效应关系。
HF是指结缔组织过度增殖和异常沉积,特别是胶原蛋白、非胶原蛋白和肝小叶门管区的蛋白多糖等。因此,细胞外基质降解和生成之间的不平衡是HF发生与发展的关键因素。因此,保护肝细胞,促进肝再生,保持胶原蛋白的正常代谢也成为预防和治疗HF的重要措施。人类有19种胶原蛋白,在肝脏中存在的有5种类型,在HF的总蛋白中胶原蛋白约占50%,主要涉及Collagen Ⅰ和Collagen Ⅲ。在肝脏中,Collagen Ⅰ占60%~70%,Collagen Ⅲ占20%~30%,是构成细胞外基质的主要成分。因此,Collagen Ⅰ和Collagen Ⅲ被认为是反映胶原蛋白在肝脏中进行新陈代谢的重要参数。李伟伟等[11]的研究结果显示所研究药物可通过抑制CollagenⅢ沉积而起到抗HF作用。张扬武等[12]的实验结果也证实了可通过抑制HSC的活化,降低Collagen Ⅰ的表达, 达到逆转HF的作用。本研究采用实时荧光定量PCR检测α-SMA、Collagen Ⅰ和Collagen Ⅲ基因表达,研究结果显示,与Normal组相比,rrPDGF-BB组α-SMA、Collagen Ⅰ、Collagen Ⅲ mRNA表达明显增高,与rrPDGF-BB组相比,不同浓度的CPhGs脂质体组均可不同程度下调α-SMA、Collagen Ⅰ和Collagen Ⅲ的mRNA表达,其中29.45 mg·L-1 CPhGs脂质体组下调作用最明显,且随着药物浓度的升高,其下调程度越明显。我们认为产生这种现象的原因在于浓度越高,其对rrPDGF-BB引起的HSC增殖的抑制效果越明显,越趋近于正常。因此,我们认为其能抑制HSC增殖,促进其凋亡,以此来阻止HF的形成。
JNK已显示对不同细胞类型的细胞增殖有积极的调节作用,JNK通过负性调节作用来抑制静止HSC的活化,从而阻止HSC的增殖,刺激MAPK信号通路,从而使其下游通路阻断,起到预防HF的作用。本研究结果显示,与Normal组比较,rrPDGF-BB组p-JNK的蛋白表达量明显增高,表明rrPDGF-BB可通过影响MAPK信号,使HSC活化增殖。不同浓度的CPhGs脂质体组,p-JNK的蛋白表达量随着药物浓度的升高逐渐降低,且不同浓度的CPhGs脂质体组p-JNK的蛋白表达量与rrPDGF-BB组比较,差异均有统计学意义。由此可见,CPhGs脂质体可在一定程度上抑制rrPDGF-BB诱导的HSC增殖与活化,促进HSC凋亡,从而抑制HF的发生、发展。本研究结果为后续实验进一步研究CPhGs脂质体抗HF作用机制提供了扎实的理论基础。期望能够寻求更多抗HF的靶向给药途径,给HF患者带来福音。
( 致谢: 本实验主要在新疆医科大学2011协同中心完成,在此特别感谢姜平、盛磊老师提供的支持与帮助,对王志强师兄和张石蕾师姐提供的帮助及指导表示衷心感谢!)
| [1] | Huang Y, Deng X, Liang J, et al. Modulation of hepatic stellate cells and reversibility of hepatic fibrosis[J]. Exp Cell Res, 2017, 352(2): 420-6. doi:10.1016/j.yexcr.2017.02.038 |
| [2] | Zhao G N, Jiang D S, Li H, et al. Interferon regulatory factors: at the crossroads of immunity, metabolism, and disease[J]. Biochim Biophys Acta, 2015, 1852(2): 365-78. doi:10.1016/j.bbadis.2014.04.030 |
| [3] | Mederacke I, Hsu C C, Troeger J S, et al. Fate tracing reveals hepatic stellate cells as dominant contributors to liver fibrosis independent of its aetiology[J]. Nat Commun, 2013, 4(7): 2823. |
| [4] | Iwaisako K, Jiang C, Zhang M, et al. Origin of myofibroblasts in the fibrotic liver in mice[J]. Proc Natl Acad Sci USA, 2014, 111(32): 3297-305. doi:10.1073/pnas.1400062111 |
| [5] | Liu T, Zhao J, Ma L, et al. Hepatoprotective effects of total triterpenoids and total flavonoids from Vitis vinifera L against immunological liver injury in mice[J]. Evid Based Complement Alternat Med, 2012, 2012(1): 969-86. |
| [6] | Yin C, Evason K J, Asahina K, et al. Hepatic stellate cells in liver development, regeneration, and cancer[J]. J Clin Invest, 2013, 123(5): 1902-10. doi:10.1172/JCI66369 |
| [7] | Puche J E, Lee Y A, Jiao J, et al. A novel murine model to deplete hepatic stellate cells uncovers their role in amplifying liver damage in mice[J]. Hepatology, 2013, 57(1): 339-50. doi:10.1002/hep.26053 |
| [8] | 宋阳, 詹磊, 黄成, 等. 瞬时感受器电位离子通道香草素受体亚家族4调控肝星状细胞活化增殖作用研究[J]. 中国药理学通报, 2016, 32(5): 681-7. Song Y, Zhan L, Huang C, et al. Regulatory effects of TRPV4 on liver fibrosis of rats[J]. Chin Pharmacol Bull, 2016, 32(5): 681-7. doi:10.3969/j.issn.1001-1978.2016.05.017 |
| [9] | 由淑萍, 赵军, 马龙, 等. 肉苁蓉苯乙醇总苷对血小板衍生生长因子诱导的肝星状细胞增殖的影响及机制[J]. 中国药理学通报, 2016, 32(9): 1231-5. You S P, Zhao J, Ma L, et al. Effects of phenylethanol glycosides from Cistanche tubulosa on proliferation of rat HSC induced by PDGF-BB and its mechanism[J]. Chin Pharmacol Bull, 2016, 32(9): 1231-5. doi:10.3969/j.issn.1001-1978.2016.09.009 |
| [10] | Xu D D, Li X F, Li Y H, et al. TIPE2 attenuates liver fibrosis by reversing the activated hepatic stellate cells[J]. Biochem Biophys Res Commun, 2018, 498(1): 199-206. doi:10.1016/j.bbrc.2017.11.178 |
| [11] | 李伟伟, 高海丽, 宋新文, 等. 吡咯烷二硫代氨基甲酸酯在二甲基亚硝胺诱导肝纤维化大鼠中的作用及机制[J]. 中华实用诊断与治疗杂志, 2018, 32(1): 5-9. Li W W, Gao H L, Song X W, et al. Role and mechanism of pyrrolidine dithiocarbamate in dimethylnitrosamine-induced hepatic fibrosis in rats[J]. Chin Pract Diagn Ther, 2018, 32(1): 5-9. |
| [12] | 张扬武, 罗伟生, 陈姗, 等. 枇杷叶熊果酸对大鼠肝星状细胞增殖抑制作用及对PPAR-γ、TGF-β1表达的影响[J]. 中国药理学通报, 2017, 33(4): 517-21. Zhang Y W, Luo W S, Chen S, et al. Effects of ursolic acid from loquat leaves on proliferation inhibition and expression of PPAR-γ, TGF-β1 in rat hepatic stellate cells[J]. Chin Pharmacol Bull, 2017, 33(4): 517-21. doi:10.3969/j.issn.1001-1978.2017.04.014 |

