


恶性肿瘤严重着威胁人类健康,如何提高肿瘤治疗效果及生存预后,是近几十年来国内外研究热点。对于中晚期恶性肿瘤,放射治疗是主要治疗方法之一,然而,实体瘤中乏氧组织的存在,严重影响放射治疗效果。研究表明,肿瘤放疗增敏剂是解决肿瘤内乏氧细胞对治疗抗拒性的有效途径之一[1]。我国自主研发的放射增敏剂马蔺子素(irisquinone,IR)是从中草药马蔺子中提取的一种醌类化合物,对放射治疗有明显的增敏作用[2]。PET/CT能够监测肿瘤内环境,通过不同显像剂更加全面准确地评价肿瘤治疗反应。随着核医学显像设备的发展,micro PET/CT能够无创、动态、定量地从分子水平观察药物在小动物体内的吸收、分布、代谢、排泄等过程。3’-脱氧-3’-18F-氟胸苷(3’-deoxy-3’-18F-fluorothymidine, 18F-FLT)作为新近开发的增殖显像剂,可反映肿瘤增殖状况,评价肿瘤放、化疗疗效[3]。本实验拟通过建立裸鼠MDA-MB231乳腺癌模型,并对其用IR进行放射增敏治疗,探讨18F-FLT micro PET/CT显像评估放射增敏疗效的价值。
1 材料与方法 1.1 细胞株与试剂MDA-MB231乳腺癌细胞株购自中科院上海细胞库。DMEM高糖培养基、胎牛血清、0.25%胰酶,均购自美国Gibco公司;IR(批号:1601255)购自山东新华制药公司;Ki-67抗体购自武汉三鹰生物科技有限公司。
1.2 实验动物32只BALB/c裸鼠,♀,4~6周龄,体质量(20±2)g,购自上海斯莱克实验动物有限责任公司,许可证号:SCXK(沪2012-0002)。
1.3 细胞培养及肿瘤接种MDA-MB231乳腺癌细胞采用含10% FBS的DMEM培养液,于5% CO2的37℃恒温培养箱(MCO-15AC型,日本SANYO公司)中培养,待细胞贴满瓶底约80%时,用含EDTA的胰酶消化制成单细胞悬液(2×1010·L-1),取0.2 mL皮下接种于裸鼠右上肢腋下,待瘤体最大直径≥1 cm时进行动物实验。
1.4 实验动物分组皮下接种成瘤率100%,将制备成功的32只裸鼠乳腺癌模型随机分为对照组、IR组、单纯放疗组、IR+放疗组,每组8只。IR组:放疗前7 d开始每日给予IR蒸馏水悬浊液灌服,剂量约为每只0.5 mg;对照组:给予蒸馏水灌服;单纯放疗组:每只裸鼠用0.5%戊巴比妥钠腹腔注射麻醉,放疗采用美国Varian23EX医用直线加速器,使用6 MeV电子线照射,单次放疗,照射野10 cm×10 cm,剂量为10 Gy;IR+放疗组:IR的灌服同IR组,放疗方法及剂量同单纯放疗组。
1.5 18F-FLT micro PET/CT显像采用德国Siemens公司Inveon micro PET/CT进行扫描显像;FLT前体购自常熟华益化工有限公司,18F-FLT由上海交通大学医学院附属新华医院PET中心生产,放化纯>95%。所有MDA-MB231乳腺癌裸鼠模型均于放疗前及放疗结束后24 h,行micro PET/CT显像。裸鼠于显像前夜禁食,可自由饮水。将裸鼠固定,于裸鼠尾静脉注射18F-FLT约5.55 MBq(150 μCi),1 h后,用异氟烷麻醉并俯卧位固定于扫描床上进行显像,CT扫描10 min,PET扫描5 min,然后图像融合。显像完成后,由2位高年资的核医学科医师对micro PET/CT图像进行分析,选择病灶放射性浓聚最高的层面,测量SUV最大值(SUVmax)。
1.6 免疫组化检测显像完成后,采取颈椎脱臼法处死裸鼠。取出肿瘤组织,用体积分数10%中性甲醛溶液固定,石蜡包埋,4 μm厚切片,行Ki-67免疫组化检查。Ki-67蛋白以细胞核呈棕黄色或细胞质同时呈棕黄色为阳性。在高倍镜下,随机选择5个视野拍照分析,计算每张照片阳性细胞所占百分比(阳性细胞数/总细胞数)。
1.7 统计学分析采用SPSS 17.0软件,计量资料以x±s表示。各组治疗前后比较采用配对t检验,多组间比较采用单因素方差分析及LSD-t检验,两组数据比较采用两样本t检验,Ki-67表达与SUVmax的相关性采用Pearson相关分析。
2 结果 2.1 18F-FLT micro PET显像结果32只裸鼠micro PET/CT显像右侧腋下均可见结节状不同程度放射性摄取增高灶,部分肿瘤内部可见片状放射性分布缺损区。放疗前,4组显像SUVmax比较,差异无统计学意义(F=0.017,P > 0.05);放疗后,4组之间SUVmax差异有统计学意义(F=123.145,P < 0.05),对照组及IR组显像SUVmax较放疗前明显升高(t=-11.339、-11.103,P < 0.05),单纯放疗组及IR+放疗组SUVmax较放疗前明显降低(t=13.516、22.753,P < 0.05),且IR+放疗组SUVmax较单纯放疗组下降更明显(t=7.065,P < 0.05)。见Tab 1、Fig 1。
| Group | Tumor SUVmax | |
| Before radiotherapy | 24 h after radiotherapy | |
| Control | 1.043±0.113 | 1.340±0.088* |
| IR | 1.045±0.097 | 1.333±0.084* |
| Radiotherapy | 1.034±0.106 | 0.789±0.109* |
| IR+radiotherapy | 1.040±0.100 | 0.610±0.099*# |
| *P < 0.05 vs before radiotherapy; #P < 0.05 vs 24h after radiotherapy | ||

|
| Fig 1 18F-FLT micro PET/CT imaging of MDA-MB231 breast cancer in nude mice 24 h after radiotherapy A: Control group; B: IR group; C: Radiotherapy group; D: IR+radiotherapy group. The red arrowhead refers to the tumor. |
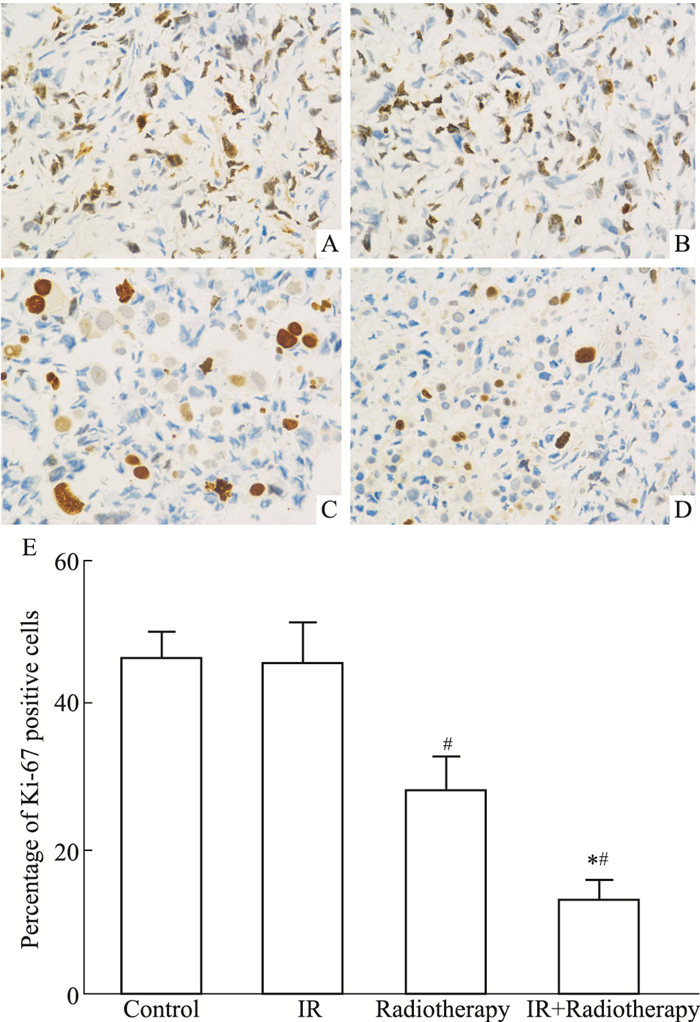
如Fig 2所示,对照组、IR组、单纯放疗组、IR+放疗组阳性细胞百分比分别为(46.43±3.69)%、(45.76±5.75)%、(28.13±4.74)%、(13.04±2.76)%,单纯放疗组及IR+放疗组阳性细胞百分比明显低于对照组(P < 0.05),IR+放疗组较单纯放疗组阳性细胞百分比更低(P < 0.05)。
|
| Fig 2 The Ki-67 immunohistochemistry in all groups of MDA-MB231 breast cancer in nude mice(×400) A: Control group; B: IR group; C: Radiotherapy group; D: IR+radiotherapy group; E: The percentage of Ki-67 positive cells. #P < 0.05 vs control group; *P < 0.05 vs radiotherapy group. |
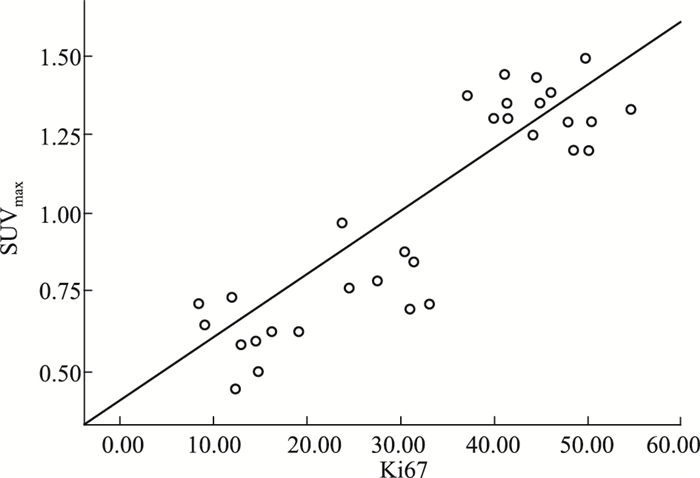
Fig 3的Pearson相关分析结果显示,Ki-67表达与SUVmax呈明显正相关(r=0.897,P < 0.05)。
|
| Fig 3 Correlation between expression of Ki-67 and SUVmax |
肿瘤的早期疗效评价直接影响肿瘤的后续治疗,关系着患者的生存及预后,应用合适的疗效评估方法可以给临床提供很大的帮助。相比传统的CT、MRI检查,正电子发射型计算机体层成像(PET/CT)对于肿瘤的诊断、分期及疗效评估有着独特的优势[4]。那些通过对实体瘤大小变化来判断治疗效果的传统方法,难以对肿瘤早期疗效进行准确评估,而PET/CT显像结合了PET功能成像与CT解剖成像的各自优点,既能准确定位,又能在实体瘤大小变化之前,更早、更准确地从功能上评估肿瘤的放疗增敏疗效[5-6]。恶性肿瘤的一大生物学特点是生长快,肿瘤细胞增殖迅速,因此,可通过检测肿瘤细胞增殖活性,评价肿瘤治疗效果[7]。18F-FLT是一种胸腺嘧啶类似物,为新近开发的细胞增殖显像剂,能够在胸腺嘧啶核苷激酶1(thymidine kinase 1,TK1)的作用下磷酸化,生成FLT-磷酸盐,滞留在细胞内。TK1是细胞DNA补救合成过程中的关键酶,在增殖细胞的S期和G1期有活性,而在静止细胞中无活性,因此,18F-FLT可以间接反映肿瘤增殖状况,评价肿瘤放、化疗疗效[8]。放射治疗通过电离辐射破坏肿瘤细胞DNA,使细胞坏死达到治疗目的,肿瘤对射线的敏感性是放射治疗是否有效的关键[9]。大多数实体瘤中存在的乏氧细胞使得其对射线不敏感,对于这种情况,使用放射增敏剂可以抑制肿瘤内乏氧细胞对射线的抗拒作用,提高放射敏感性,从而增加治疗效果[1]。IR是我国自主研发的一种放射增敏剂,它通过增加乏氧细胞DNA单键断裂,抑制恶性肿瘤细胞DNA合成及断裂后的修复,增加对放射治疗的敏感性[2]。Ki-67是一种细胞核增殖抗原,表达于细胞周期的S、G1、G2、M期, 而在G0期不表达[10]。Ki-67的表达与细胞增殖活性及预后密切相关,Ki-67表达高预示着细胞增殖活性高,因此,其可反映细胞增殖状态,同时Ki-67也可作为一种评估肿瘤治疗及预后判断的指标[11-12]。
本实验对乳腺癌实体瘤行放射治疗,使用放射增敏剂IR,并用18F-FLT micro PET/CT显像评估放射治疗疗效。结果显示,单纯放疗组及IR+放疗组SUVmax均较放疗前明显下降,说明在放射治疗后,肿瘤细胞DNA被破坏,肿瘤增殖受到抑制,滞留在细胞内的18F-FLT减少,因此,在micro PET/CT显像中,肿瘤病灶的放射性摄取下降。IR+放疗组较单纯放疗组SUVmax下降更明显,表明使用IR增加了对乳腺癌放射治疗的效果。免疫组化结果显示,单纯放疗组与IR+放疗组Ki-67的表达明显低于对照组,IR+放疗组表达更低,说明放射治疗后,肿瘤细胞的增殖活性降低,而使用放射增敏剂的IR+放疗组对放射治疗更敏感。18F-FLT micro PET/CT显像SUVmax与Ki-67表达呈正相关,进一步验证了18F-FLT micro PET/CT显像能反映肿瘤治疗早期细胞增殖活性的变化。
综上所述,IR对裸鼠乳腺癌具有放射增敏作用,18F-FLT micro PET/CT显像可以通过反映肿瘤细胞增殖活性的变化,评估IR对乳腺癌的放射增敏作用。
| [1] | Tian J, Zhao H, Nolley R, et al. Darinaparsin: solid tumor hypoxic cytotoxin and radiosensitizer[J]. Clin Cancer Res, 2012, 18(12): 3366-76. doi:10.1158/1078-0432.CCR-11-3179 |
| [2] | Xu H, Sun G, Wang H, et al. Dynamic observation of the radiosensitive effect of irisquinone on rabbit VX2 lung transplant tumors by using fluorine-18-deoxyglucose positron emission tomography/computed tomography[J]. Nucl Med Commun, 2013, 34(3): 220-8. doi:10.1097/MNM.0b013e32835d3730 |
| [3] | Yamamoto Y, Ono Y, Aga F, et al. Correlation of 18F-FLT uptake with tumor grade and Ki-67 immunohistochemistry in patients with newly diagnosed and recurrent gliomas[J]. J Nucl Med, 2012, 53(12): 1911-5. doi:10.2967/jnumed.112.104729 |
| [4] | 杨超, 丘建燊, 张芨, 等. 18F-FDG PET/CT在肺内多发病灶穿刺部位选择中的临床价值[J]. 中国临床医学影像杂志, 2017, 28(1): 30-4. Yang C, Qiu J R, Zhang J, et al. Clinical value of 18F-FDG PET/CT in puncture site selection for multiple lung lesions[J]. Chin Clin Med Imaging, 2017, 28(1): 30-4. doi:10.3969/j.issn.1008-1062.2017.01.009 |
| [5] | 李亚明. 功能影像与肿瘤化疗疗效评价[J]. 中国实用内科杂志, 2012, 32(4): 243-4. Li Y M. Functional imaging: open up new areas of cancer chemotherapy efficacy evaluation[J]. Chin J Pract Intern Med, 2012, 32(4): 243-4. |
| [6] | Zeng Y C, Wu R, Xu Z G, et al. Safety and radiation-enhancing effect of sodium glycididazole in locoregionally advanced laryngeal cancers previously treated with platinum-containing chemotherapy regimens: A preliminary report[J]. Cancer Radiother, 2010, 14(1): 59-64. doi:10.1016/j.canrad.2009.06.022 |
| [7] | Nakajo M, Kajiya Y, Jinguji M, et al. Current clinical status of 18F-FLT PET or PET/CT in digestive and abdominal organ oncology[J]. Abdom Radiol (NY), 2017, 42(3): 951-61. doi:10.1007/s00261-016-0947-9 |
| [8] | Qi S, Zhongyi Y, Yingjian Z. 18F-FLT and 18F-FDG PET/CT in predicting response to chemoradiotherapy in nasopharyngeal carcinoma: preliminary results[J]. Sci Rep, 2017, 7: 40552. doi:10.1038/srep40552 |
| [9] | 张丹, 韩苏夏. 放射治疗及放射治疗增敏研究进展[J]. 西部医学, 2013, 25(9): 1281-3. Zhang D, Han S X. Recent advances in radiotherapy and radiotherapy sensitization[J]. Med J West China, 2013, 25(9): 1281-3. doi:10.3969/j.issn.1672-3511.2013.09.001 |
| [10] | Pezzilli R, Partelli S, Cannizzaro R, et al. Ki-67 prognostic and therapeutic decision driven marker for pancreatic neuroendocrine neoplasms (PNENs): a systematic review[J]. Adv Med Sci, 2016, 61(1): 147-53. doi:10.1016/j.advms.2015.10.001 |
| [11] | Erler B S, Presby M M, Finch M, et al. CD117, Ki-67 and p53 predict survival in neuroendocrine carcinomas, but not within the subgroup of small cell lung carcinoma[J]. Tumour Biol, 2011, 32(1): 107-11. doi:10.1007/s13277-010-0104-y |
| [12] | 司玲玲, 马俊, 任欢欢, 等. 刺槐素对乳腺癌T47D细胞增殖的影响[J]. 中国药理学通报, 2017, 33(2): 260-7. Si L L, Ma J, Ren H H, et al. Effects of acacetin on T47D cell proliferation[J]. Chin Pharmacol Bull, 2017, 33(2): 260-7. doi:10.3969/j.issn.1001-1978.2017.02.022 |

