

光动力疗法(photodynamic therapy,PDT)是一种美国FDA批准的治疗恶性肿瘤的新方法,起源于20世纪70年代,其原理是恶性肿瘤选择性地摄入并潴留光敏剂,在特定波长光激发下,引发一系列光化学反应,释放出单态氧,杀死肿瘤组织,产生治疗作用[1]。光敏剂是决定PDT疗效的重要因素之一。癌光啉(代号:PSD-007)是由多种有活性血卟啉衍生物组成的混合物,如3,8-(1-甲氧乙基) -8(3) -乙酰基-次卟啉Ⅸ(MVD)、3(8) -(1-甲氧乙基) -8 (3) -(1-羟乙基) -次卟啉Ⅸ(MHD)、3,8-二(1-甲氧乙基) -次卟啉Ⅸ(DMD)、3 (8) -(1-羟乙基) -8 (3) -乙酰基-次卟啉Ⅸ(HVD)、原卟啉Ⅸ(Pp)、血卟啉Ⅸ(HP)等[2]。与第1代光敏剂HpD相比,PSD-007具有避光时间短、单线态氧产率高、对肿瘤组织选择性摄入率高、对正常组织毒性小、在人体正常组织内代谢速度快等优点,针对肿瘤治疗有较好的疗效,是国内光敏剂研究的热点。
氧化损伤是阿尔茨海默病、帕金森病等神经退行性疾病重要的发病机制。具有清除氧自由基的中药是治疗神经退行性疾病的热点,抗氧化也是预防各种疾病的热点。槲皮素(quercetin,Que)化学名为3,3′,4′,5,7-五羟基黄酮,存在于许多植物的花、叶、果实中,其药理作用广泛,具有抗癌、抗炎、心血管系统保护等作用,尤其具有明显的抗氧化和清除自由基的作用[3-4]。茶多酚(tea polyphenol, TP)属黄烷醇类,是从绿茶叶中提取的多酚类物质,是茶叶的主要活性成份之一,主要包括4种成分:表没食子儿茶素没食子酸酯、表没食子儿茶素、表儿茶素没食子酸酯、表儿茶素[5]。TP除具有抗突变、降血压、降血脂、防治心血管疾病、抗氧化、抗菌消炎等功效外,还具有抑制淋巴细胞增殖[6]、降低高尿酸血症、抗氧化作用[7]、抗癌防癌等活性[8]。实验表明TP可透过血脑屏障,清除自由基,提高Aβ损伤的神经细胞的存活率,维持细胞内线粒体结构和功能的完整,保护脑细胞免受神经毒素损伤[9]。抗氧化剂对PDT效应的影响仅有少量报道,抗氧化剂对PDT效应是否有影响尚有争议。本研究利用PDT氧化损伤PC12细胞,在此基础上研究槲皮素、茶多酚对PDT效应的影响,以期为黄酮类和多酚类化合物在PDT临床治疗方面的研究和利用积累资料。
1 材料与方法 1.1 细胞与试剂大鼠肾上腺嗜铬瘤细胞(PC12细胞,无分化),购于北京协和医学院基础研究所细胞中心。槲皮素、茶多酚购自上海源叶生物科技有限公司(用DMSO溶剂配成储备液);PSD-007由中国医学科学院生物医学工程研究所激光医学实验室馈赠;DMEM高糖培养基购自美国Hyclone公司;胎牛血清购自美国Gibco公司;MTT购自美国Amresco公司;乳酸脱氢酶(lactic dehydrogenase,LDH)试剂盒购自碧云天生物技术有限公司;其他试剂均为分析纯。
1.2 仪器CO2细胞培养箱、Milli-Q超纯水系统(美国Thermo公司);超净工作台(苏州安泰空气技术有限公司);Safire2酶标仪(美国TECAN公司);3K30型高速冷冻离心机(德国Sigma公司);倒置显微镜(上海光学仪器)。
1.3 细胞培养PC12细胞接种于DMEM高糖培养基(含10%小牛血清、50 kU·L-1青霉素、50 kU·L-1链霉素),于37℃、5% CO2条件下培养,每3~4 d传代1次。待细胞呈对数期增长时用于实验。
1.4 MTT法检测细胞存活率细胞以3×104/孔接种96孔板,每孔加入20 μL MTT溶液(5 g·L-1),37℃孵育4 h后,每孔加180 μL DMSO溶解甲臜蓝紫色颗粒,震荡混匀后,于570 nm测定各孔吸光度值(optical density,OD)。按下式计算细胞存活率:细胞存活率=(实验组OD570/空白对照组OD570)×100%。
1.5 槲皮素和茶多酚对PC12细胞毒性检测待PC12细胞呈对数期增长时消化细胞,以每孔3×104细胞接种于96孔板中,每孔100 μL。次日弃培养基,200 μL PBS洗1次细胞后,分别加入槲皮素(6.25、12.5、25、50、100 μmol·L-1)、茶多酚(6.25、12.5、25、50、100 μmol·L-1)的无血清培养基100 μL。于37℃、5% CO2条件下孵育24 h。PC12细胞空白对照组,不加其他干预。每组4个复孔取平均值,MTT法检测细胞存活率。
1.6 PSD-007介导的PDT对PC12细胞的杀伤作用取对数生长期的PC12细胞接种于96孔培养板中,每孔3×104个细胞。24 h后,加入光敏剂PSD-007溶液(终浓度0、3.125、6.25、12.5、25、50 mg·L-1),每组4个复孔,避光孵育24 h测定暗毒性。孵育4 h后,换全培养基孵育2 h后,每孔给予630 nm激光照射,能量密度4.8 J/cm2(20 mW/cm2,4 min)。24 h后,MTT法检测细胞存活率。空白对照组PC12细胞不加其他干预,激光照射对照组仅以4.8 J/cm2激光照射。
1.7 MTT法检测槲皮素和茶多酚对PSD-007介导的PDT效应的影响对数生长期的PC12细胞接种于96孔板中。实验分为5组:空白对照组、PSD-007组(10 mg·L-1)、LASER组(激光照射4.8 J/cm2)、PDT损伤组(10 mg·L-1 PSD-007,4.8 J/cm2)、槲皮素处理组(12.5、25、50 μmol·L-1)、茶多酚处理组(12.5、25、50 μmol·L-1),每组4个复孔,对照组不加任何干预。PDT损伤组加入10 mg·L-1的PSD-007 100 μL,4 h后,以630 nm激光照射4 min,能量密度为4.8 J/cm2;槲皮素、茶多酚处理组分别加入槲皮素或茶多酚溶液100 μL,4 h后,分别加入10 mg·L-1的PSD-007溶液100 μL,4 h后,弃上清,加入全培养基100 μL。孵育2 h后,给予630 nm激光照射,能量密度为4.8 J/cm2。继续培养24 h后,MTT法检测细胞的活性。
1.8 LDH法检测槲皮素和茶多酚对PSD-007介导PDT效应的影响LDH正常情况下存在于细胞内,培养上清LDH活性极低。只有当细胞膜受破坏,膜通透性增高,胞内LDH释放至细胞外,培养上清LDH活性才会升高,而活细胞无此功能,所以培养上清中LDH的含量可反映细胞的死亡或损伤程度。采用LDH法检测槲皮素、茶多酚对PSD-007介导的PDT的影响,取对数生长期的PC12细胞接种于96孔培养板中,实验分组处理同“1.7”,每组4个复孔。各组放入CO2培养箱30 min后,吸去上清,每孔加入150 μL LDH释放剂,摇晃均匀后孵育1 h。每孔吸取上清120 μL放入新孔中,并做好标记。每孔再加入60 μL LDH检测工作液,混匀后避光放置30 min。用酶标仪在490 nm波长下检测细胞LDH活性。
1.9 统计学方法多组间比较采用单因素方差分析,两两比较采用SNK法。
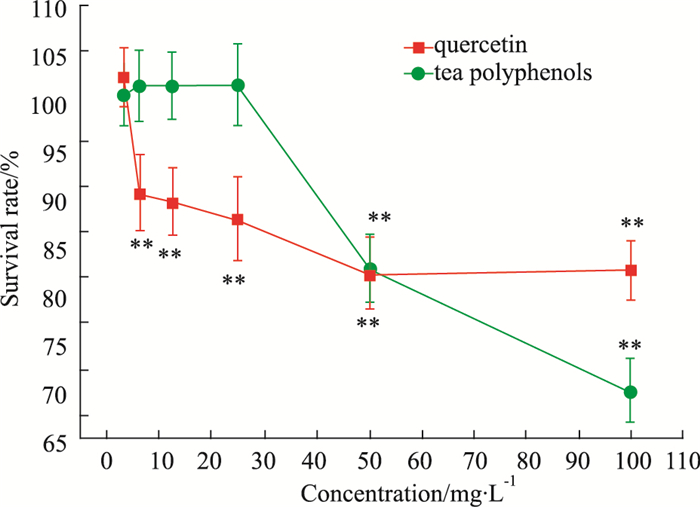
2 结果 2.1 槲皮素和茶多酚对PC12细胞的毒性如Fig 1所示,6.25 μmol·L-1槲皮素使细胞存活率降低10.7%,50~100 μmol·L-1槲皮素使细胞存活率降低约21.5%。茶多酚6.25~25 μmol·L-1组细胞存活率无明显变化;茶多酚(25~100 μmol·L-1)随浓度增加,细胞存活率降低,100 μmol·L-1茶多酚使细胞存活率降低了33.3%。
|
| Fig 1 Cytotoxicity of quercetin and tea polyphenols on PC12 cells (x±s, n=4) **P < 0.01 vs control |
以4.8 J/cm2激光照射后,激光照射对照组细胞存活率100.4%,说明4.8 J/cm2激光对细胞存活率没有影响。如Fig 2所示,PSD-007(3.25~25 μmol·L-1)对PC12细胞存活率无明显影响,大于25 mg·L-1时PC12细胞的存活率开始下降,50 mg·L-1时细胞存活率为90%。随着PSD-007浓度的增加,PDT杀伤效应增强,PC12细胞的存活率逐渐下降,在25 μmol·L-1浓度时趋于稳定,细胞存活率为65%,不再有明显降低。总之,光敏剂PSD-007浓度低于25 mg·L-1时,几乎没有暗毒性,可以用于后续PDT实验。

|
| Fig 2 Effects of PSD-007 and PSD-007 induced PDT on survival rates of PC12 cells(x±s, n=4) **P < 0.01 vs control |
如Fig 3所示,PDT组细胞存活率为83.8%,槲皮素(12.5、25、50 μmol·L-1)组细胞存活率分别增加1.166倍、1.134倍、1.129倍。。槲皮素(12.5~50 μmol·L-1)对光动力效应具有拮抗作用,对PC12细胞具有保护作用;茶多酚(12.5、25、50 μmol·L-1)组细胞存活率降低14.0%、8.8%、17.2%,茶多酚(12.5~50 μmol·L-1)对PC12细胞不但没有保护作用,反而抑制PC12细胞活性,茶多酚与光动力效应具有协同作用。

|
| Fig 3 Effects of quercetin(A) and tea polyphenols(B) on PSD-007 induced PDT(x±s, n=4) ##P < 0.01 vs control; **P < 0.01 vs PDT |
如Fig 4A所示,与PDT组相比,槲皮素(12.5、25、50 μmol·L-1)组PC12细胞上清中LDH明显降低(P < 0.01)。如Fig 4B所示,与PDT组相比,茶多酚(12.5、25、50 μmol·L-1)组PC12细胞上清中LDH无明显变化(P > 0.05)。空白对照组、PSD-007组、LASER组PC12细胞上清中LDH活性很低。

|
| Fig 4 Effects of Que(A) and TP(B) on LDH in PC12 cell supernatant (x±s, n=4) ##P < 0.01 vs control; **P < 0.01 vs PDT |
PDT基于细胞摄取光敏剂后,光敏剂经合适波长光激发后,可发生Ⅰ型和Ⅱ型光动力反应,产生活性氧。首先发生Ⅰ型反应,激发态的单线态氧直接损伤细胞膜或分子,通过质子或电子传递,生成活性阴离子或阳离子,继续与氧和水反应,生成自由基和活性氧。PDT产生的单线态氧等活性氧介导的氧化应激,是PDT引起细胞损伤的主要细胞毒性剂。氧化应激是由自由基在体内产生的一种负面作用,被认为是导致衰老和疾病的一个重要因素。在神经退行性病变中有活性氧增加现象,抗氧化剂可以减缓氧化应激带来的危害。本文选择使用光动力疗法对PC12细胞造成氧化损伤,建立一种检测体内药物抗氧化能力的新方法,为抗氧化剂的新药筛选建立一个新模型——PDT氧化应激模型法,可用于高通量筛选的新药药效筛选模型。
据报道,γ射线、X射线电离辐射激发机体产生大量自由基,槲皮素能减轻辐照后细胞内氧化损伤,其浓度在24 μmol·L-1时防护效果最佳[10-11]。槲皮素低浓度(< 100 μmol·L-1)时对老年性黄斑变性人视网膜色素上皮细胞的氧化性损伤具有保护作用[12]。PDT后产生氧自由基氧化损伤PC12细胞,本实验研究发现,槲皮素在6.25~50 μmol·L-1时,PC12细胞存活率约90%,抑制细胞增殖,槲皮素(50~100 μmol·L-1)表现出明显的细胞毒性。槲皮素(12.5~25 μmol·L-1)降低了PDT对PC12细胞的杀伤率,提高了PC12细胞的存活率,降低了上清LDH含量,说明细胞膜是槲皮素保护作用的靶点,槲皮素12.5 μmol·L-1对细胞保护作用最佳。槲皮素具有抗癌作用,但对PDT效应具有拮抗作用,具有双向性,与文献报道一致[12]。
茶多酚是含有2个以上羟基的多酚类物质,具有很强的供氢能力,可以终止自由基链反应,因而被广泛作为抗氧化剂应用[8]。本实验研究发现:茶多酚(6.25~25 μmol·L-1)组PC12细胞存活率没有降低,茶多酚(25~100 μmol·L-1)随浓度增加,细胞存活率逐渐降低,100 μmol·L-1时降低到70%,证明茶多酚具有抗肿瘤作用,与文献报道[13],茶多酚是一种具有很强生物学活性抗肿瘤药物,已被证实对多种恶性肿瘤均有较强抵抗作用的结果一致。茶多酚抗癌机制为抑制致癌物前体的代谢活化,抑制肿瘤细胞DNA的复制,减少DNA损伤,阻断AP-1信号通路等[4]。与PDT组相比,茶多酚+PDT组PC12细胞存活率明显降低(P < 0.01),12.5~50 μmol·L-1茶多酚对PDT损伤细胞膜几乎没有保护作用,与PDT对PC12细胞具有协同杀伤作用。
抗氧化剂对PDT氧化是否有保护作用,具有争议。Frank等[14]发现,维生素C抑制5-ALA-PDT对癌细胞的氧化作用。Shevchuk等[15]发现,t-丁基-4-羟基茴香醚可以提高PDT的效率。Kelley等[16]证明,用抗氧化剂金丝桃素介导的PDT对HL-60细胞没有明显的保护作用。本实验用PSD-007诱导PDT氧化损伤PC12细胞,建立抗氧化药物的细胞模型,可用于高通量药物活性筛选,打破目前抗氧化实验只能在体外化学环境中进行的局限性。初步筛选出天然抗氧化剂槲皮素对PSD-007损伤PC12细胞具有保护作用,茶多酚对PSD-007损伤PC12细胞具有协同作用(无保护作用)。除了细胞膜作用靶点外,其他作用机制还需要进一步研究。建立或完善天然抗氧化剂对光动力效应影响的数据库,指导接受光动力疗法的病人的饮食,有待进一步丰富资料。
| [1] | Dolmans D E, Fukumura D, Jain R K. Photodynamic therapy for cancer[J]. Nat Rev Cancer, 2003, 3(5): 380-7. doi:10.1038/nrc1071 |
| [2] | 陈文晖, 许德余, 殷祥生. 新肿瘤光化学诊治剂(PSD-007)的化学组成的研究[J]. 现代应用药学, 1993, 10(6): 12-4. Chen W H, Xu D Y, Yin X S. Studies on determination of the chemical composition of the new tumor-photochemodiagnostic & phtochemotherapeutie agent (PsD-007)[J]. Chin J Mod Applied Pharm, 1993, 10(6): 12-4. |
| [3] | Saviranta N M, Veeroos L, Granlund L J, et al. Plant flavonol quercetinand isoflavone biochanin a differentially induce protection a-gainst oxidative stress and inflammation in ARPE-19 cells[J]. Food Res Int, 2011, 44(1): 109-13. doi:10.1016/j.foodres.2010.10.056 |
| [4] | 张薇, 何龙, 刘潇忆, 等. 槲皮素通过影响吲哚胺-2, 3-双加氧酶活性抑制HeLa细胞增殖的研究[J]. 中国药理学通报, 2018, 34(2): 219-24. Zhang W, He L, Liu X Y, et al. Quercetin inhibits proliferation of human cervical carcinoma HeLa cells through affecting tryptophan metabolism[J]. Chin Pharmacol Bull, 2018, 34(2): 219-24. doi:10.3969/j.issn.1001-1978.2018.02.015 |
| [5] | 翁鹭娜, 黄河宁. 茶多酚抑制肿瘤的分子机制研究进展[J]. 海峡药学, 2008, 20(4): 7. Weng L N, Huang H N. Progress in tumor inhibition molecular mechanism of tea polyphenols[J]. Str Pharm J, 2008, 20(4): 7. doi:10.3969/j.issn.1006-3765.2008.04.003 |
| [6] | 李伟, 王遂泉, 吴辛刚, 等. 茶多酚有效成分对淋巴细胞增殖的抑制和抗氧化作用[J]. 中国药理学通报, 2015, 31(2): 294-5. Li W, Wang S Q, Wu X G, et al. Effects of active ingredients of tea polyphenol on inhibiting lymphocyte proliferation and antioxidation[J]. Chin Pharmacol Bull, 2015, 31(2): 294-5. doi:10.3969/j.issn.1001-1978.2015.02.029 |
| [7] | 陈刚, 谭明亮. 茶多酚对高尿酸血症小鼠尿酸产生与排泄的影响及机制研究[J]. 中国药理学通报, 2017, 33(2): 218-22. Chen G, Tan M L. Effect of green tea polyphenols on uric acid level in potassium oxonate-induced hyperuricemic mice and mechanism[J]. Chin Pharmacol Bull, 2017, 33(2): 218-22. doi:10.3969/j.issn.1001-1978.2017.02.015 |
| [8] | Thangapazham R L, Singh A K, Sharma A, et al. Green tea polyphenols and its constituent epigallocatechin gallate inhibits proliferation of human breast cancer cells in vitro and in vivo[J]. Cancer Lett, 2007, 245(1-2): 232-41. doi:10.1016/j.canlet.2006.01.027 |
| [9] | Li Q S, Zou L L, Fu T, et al. Excretion of four catechins in tea polyphenols in rats[J]. Chin Herb Med, 2009, 1(1): 59-65. |
| [10] | Devipriya N, Sudheer A R, Srinivasan M, et al. Quercetin ameliorates gamma radiation-induced DNA damage and biochemical changes in human peripheral blood lymphocytes[J]. Mutat Res, 2008, 654(1): 1-7. doi:10.1016/j.mrgentox.2008.03.003 |
| [11] | 喻晶, 张继青, 葛宁, 等. 槲皮素对大剂量X线暴露所致PC12细胞氧化性损伤的保护作用[J]. 中国药理学与毒理学杂志, 2013, 27(1): 34-7. Yu J, Zhang J Q, Ge N, et al. Protective effect of quercetin against oxidative damage induced by high-dose X-ray exposure in PC12 cells[J]. Chin J Pharmacol Toxicol, 2013, 27(1): 34-7. doi:10.3867/j.issn.1000-3002.2013.01.007 |
| [12] | Kook D, Wolf A H, Yu A L, et al. The protective effect of quercetin against oxidative stress in the human RPE in vitro[J]. Invest Ophthalmol Vis Sci, 2008, 49(4): 1712-20. doi:10.1167/iovs.07-0477 |
| [13] | 陈淑珍, 甄永苏. 茶多酚的分子作用靶点及其在抗肿瘤药物实验治疗中的作用[J]. 药学学报, 2013, 48(1): 1-7. Chen S Z, Zhen Y S. Molecular targets of tea polyphenols and its roles of anticancer drugs in experimental therapy[J]. Acta Pharm Sin, 2013, 48(1): 1-7. doi:10.3969/j.issn.1008-7303.2013.01.01 |
| [14] | Frank J, Flaccus A, Schwarz C, Lambert C. Ascorbic acid suppresses cell death in rat DS-sarcoma cancer cells induced by 5-aminolevulinic acid-based photodynamic therapy[J]. Free Radic Biol Med, 2006, 40(5): 827-36. doi:10.1016/j.freeradbiomed.2005.10.034 |
| [15] | Shevchuk I, Chekulayev V, Chekulayeva L. Enhancement of the efficiency of photodynamic therapy of tumours by t-butyl-4-hydroxyanisole[J]. J Photochem Photobiol B, 1998, 45(2-3): 136-43. doi:10.1016/S1011-1344(98)00172-9 |
| [16] | Kelley E E, Domann F E, Buettner G R, et al. Increased efficacy of in vitro Photofrin photosensitization of human oral squamous cell carcinoma by iron and ascorbate[J]. J Photochem Photobiol B, 1997, 40(3): 273-7. doi:10.1016/S1011-1344(97)00068-7 |

