


2. 广州中医药大学 第一临床医学院,广东 广州 510006;
3. 暨南大学附属第一医院口腔医疗中心,广东 广州 510630;
4. 暨南大学口腔医学院,广东 广州 510630
 ,
XIE Zhao-yu1,
JIN Jia-qi1,
LAI Jie-qing2,
LIAN Da-wei1,
HUANG Lin-yan4,
HUANG Yi3,4,
CHEN Yang1
,
XIE Zhao-yu1,
JIN Jia-qi1,
LAI Jie-qing2,
LIAN Da-wei1,
HUANG Lin-yan4,
HUANG Yi3,4,
CHEN Yang1

2. the First School of Clinical Medicine, Guangzhou University of Chinese Medicine, Guangzhou 510000, China;
3. Dept of Stomatology, the First Affiliated Hospital, Jinan University, Guangzhou 510630, China;
4. School of Dental Medicine, Jinan University, Guangzhou 510630, China
牙周炎是非特异性的慢性感染性疾病, 牙颈部及龈沟内牙菌斑中的微生物是其主要感染源, 是常见的口腔慢性疾病,也是牙齿非正常脱落的重要原因,严重威胁着我国居民的口腔健康。根据卫计委2017年第四次全国口腔健康流行病学调查报告显示在35~44岁居民中,口腔内牙石检出率为96.7%,与10年前持平;牙龈出血检出率为87.4%比十年前上升了10.1%。牙周膜成纤维细胞(periodontal ligament fibroblasts, PDLFs)可以对牙周组织进行修复和改建,是牙周膜组织中数目最大、最主要的细胞类型,对牙周炎发展过程具有重要作用[1]。牙龈卟啉单胞菌(porphyromonasgingivalis, P.g)是牙周炎的主要致病菌,是牙周膜成纤维细胞产生炎症反应的主要因素[2]。
近代张锡纯提出牙疼是因为胃热上炎,血热并于牙龈作痛,并伴有牙龈出血溃烂,因此治宜清热止血;大黄是临床常用的清热止血药,有临床报告表示在牙周袋局部用大黄治疗牙周炎能有效阻断炎症的发展[3]。芦荟大黄素(aloe-emodin, AE)是大黄重要的蒽醌类有效成分,有较强的抗厌氧菌及抗炎作用,且极佳的抗氧化损伤的作用[4]。但关于AE抗炎机制的研究却少见报道。因此本研究通过观察AE对牙龈卟啉单胞菌脂多糖(Porphyromonasgingivalislipopolysaccharide, P.g-LPS)诱导牙周膜成纤维细胞Nlrp3炎症小体活化的影响,探讨其机制。
2 材料和方法 2.1 实验材料及试剂 2.1.1小鼠牙周膜成纤维细胞(mouse periodontal ligament fibroblasts, mPDLFs)购自武汉Procell公司,货号:CP-M199。
2.1.2P.g-LPS(tlrl-pglps)、AE(A7687)购自美国sigma公司。
2.1.30.25%胰酶(25200056)、DMEM培养基(11995065)、胎牛血清(FBS) (16140071)购自美国Gibco公司;ROS试剂盒购自中国南京建成生物研究所(E004);蛋白酶抑制剂(Cocktail)购自美国sigma公司;RIPA Buffer购自美国Millipore公司;脱脂牛奶购自美国Becton, Dickinson and Company;BCA试剂盒(P0028)及蛋白上样缓冲液购自中国碧云天公司;PVDF膜购自美国Millipore公司;anti-β-actin(BM0627)(1:1 000)购自中国BOSTER;anti-caspase-1(sc-514)(8:5 000)购自美国Santa公司;anti-Nlrp3(15101S)(1:1 000)、anti-TXNIP(14715S)(1:1 000)、anti-rabbit IgG(7074S)(1:1 500)、anti-mouse IgG(4408S)(3:5 000)购自美国CST公司;PrimeScriptTM RT reagent kit with gDNAEeaser(RR047A)购自TaKaRa公司;RNAiso Plus、SYBR GREEN(RR820A)购自日本TaKaRa公司。
2.1.4化学发光成像分析系统(TANON 5200)购自中国TANON公司;实时定量荧光PCR仪(CFX96 TouchTM)购自美国Bio-rad公司。
2.2 细胞培养和给药小鼠牙周膜成纤维细胞以10%FBS的高糖DMEM培养基在37℃、5% CO2饱和湿度的环境中培养,每2~3天传代。将无血清的DMEM将0.25%胰酶稀释3倍用于消化。P.g-LPS来自牙龈卟啉单胞菌,用培养基溶解并稀释至2 μg·mL-1作为刺激剂;AE以0.05、0.1、0.3、0.5 μmol·L-1浓度分别给药,并在上述环境中培养24 h备用。
2.3 活性氧(Reactive oxygen species,ROS)实验采用DCFH-DA作为活性氧探针。细胞铺板后6 h给药,培养24 h后,弃去培养基,PBS清洗。将DCFH-DA按1:4 000用培养基稀释后,加入细胞培养板中,37℃孵育30 min,并在荧光显微镜下观察。0.25%胰酶消化细胞后,1 000 r·min-1离心5 min收集细胞,PBS洗两次,离心收集细胞沉淀物。将收集好的细胞沉淀物用PBS重悬,用荧光酶标仪进行检测。检测时激发光波长为485 nm,发射光波长525 nm。
2.4 Western blot总蛋白利用RIPA法提取,并用BCA法测总蛋白浓度。加入适量蛋白上样缓冲液并在100℃中变性5分钟,随后4℃保存备用。利用12% SDS-PAGE凝胶110V恒压分离,之后110V恒压转膜到PVDF膜上。利用5%脱脂牛奶为封闭液,封闭2 h。对应的一抗在室温下孵育1 h后转移至4℃孵育过夜,二抗室温孵育2 h。最后用Tanon化学发光成像分析系统采集图像,并分析灰度值。每组实验重复3次。
2.5 RNA的提取和实时定量PCR总RNA用RNAiso Plus提取。总RNA利用UV-Vis测定浓度,A260/A280值均在1.8~2.2范围内。逆转录反应用PrimeScript RT reagent Kit with gDNA Eraser,依照说明书进行。实时定量PCR用SYBR Green Realtime PCR Master Mix采用两步法进行反应,第一步95℃ 30秒,第二步95℃ 5秒;60℃ 30秒循环40次。实验利用Real-Time PCR仪进行,反应重复三次。引物序列如下:小鼠Nlrp3基因:5′-ATTRACCRCGCRCCGRAGARAAGRG-3′ (forward primer),5′- TCGRCAGRCAARAGARTCCRACARCAG -3′ (reverse primer);小鼠caspase-1基因:5′-GAGCTGATGTTGACCTCAGAG-3′ (forward primer),5′- CTGTCAGAAGTCTTGTGCTCTG -3′ (reverse primer);内参基因为β-actin:5′-CCCATCTATGAGGGTTACGC-3′(forward primer),5′- TTTAATGTCACGCACGATTTC-3′ (reverse primer)。
2.6 统计学分析数据为三次实验结果的平均值和标准偏差(x±s),数据用SPSS 17软件One-Way ANOVA(完全随机设计的单因素方差分析)统计方法处理,方差齐时,组间比较采用LSD方法;方差不齐时,组间比较采用DunnettT3法。P < 0.05视为有显著性差异。
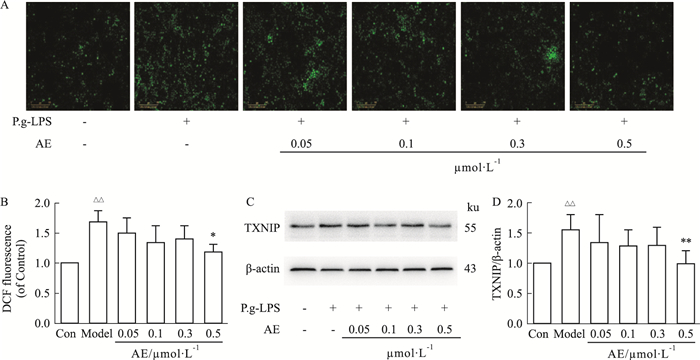
3 结果 3.1 AE对mPDLFs产生ROS能力及硫氧还蛋白相互作用蛋白(thioredoxin-interacting protein,TXNIP)表达量的影响如图 1所示,P.g-LPS刺激mPDLFs 24 h后,ROS的产生量明显高于空白对照组。在使用AE治疗后,ROS的产生被抑制,并在0.5 μmol·L-1时降到最低,与模型组相比,有统计学差异。P.g-LPS使小鼠牙周膜成纤维细胞中TXNIP的表达明显增高。在给予AE后,TXNIP的表达有下降的趋势,当AE的剂量在0.5 μmol·L-1时与模型组有统计学差异。
|
| Fig 1 The effect of AE on ROS production and TXNIP expression in mPDLFs induced by P.g-LPS.A and B the effect of AE on ROS production in P.g-LPS-induced mPDLFs. C and D the effect of AE on TXNIP expression in P.g-LPS-induced mPDLFs. ΔΔP < 0.01 vs control; *P < 0.05, **P < 0.01 vs model (P.g-LPS) |

|
| Fig 2 The effect of AE on the transcription and expression of Nlrp3 in mPDLFs induced by P.g-LPS. ΔP < 0.05, ΔΔP < 0.01 vs control; *P < 0.05, **P < 0.01 vs model (P.g-LPS) |
|
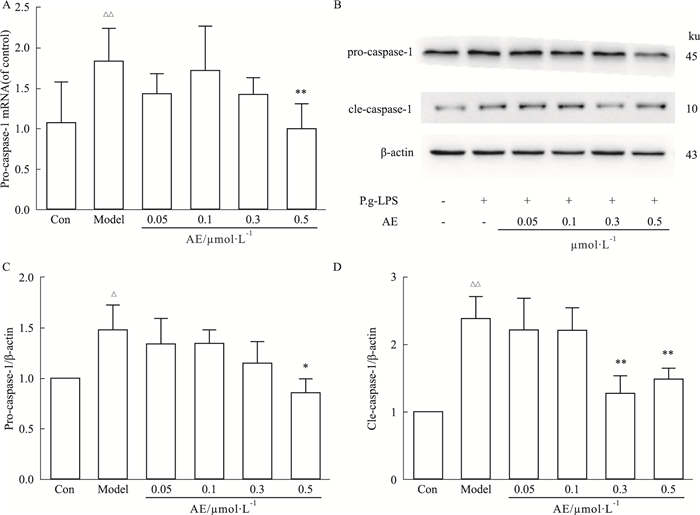
| Fig 3 The effect of AE on the transcription and expression of Pro-caspase-1 and cle-caspase-1 expression in mPDLFs induced by P.g-LPS. ΔP < 0.05, ΔΔP < 0.01 vs control; *P < 0.05, **P < 0.01 vs model (P.g-LPS) |
P.g-LPS使mPDLFs中Nlrp3的转录水平明显高于空白对照组。给予AE后,随着AE剂量的增加,其转录水平随之降低。在WB实验中,模型组的Nlrp3的表达量明显高于空白对照组,给予不同浓度AE后也随之下降。AE对Nlrp3的转录与表达的阻断自最小剂量开始与模型组有统计学差异。
3.3 AE对P.g-LPS诱导mPDLFs中前体caspase-1(pro-caspase-1)转录与表达及活化caspase-1(cle-caspase-1)表达的影响模型组的前体caspase-1的转录水平明显高于空白对照组,给予AE后,随着AE剂量的增加,其转录水平随之降低。同时,模型组的前体caspase-1的蛋白表达量及相应的活化caspase-1均明显高于空白对照组,给予不同浓度AE后均随之下降。前体caspase-1的转录水平与蛋白表达量均当AE在0.5 μmol·L-1时与模型组有统计学差异。与前体caspase-1相似,P.g-LPS令mPDLFs大量表达活化caspase-1,当给予AE治疗后其表达量下降,并自0.3 μmol·L-1的剂量开始与模型组有统计学差异。
4 讨论本研究证明AE对P.g-LPS引起的牙周膜成纤维细胞损伤具有保护作用,其作用是通过抑制P.g-LPS引起的牙周膜成纤维细胞ROS-TXNIP通路活化,减缓Nlrp3-inflammasome组成蛋白的聚集及活化程度实现的,除此之外,研究还发现AE的保护作用具有浓度依赖性的变化。
在近年来的研究中发现,牙周炎作为一种顽固性的慢性病变,它的发生发展与Nlrp3-inflammasome关系密切,其重要原因是Nlrp3-inflammasome被认为是慢性疾病的中心致病环节[5-6]。Nlrp3-inflammasome可以调控细胞焦亡[7]、破坏细胞骨架[8]、影响细胞功能蛋白的合成、代谢或分泌[9]等细胞功能和活力。Nlrp3-inflammasome,由三部分构成:Nlrp3蛋白与衔接蛋白——ASC及细胞凋亡蛋白酶前体(pro-caspase-1)[10]。研究指出,P.g作为导致牙周炎的主要病原体,其分泌的P.g-LPS可以通过刺激巨噬细胞、成纤维细胞和上皮细胞等分泌IL-1,IL-6,IL-8,TNF和前列腺素E等多种炎性介子导致牙周结缔组织的破坏和牙槽骨的吸收[2]。而某些特定的炎性介质如IL-1与Inflammasome关系密切。由上不难看出,Nlrp3炎症小体通路是抗炎药物发挥药效的潜在靶点[5],因此在本研究中,将AE的抗炎作用是否与Nlrp3炎症小体关联作为研究重点。活化caspase-1来自于活化的Nlrp3-inflammasome对前体caspase-1的剪切,是Nlrp3-inflammasome最终发挥病理生理活性的重要“效应器”[11];它的生成使IL-1β、IL-18等炎性介质大量释放,最终导致细胞功能紊乱,造成细胞的损伤,因而阻断活化caspase-1的生成是AE抑制Nlrp3-inflammasome活性的关键标志。本实验证明活化caspase-1的活化程度的减弱与AE剂量呈依赖性关系,这一现象反映了AE可以降低Nlrp3-inflammasome的聚集及活化。为了探究AE抑制Nlrp3-inflammasome活化的机制,我们首先检测了Nlrp3及前体caspase-1的基因与蛋白表达,0.05至0.5μmol·L-1的AE均可以明显的降低Nlrp3的基因和蛋白表达,然而仅在AE最大剂量(0.5 μmol·L-1)时候可以抑制前体caspase-1的基因和蛋白,基于此我们推测AE可能通过抑制核转录水平抑制了Nlrp3-inflammasome相关蛋白的表达,阻断了活化途径。
同时我们为了进一步的说明AE抑制Nlrp3-inflammasome聚集及活化的作用通路,我们初步尝试探究了影响Nlrp3-inflammasome活化的主要应答机制——氧化应激作用。研究指出,抗氧化能力的丧失是导致牙周炎的关键因素,过量生成的ROS对mPDLFs有明显的促炎作用,是mPDLFs发生病理损伤的早期信号,直接导致了后续的牙周组织的病理损伤并导致附着丧失乃至失牙[11-12]。过量产生的ROS可通过活化多种促炎转录因子上调Nlrp3及其下游蛋白的转录水平及蛋白质表达量[13],其中包括NF-κB,这是Nlrp3-inflammasome发挥作用的关键调控因子[10]。在以往的报道中AE具备重要的抗氧化性[4],我们的结果也同样表明P.g-LPS会诱导细胞释放大量的ROS,而AE表现出清除ROS的作用。同时最近一项研究表明,由于活性氧(ROS)过度累积而被切割分离的TXNIP能与Nlrp3形成聚合物,大幅促进了Nlrp3的聚集,最终形成高度活化的Nlrp3-inflammasome六聚体复合物,具有强大的生理病理活性[14-15]。进而我们继续检测与ROS密切相关的TXNIP表达,其在AE最大剂量(0.5 μmol·L-1)下出现明显降低的结果,这与AE抑制Nlrp3-inflammasome活化结果遥相呼应。所以我们认为AE可能通过抑制ROS的产生调节TXNIP在细胞内的释放从而抑制Nlrp3-inflammasome聚集活化起到防治牙周膜成纤维细胞慢性损伤的作用。
综上所述,我们认为AE可以减少Nlrp3、前体caspase-1及活化caspase-1的生成而阻断Nlrp3-inflammasome活化的通路,其是通过抑制ROS-TXNIP介导的Nlrp3-inflammasome的聚集过程实现的。通过此通路共同抑制了P.g-LPS诱导的牙周膜成纤维细胞Nlrp3-inflammasome活化是AE表现出抗早期炎症的重要机制之一。因此,本研究证明AE在辅助治疗牙周炎方面有极大的潜能,并为治疗慢性牙周炎提供了新的作用靶点和药物选择方向。
( 致谢: 本实验在广州中医药大学中药学院中药心血管药理实验室完成,非常感谢本课题组全体老师和同学对本实验的指导和帮助。)
| [1] | Koka S, Reinhardt R A. Periodontal pathogen-related stimulation indicates unique phenotype of primary cultured human fibroblasts from gingiva and periodontal ligament: implications for oral health disease[J]. J Prosthet Dent, 1997, 77(2): 91-196. |
| [2] | Gölz L, Memmert S, Rath-Deschner B, et al. LPS from P. gingivalis and hypoxia increases oxidative stress in periodontal ligament fibroblasts and contributes to periodontitis[J]. Mediators Inflamm, 2014, 2014: 986264. |
| [3] | 杨明华, 李升, 肖健平, 林楠. 中药大黄素治疗中重度牙周炎的临床观察[J]. 口腔医学研究, 2008, 24(3): 305-7. Yang M H, Li S, Xiao J P, Lin N. Clinical observation of emodin on the treatment of moderate to severe periodontitis.[J]. J Oral Sci Res, 2008, 24(3): 305-7. |
| [4] | Tao L, Xie J, Wang Y, et al. Protective effects of aloe-emodin on scopolamine-induced memory impairment in mice and H2O2-induced cytotoxicity in PC12 cells[J]. Bioorg Med Chem Lett, 2014, 24(23): 5385-9. doi:10.1016/j.bmcl.2014.10.049 |
| [5] | 周星, 叶丽风, 吴艳娇, 等. Nlrp3炎症小体与心血管疾病的研究进展[J]. 转化医学电子杂志, 2017, 4(10): 81-7. Zhou X, Ye L F, Wu Y J, et al. Research progress of association between Nlrp3inflammasome activation and cardiovascular disease[J]. E-J Translat Med, 2017, 4(10): 81-7. doi:10.3969/j.issn.2095-6894.2017.10.019 |
| [6] | Shibata K. Historical aspects of studies on roles of the inflammasome in the pathogenesis of periodontal diseases[J]. Mol Oral Microbiol, 2018, 33(3): 203-11. doi:10.1111/omi.2018.33.issue-3 |
| [7] | Schroder K, Tschopp J. The inflammasomes[J]. Cell, 2010, 140(6): 821-32. doi:10.1016/j.cell.2010.01.040 |
| [8] | Misawa T, Takahama M, Kozaki T, et al. Microtubule-driven spatial arrangement of mitochondria promotes activation of the NLRP3 inflammasome[J]. Nat. Immunol, 2013, 14(5): 454-61. doi:10.1038/ni.2550 |
| [9] | Li X, Zhang Y, Xia M, et al. Activation of Nlrp3 inflammasomes enhances macrophage lipid-deposition and migration: implication of a novel role of inflammasome in atherogenesis[J]. PLoS ONE, 2014, 9(1): e87552. doi:10.1371/journal.pone.0087552 |
| [10] | Abais J M, Xia M, Zhang Y, et al. Redox regulation of NLRP3 inflammasomes: ROS as trigger or effector[J]. Antioxid Redox Signal, 2015, 22(13): 1111-29. doi:10.1089/ars.2014.5994 |
| [11] | Tschopp J, Schroder K. NLRP3 inflammasome activation: The convergence of multiple signalling pathways on ROS production?[J]. Nat Rev Immunol, 2010, 10(3): 210-5. doi:10.1038/nri2725 |
| [12] | Liu C, Mo L, Niu Y, et al. The Role of Reactive Oxygen Species and Autophagy in Periodontitis and Their Potential Linkage[J]. Front Physiol, 2017, 8: 439. doi:10.3389/fphys.2017.00439 |
| [13] | Luo B, Li B, Wang W, et al. NLRP3 gene silencing ameliorates diabetic cardiomyopathy in a type 2 diabetes rat model[J]. PLoS ONE, 2014, 9(8): e104771. doi:10.1371/journal.pone.0104771 |
| [14] | Zhou R, Tardivel A, Thorens B, et al. Thioredoxin-interacting protein links oxidative stress to inflammasome activation[J]. Nat. Immunol, 2010, 11(2): 136-41. doi:10.1038/ni.1831 |
| [15] | 莫与琳, 杨亚军, 崔燎. TXNIP介导的氧化应激在疾病中的作用机制[J]. 中国药理学通报, 2018, 34(01): 16-9. Mo Y L, Yang Y J, Cui L. Action and mechanism of oxidative stress mediated by TXNIP in diseases[J]. Chin Pharmacol Bull, 2018, 34(01): 16-9. doi:10.3969/j.issn.1001-1978.2018.01.005 |