

2. 南京中医药大学 江苏省方剂高技术研究重点实验室,江苏省中药资源产业化过程协同创新中心,江苏 南京 210023
2. Jiangsu Key Lab for High Technology Research of TCM Formulae and Jiangsu Collaborative Innovation Center of Chinese Medicinal Resources Industrialization, Nanjing University of Chinese Medicine, Nanjing 210023, China
抑郁症是区别于简单情绪障碍的一种持续时间长且反复发作,以情绪低落、悲伤、失望、兴趣下降为主要特征的慢性精神疾病。目前被广泛用于抑郁症治疗的抗抑郁药,如5-羟色胺重摄取抑制剂(selective serotonin reuptake inhibitor,SSRI)普遍存在起效缓慢、副作用大、易复发等缺陷,使得其临床用药受到了极大的限制。为了尽可能减少类似抗抑郁药副作用的发生,从天然产物的有效成分、药用植物以及中药复方中获取抗抑郁的有效药物已逐渐成为关注的热点[1]。
神经营养因子是神经网络可塑性和神经网络信息的重要调节者,研究已经证实神经营养因子在抑郁及抑郁的治疗中发挥着重要的作用[2]。其中脑源性神经营养因子(brain derived neurotrophic factor,BDNF)广泛分布于大脑中,特别是海马齿状回和皮层中。文献报道,预先培养的BDNF能够明显抑制由谷氨酸盐引起的兴奋性毒性对海马神经的损害[3],其受体原肌球蛋白受体激酶B(tropomyosin receptor kinase B,TrkB)能够引发多重信号转导反应,这对于细胞的存活至关重要[4]。同时近来研究证实,炎症在抑郁疾病中的重要调节作用。并且抑郁也能被许多的炎症刺激所诱发,使用抗炎药物之后,抑郁症状能有所改善[5]。因此,我们推测BDNF/TrkB信号通路以及炎症相关的调节物质与抑郁行为相关。
越鞠丸始载于著名医家朱震亨的《丹溪心法》中,其组成为川芎、苍术、香附、神曲、栀子各等分,以行气开郁、疏肝理脾而治气郁为主要作用。课题组前期已通过药理实验证实越鞠丸对抑郁样小鼠具有缓解作用,并确认其具有潜在的快速抗抑郁效力,且与BDNF、TrkB蛋白的表达上调有关[6]。同时,由于药对是方剂配伍的一种特殊形式,是方剂的最小配伍单位。因此,本研究以药对研究为切入点,对中药复方越鞠丸抗抑郁作用配伍规律进行研究,并探讨其作用机制,以期为更深入的复方药物配伍作用规律的研究奠定基础。
1 材料 1.1 实验动物昆明种♀小鼠264只,体质量20~25 g,由常州卡文斯实验动物公司提供,动物合格证编号:SCXK(苏)2016-0010。动物房室温为25℃,昼夜交替12 h,湿度46%,动物正常饮食进水。
1.2 药物与试剂越鞠丸全方五味药依据药物处方筛选实验进行等比例配伍,均购于南京中医药大学国医堂门诊。蔗糖购于国药试剂化学有限公司(批号:20170406);盐酸氯胺酮(ketamine,Ket)由福建古田制药厂提供(批号:20170301),并用0.9%的生理盐水配成30 g·L-1的药液;RIPA裂解液(货号:0013B)购于Beyotime公司;蛋白酶抑制剂Cocktail(货号:5871S)购于Cell Signaling Technology公司;IL-6[货号:KGEHC007(H)-1]和TNF-α(货号:KGEMC123-1)ELISA试剂盒购于江苏凯基生物技术公司;抗BDNF抗体(sc-546)购自Santa Cruz公司;一抗TrkB(货号:4603S)、GAPDH(货号:5174S)、p-NF-κB p65(货号:3033S)、NF-κB p65(货号:4764S)、p-IκBα(货号:5209S)、IκBα(货号:4812S)均购于Cell Signaling Technology公司。
1.3 仪器旋转蒸发仪(河南巩义矛华仪器设备有限公司),凝胶成像及分析系统(Tannon公司),小鼠悬尾强迫游泳实验视频分析系统(上海吉量软件公司),Nanodrop2000超微量分光光度计(Thermo公司),蛋白电泳及转膜系统(Bio-Rad公司)。
2 方法 2.1 小鼠急性给药筛选抗抑郁关键药对 2.1.1 分组与给药以越鞠丸原方配比为基础,将180只小鼠分3批,依次进行处方筛选实验。将筛选组别定为(1)全方;(2)栀子、香附、苍术、川芎;(3)栀子、川芎、香附;(4)栀子、香附、苍术;(5)栀子、川芎、苍术;(6)香附、川芎、苍术;(7)栀子、苍术;(8)栀子、川芎;(9)苍术、川芎;(10)川芎、香附;(11)栀子、香附。越鞠丸及各给药组醇提物的制备及给药剂量依据前期课题组已发表文献[7],各单味药剂量均为2.7 g·kg-1。因神曲乃入脾胃,助消化之品,考虑其不应是主治抑郁症之药。选择小鼠悬尾实验作为评价方法。设计如下给药方案:第1批:取48只小鼠,分为空白对照组、(1)组(13.5 g·kg-1)、(2)组(10.8 g·kg-1)、阳性药氯胺酮组(Ket 30 mg·kg-1),每组小鼠12只,灌胃24 h后进行小鼠悬尾实验,实验结果作为第2批药物设计分组依据。第2批:取72只小鼠,分为空白对照组、(3)组(8.1 g·kg-1)、(4)组(8.1 g·kg-1)、(5)组(8.1 g·kg-1)、(6)组(8.1 g·kg-1)、阳性药氯胺酮组(Ket 30 mg·kg-1),每组小鼠12只,灌胃24 h后进行小鼠悬尾实验,实验结果作为第3批药物设计分组依据。第3批:取84只小鼠,分为空白对照组、(7)组(5.4 g·kg-1)、(8)组(5.4 g·kg-1)、(9)组(5.4 g·kg-1)、(10)组(5.4 g·kg-1)、(11)组(5.4 g·kg-1)、阳性药氯胺酮组(Ket 30 mg·kg-1),每组小鼠12只。灌胃24 h后进行小鼠悬尾实验。
2.1.2 小鼠悬尾实验小鼠尾端用胶布固定,放入通用隔音行为箱内,并倒挂于悬挂钩上,保持其尾尖距胶布大约1 cm。小鼠为了摆脱不正常的体位而挣扎活动,活动一段时间即出现间断性不动,表现出绝望状态。记录小鼠6 min内的活动情况,分析后4 min内小鼠的不动时间作为绝望时间。
2.2 栀子-川芎药对对慢性应激性抑郁症小鼠行为学的影响及作用机制 2.2.1 模型建立60只昆明种小鼠,适应3 d,以有效药对筛选实验的结果为基础,将其随机分为对照组(CG)、模型组(MG)、氯胺酮组(Ket 30 mg·kg-1)、慢性不可预知性刺激+给药组(5.4 g·kg-1,MH)、慢性不可预知性刺激+给药组(2.7 g·kg-1,MM)、慢性不可预知性刺激+给药组(1.35 g·kg-1,ML)6组,每组10只。GC组小鼠5只/笼,MG组及给药组小鼠均单笼饲养。建立慢性不可预知应激性抑郁症小鼠模型,刺激方式包括禁食禁水各24 h、4℃冰水中游泳5 min、夹尾l min、振荡5 min(160 Hz)、40℃环境5 min、昼夜颠倒24 h,共7种刺激,保证小鼠每日作用1种刺激,每种刺激累计出现2~3次,同种刺激随机出现,使动物无法预料何种刺激会发生。造模3周后,各给药组单次给药,CG组和MG组每天给予生理盐水,于给药24 h后进行糖水消耗、悬尾实验以及强迫游泳实验。
2.2.2 行为学测试 2.2.2.1 糖水消耗实验依据文献[7],在给药24 h后进行测试,预先禁食禁水24 h,后将所有小鼠单笼放置,同时给予小鼠1%的蔗糖水溶液与纯水各1瓶,实验前称取带水瓶重,放置2 h后,再次称量带水瓶重,同时计算蔗糖水和纯水消耗量,得出糖水偏好率:糖水偏好率/%=糖水消耗/总液体消耗×100%。
2.2.2.2 小鼠强迫游泳实验依据文献[6],在给药24 h后进行实验,在实验前预先调整实验室温度至26℃,将3 L水倒入体积约5 L(直径18 cm×高25 cm)实验用玻璃瓶中,水温调节为24~26℃,玻璃烧瓶放置于隔音行为箱中。之后将小鼠依次放入玻璃烧杯内,观察记录6 min内小鼠活动情况,并分析后4 min内小鼠游泳的不动时间作为绝望时间。
2.2.2.3 小鼠悬尾实验依据文献[6],在给药24 h后进行实验,方法同“2.1.2”。
2.2.3 细胞因子IL-6、TNF-α水平的测定行为学实验结束后,小鼠经断头取脑组织,于冰上分离海马组织置于EP管中,-80℃冰箱保存。依据ELISA试剂盒说明书,检测海马组织匀浆液中细胞因子IL-6、TNF-α水平。
2.2.4 Western blot法检测小鼠海马组织中相关蛋白表达行为学实验结束之后,小鼠断头取脑中海马体,并提取小鼠海马蛋白,测定蛋白样品浓度。依据BDNF、p-NF-κB p65、NF-κB p65、p-IκBα、IκBα、TrkB蛋白的分子量,选择适当的聚丙烯酰胺凝胶(15%、10%、10%、12%、12%、6%的胶)电泳分离蛋白质,之后于300 mA,1 h恒流条件下冰浴转膜,将蛋白转至PVDF膜上。并将裁剪好的PVDF膜放入BSA封闭液中室温摇床1 h,然后将膜分别放入预先加有一抗的抗体盒中,4℃冰箱摇床过夜。次日用TBST缓冲溶液洗膜3次,将PVDF膜分别放入加有对应二抗的抗体盒中,摇床上室温孵育1 h,ECL显影。采集并分析目的蛋白条带灰度值。
2.3 数据统计与分析运用SPSS 17.0软件对多组间实验数据进行单因素方差分析,实验结果以x±s表示。
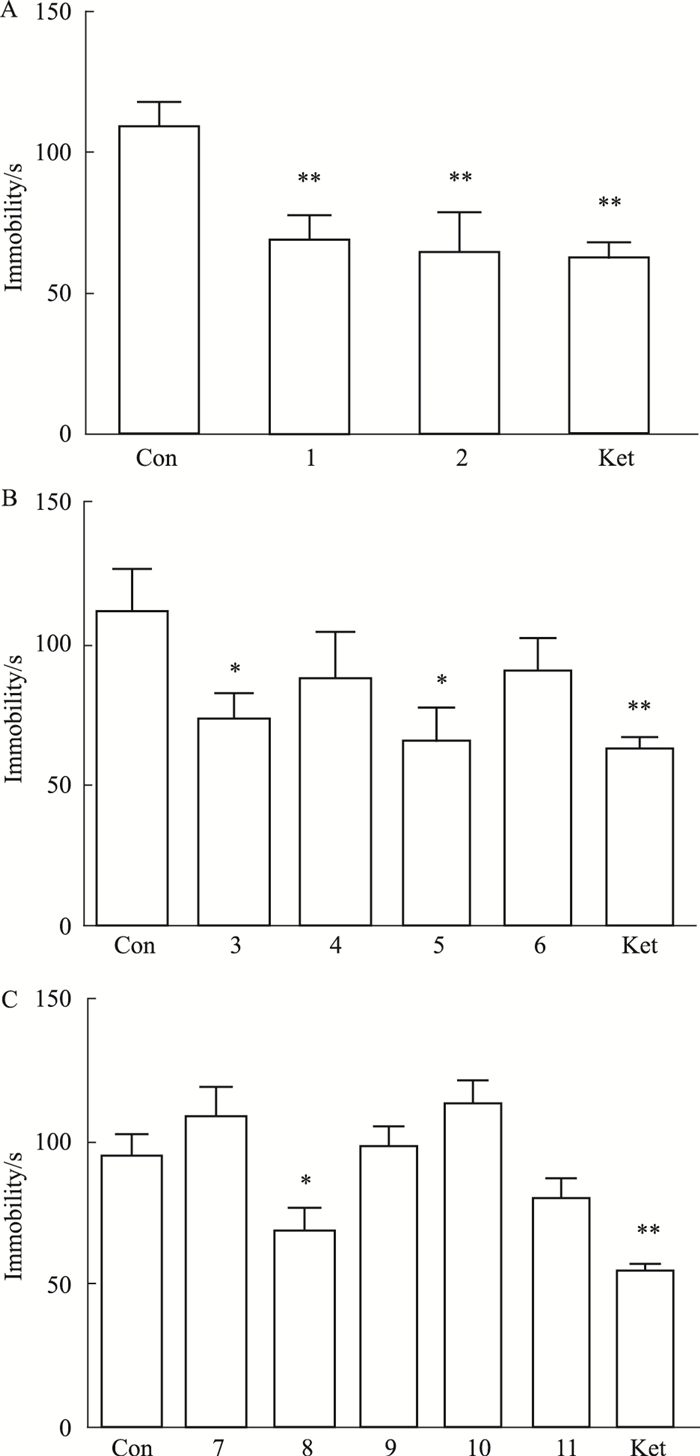
3 结果 3.1 小鼠急性给药筛选抗抑郁关键药对 3.1.1 给予药物24 h后对第1批小鼠悬尾实验的影响如Fig 1A所示,给药24 h后,与空白组相比,(1)、(2)组小鼠及Ket组在悬尾实验中不动时间明显降低(P < 0.01)。
|
| Fig 1 Immobility time of mice in tail suspension test (x±s, n=12) A: Immobility time of the first cohort of mice in tail suspension test at 24 h; B:Immobility time of the second cohort of mice in tail suspension test at 24 h; C: Immobility time of the third cohort of mice in tail suspension test at 24 h. 1: QuanFang; 2:XiangFu, ChuanXiong, ZhiZi, CangZhu; 3:ChuanXiong, XiangFu, ZhiZi; 4:CangZhu, XiangFu, Zhizi; 5: CangZhu, ChuanXiong, ZhiZi; 6:ChuanXiong, XiangFu, CangZhu; 7: ZhiZi, CangZhu; 8: ZhiZi, ChuanXiong; 9:CangZhu, ChuanXiong; 10: ChuanXiong, XiangFu; 11: ZhiZi, XiangFu. *P < 0.05, **P < 0.01 vs control. |
如Fig 1B所示,给药24 h后,与空白组相比,(3)、(5)组给药小鼠在悬尾实验中不动时间明显降低(P < 0.05),Ket组不动时间明显下降(P < 0.01),其余各组与空白组相比差异无显著性。
3.1.3 给予药物24 h后对第3批小鼠悬尾实验的影响如Fig 1C所示,给药24 h后,与空白组相比,(8)组小鼠在悬尾实验中不动时间明显降低(P < 0.05),Ket组不动时间明显降低(P < 0.01),其余各组与空白组相比差异无显著性。
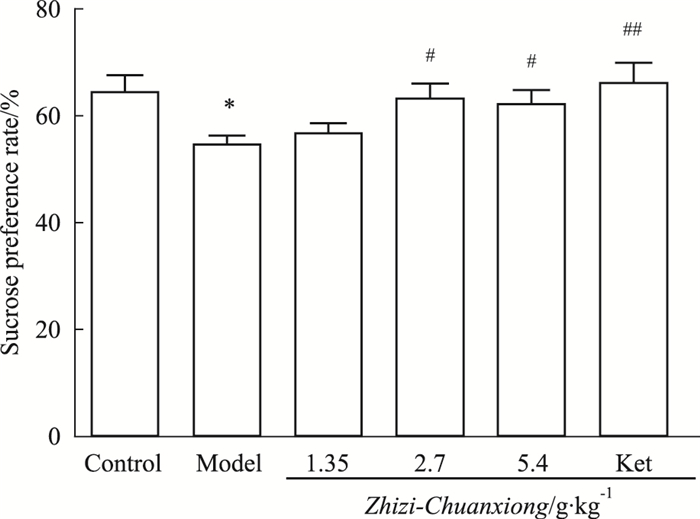
3.2 栀子-川芎药对对慢性应激性抑郁症小鼠行为学的影响及作用机制 3.2.1 动物模型建立情况造模3周及之后给药期间,空白对照组小鼠均饮食正常,其余各组均未出现死亡现象。Fig 2糖水测试结果显示,MG组小鼠糖水消耗量明显低于CG组(P < 0.05),提示成功诱导小鼠产生类似焦虑、兴趣缺失等抑郁样行为。而MM、MH组小鼠糖水消耗量明显高于MG组,提示药物治疗改善了小鼠的抑郁症状(P < 0.05),Ket与MG组相比糖水消耗量明显升高(P < 0.01)。
|
| Fig 2 Effect of CUMS on sucrose preference of mice (x±s, n=10) *P < 0.05 vs CG; #P < 0.05, ##P < 0.01 vs MG |
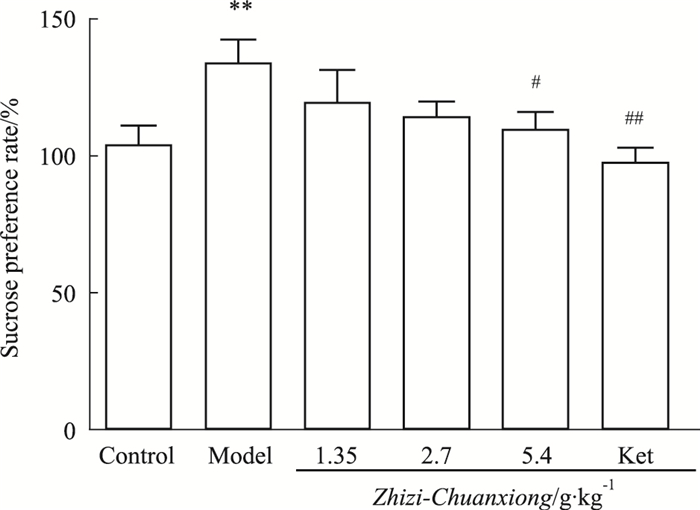
给药24 h后,Fig 3强迫游泳实验结果显示,与空白对照CG组相比,MG组小鼠在强迫游泳中不动时间明显升高(P < 0.01);与MG组相比,给药MH组小鼠不动时间明显下降(P < 0.05),Ket组不动时间明显降低(P < 0.01)。
|
| Fig 3 Immobility time of mice in forced swimming test (x±s, n=10) **P < 0.01 vs CG; #P < 0.05, ##P < 0.01 vs MG |
给药24 h后,Fig 4小鼠悬尾实验结果显示,与空白对照CG组相比,MG组小鼠在悬尾实验中不动时间明显升高(P < 0.01);与MG组相比,给药MM、MH组及Ket组小鼠不动时间明显下降(P < 0.01)。

|
| Fig 4 Immobility time of mice in tail suspension test (x±s, n=10) **P < 0.01 vs CG; ##P < 0.01 vs MG |
小鼠海马体中促炎症因子IL-6和TNF-α的表达情况反映栀子、川芎的抗炎作用。Fig 5结果显示,与空白对照CG组相比,MG组小鼠海马组织中促炎症因子IL-6和TNF-α的水平明显升高(P < 0.01);与MG组相比,给药ML组小鼠海马组织中IL-6水平明显降低(P < 0.05),同样的,给药ML、MM、MH组小鼠海马组织中IL-6和TNF-α的水平明显降低(P < 0.01)。

|
| Fig 5 IL-6 and TNF-α expressions in hippocampus (x±s, n=7) **P < 0.01 vs CG; #P < 0.05, ##P < 0.01 vs MG |
为了进一步揭示栀子-川芎抗抑郁作用的机制,对小鼠海马组织中相关炎症蛋白进行检测。Fig 6结果显示,与空白对照CG组相比,MG组小鼠海马组织中p-NF-κB p65、p-IκBα的表达明显升高(P < 0.01);与MG组相比,给药ML、MM、MH组小鼠海马组织中p-NF-κB p65的表达明显降低(P < 0.05,P < 0.01),给药ML、MH组小鼠海马组织中p-IκBα的表达也明显降低(P < 0.05,P < 0.01)。

|
| Fig 6 NF-κB p65, IκBα and BDNF, TrkB expressions at 24 h (x±s, n=7) **P < 0.01 vs CG, #P < 0.05 vs MG, ##P < 0.01 vs MG |
Fig 6结果显示,与空白对照CG组相比,MG组小鼠海马组织中BDNF、TrkB的表达明显降低(P < 0.01);与MG组相比,给药MM、MH组小鼠海马组织中BDNF的表达明显升高(P < 0.01),给药MH组小鼠海马组织中TrkB的表达也明显升高(P < 0.05)。
4 讨论本研究以中药复方越鞠丸为基础,通过处方筛选结合小鼠悬尾行为绝望测试,得到栀子-川芎药对为其发挥抗抑郁作用的活性基础药对,并通过药效学及分子学实验,进一步对栀子-川芎药对抗抑郁活性的生物学机制进行了研究,为进一步揭示越鞠丸治疗抑郁症的物质基础及生物学机制提供了参考价值。
由于具有预测的高准确性,小鼠悬尾实验普遍被用来作为抑郁评估的行为验证实验,广泛应用于抗抑郁药物的初筛。从以越鞠丸为基础的逐步处方筛选,到栀子-川芎组合能够明显降低小鼠在悬尾实验中的不动时间,表明通过处方筛选实验得到的越鞠丸活性基础药对能够对小鼠抑郁行为起到积极作用。
中医在治疗抑郁症方面有着多年的实践基础,著名医家朱丹溪以内伤情志致郁为基础,倡气、血、湿、痰、热、食“六郁”之说,并拟越鞠丸以“解诸郁”,成为后世主治郁证的著名方剂[8]。近年来,以越鞠丸为基础的抗抑郁研究方兴未艾,蒋麟等[9]以越鞠丸为基础,以动物行为绝望实验为筛选方法,初步证实了栀子-川芎组合的抗抑郁作用;尉小慧等[10]以越鞠丸及各单位药醇提物对小鼠的抗抑郁作用进行研究,发现越鞠丸全方抗抑郁效果明显,而川芎、栀子、香附、苍术具备一定抗抑郁样活性趋势,但只有苍术对小鼠悬尾模型有明显作用,川芎对小鼠强迫游泳模型有明显作用。提示越鞠丸全方抗抑郁作用与香附、苍术、川芎、栀子4味药有关,与神曲无关。此外,本课题组前期研究发现,越鞠丸及单味药栀子具有潜在的快速抗抑郁作用[7],并发现栀子黄素类成分(又称藏红花素类)可能是其抗抑郁药效物质基础之一[11]。本研究进一步显示,栀子为主,川穹为辅,两者相使作用;川穹可以降低栀子的使用剂量,协同产生抗抑郁作用,这种协同作用是药对基本功能的体现。
细胞因子广泛参与于机体的免疫、应激以及炎症的调节之中,是内分泌系统与中枢神经系统之间重要的信号传递因子。其中,转录因子NF-αB家族通过调控包括IL-6、TNF-α等多种炎症基因的表达,调节免疫应答和炎症反应。越来越多研究表明,细胞因子、炎性介质等生物活性分子含量的改变,以及对先天免疫系统和炎症进程持久性的激动与抑郁症的发生、发展关系密切[12]。同时,焦虑、抑郁等负性情绪可引起下丘脑-垂体-肾上腺轴(hypothalamus-pituitary-adrenal axis,HPA)的负反馈失调,继而引起免疫功能的异常。有研究证实,抑郁症的发病进程中存在免疫激活,且抑郁症患者血中炎症细胞因子水平的上升与病情严重程度呈正相关。而IL-6、TNF-α等细胞因子是HPA轴的有效活化因子[13]。因此,我们在实验中观察海马体中IL-6和TNF-α水平的变化。结果表明,模型组小鼠海马体中的两种促炎症因子的水平明显升高,而川芎、栀子组的两种促炎症因子水平明显降低。
BDNF作为神经营养因子家族主要成员,其通过与TrkB的相互作用维持着神经元的存活和功能,其快速表达增加可改善突触可塑性,进而产生快速抗抑郁作用[14]。激活TrkB/BDNF信号通路受体,可引发多重信号级联反应,这对于维持海马体神经元正常的生理功能至关重要[15]。我们目前的工作揭示,栀子、川芎组合可以明显恢复BDNF和TrkB的水平,可能是其改善神经可塑性,产生快速抗抑郁作用的机制之一。
综上,本研究通过对越鞠丸进行处方筛选实验,得到了其发挥抗抑郁作用的川芎-栀子基础药对组合,并通过药效学及分子学实验,对其作用的生物学机制进行了阐释。为抗抑郁药理研究的动物模型提供参考,并为今后对越鞠丸的进一步研究提供了依据。
( 致谢: 本实验于南京中医药大学中医脑病重点实验室完成,对参与实验的老师和同学致以最真挚的谢意!)
| [1] | 王旭东, 乔明琦, 张樟进, 等. 中医药治疗抑郁症的研究进展[J]. 南京中医药大学学报, 2016, 32(1): 93-6. Wang X D, Qiao M Q, Zhang Z J, et al. Progress in the treatment of depression in traditional Chinese medicine[J]. J Nanjing Univ TCM, 2016, 32(1): 93-6. |
| [2] | Garcia L S, Comim C M, Valvassori S S, et al. Ketamine treatment reverses behavioral and physiological alterations induced by chronic mild stress in rats[J]. Prog Neurop Biol Psychiat, 2009, 33(3): 450-5. doi:10.1016/j.pnpbp.2009.01.004 |
| [3] | Almeida R D, Manadas B J, Melo C V, et al. Neuroprotection by BDNF against glutamate-induced apoptotic cell death is mediated by ERK and PI3-kinase pathways[J]. Cell Death Differ, 2005, 12(10): 1329-43. doi:10.1038/sj.cdd.4401662 |
| [4] | Jiang X, Tian F, Mearow K, et al. The excitoprotective effect of N-methyl-D-aspartate receptors is mediated by a brain-derived neurotrophic factor autocrine loop in cultured hippocampal neurons[J]. J Neurochem, 2005, 94(3): 713-22. doi:10.1111/(ISSN)1471-4159 |
| [5] | Köhler O, Benros M E, Nordentoft M, et al. Effect of anti-inflammatory treatment on depression, depressive symptoms, and adverse effects: a systematic review and meta-analysis of randomized clinical trials[J]. Jama Psychiatry, 2014, 71(12): 1381-91. doi:10.1001/jamapsychiatry.2014.1611 |
| [6] | 任荔, 陶伟伟, 薛文达, 等. 越鞠丸石油醚部位潜在的快速抗抑郁作用与BDNF、TrkB蛋白表达的上调相关[J]. 中国药理学通报, 2015, 31(12): 1754-9. Ren L, Tao W W, Xue W D, et al. Potent rapid antidepressant effects of petroleum ether fraction of Yueju pill associated with BDNF and TrkB up-regulation[J]. Chin Pharmacol Bull, 2015, 31(12): 1754-9. doi:10.3969/j.issn.1001-1978.2015.12.025 |
| [7] | Tang J, Xue W, Xia B, et al. Involvement of normalized NMDA receptor and mTOR-related signaling in rapid antidepressant effects of Yueju and ketamine on chronically stressed mice[J]. Sci Rep, 2015, 5(5): 13573. |
| [8] | 朱丹溪. 丹溪心法[M]. 北京: 中国医药科技出版社, 2012: 1-10. Zhu D X. Dan brook heart law[M]. Beijing: China Medical Science Press, 2012: 1-10. |
| [9] | 蒋麟. 以越鞠丸为基础的抗抑郁中药复方药理作用及其机理研究[D]. 成都: 成都中医药大学, 2004. Jiang L. Study on the pharmacological action and mechanism of anti-depressant traditional Chinese medicine based on yueju pill[D]. Chengdu: Chengdu University of TCM, 2004. |
| [10] | 尉小慧, 徐向东, 沈敬山, 等. 越鞠丸及各单味药醇提物对小鼠的抗抑郁作用研究[J]. 中国药房, 2009, 20(3): 166-8. Wei X H, Xu X D, Shen J S, et al. Study on the anti-depressant effect of Yueju pill and mono-flavoured alcohol extract on mice[J]. Chin Pharm, 2009, 20(3): 166-8. |
| [11] | Wu R Y, Tao W W, Zhang H L, et al. Instant and persistent antidepressant response of gardenia yellow pigment is associated with acute protein synthesis and delayed upregulation of BDNF expression in the hippocampus[J]. ACS Chem. Neurosci, 2016, 7(8): 1068-76. doi:10.1021/acschemneuro.6b00011 |
| [12] | Capuron L, Hauser P, Hinzeselch D, et al. Treatment of cytokine-induced depression[J]. Brain Behav Immun, 2002, 16(5): 575-80. doi:10.1016/S0889-1591(02)00007-7 |
| [13] | 李恒芬, 贾福军. 负性生活事件对抑郁症患者血清细胞因子水平的影响[J]. 中国神经精神疾病杂志, 2004, 30(1): 33-5. Li H F, Jia F J. The effect of negative sex life on serum cytokine levels in patients with depression[J]. Chin J Nerv Ment Dis, 2004, 30(1): 33-5. doi:10.3969/j.issn.1002-0152.2004.01.009 |
| [14] | Ma Z, Zang T, Birnbaum S G, et al. TrkB dependent adult hippocampal progenitor differentiation mediates sustained ketamine antidepressant response[J]. Nat Commun, 2017, 8(1): 1668. |
| [15] | Zhang F, Kang Z, Li W, et al. Roles of brain-derived neurotrophic factor/tropomyosin-related kinase B (BDNF/TrkB) signalling in Alzheimer's disease[J]. J Clin Neurosci, 2012, 19(7): 946-9. doi:10.1016/j.jocn.2011.12.022 |

