

2. 沈阳市妇婴医院麻醉科,辽宁 沈阳 110003
2. Shenyang Women's and Children's Hospital, Shenyang 110003, China
脊髓缺血/再灌注损伤(spinal cord ischemia/reperfusion injury, SCIRI)是缺血脊髓组织恢复血液灌注后的二次损伤,是胸腹主动脉瘤手术患者的主要并发症[1]。手术治疗仍是治疗的主要选择,但效果欠佳。microRNA在转录后水平调控基因表达,是目前研究基因治疗和寻找药物靶点的重要工具[2],许多基因表达的改变已经在脊髓二次损伤中扮演重要的角色。七氟烷是广泛应用于临床的吸入麻醉药,已有研究证明,七氟烷预处理通过调控microRNA保护心、肺等器官[3-4]。本课题组在前期大鼠SCIRI的微阵列芯片分析中发现,miR-199a-5p在大鼠SCIRI手术组比假手术组明显降低,七氟烷预处理后miR-199a-5p明显升高。本研究旨在探讨miR-199a-5p在七氟醚预处理大鼠SCIRI中的作用及相关机制。
1 材料与方法 1.1 材料 1.1.1 实验动物SPF级成年健康♂SD大鼠24只,体质量220~280 g,由中国医科大学实验动物中心提供,动物合格证和使用许可证号分别为:SCXK(辽)013-0001、SYXK(辽) 013-0007。动物实验部分已经通过中国医科大学伦理委员会批准。
1.1.2 试剂七氟烷(丸石制药株式会社);伊文思蓝(美国Sigma公司);反转录试剂盒(DBI公司);TRIzol (TaKaRa公司);RNasin(美国Promega公司产品);TUNEL试剂盒(Roche公司);抗caspase-9、Bcl-2、GAPDH抗体(Abcam公司)。
1.1.3 仪器R407小动物呼吸机(深圳市瑞沃德生命科技有限公司);BX-60荧光显微镜(日本Olympus公司);Stratagene Mx3000P Real time PCR仪(美国Agilent公司);DYY-7C电泳仪(北京六一仪器厂)。高速离心机TGL-16G (上海安亭科学仪器厂),水平电泳仪GDS7600(北京东方仪器厂产品),凝胶扫描系统DF-23B(英国UVP公司)。
1.2 动物模型的建立与分组大鼠随机分为3组(n=8):假手术组(Sham组)、模型组(I/R组)、七氟烷+模型组(SEVO+I/R组)。Sham组游离主动脉弓,不夹闭胸主动脉;I/R组单纯建立大鼠缺血/再灌注损伤模型:将100 g·L-1水合氯醛腹腔注射麻醉大鼠(3.5 mL·kg-1),气管切开,气管内插管连呼吸机。深层切口起胸廓顶端,并向左侧第2肋骨胸骨结合部延伸,截断左侧第1、2肋骨,分离主动脉弓,将微血管夹放置在左颈总动脉和左锁骨下动脉之间的主动脉弓上,阻断时间为14 min,移除血管夹,逐层关闭胸腔和皮肤。远端动脉压持续下降至0.665 kPa以下,证明阻断成功。模型制备过程中,以电加热毯保温,维持直肠温度36.5~37.5℃。SEV+I/R组的大鼠先放入自制密闭箱,规格为45 cm×32 cm×23 cm,保留自主呼吸,两端各有1个进气孔及出气孔,底部铺薄层钠石灰,进气端接麻醉机,设定七氟烷吸入浓度为40%,出气端接麻醉气体检测仪,调整挥发罐和新鲜气流量至出气端七氟烷浓度为2.4%,吸入3 h七氟烷[5]。吸毕,行大鼠腹腔内麻醉,气管切开处气管内插管,连接呼吸机,随后开胸手术,动脉夹夹闭主动脉弓14 min。各组于术后48 h进行Basso Beattie Bresnahan(BBB)评分后,断头取髓(L4~6)。
1.3 大鼠双后肢运动功能评价采用Basso Beattie Bresnahan(BBB)评分标准,对各组大鼠在SCIRI 48 h时,进行后肢运动神经功能评分并记录。
1.4 TUNEL检测脊髓组织细胞凋亡程度选择厚度为4 μm的石蜡切片进行脱蜡,逐级乙醇水化,PBS漂洗,蛋白酶K储存液覆盖组织60 min,缓冲液洗3次,向组织样品标本上滴加20 mg·L-1不含DNase的蛋白酶K,置于20~37℃环境下反应15~30 min。缓冲液洗3次,添加TUNEL反应混合液,置于湿盒内,37℃恒温孵育2 h,PBS漂洗3次后,加内源酶阻断剂,PBS洗3次,切片甩干,加适量converter-POD,覆盖组织,置于湿盒内,37℃孵育30 min,PBS洗3次。DAB显色液显色10 min,流水冲洗后常规脱水,中性树胶封片。显微镜下观察,细胞核呈现棕黄色或棕褐色为凋亡阳性细胞,统计并计算凋亡细胞率。光镜下观察凋亡细胞,每组于凋亡细胞分布区域随机选24个高倍视野(×400),每组8只大鼠各取1张切片,每张切片取3个视野,计算凋亡细胞数。
1.5 EB测定血-脊髓屏障(blood-spinal cord barrier, BSCB)完整性脊髓缺血/再灌注损伤48 h,大鼠尾部静脉注射2% EB,1 h后处死大鼠,剖胸后,由右心室匀速注入生理盐水冲洗血管内染料,取出L4~6脊髓,置于4%多聚甲醛,沉糖,在冰冻切片机上-20℃连续切片(10 μm),置于荧光显微镜红色激光下观察。依照荧光光斑的大小、疏密、强弱来评价脊髓组织中EB外渗量。
1.6 Real-time qPCR检测脊髓缺血/再灌注损伤48 h后,各组取适量L4~6段脊髓组织,按照TRIzol操作说明书,提取RNA。以1 μg总RNA为模板,按照Bestar qPCR RT Kit说明书配制逆转录反应体系,总体系为20 μL,合成cDNA第一链。按照DBI Bestar SYBRGreen qPCR masterMix反应试剂盒的产品说明进行反应。荧光定量PCR仪进行荧光定量PCR实验。miRNA选用U6作为内参基因。所使用引物序列如下: miRNA-199a-5p上游引物5′-CTCAACTGGTGTCGTGGAGTCGGCAATTCAGTTGAG GAACAGGTA-3′,下游引物5′-ACACTCCAGCTGG GCCCAGTGTTCAGACTACC-3′;U6上游引物5′-CTCGCTTCGGCAGCACA-3',下游引物5′-AACGCTTCACGAATTTGCGT-3′。
1.7 Western blot脊髓缺血/再灌注损伤后48 h,取L4~6段脊髓组织,迅速放入液氮后,-80℃冷冻保存。取40 mg脊髓组织剪碎后,加入0.5 mL裂解液,匀浆,4℃、14 000 r·min-1离心15 min,取上清为总蛋白液。BCA法蛋白电量,SDS聚丙烯酰胺胶电泳,加入封闭液,室温封闭2 h,加入一抗caspase-9(1 :4 000)、Bcl-2(1 :1 000),4℃孵育过夜。TBST漂洗3次,每次10 min,加入HRP标记的二抗,室温孵育2 h,TBST洗涤,化学发光,显影,定影,采用Image-Pro Plus 6.0凝胶图像处理系统分析条带光密度值。
1.8 统计学处理采用SPSS 17.0统计学软件进行分析,数据以x±s表示,组间比较采用单因素方差分析ANOVA(LSD test)。
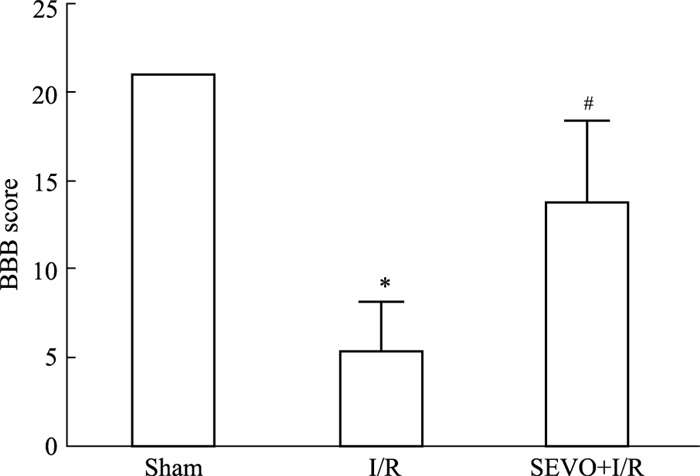
2 结果 2.1 大鼠神经运动功能变化如Fig 1所示,与Sham组比较,I/R组BBB评分明显降低(P < 0.05);与I/R组比较,SEVO+I/R组BBB评分明显增高(P < 0.05)。
|
| Fig 1 BBB score at 48 h after SCIRI (x±s, n=8) *P < 0.05 vs sham group; #P < 0.05 vs I/R group |
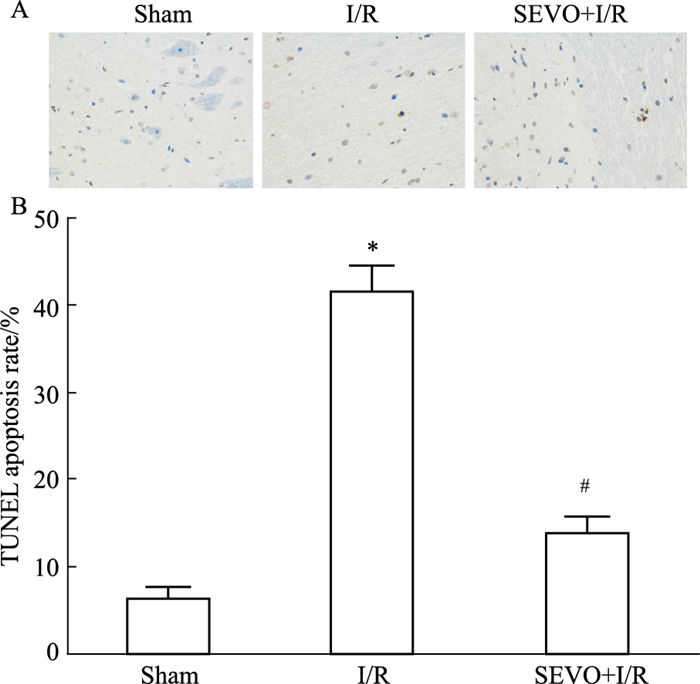
Fig 2的TUNEL染色结果显示,脊髓缺血/再灌注后,神经元胞核较大,主要分布于前角和中间带,部分细胞可见核固缩,深染,位于细胞的一侧;七氟烷预处理组凋亡神经元数目明显减少。用Sham组、I/R组、SEVO+I/R组凋亡细胞核占正常细胞核的百分比,评估脊髓细胞的凋亡率。结果显示,与Sham组相比,I/R组的凋亡率明显增加,而SEVO+I/R组凋亡率降低(P < 0.05),表明七氟烷预处理能减少因SCIRI引起的细胞凋亡。
|
| Fig 2 Apoptosis at 48 h after SCIRI groups by TUNEL A: Apoptotic cells at 48 h after SCIRI groups by TUNEL; B: The percentage of TUNEL apoptotic cells at 48 h after SCIRI (x±s, n=8). *P < 0.05 vs sham group; #P < 0.05 vs I/R group. |
SCIRI后,BSCB破坏,EB外渗增加,通透性增加。造模后48 h,在荧光显微镜下,Sham组脊髓组织内几乎均未见红色荧光,I/R组48 h时脊髓组织中红色荧光明显增多;与I/R组相比,SEVO+I/R组红色荧光明显减弱(Fig 3)。

|
| Fig 3 BSCB integrity at 48 h after SCIRI in three groups by EB extravasation fluorescence |
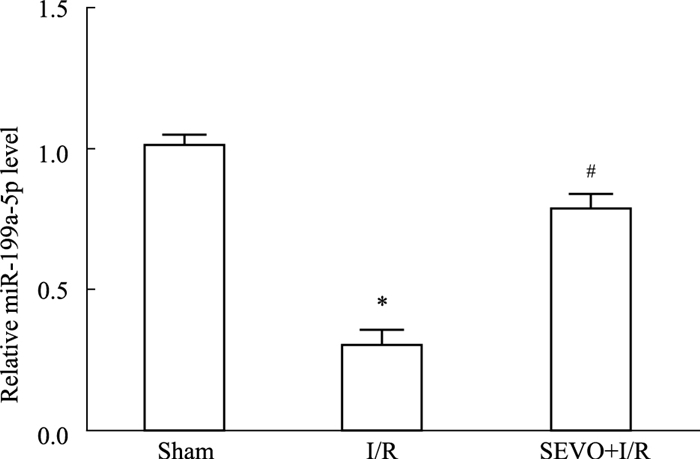
如Fig 4所示,与Sham组相比,I/R组miR-199a-5p表达明显降低(P < 0.05);与I/R组相比,SEVO+I/R组miR-199a-5p表达明显增高(P < 0.05)。
|
| Fig 4 miR-199-5p expression at 48 h after SCIRI (x±s, n=8) *P < 0.05 vs sham group; #P < 0.05 vs I/R group |
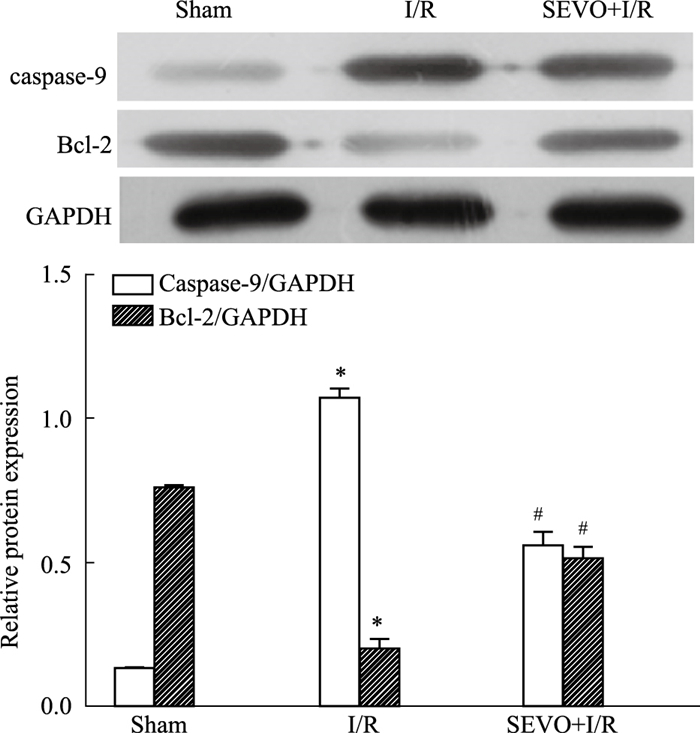
如Fig 5所示,与Sham组相比,I/R组caspase-9表达明显增高,Bcl-2表达明显降低(P < 0.05);与I/R组相比,SEVO+I/R组caspase-9表达明显减少,Bcl-2表达明显增加(P < 0.05)。
|
| Fig 5 Expression of caspase-9 and Bcl-2 at 48 h after SCIRI (x±s, n=8) *P < 0.05 vs sham group; #P < 0.05 vs S group |
microRNA(miRNA)是由18~24个核苷酸分子组成的短链非编码RNA分子,miRNA是一类具有强大功能的代谢调节分子,可以特异性沉默mRNA,在转录后水平调控基因的表达[6]。miR-199a-5p在许多组织里都有表达,脊髓表达丰富[7]。目前研究表明,七氟烷通过调控miR-200c,保护肝缺血/再灌注损伤[8],通过减少miR-15b表达,发挥抗凋亡作用,对脑缺血有保护作用[9]。在脑缺血/再灌注损伤模型中,七氟烷能够减少神经细胞细胞凋亡,减轻脑水肿,缩小局灶性脑梗死体积,进而改善远期神经功能[10]。在本实验中,七氟烷对SCIRI有很好的保护作用,这与既往七氟烷对SCIRI研究结果一致。以往研究七氟烷保护SCIRI机制时,大多集中在氧化应激、炎症反应、离子环境改变等,但这些都是研究信号通路的中下游途径。本研究以miRNA为出发点,从分子生物学角度,对七氟烷预处理作用于大鼠SCIRI的保护机制进行研究,发现大鼠吸入2.4%七氟烷预处理3 h,能够增加miR-199a-5p表达,减少脊髓组织细胞凋亡率,减少血-脊髓屏障通透性,对大鼠SCIRI发挥保护作用。说明七氟烷通过上调miR-199a-5p,保护SCIRI,与前期微阵列芯片分析结果一致。
一般认为BSCB破坏是SCIRI中最直接的病理改变[11]。正常情况下,EB不能通过BSCB,只有屏障结构破坏的情况下,才发生渗漏。本研究发现,脊髓缺血/再灌注损伤后,miR-199a-5p表达下调,BSCB破坏;七氟烷预处理后,miR-199a-5p表达上调,明显降低了EB荧光外渗程度,说明BSCB破坏减轻,对脊髓有保护作用。血-脊屏障与血脑屏障相似,通过防止有害物质侵入,减少脊髓微环境波动,维持神经系统内环境相对稳定。七氟烷可以通过维持BSCB的完整性,减轻大鼠SCIRI[12]。最近研究发现,在肠癌发展过程中,过度表达miR-199a-5p可以减少盘状结构域受体1(discoidin domain receptor 1, DDR1)、基质金属蛋白酶2(matrix matalloproteinases 2, MMP-2)的表达[13]。DDR1主要功能是调控胶原的合成及降解,与血脑屏障密切相关,而MMP-2增加血脊屏障通透性,DDR1、MMP-2的增加,破坏BBB和BSCB[14-15],miR-199a-5p可以抑制DDR1、MMP-2的表达。我们推测,七氟烷预处理通过上调miR-199a-5p保护BBSB,减轻SCIRI,这与本实验结果一致。本实验结果显示,缺血/再灌注前给予2.4%七氟烷预处理3 h,可以提高动物后肢运动功能的评分,同时提高了Bcl-2蛋白表达,降低caspase-9的表达,减少脊髓细胞凋亡,表明七氟烷预处理通过miR-199a-5p调控下游凋亡蛋白,保护SCIRI。
综上所述,七氟烷通过上调miR-199a-5p,减轻血-脊屏障的破坏,减少细胞凋亡,保护脊髓缺血/再灌注损伤。但miR-199a-5p作用于哪个靶基因,通过哪条凋亡通路保护SCIRI,仍需我们进一步研究。
( 致谢: 本实验在中国医科大学附属第一医院实验中心、麻醉科实验室完成,在此对以上实验室和实验过程中给予指导和帮助的老师表示感谢! )
| [1] | Katsargyris A, Oikonomou K, Kouvelos G, et al. Spinal cord ischemia after endovascular repair of thoracoabdominal aortic aneurysms with fenestrated and branched stent grafts[J]. Vasc Surg, 2015, 62(6): 1450-5. doi:10.1016/j.jvs.2015.07.066 |
| [2] | 方波, 张颖, 马虹. miR-122a对大鼠脊髓缺血/再灌注损伤后血-脊髓屏障的影响[J]. 中国药理学通报, 2017, 33(5): 703-6. Fang B, Zhang Y, Ma H. Effects of mir-122a on blood-spinal cord barrier after spinal cord ischemia/reperfusion injury in rats[J]. Chin Pharmacol Bull, 2017, 33(5): 703-6. doi:10.3969/j.issn.1001-1978.2017.05.022 |
| [3] | Xie X J, Fan D M, Xi K, et al. Suppression of microRNA-135b-5p protects against myocardial ischemia/reperfusion injury by activating JAK2/STAT3 signaling pathway in mice during sevoflurane anesthesia[J]. Biosci Rep, 2017, 37(3): pii: BSR20170186. doi:10.1042/BSR20170186 |
| [4] | Zhao X, Wang X, Wang F, et al. Poly r(C) binding protein 1-mediated regulation of microRNA expression underlies post-sevoflurane amelioration of acute lung injury in rats[J]. J Cell Physiol, 2018, 233(4): 3048-54. doi:10.1002/jcp.v233.4 |
| [5] | Takeuchi J, Sakamoto A, Takizawa T. Sevoflurane anesthesia persistently downregulates muscle-specific microRNAs in rat plasma[J]. Int J Mol Med, 2014, 34(1): 291-8. doi:10.3892/ijmm.2014.1739 |
| [6] | Ji H P, Xiong Y, Song W T, et al. MicroRNA-28 potentially regulates the photoreceptor lineage commitment of Müller glia-derived progenitors[J]. Sci Rep, 2017, 7: 11374. doi:10.1038/s41598-017-11112-4 |
| [7] | Wang Y, Luo J, Wang X, et al. MicroRNA-199a-5p induced autophagy and inhibits the pathogenesis of ankylosing spondylitis by modulating the mTOR signaling via directly targeting Ras homolog enriched in brain(Rheb)[J]. Cell Physiol Biochem, 2017, 42(6): 2481-91. doi:10.1159/000480211 |
| [8] | Wu Y, Gu C, Huang X. Sevoflurane protects against hepatic ischemia/reperfusion injury by modulating microRNA-200c regulation in mice[J]. Biomed Pharmacother, 2016, 84: 1126-36. doi:10.1016/j.biopha.2016.10.024 |
| [9] | Shi H, Sun B L, Zhang J, et al. miR-15b suppression of Bcl-2 contributes to cerebral ischemic injury and is reversed by sevoflurane preconditioning[J]. CNS Neurol Disord Drug Targets, 2013, 12(3): 381-91. doi:10.2174/1871527311312030011 |
| [10] | Wang J K, Wu H F, Zhou H, et al. Postconditioning with sevoflurane protects against focal cerebral ischemia and reperfusion injury involving mitochondrial ATP-dependent potassium channel and mitochondrial permeability transition pore[J]. Neurol Res, 2015, 37(1): 77-83. doi:10.1179/1743132814Y.0000000410 |
| [11] | Fang B, Li X Q, Bi B, et al. Dexmedetomidine attenuates blood-spinal cord barrier disruption induced by spinal cord ischemia reperfusion injury in rats[J]. Cell Physiol Biochem, 2015, 36(1): 373-83. doi:10.1159/000430107 |
| [12] | Li X Q, Lv H W, Tan W F, et al. Role of the TLR4 pathway in blood-spinal cord barrier dysfunction during the bimodal stage after ischemia/reperfusion injury in rats[J]. J Neuroinflammation, 2014, 11: 62. doi:10.1186/1742-2094-11-62 |
| [13] | Hu Y, Liu J, Jiang B, et al. MiR-199a-5p loss up-regulated DDR1 aggravated colorectal cancer by activating epithelial-to-mesenchymal transition related signaling[J]. Dig Dis Sci, 2014, 59(9): 2163-72. doi:10.1007/s10620-014-3136-0 |
| [14] | Zhu M, Xing D, Lu Z, et al. DDR1 may play a key role in destruction of the blood-brain barrier after cerebral ischemia-reperfusion[J]. Neurosci Res, 2015, 96: 14-9. doi:10.1016/j.neures.2015.01.004 |
| [15] | Lee J Y, Kim H S, Choi H Y, et al. Fluoxetine inhibits matrix metalloprotease activation and prevents disruption of blood-spinal cord barrier after spinal cord injury[J]. Brain, 2012, 135: 2375-89. doi:10.1093/brain/aws171 |

