

治疗类风湿关节炎(rheumatoid arthritis, RA)药物主要包括疾病调修抗风湿药物(disease-modifying antirheumatic drugs, DMARDs)、非甾体抗炎药物(nonsteroidal anti-inflammatory drugs, NSAIDs)、生物制剂等。DMARDs是阻止RA病程和预防并发症的一线药物,NSAIDs能够较好控制RA症状,生物制剂治疗RA显示远期疗效和潜在前景,但是这些药物疗效和不良反应在RA患者中存在个体差异[1]。编码药物代谢酶、药物转运体和药物靶点的基因存在多态性,而影响药物代谢动力学和药效学,是引起个体间药物疗效和不良反应差异的重要机制[2]。本文综述了基因多态性对治疗RA药物疗效和不良反应的影响。
1 基因多态性对DMARDs疗效和不良反应的影响DMARDs被广泛用于RA临床治疗,然而40%~60%的RA患者对DMARDs应答没有达到满意效果,并且约15%~30%患者伴有不良反应[1]。药物转运体和代谢酶等基因多态性影响DMARDs的疗效和毒副作用。
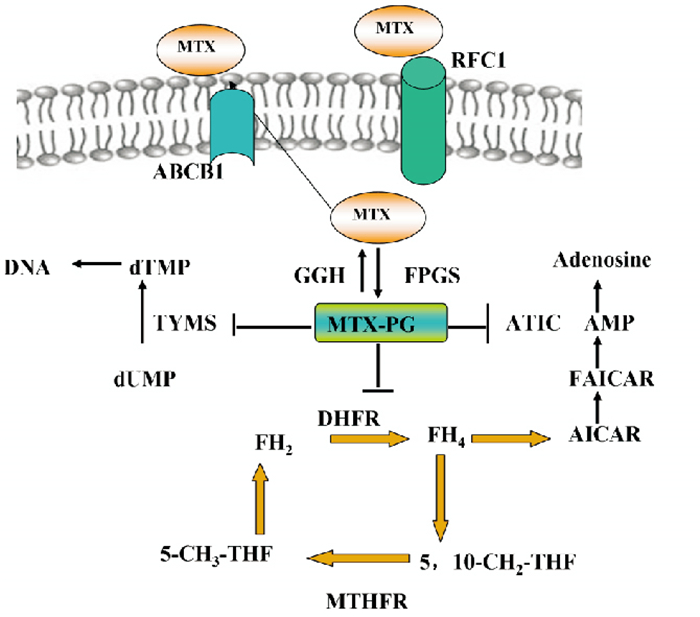
1.1 叶酸途径中酶的基因多态性影响甲氨蝶呤敏感性和不良反应甲氨蝶呤(methotrexate, MTX)是目前临床广泛使用的DMARDs。MTX直接抑制叶酸途径中的酶,包括二氢叶酸还原酶(dihydrofolate reductase, DHFR)、胸苷酸合酶(thymidylate synthase, TYMS)和5-氨基咪唑-4-甲酰胺核糖核苷酸甲基转移酶(5-aminoimidazole-4-carboxamide ribonucleotide transformylase, AICAR) [3],进而抑制嘌呤、嘧啶合成和DNA修复,影响细胞内叶酸和腺苷代谢,见Fig 1。编码DHFR、亚甲基四氢叶酸还原酶(methylenetetrahydrofolate reductase, MTHFR)、叶酸还原载体1(reduced folate carrier 1, RFC1)、ATP结合蛋白(ATP-binding cassette, ABC)、TYMS等基因多态性与MTX应答相关[4]。
|
| Fig 1 Cellular pathway of methotrexate Methotrexate (MTX), a folate analog, is a competitive inhibitor of the enzyme DHFR. Inside the cell, MTX is polyglutamated by the enzyme FPGS. Polyglutamation can be reversed by the enzyme GGH. MTX-PG has several important functions. It retains MTX within the cell and inhibits DHFR, which reduces DHF to THF. MTX-PG also inhibits TYMS, which converts deoxyuridylate to deoxythymidylate in the de-novo pyrimidine biosynthetic pathway. |
DHFR基因位于5号染色体上(5q11.2-q13.2),可被MTX直接抑制。低水平DHFR基因扩增或突变可能参与MTX抵抗。DHFR3个基因多态性rs12517451、rs10072026、rs1643657与MTX不良反应相关。DHFR增强子基因多态性63/91影响MTX的不良反应。对243名RA患者基因多态性分型,并评价对MTX治疗应答和不良反应,发现第63位等位基因9 bp缺失,第91位1个重复基序多态性对MTX毒性有保护作用[5]。
MTHFR基因位于1号染色体上(1p36.3),在还原叶酸的再生中非常重要,可被MTX间接抑制。MTHFR基因变异可影响MTX敏感性及毒性。MTHFR的活性和MTX代谢受677 C/T和1298 A/C的影响。677 C/T(rs1801133)多态性会导致不耐热MTHFR产生,降低酶的活性,而增加胃肠不良反应、肝脏毒性。因此MTHFR C677T可预测发生MTX毒性易感性。677T等位基因患者中MTX不良反应发生率较高。MTX的毒性可导致10%~30%RA病人终止MTX治疗[6]。Caliz等[7]通过468例RA病人证明了677 C/T多态性与MTX毒性也是相关的。另外,MTHFR C677T多态性RA患者补充叶酸会增加MTX毒性的危险性。A1298C的C等位基因患者不能使用高剂量(> 6 mg/周)超过1年的MTX治疗时间(Tab 1)[8]。
| 名称 | 多态性位点 | 等位基因 | 与效应相关性 | 与基因改变相关的药物应答 |
| MTHFR | 677 | C/T | MTHFR中C677T上T等位基因降低了MTHFR酶活性 | 增加了MTX的敏感性和毒性[8] |
| 1298 | A/C | 与疗效相关 | 在A1298C上C等位基因的病人不可能用高剂量MTX治疗[8] | |
| RFC-1 | 80 | G/A | 与MTX摄取作用相关 | G80A单核苷酸多态性与更好的MTX应答正相关[9] |
| ABC | 3435 | C/T | C/C和C/T对活动性RA有更大风险。3435T等位基因似乎有保护作用。 | 3435T等位基因对MTX和prednisone有更好应答[10] |
| TYMS | 1494 | TTAAAG | 重复单元越多,TYMS的mRNA表达和活性越高。 | MTX疗效更低[11] |
| NAT2 | NAT2*4 | 编码快乙酰化状态 | 降低柳氮磺胺吡啶毒性风险[12] | |
| NAT2*5A, NAT2*5B, NAT2*5C, NAT2*6 NAT2*7 | 外显子2中几个单核苷酸多态性组合 | 编码慢乙酰化状态 | 增加毒性柳氮磺胺吡啶的浓度[14] | |
| TPMT | TPMT*2 (238) | G/C | 低的或中度TPMT活性 | 与咪唑硫唑嘌呤血液学和胃肠毒性相关[15]。 |
| TPMT*3A (460) | G/A | 低的或中度TPMT活性 | 与咪唑硫唑嘌呤血液学和胃肠毒性相关[16]。 | |
| TPMT*3A (719) | A/G | 低的或中度TPMT活性 | 与咪唑硫唑嘌呤血液学和胃肠毒性相关[16]。 | |
| TPMT*3C (719) | A/G | 低的或中度TPMT活性 | 与咪唑硫唑嘌呤血液学和胃肠毒性相关[16]。 | |
| CYP1A2 | -163 | C/A | CYP1A2*1F与更高的可诱导酶相关 | 降低来氟米特疗效[18]。 |
| CYP2C19 | CYP2C19*2, *3 | 消除酶活性 | 与来氟米特药物相互作用及毒性相关[19] | |
| CYP2C19*17 | 增加酶活性 | 降低来氟米特疗效[19]。 | ||
| CYP2C9 | CYP2C9*3 | 降低酶活性 | 与来氟米特药物相互作用及毒性相关[19] | |
| TNFRSF1B | 196 | T/G | 影响对Infliximab的应答 | T/T基因型有更好的应答,而A/A基因型与治疗失败相关[25]。 |
| BAFF | -871 | C/T | 影响对rituximab的应答 | CC基因型与rituximab高的应答率明显相关[29] |
| FcγR ⅢA | 158 | V/F | 影响对rituximab的应答 | Ⅴ等位基因与更高的应答率明显相关[30] |
RFC1基因位于21号染色体上(21q22.3),其基因多态性影响MTX的转运[9]。RFC1 G80A多态性与MTX摄取有关,并且RFC1启动子区61 bp重复序列多态性增加了RFC1转录活性。在RA患者中,G80A单核苷酸多态性(single nucleotide polymorphism, SNP)与对MTX良好应答呈正相关,RFC 80A突变体与MTX良好应答及较长疾病缓解期相关联,提示RFC 80A突变体是增加MTX疗效的标志物(Tab 1)。RFC3的SNP位点-43T/C可减少RFC1的表达,并改变MTX摄取,进而影响MTX毒性和疗效。可溶性载体转运蛋白(solute carrier,SLCs)也参与MTX摄取和清除,SLC19A1 rs7499、SLC46A1 rs2239907、SLCO1B1 rs4149056似乎与增加MTX毒性的风险有关。SLC19A1单倍体rs7499、rs1051266、rs2838956有助于预测发生MTX毒性的风险[5]。
P-糖蛋白是由7号染色体(7q21.1)上的ABCB1基因编码。MTX流出细胞由ABC转运蛋白介导。ABC转运体家族有多个亚型,可影响患者对MTX的应答。携带ABCB1基因外显子3435(C>T)T等位基因,对MTX具有更好应答,与症状缓解和不良事件发生率呈明显正相关。3435C/C和3435C/T基因型人群与3435T/T基因型人群相比,患RA风险更高(Tab 1)。除了3435 C/T ABCB1多态性外,2677 GA/T基因型也与药物不良反应和疗效相关[10]。
TMYS基因位于18号染色体(18p11.32),有两个基因多态性,并影响患者对MTX应答。TYMS基因的5′-非翻译区中存在28 bp多态性串联重复序列,重复元件数目越高,mRNA表达和酶活性越高,MTX疗效越低(Tab 1)。另一TYMS多态性是3′-UTR核苷酸1494处的6 bp TTAAAG缺失。这种缺失降低TYMS mRNA稳定性和表达,而增加MTX疗效[11]。
1.2 NAT2基因多态性对于预测柳氮磺胺吡啶不良反应具有重要意义柳氮磺胺吡啶(sulfasalazine, SASP)是另一种治疗RA的DMARDs。SASP可抑制炎性细胞因子如IL-6、TNF-α及叶酸依赖性酶的产生,导致淋巴细胞功能受损,诱导中性粒细胞和巨噬细胞凋亡。SASP及其代谢产物磺胺吡啶血浆水平受编码N-乙酰转移酶2(N-acetyl transferase 2, NAT2)和ABC蛋白G2(ABC protein G2, ABCG2)基因多态性影响[5]。Wiese等[12]发现,编码NAT2和ABCG2的基因变异与SASP应答和不良反应相关。229例病人出现不良反应受到NAT2基因型影响,141名病情缓解患者与ABCG2基因型相关。
NAT2基因位于8号染色体上(8P22),其基因多态性影响乙酰化速度。与快速乙酰化相比,慢乙酰化更容易产生SASP毒性,NAT2变异型与高浓度毒性SASP中间产物明显相关。粒白细胞缺乏症病人中慢乙酰化比例明显升高(Tab 1)。在慢乙酰化基因型群体中,SASP和乙酰基嘧啶的表观消除半衰期延长。SASP的峰浓度(Cmax)和药时曲线下面积(area under curve, AUC)值较高,而乙酰基嘧啶的平均峰浓度值较低。344位T突变为C对于慢乙酰化病人的酶活力影响最大,590位G突变为A次之,857位G突变为A对酶的活性影响最小[13]。野生型NAT2*4等位基因编码快速乙酰化状态。NAT2*5A、NAT2*5B、NAT2*5C、NAT2*6和NAT2*7是编码慢乙酰化状态的最常见突变体[14]。慢乙酰化病人比快乙酰化病人更容易发生不良反应。NAT2多态性对于预测SASP毒性风险非常重要。因此,在SASP给药前,分析NAT2基因型是避免SASP毒性的有效手段。
1.3 硫代嘌呤甲基转移酶基因突变增加硫唑嘌呤的毒性硫唑嘌呤是6-巯基嘌呤(6-mercaptopurine, 6-MP)的前体药,必须通过嘌呤合成途径转化为活性硫嘌呤核苷酸,才发挥细胞毒作用。6-MP通过次黄嘌呤磷酸核糖基转移酶转化为6-硫鸟嘌呤核苷酸。另一种代谢途径是通过硫代嘌呤甲基转移酶(thiopurine methyltransferase, TPMT)使6-MP失活。当TPMT缺陷时,具有细胞毒性硫鸟嘌呤核苷酸累积,毒性增加[15]。TPMT基因有3个基因突变体:TPMT*2(G238C)、TPMT*3A(G460A和A719G)、TPMT*3C(A719G),并决定酶的活性。90%人群有高的TPMT酶活性,10%人群有中等酶活性,仅0.2%~0.3%人群有低的酶活性(Tab 1)[16]。对于低TPMT活性患者,常规剂量的硫唑嘌呤可能导致严重的毒性。因此,TPMT基因分型有助于预测硫唑嘌呤毒性。
1.4 嘧啶合成关键酶和细胞色素P450酶多态性与来氟米特药物相互作用和毒性相关来氟米特(leflunomide, LEF)是治疗RA的新型DMARDs。体内LEF被转化成活性代谢物A771726[2-氰基-3-羟基-N-[4-(三氟甲基)苯基] -2-丁烯酰胺]。LEF的主要靶分子二氢叶酸脱氢酶(dihydrogen orotic acid dehydrogenase, DHODH),抑制嘧啶核糖核苷酸的合成并导致淋巴细胞增殖减少。O′Doherty等[17]报道携带DHODH单倍型与低的LEF应答相关。表明该单倍型连锁不平衡变异可能降低了LEF疗效。
细胞色素P450(cytochromes P450,CYP450s)CYP1A2、CYP2C19、CYP3A4在LEF转化为代谢产物A771726中起重要作用。CYP1A2多态性影响LEF毒性。CYP1A2*1F CC基因型患者与CYP1A2*1F A等位基因携带者相比,LEF诱导的毒性风险高9.7倍。CYP1A2基因163位C突变为A(rs762551)与更高的酶诱导性相关[18]。CYP2C19表型与因LEF毒性而致LEF停用相关。CYP2C19存在两个有缺陷的等位基因(CYP2C19*2, rs4244285和CYP2C19*3, rs4986893),而导致酶的活性消失。CYP2C19*17等位基因(rs12248560)导致酶的活性增加。LEF代谢酶的遗传变异也影响LEF代谢产物浓度,并与治疗应答相关。与非携带者相比,CYP2C19*2等位基因携带者A771726的清除率高71%。A771726平均稳态血浆浓度与治疗应答相关,血浆A771726浓度更高的患者,C反应蛋白(C-reactive protein, CRP)水平降低幅度更大。虽然CYP2C9不是LEF主要代谢酶,但CYP2C9*3纯合患者存在LEF药物相互作用和毒性的病例(Tab 1),如发生LEF诱导的严重肝炎[19]。
1.5 MTHFR基因多态性影响羟基氯喹的毒副作用羟基氯喹因其价格低廉和长期的使用经验而在临床仍广泛使用。然而,在一些患者中具有毒性作用,限制了其使用范围。羟基氯喹缓解RA患者的症状与携带MTHFR677T和1298C等位基因相关,C677C > T和A1298A > C MTHFR等位基因是与缓解频率增加相关的独立因素,表明降低MTHFR的活性可能会有更好的治疗效果。分析677C > T和1298A > C MTHFR多态性可能是预测RA患者羟基氯喹治疗效果的有效手段[7]。
1.6 RA病理机制中细胞因子基因多态性影响DMARDs药物疗效和不良反应IL-17和IL-6等炎症细胞因子在RA发病中的作用已经得到证实,而且靶向IL-17和IL-6治疗RA也成为研究热点。RA患者存在IL-17A多态性,且与疾病严重程度和DMARDs疗效有关。IL-17多态性rs2275913与RA疾病严重度密切关联,需要更多的DMARDs控制疾病。RA患者与健康对照间IL-17 rs2275913单核苷酸多态性有明显差异。与IL-17 rs2275913阴性RA患者相比,IL-17 rs2275913阳性的RA患者,需要3种DMARDs控制病情。另外,rs2275913的出现也许提示发生RA的危险性[20]。IL-6基因多态性也与RA患者MTX和来氟米特治疗应答有关。墨西哥人中,IL-6-174G/G基因型具有更高的LEF治疗失败的风险[21]。
2 CYP450酶基因多态性影响NSAIDs疗效和不良反应NSAIDs通过环氧化酶(cyclooxygenase, COX)抑制花生四烯酸产生前列腺素,发挥抗炎作用。目前,临床上常用的NSAIDs主要包括塞来昔布、布洛芬、双氯芬酸、美洛昔康、萘普生等。细胞色素CYP2C多态性与NSAIDs疗效和不良反应存在关联[22]。CYP2C8*3和CYP2C9*2*3突变体对布洛芬和双氯芬酸药代动力学影响大。与野生型携带者相比,CYP2C8*3*3和CYP2C8*1*3携带者右旋(R)-布洛芬半衰期明显延长。CYP2C8*3纯合子中,R-和S-布洛芬清除率几乎是野生型纯合子清除率的九分之一。与野生型携带者相比,CYP2C8*3和CYP2C8*4携带者具有较高的双氯芬酸/ 5-羟基-双氯芬酸浓度比。在安全性方面,CYP2C8*3携带者不良反应较少,十二指肠出血与携带CYP2C9*3强烈相关。布洛芬血浆浓度受CYP2C9基因型影响。CYP 2C9*2、CYP 2C9*3、CYP2C8*3突变体携带者比其他基因型显示较低的布洛芬代谢[22]。
美洛昔康是针对骨关节炎(osteoarthritis, OA)和RA的NSAIDs,然而不良反应较多。不良反应风险可能随着药物使用的持续时间而增加。CYP2C9在美洛昔康代谢中起重要作用,可能是临床相关的不良反应危险因素。携带CYP2C9*3/*3基因型患者显示底物特异性降低。CYP2C9*1/*13基因型与美洛昔康代谢减少和药效学增加有关。与CYP2C9*1/*1和CYP2C9*1/*3个体相比,CYP2C9*3/*3个体美洛昔康清除率明显降低。表明CYP2C9*3/*3个体因抑制COX-1而发生不良反应的风险相对高[23]。
塞来昔布是治疗RA和OA的COX-2选择性抑制剂,主要由肝脏CYP2C9酶代谢。CYP2C9*3/*3受试者与CYP2C9*1/*1和CYP2C9*1/*3、*1/*13受试者相比,塞来昔布AUC、半衰期、口服清除率明显升高。CYP2C9*3和CYP2C9*13等位基因明显影响塞来昔布的血浆浓度[24]。塞来昔布在儿童体内代谢显示,CYP2C9*3纯合子患儿的塞来昔布AUC是CYP2C9*1/*1或*1/*2基因型的8-9倍。成人中CYP2C9*3/*3个体塞来昔布AUC是CYP2C9*1/*3或*1/*1个体的7倍[20]。因此,对于减少塞来昔布副作用,美国食品药品监督管理局批准塞来昔布药物标签说明:“基于基因型或曾怀疑CYP2C9其他底物是不良代谢者的患者应慎用塞来昔布,不良代谢者(即CYP2C9*3/*3)中以最低推荐剂量的一半开始治疗”。
3 药物靶点(细胞因子或受体)基因多态性影响生物制剂疗效和不良反应炎性因子和免疫细胞在RA及红斑狼疮等自身免疫疾病炎症反应和免疫应答过程中起着重要作用。随着对炎症过程的深入研究,促进了以细胞因子或免疫细胞为靶点生物制剂的研发,并广泛用于临床治疗RA等自身免疫疾病。然而,并非所有患者均对生物制剂呈现出良好应答,细胞因子或受体基因多态性影响生物制剂疗效和不良反应[25]。
3.1 TNF-α启动子和受体基因多态性影响TNF-α拮抗剂的应答在常规DMARDs治疗失败后,TNF-α拮抗剂是主要的治疗选择。TNF-α拮抗剂对一些RA患者显示明显疗效。目前,临床用于治疗RA的3个TNF-α拮抗剂是依那西普、英夫利昔单抗、阿达木单抗。然而,对TNF-α拮抗剂应答存在个体差异,只有60%的病人显示对TNF-α拮抗剂满意应答[25]。
TNF-α基因位于染色体6p21上,位于TNF-α启动子区域的多态性与高水平TNF-α、RA遗传易感性和对临床治疗应答有关。其中,-38(rs361525)、-308(rs1800629)和-857(rs1799724)被广泛研究。通过评价DAS28发现TNF基因区域中8个SNP与对依那西普应答之间存在关联。与TNF-308AA基因型相比,TNF-308GG基因型有更好应答。TNF启动子区域中的-308G/A SNP影响对英夫利昔单抗应答。G/G基因型患者对英夫利昔单抗表现出更好的应答。推测TNF-308多态性通过影响循环TNF水平,影响对英夫利昔单抗的应答[2]。
3.2 Fcγ受体多态性影响TNF拮抗剂应答Fcγ受体(Fcγ receptor, FCGR)在识别免疫复合物中起重要作用。阿达木单抗、英夫利昔单抗和依那西普可结合FCGR的IgG1 Fc部分。FCGR2A表达在单核巨噬细胞、中性粒细胞和血小板上,C蛋白酪氨酸磷酸酶受体(protein tyrosine phosphatase receptor type C, PTPRC)和FCGR2A多态性在RA发病中发挥关键的作用。RA中,PTPRC rs10919563 A/G和FCGR2A R131H多态性影响TNF拮抗剂应答。与PTPRC G等位基因患者相比,PTPRC rs10919563A等位基因患者对TNF阻滞剂应答差。FCGR2A H等位基因患者与FCGR2A RR基因型相比,对阿达木单抗治疗应答差[26]。而FCGR3B多态性与阿达木单抗引起的超敏反应有关。FCGR3B NA1/NA1、NA1/NA、NA2/NA2等位基因患者阿达木单抗治疗出现超敏反应发生率分别是75%、13%、13%。而且NA1/NA1是针对阿达木单抗超敏反应的一个独立相关因素[27]。
3.3 IL-6基因多态性影响RA患者对依那西普的应答-174G/C IL-6基因多态性与IL-6水平相关,并影响RA患者对依那西普治疗应答。使用TaqMan等位基因鉴别技术对IL-6-174G/C(rs1800795)基因突变体进行基因分型,发现位于IL-6基因启动子的负调节结构域的-174G/C多态性(rs1800795)影响转录调节。IL-6-174*C等位基因与增加的IL-6和CRP水平相关。-174G/C与依那西普治疗应答明显关联。与-174*C携带患者相比,-174*GG患者存在更高的应答率,表明这种多态性可能是RA对依那西普应答的遗传标记。77例急性RA患者接收依那西普治疗后,分别在基线、治疗6个月及12个月评价疗效。治疗后12个月,IL-6-174G/G基因型病人应答率(DAS28改善 > 1.2)明显增加(95.7%),而G/C或CC基因型病人应答率分别是75.6%和44.4%。提示IL-6-174GG基因型病人对依那西普应答优于G/C或CC基因型病人[28]。
3.4 B细胞活化因子及Fc受体基因多态性影响患者对CD20单抗应答RA中B细胞可以通过分泌促炎细胞因子和产生类风湿因子(RF),引发和促进炎症反应。靶向B细胞耗竭为治疗RA提供了可能策略。利妥昔单抗(rituximab)是靶向B细胞的抗CD20单克隆抗体,可以有效治疗RA。B细胞活化因子(B cell activating factor, BAFF)是TNF配体超家族成员,在B细胞刺激和自身免疫细胞存活中起重要作用。BAFF的-871C> T多态性似乎影响RA患者对利妥昔单抗的应答(Tab 1)。Ruyssen-Witrand等[29]开展了一个开放试验,224例基因分型RA病人接收第一阶段利妥昔单抗治疗,根据BAFF-871C > T基因多态性,分析了EULAR(European League Against Rheumatism)应答率。发现CC基因型患者对利妥昔单抗应答率明显高于TT基因型患者,分别为92%(CC基因型)和64%(TT基因型)。这些结果在RF阳性的病人中进一步得到证实。
Fc受体等位基因多态性对利妥昔单抗Fc片段有不同亲和力,与FCGR3A 158 F等位基因患者相比,FCGR3A 158Ⅴ等位基因患者对利妥昔单抗应答更好[49-50]。利妥昔单抗在携带高亲和力Ⅴ等位基因患者中,减少外周B细胞更有效,表明FCGR3A Ⅴ等位基因携带者对利妥昔单抗有更好的应答潜力,而FCGR3A V/F多态性与对利妥昔单抗治疗无应答相关(Tab 1)。Ruyssenwitrand等[30]也评估了RA患者ⅢA型Fcγ受体基因与RA患者利妥昔单抗治疗应答间的关联,ⅢA型Fcγ受体的158V/F基因多态性影响对利妥昔单抗的应答。在111个病人中,有90人(81%)显示应答,其中30人(27%)有良好应答。Ⅴ等位基因携带与利妥昔单抗更高应答率具有明显独立相关性。
4 总结与展望药物遗传学及基因组学研究揭示了药物代谢酶、药物转运体、细胞因子及其受体等的基因多态性。这些基因多态性影响了RA药物的疗效和不良反应。研究基因多态性可以为RA患者个体化治疗选择合适药物和剂量,减少不良反应以及开发新的治疗药物提供线索和依据。目前,大多数进行的RA药物遗传学及基因组学研究样本量不够大,因此,还需要大规模的随机前瞻性研究来有效地重复和验证已有的研究结论。临床个体化治疗,遵循量体裁衣原则,未来几年RA药物基因组学研究的主要目的之一是在目前药物基础上,根据患者的基因多态性选择合适的药物,或者根据病人基因多态性特点研发靶点更精确的新药。而使用先进的技术、大样本和高质量的临床相关数据,对实现这一目标至关重要。
| [1] | 魏伟. 炎症免疫反应软调节[J]. 中国药理学通报, 2016, 32(3): 297-303. Wei W. Soft regulation of inflammatory immune responses[J]. Chin Pharmacol Bull, 2016, 32(3): 297-303. doi:10.3969/j.issn.1001-1978.2016.03.001 |
| [2] | Castaneda S, Lopez-Mejias R, Gonzalez-Gay M A. Gene polymorphisms and therapy in rheumatoid arthritis[J]. Expert Opin Drug Metab Toxicol, 2016, 12(3): 225-9. doi:10.1517/17425255.2016.1141405 |
| [3] | Hughes L B, Beasley T M, Patel H, et al. Racial or ethnic differences in allele frequencies of single-nucleotide polymorphisms in the methylenetetrahydrofolate reductase gene and their influence on response to methotrexate in rheumatoid arthritis[J]. Ann Rheum Dis, 2006, 65(9): 1213-8. doi:10.1136/ard.2005.046797 |
| [4] | Stamp L K, Roberts R L. Effect of genetic polymorphisms in the folate pathway on methotrexate therapy in rheumatic diseases[J]. Pharmacogenomics, 2011, 12(10): 1449-63. doi:10.2217/pgs.11.86 |
| [5] | Jekic B, Vejnovic D, Milic V, et al. Association of 63/91 length polymorphism in the DHFR gene major promoter with toxicity of methotrexate in patients with rheumatoid arthritis[J]. Pharmacogenomics, 2016, 17(15): 1687-91. doi:10.2217/pgs-2016-0090 |
| [6] | Tasbas O, Borman P, Gurhan K H, et al. The frequency of A1298C and C677T polymorphisms of the methylentetrahydrofolate gene in Turkish patients with rheumatoid arthritis:relationship with methotrexate toxicity[J]. Open Rheumatol J, 2011, 5: 30-5. doi:10.2174/1874312901105010030 |
| [7] | Caliz R, Del A J, Balsa A, et al. The C677T polymorphism in the MTHFR gene is associated with the toxicity of methotrexate in a Spanish rheumatoid arthritis population[J]. Scand J Rheumatol, 2012, 41(1): 10-4. doi:10.3109/03009742.2011.617312 |
| [8] | Shao W, Yuan Y, Li Y. Association between MTHFR C677T polymorphism and methotrexate treatment outcome in rheumatoid arthritis patients:a systematic review and meta-analysis[J]. Genet Test Mol Biomarkers, 2017, 21(5): 275-85. doi:10.1089/gtmb.2016.0326 |
| [9] | Hayashi H, Tazoe Y, Tsuboi S, et al. A single nucleotide polymorphism of reduced folate carrier 1 predicts methotrexate efficacy in Japanese patients with rheumatoid arthritis[J]. Drug Metab Pharmacokinet, 2013, 28(2): 164-8. doi:10.2133/dmpk.DMPK-12-NT-038 |
| [10] | Kravljaca M, Perovic V, Pravica V, et al. The importance of MDR1 gene polymorphisms for tacrolimus dosage[J]. Eur J Pharm Sci, 2016, 83: 109-13. doi:10.1016/j.ejps.2015.12.020 |
| [11] | Jekic B, Lukovic L, Bunjevacki V, et al. Association of the TYMS 3G/3G genotype with poor response and GGH 354GG genotype with the bone marrow toxicity of the methotrexate in RA patients[J]. Eur J Clin Pharmacol, 2013, 69(3): 377-83. doi:10.1007/s00228-012-1341-3 |
| [12] | Wiese M D, Alotaibi N, O′Doherty C, et al. Pharmacogenomics of NAT2 and ABCG2 influence the toxicity and efficacy of sulphasalazine containing DMARD regimens in early rheumatoid arthritis[J]. Pharmacogenomics J, 2014, 14(4): 350-5. doi:10.1038/tpj.2013.45 |
| [13] | Kuhn U D, Anschutz M, Schmucker K, et al. Phenotyping with sulfasalazine-time dependence and relation to NAT2 pharmacogenetics[J]. Int J Clin Pharmacol Ther, 2010, 48(1): 1-10. doi:10.5414/CPP48001 |
| [14] | Soukup T, Dosedel M, Nekvindova J, et al. Genetic polymorphisms in metabolic pathways of leflunomide in the treatment of rheumatoid arthritis[J]. Clin Exp Rheumatol, 2015, 33(3): 426-32. |
| [15] | Colleoni L, Kapetis D, Maggi L, et al. A new thiopurine s-methyltransferase haplotype associated with intolerance to azathioprine[J]. J Clin Pharmacol, 2013, 53(1): 67-74. doi:10.1177/0091270011435989 |
| [16] | Seinen M L, van Bodegraven A A, van Kuilenburg A B, et al. High TPMT activity as a risk factor for severe myelosuppression during thiopurine therapy[J]. Neth J Med, 2013, 71(4): 222. |
| [17] | O′Doherty C, Schnabl M, Spargo L, et al. Association of DHODH haplotype variants and response to leflunomide treatment in rheumatoid arthritis[J]. Pharmacogenomics, 2012, 13(12): 1427-34. doi:10.2217/pgs.12.118 |
| [18] | Bohanec G P, Rozman B, Tomsic M, et al. Genetic polymorphism of CYP1A2 and the toxicity of leflunomide treatment in rheumatoid arthritis patients[J]. Eur J Clin Pharmacol, 2008, 64(9): 871-6. doi:10.1007/s00228-008-0498-2 |
| [19] | Sevilla-Mantilla C, Ortega L, Agúndez J A, et al. Leflunomide-induced acute hepatitis[J]. Dig Liver Dis, 2004, 36(1): 82-4. doi:10.1016/j.dld.2003.06.002 |
| [20] | Garcia DLPM, Mendez C R, Garrido G E, et al. Polymorphism rs2275913 of interleukin-17A is related to more intensive therapy with disease-modifying anti rheumatic drugs in Mexican patients with rheumatoid arthritis[J]. Acta Reumatol Port, 2017, 42(2): 155-61. |
| [21] | Ruiz-Padilla A J, Gamez-Nava J I, Saldana-Cruz A M, et al. The -174G/C interleukin-6 gene promoter polymorphism as a genetic marker of differences in therapeutic response to methotrexate and leflunomide in rheumatoid arthritis[J]. Biomed Res Int, 2016, 2016: 4193538. |
| [22] | Krasniqi V, Dimovski A, Domjanovic I K, et al. How polymorphisms of the cytochrome P450 genes affect ibuprofen and diclofenac metabolism and toxicity[J]. Arh Hig Rada Toksikol, 2016, 67(1): 1-8. doi:10.1515/aiht-2016-67-2754 |
| [23] | Lee H I, Bae J W, Choi C I, et al. Strongly increased exposure of meloxicam in CYP2C9*3/*3 individuals[J]. Pharmacogenet Genomics, 2014, 24(2): 113-7. doi:10.1097/FPC.0000000000000025 |
| [24] | Kim S H, Kim D H, Byeon J Y, et al. Effects of CYP2C9 genetic polymorphisms on the pharmacokinetics of celecoxib and its carboxylic acid metabolite[J]. Arch Pharm res, 2017, 40(3): 382-90. doi:10.1007/s12272-016-0861-2 |
| [25] | Fisher M D, Watson C, Fox K M, et al. Dosing patterns of three tumor necrosis factor-blockers among patients with rheumatoid arthritis in a large United States managed care population[J]. Curr Med Res Opin, 2013, 29(5): 561-8. doi:10.1185/03007995.2013.786693 |
| [26] | Lee Y H, Bae S C. Associations between PTPRC rs10919563 A/G and FCGR2A R131H polymorphisms and responsiveness to TNF blockers in rheumatoid arthritis:a meta-analysis[J]. Rheumatol Int, 2016, 36(6): 837-44. doi:10.1007/s00296-016-3476-5 |
| [27] | Tsukamoto M, Kameda H, Ohshige T, et al. Fcgamma receptor 3B polymorphism is associated with hypersensitivity reactions to adalimumab in Japanese patients with rheumatoid arthritis[J]. Mod Rheumatol, 2017, 27(5): 778-81. doi:10.1080/14397595.2016.1254709 |
| [28] | Jancic I, Arsenovic-Ranin N, Sefik-Bukilica M, et al. -174G/C interleukin-6 gene promoter polymorphism predicts therapeutic response to etanercept in rheumatoid arthritis[J]. Rheumatol Int, 2013, 33(6): 1481-6. doi:10.1007/s00296-012-2586-y |
| [29] | Ruyssen-Witrand A, Rouanet S, Combe B, et al. Association between -871C > T promoter polymorphism in the B-cell activating factor gene and the response to rituximab in rheumatoid arthritis patients[J]. Rheumatology (Oxford), 2013, 52(4): 636-41. doi:10.1093/rheumatology/kes344 |
| [30] | Ruyssenwitrand A, Rouanet S, Combe B, et al. Fcγ receptor type ⅢA polymorphism influences treatment outcomes in patients with rheumatoid arthritis treated with rituximab[J]. Ann Rheum Dis, 2012, 71(6): 875. doi:10.1136/annrheumdis-2011-200337 |

