

2. 安徽医科大学附属省立医院药剂科,安徽 合肥 230001
2. Dept of Pharmacy, Anhui Provincial Hospital, Anhui Medical University, Hefei 230001, China
糖尿病肾病(diabetic nephropathy, DN)是糖尿病最常见、最严重的微血管并发症之一,也是终末期肾衰竭的主要诱因之一[1-2]。DN的发病机制十分复杂,涉及到糖脂代谢紊乱、血流动力学异常、炎症介质释放、细胞因子、氧化应激、细胞凋亡等多种因素的作用,这些作用最终导致肾小球滤过屏障的破坏和组织学变化,包括肾小球系膜扩张、肾小管间质纤维化和结节性肾小球硬化等[3]。足细胞即肾小球脏层上皮细胞,为高度分化的终末期细胞,位于肾小球基底膜(glomerular basement membrane, GBM)的最外层,与内皮细胞层、肾小球基底膜共同构成了肾小球的3层滤过屏障,以保证肾小球毛细血管壁的选择通透性。作为肾脏组织中重要的固有细胞,足细胞功能的改变在DN的发生、发展过程中起着至关重要的作用。足细胞具有多种功能,在正常情况下,足细胞能够合成GBM的主要成分,是维持肾小球滤过屏障结构和功能正常的主要细胞[4]。小檗碱(berberine, BBR)为黄连根茎中主要成分,研究表明,BBR具有降血糖、抗炎、调节异常脂质代谢、改善胰岛素抵抗、减轻肾脏损伤作用。有研究报道,足细胞在高糖及糖基化终末产物作用下,可引起足细胞骨架蛋白重构及分布异常,并诱导足细胞凋亡,BBR能改善高糖及糖基化终末产物引起的足细胞骨架蛋白损伤,并抑制足细胞的凋亡[5]。本实验将通过高糖诱导肾小球足细胞模拟DN环境,进一步探讨BBR对高糖诱导损伤足细胞功能的保护作用,为BBR治疗DN提供理论依据。
1 材料 1.1 细胞株小鼠肾小球足细胞株,购自北京北纳创联生物技术研究院,由中国医学科学院基础医学研究所建系。于37℃水浴中复苏,再将细胞转移至培养瓶中,加入含10%胎牛血清、0.2% γ-干扰素、1%双抗的RPMI 1640培养液,置于37℃、5% CO2细胞培养箱中培养。
1.2 药物BBR由安徽省立医院药剂科提取纯化,经RP-HPLC法检测纯度大于96.5%[6]。样品分析使用C18柱(250 mm×4.6 mm,5 μm),流动相为乙腈-0.033 mol·L-1磷酸二氢钾溶液(48:52),流速为1.0 mL·min-1,检测波长为263 nm,柱温25℃。称取40.365 g BBR粉末,加入10 mL生理盐水,加热涡旋混匀至完全溶解,配制浓度为1.2×104 μmol·L-1的储备液,0.22 μm无菌过滤器处理后,分装冻存。临用前加热溶解后,稀释适当倍数,达到所需浓度即可使用。
1.3 试剂小鼠重组γ干扰素(货号:315-05-100),美国Protech公司;RPMI Medium Modified培养液(货号:SH30809.01),赛默飞世尔生物化学制品公司;胎牛血清:杭州四季青公司;己糖激酶(货号:N4006)、二甲基亚砜、D(+)Glucose(货号:G-8270)、MTT粉末,均购自美国Sigma公司;Annexin V-FITC/PI细胞凋亡检测试剂盒(货号:BB-4101-100T),贝博生物有限公司;β-actin(批号:151110)、辣根酶标记山羊抗小鼠IgG(货号:ZB-2305)、辣根酶标记山羊抗兔IgG(货号:ZB-2301),均购自北京中杉金桥生物公司;抗desmin蛋白多克隆抗体(货号:bs-1026R),北京博奥森生物公司;抗podocin蛋白多克隆抗体(货号:sc-21009),美国Santa Cruz公司;抗nephrin蛋白单克隆抗体(货号:ab136894),艾博抗贸易公司。
1.4 仪器超净工作台(江苏苏州安泰空气技术有限公司);CO2细胞培养箱(Thermo Fisher Scientific公司);FC500流式细胞仪(美国贝克曼库尔特公司);Powerpac164-5070电泳仪(美国Bio-Rad公司);LAS4000Mini型化学发光成像分析仪(美国GE公司);BX53正置显微镜(日本Olympus光学工业株氏会社);Infinite M1000 PRO多功能酶标仪(瑞士Tecan公司)。
2 方法 2.1 细胞增殖检测采用MTT法检测细胞增殖活性。取对数生长期的足细胞,调整细胞密度至2×104个/孔,接种于96孔板,每孔100 μL,于37℃、5% CO2培养箱中静置培养24 h。分别加入高糖(葡萄糖浓度30 mmol·L-1)及BBR (终浓度分别为30、60、90 μmol·L-1),同时设置高糖模型组(葡萄糖浓度30 mmol·L-1)和正常对照组。24 h后,每孔加入5 g·L-1的MTT溶液10 μL,继续孵育4 h,吸弃孔中培养上清液,每孔加入150 μL的DMSO,震荡混匀10 min,酶标仪测定490 nm处各孔的吸光度值,计算细胞存活率,绘制细胞活力柱状图, 每组设5个复孔。
2.2 细胞凋亡检测采用Annexin V-FITC/PI双染法检测足细胞凋亡,分组与加药处理同“2.1”项,足细胞培养24 h后,离心收集各组细胞,将1×106个细胞悬浮于500 μL工作液中,分别加入10 μL Annexin V染液,混匀,室温避光孵育10 min,再分别加入5 μL PI染液,室温避光孵育5 min,流式细胞仪检测细胞凋亡百分率。
2.3 Transwell检测细胞迁移能力将Transwell小室放于24孔板中,在Transwell下室中加入含10%胎牛血清的RPMI 1640培养基,并分别加入不同浓度的BBR(30、60、90 μmol·L-1)和高糖刺激;用含1%胎牛血清的RPMI 1640培养基将足细胞制成单细胞悬液,计数,种于Transwell小室,每孔细胞数约为2×104个,放置37℃培养箱培养24 h,;取出Transwell小室,用PBS轻轻漂洗2遍,结晶紫染色,Transwell上室中未迁移的细胞用棉签轻轻擦去,倒置显微镜下观察、计数、拍照。每个样本随机选取10个视野,计算每个视野的细胞数。
2.4 Western blot检测相关蛋白表达取对数生长期细胞,分组与加药处理同“2.1”项,以1×108个/孔将细胞接种于6孔板,处理24 h后,离心收集细胞,用RIPA裂解液提取细胞总蛋白,并测定蛋白浓度。蛋白样品中加入等体积的蛋白上样缓冲液,沸水煮沸5 min,进行SDS-PAGE凝胶电泳,转移至PVDF膜上,含5%脱脂牛奶-0.05%吐温的PBS溶液中37℃封闭2 h,TPBS溶液洗3次,PBS溶液洗1次;一抗4℃孵育过夜;次日TPBS漂洗3次,加入辣根过氧化酶标记的二抗,37℃孵育2 h,ECL显色。利用Image J软件分析各组灰度值,以β-actin为内参计算各蛋白的变化。
2.5 细胞黏附实验测定足细胞的黏附功能传代消化足细胞后,分组与加药处理同“2.1”项。将足细胞种于预先用I型鼠尾胶原铺板的96孔板,细胞浓度约为1×105个/孔,待细胞大部分贴壁后,弃去培养液,用PBS洗去未贴壁细胞,配制含有3.75 mmol·L-1己糖激酶和0.25% Triton X-100的枸橼酸缓冲液,将上述液体混合均匀后加入培养孔内(每孔60 μL),37℃孵育1 h,孵育结束后取出,再加入含有5 mmol·L-1依地酸二钠的甘氨酸缓冲液,每孔90 μL(pH 10.4),测定405 nm处的吸光度值。以正常对照组吸光度值为黏附能力100%作为对照,计算其他各组足细胞黏附能力。
2.6 统计学分析实验结果使用SPSS 16.0软件对所得数据进行分析处理,数据以x±s表示,计量资料的组间差异比较采用One-Way ANOVA。
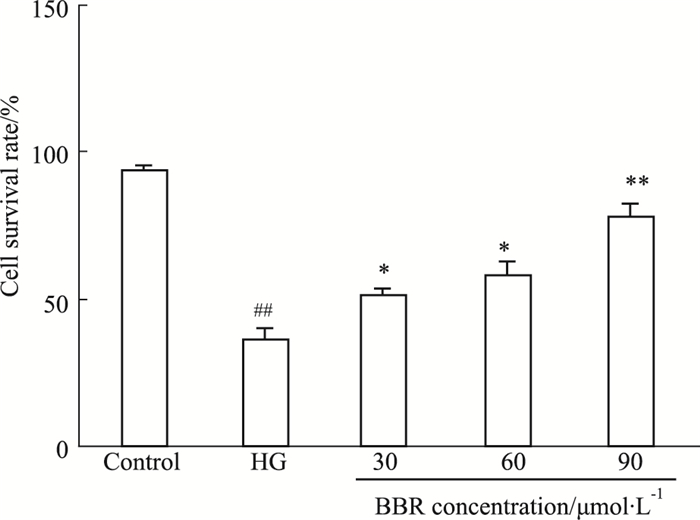
3 结果 3.1 BBR对高糖损伤足细胞存活率的影响Fig 1的MTT结果显示,给予高糖刺激24 h后,与正常对照组相比较,高糖组细胞存活率明显降低;与高糖组比较,BBR(30、60、90 μmol·L-1)能不同程度促进足细胞增殖,且呈浓度相关性。
|
| Fig 1 Effect of BBR on viability of HG-induced podocytes (x±s, n=5) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group |
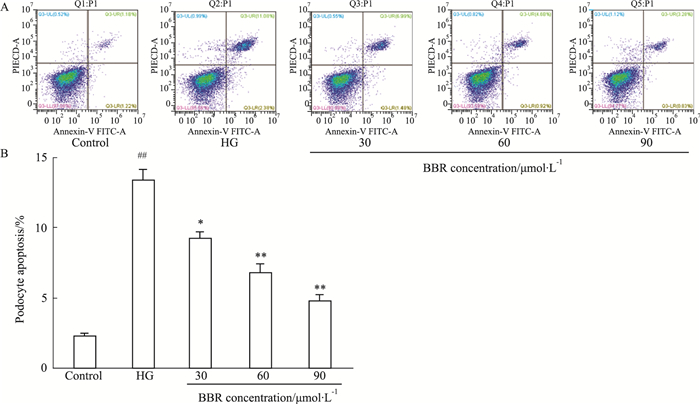
采用Annexin V-FITC/PI双染法检测足细胞凋亡情况。Fig 2流式细胞仪检测结果显示,与正常对照组相比,高糖能明显诱导足细胞的凋亡;与高糖组比较,BBR(30、60、90 μmol·L-1)能明显降低足细胞的凋亡率,改善足细胞的凋亡。
|
| Fig 2 Effect of BBR on apoptosis of HG-induced podocytes (x±s, n=3) A: Annexin V-FITC/PI double staining assay detected the effect of BBR on apoptosis of podocytes; B: Quantitative analysis showed the percentage of the apoptotic podocytes relative to different groups using CytExpert software. ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group. |
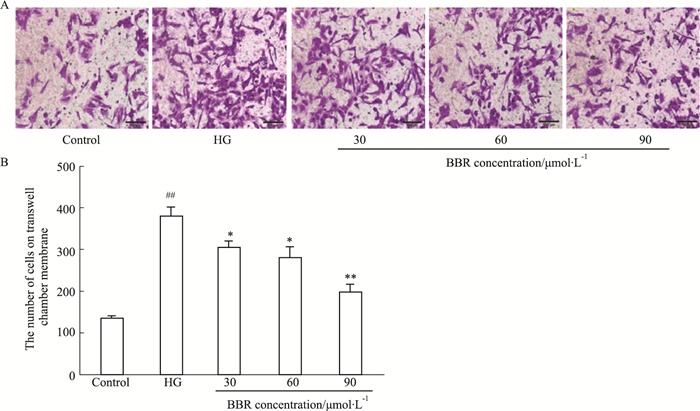
Fig 3的Transwell迁移实验结果显示,与正常对照组相比,高糖能明显增加迁移至Transwell下室的足细胞数量;与高糖组相比,BBR(30、60、90 μmol·L-1)能明显减少迁移至Transwell下室的足细胞数量。
|
| Fig 3 Effect of BBR on migration ability of HG-induced podocytes (x±s, n=3) A: Cell transwell assay detected the effect of BBR on cell migration ability of podocytes, scale bar=100 μm; B: Quantitative analysis showed the number of cells on transwell chamber membrane. ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group. |
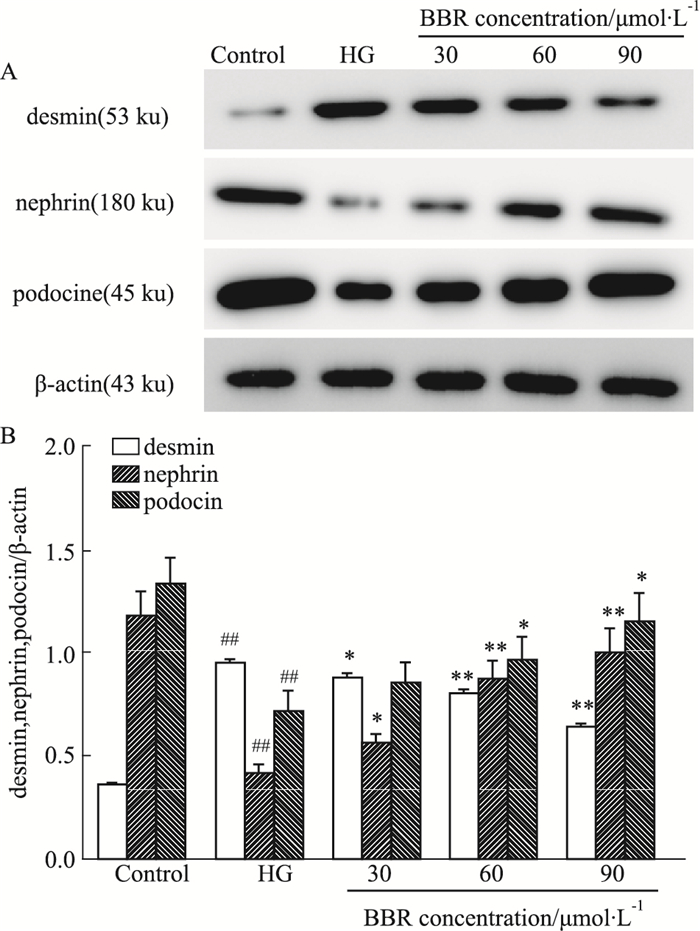
nephrin、podocin、desmin蛋白是维持足细胞功能完整性的重要蛋白。Fig 4的Western blot结果显示,与正常对照组比较,高糖能明显降低足细胞内nephrin、podocin的表达水平, 升高足细胞内desmin蛋白的表达;与高糖组相比,BBR(30、60、90 μmol·L-1)能不同程度升高足细胞内nephrin和podocin的表达水平,降低足细胞内desmin蛋白的表达。
|
| Fig 4 Effect of BBR on expression of desmin, nephrin and podocin proteins(x±s, n=3) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group |
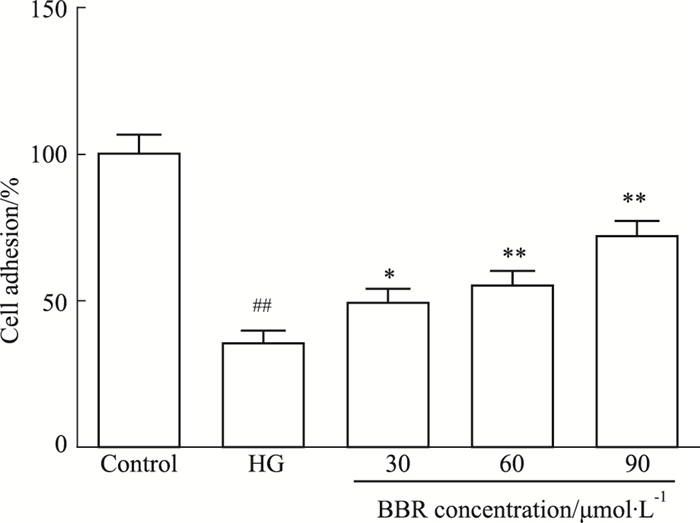
Fig 5黏附能力测定结果显示,与正常对照组比较,高糖能明显降低足细胞的黏附水平;与高糖组比较,BBR(30、60、90 μmol·L-1)能不同程度提高足细胞的黏附能力。
|
| Fig 5 Effect of BBR on podocyte adhesion ability induced by HG analyzed by cell adhesion assay (x±s, n=4) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group |
肾小球足细胞是肾脏中重要的固有细胞,足细胞的损伤与肾脏疾病的进展具有密切的关系。在疾病状态下,足细胞是肾小球疾病损伤的靶细胞,当足细胞的丢失超过其增殖能力时,剩余的足细胞不足以完全覆盖GBM的表面,造成足细胞脱落位点处GBM的裸露,裸露的GBM与鲍曼囊的壁层直接接触并发生了黏连,导致肾小球毛细血管袢结构毁损,并出现继发性透明样物质的沉积,最后肾小球硬化形成[7]。由此可见,损伤后的足细胞数量减少在肾小球硬化的发生过程中起了关键性的作用。足细胞表型是以在足细胞裂孔隔膜(slit diaphragm, SD)上表达的各种膜蛋白为特征性表现,nephrin和podocin是足细胞成熟的标志性分子,也是维持SD完整性和肾小球滤过功能的重要结构分子[8]。desmin作为足细胞骨架中间丝蛋白的一种,与α-平滑肌肌动蛋一样,属于肌源性细胞标志,正常情况下肾小球系膜细胞可偶见少量表达,而足细胞无明显表达。当足细胞因各种原因发生损伤时,可大量表达desmin而发生表型转化,其原因可能是足细胞骨架重新排列。因此,desmin可作为足细胞损伤的标志[9-10]。
黄连根茎中主要成分为BBR,有降血糖、调节血脂的作用,是黄连治疗DN的物质基础。课题组前期研究发现,BBR可能通过调节血管内皮生长因子和G蛋白偶联受体(G protein-coupled receptor, GPCR)的表达,调节GPCR的脱敏和GPCR-G蛋白-AC-cAMP信号通路,从而抑制系膜细胞炎性细胞因子的分泌和过度增殖。上述研究结果提示,BBR可以减轻DN大鼠肾损害,发挥肾脏保护作用[6, 11-13]。本研究在体外用高糖刺激足细胞,观察对足细胞增殖、凋亡、迁移、黏附功能及足细胞nephrin、podocin、desmin蛋白表达的影响。结果表明,BBR对高糖诱导的足细胞功能具有明显的保护作用,可明显促进足细胞增殖,抑制足细胞的凋亡和迁移,提高足细胞的黏附能力及足细胞上标志蛋白nephrin、podocin的表达,降低足细胞desmin蛋白的水平。
综上所述,本研究揭示了高糖能损伤足细胞的功能,促进足细胞的凋亡和迁移,BBR能明显改善高糖引起的足细胞损伤,其机制可能与调控足细胞特有的nephrin、podocin、desmin蛋白表达有关,具体机制有待进一步加以探究。
( 致谢: 本实验完成于安徽医科大学临床药理研究所实验室,实验过程中得到临床药理研究所全体老师和同学的帮助,在此表示感谢。)
| [1] | Wouters O J, O'Donoghue D J, Ritchie J, et al. Early chronic kidney disease: diagnosis, management and models of care[J]. Nat Rev Nephrol, 2015, 11(8): 491-502. doi:10.1038/nrneph.2015.85 |
| [2] | Leung W K, Gao L, Siu P M, et al. Diabetic nephropathy and endothelial dysfunction: current and future therapies, and emerging of vascular imaging for preclinical renal-kinetic study[J]. Life Sci, 2016, 166: 121-30. doi:10.1016/j.lfs.2016.10.015 |
| [3] | Mizuno T, Hayashi T, Kato R, et al. Risk factors for an early dialysis start in patients with diabetic nephropathy end-stage renal disease[J]. Ther Clin Risk Manag, 2014, 10: 73-6. |
| [4] | Gorriz J L, Martinez-Castelao A. Proteinuria: detection and role in native renal disease progression[J]. Transplant Rev (Orlando), 2012, 26(1): 3-13. doi:10.1016/j.trre.2011.10.002 |
| [5] | 李芮, 王会玲, 刘楠梅, 等. 小檗碱在高糖及糖基化终末产物诱导足细胞损伤中的保护作用[J]. 中华肾病研究电子杂志, 2016, 5(4): 168-71. Li R, Wang H L, Liu N M, et al. Protective effect of berberine on podocyte injury induced by high glucose and advanced glycation end products[J]. Chin J Nephrol, 2016, 5(4): 168-71. |
| [6] | Tang L Q, Wang F L, Zhu L N, et al. Berberine ameliorates renal injury by regulating G proteins-AC-cAMP signaling in diabetic rats with nephropathy[J]. Mol Biol Rep, 2013, 40(6): 3913-23. doi:10.1007/s11033-012-2468-0 |
| [7] | Li Z, Xu J, Xu P, et al. Wnt/β-catenin signalling pathway mediates high glucose induced cell injury through activation of TRPC6 in podocytes[J]. Cell Prolif, 2013, 46: 76-85. doi:10.1111/cpr.12010 |
| [8] | Liu Y. Newinsights into epithelial-mesenchymal transition in kidney fibrosis[J]. Am Soc Nephrol, 2010, 21(2): 212. doi:10.1681/ASN.2008121226 |
| [9] | 王竹, 刘俊田, 孙万森, 等. 祛风通络方对阿霉素肾病大鼠足细胞Desmin及CD2AP蛋白的影响[J]. 中国中西医结合杂志, 2014, 34(2): 203-8. Wang Z, Liu J T, Sun W S, et al. Effect of Qufeng Tongluo Recipe on expression of desmin and CD2AP proteins in adriamycin-induced nephropathy rats: an experiment alresearch[J]. Chin J Integr Trad West Med, 2014, 34(2): 203-8. |
| [10] | Wang Z, Liu J, Sun W. Effects of asiaticoside on levels of podocyte cytoskeletal proteins and renal slit diaphragm proteins in adriamycin-induced rat nephropathy[J]. Life Sci, 2013, 93(8): 352-8. doi:10.1016/j.lfs.2013.07.010 |
| [11] | Yang Y, Ni W J, Cai M, et al. The renoprotective effects of berberine via the EP4-Gαs-cAMP signaling pathway in different stages of diabetes in rats[J]. Recept Signal Transduct Res, 2014, 34(6): 445-55. doi:10.3109/10799893.2014.917324 |
| [12] | Tang L Q, Liu S, Zhang S T, et al. Berberine regulates the expression of E-prostanoid receptors in diabetic rats with nephropathy[J]. Mol Biol Rep, 2014, 41(5): 3339-47. doi:10.1007/s11033-014-3196-4 |
| [13] | 倪伟建, 丁海华, 唐丽琴, 等. 小檗碱对糖尿病肾病大鼠肾组织VEGF表达的影响[J]. 中国药理学通报, 2015, 31(6): 795-800. Ni W J, Ding H H, Tang L Q, et al. Effect of berberine on the expression of VEGF in renal tissue of diabetic nephropathy rats[J]. Chin Pharmacol Bull, 2015, 31(6): 795-800. |
文章信息
-
文章历史
- 收稿日期: 2018-03-16
- 修回日期: 2018-04-21
- 网络出版时间: 2018-07-02 13:54

