

2. 南昌大学 药学院药理重点实验室,江西 南昌 330006;
3. 南昌大学 江西省医学科学院,江西 南昌 330006
2. Key Lab of Pharmacology, School of Pharmaceutical Science, Nanchang University, Nanchang 330006, China;
3. Academy of Medical Sciences, Nanchang University, Nanchang 330006, China
血管平滑肌细胞(vascular smooth muscle cells, VSMCs)异常增殖和表型转化是高血压、动脉粥样硬化、血管成形术后狭窄等血管重构病变发生、发展的重要病理基础。缝隙连接蛋白43(connexin43,Cx43)是构成VSMCs间缝隙连接的主要连接蛋白,参与调节VSMCs功能。近年来的大量研究发现,Cx43表达异常增高是多种病理因素诱导VSMCs增殖的重要机制,而靶向抑制Cx43成为药物和基因手段改善血管重构的研究热点[1]。血管壁局部肾素-血管紧张素-醛固酮系统亢进导致的血管紧张素Ⅱ(angiotensin Ⅱ,Ang Ⅱ)增高,是诱导VSMCs增殖和表型转换的重要病理因素。研究表明,AngⅡ诱导的VSMCs功能改变与Cx43表达增高有关。在大鼠胸主动脉和人隐静脉平滑肌的研究均发现,Ang Ⅱ可剂量依赖性地上调Cx43表达。Alonso等[2]的研究进一步发现,AngⅡ可激活NF-κB途径,导致p65-NF-κB核转位,后者可与编码Cx43的Gja1基因启动子结合,从而促进Cx43表达。
吴茱萸作为传统中药,在临床上被应用了数千年,其主要有效成分吴茱萸次碱(rutaecarpine, Rut)具有广泛的心血管保护效应,如抗炎、抗血栓、舒血管等[3]。Rut作为一种天然产物提取物,可能通过多靶点发挥药理学作用,其中辣椒素受体(transient receptor potential vanilloid 1, TRPV1)被认为是Rut发挥心血管保护作用的重要靶点[3]。TRPV1广泛分布于血管组织中,血管内皮细胞和平滑肌细胞均有表达。我们实验室前期在血管内皮的研究中发现,Rut可抑制溶血性磷脂酰胆碱[4]和Ox-LDL诱导的内皮Connexin表达模式的改变,从而改善内皮功能[5],其机制与激活TRPV1有关。因此,本研究以大鼠胸主动脉平滑肌细胞为研究对象,探讨Rut对AngⅡ诱导的Cx43表达改变及VSMCs功能变化的影响,并探讨其机制是否涉及TRPV1/NF-κB途径。
1 材料与方法 1.1 药品与试剂Rut(纯度>99%,上海君拓生物技术有限公司);AngⅡ、TRPV1的竞争性拮抗剂辣椒卓平(Capsazepine,CAPZ),均购自美国Sigma公司;CCK-8(北京全式金生物技术有限公司);EdU检测试剂盒(广州锐博生物技术有限公司);α-平滑肌肌动蛋白(α-smooth muscle actin, α-SMA)和调宁蛋白(Calponin)抗体(Proteintech公司);Cx43和NF-κB p65抗体(CST公司);免疫细胞化学试剂盒(SP-9001,北京中杉金桥有限公司);抗Cyclin D1抗体、细胞周期试剂盒(江苏碧云天生物技术有限公司);BCA蛋白定量试剂盒、胞质/核蛋白提取试剂盒(北京普利莱生物技术有限公司)。
1.2 仪器酶联免疫检测仪、电泳仪和自动曝光仪(美国Bio-Rad公司);流式细胞仪(美国Becton Dickinson公司);荧光显微镜(日本Olympus公司)。
1.3 实验分组取大鼠胸主动脉,组织贴块法原代培养VSMCs,采用含10% FBS的DMEM培养基培养,传代后取3~8代用于后续实验。按实验目的加入不同的处理因素:①正常对照组(Control);②AngⅡ损伤组:加入AngⅡ(终浓度为1 μmol·L-1)孵育VSMCs 24 h;③~⑤Rut(低、中、高)保护组:加入Rut(终浓度为0.3、1.0、3.0 μmol·L-1)孵育VSMCs后,再加入AngⅡ继续孵育24 h;⑥CAPZ+Rut(H)组:用TRPV1受体阻断剂CAPZ(10 μmol·L-1)预处理细胞10 min后,再加入Rut(3.0 μmol·L-1)孵育10 min,后加入AngⅡ继续孵育24 h。
1.4 Western blot检测Cx43、Cyclin D1、α-SMA、Calponin蛋白表达水平裂解细胞并提取总蛋白样品,经BCA法蛋白定量,变性。制胶,上样,聚丙烯酰胺凝胶电泳,湿法转膜。5%的脱脂牛奶室温封闭2 h,与一抗(1:1 000稀释)结合,4℃孵育过夜。洗膜,与二抗结合(1:5 000稀释),室温孵育1 h。洗膜,加入ECL化学发光液于自动曝光仪下检测。使用Image J软件进行灰度分析,以β-actin或GAPDH的密度值为内参,计算相对密度,作为蛋白表达水平进行比较分析。
1.5 Western blot结合免疫细胞化学检测NF-κB p65核转位收集细胞至1.5 mL EP管,4℃、12 000 r·min-1离心5 min, 弃去PBS,于沉淀中加入100 μL CEB-A,剧烈振荡后冰浴15 min;于裂解物体积中加入5 μL CEB-B,冰浴1 min。4℃、12 000 r·min-1离心5 min,沉淀即是核粗提物,上清为粗制的胞质蛋白组分。将上清转入另一预冷的离心管,再次离心沉淀,取上清即是胞质蛋白组分。取上述核粗提物沉淀,加入100 μL CEB-A和5 μL CEB-B振荡,冰浴1 min,离心弃上清,重复此步骤。在离心沉淀中加入100 μL预冷的NEB,冰浴30 min,离心,取上清即为核蛋白组分。其余步骤同“1.4”。
免疫细胞化学:4%多聚甲醛固定细胞30 min,PBS清洗3次;3%过氧化氢37℃孵育10 min,PBS清洗3次;正常羊血清工作液37℃孵育10 min;NF-κB p65(1:100稀释)一抗4℃孵育过夜。加入二抗于37℃孵育15 min;链霉素卵白素工作液37℃孵育15 min;加入新配制的DAB溶液2 min后,于显微镜下观察细胞着色情况。
1.6 CCK-8和EdU试剂盒检测VSMCs增殖 1.6.1 CCK-8法将VSMCs消化后制成单细胞悬液,以每孔5×105个细胞均匀接种于96孔板,每孔200 μL,每组6个复孔,同时设置调零孔(只加等体积培养基,不加细胞)。24 h后向各孔加入20 μL的CCK-8试剂,在细胞培养箱中避光继续孵育1~4 h,终止培养,在450 nm波长处用酶标仪检测各孔吸光度。细胞活力(OD)=样品吸光度值-调零孔。
1.6.2 EdU标记法用无血清培养基按1 000:1稀释EdU试剂A;各组加入100 μL孵育2 h;4%多聚甲醛室温固定30 min;于各孔加入2×10-3 mg·L-1甘氨酸溶液,5 min后用PBS洗3次;加入1×Apollo染色液100 μL,避光孵育30 min,弃去,加入100 μL通透液,室温10 min;加入甲醇100 μL,清洗2次;制备适量1×Hoechst 33342反应液,各孔加入100 μL,避光孵育30 min,PBS洗3次;染色结束后,立刻于显微镜下拍照记录。
1.7 流式细胞术测定VSMCs细胞周期变化胰酶消化并收集细胞,转移到离心管,2 000×g离心5 min沉淀细胞。PBS洗涤2次,离心除上清。用70%乙醇于4℃固定过夜。再次离心沉淀细胞,PBS清洗去上清,最后向各管加入0.5 mL PI,轻轻吹打细胞沉淀,使之与染料充分接触,37℃水浴避光孵育30 min,转移至流式管,立即用流式细胞仪检测。
1.8 统计学方法实验数据均以x±s表示,组间数据比较采用单因素方差分析。
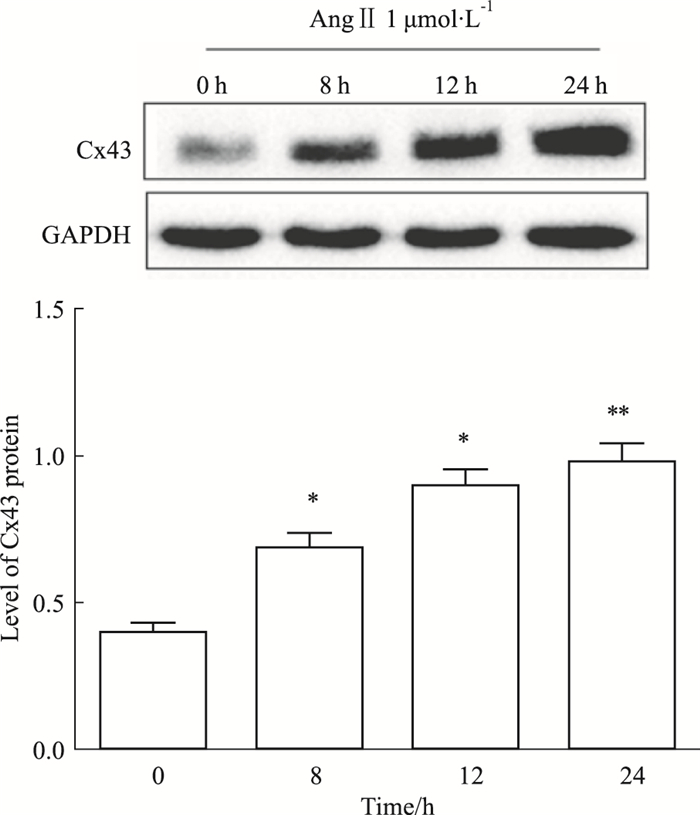
2 结果 2.1 AngⅡ对平滑肌细胞Cx43蛋白表达的影响Fig 1的Western blot结果显示,AngⅡ孵育VSMCs可时间依赖性上调Cx43的表达,8 h时Cx43水平明显上调,24 h作用最为明显(P<0.01)。
|
| Fig 1 Effect of AngⅡ treatment on expression of Cx43 in VSMCs(x±s, n=3) *P < 0.05, **P < 0.01 vs control group |
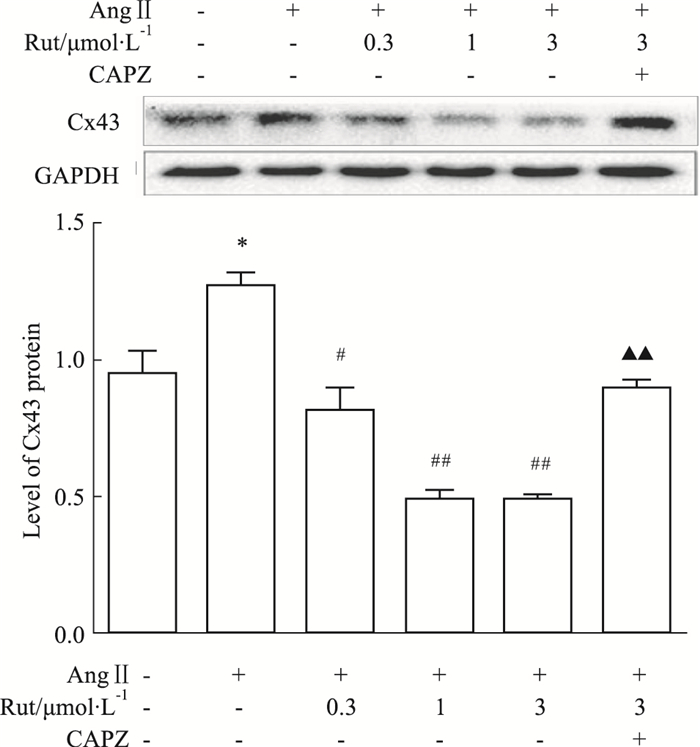
如Fig 2所示,不同浓度的Rut均能明显抑制AngⅡ诱导的Cx43表达上调,预先给予TRPV1阻断剂CAPZ可取消这一效应(P<0.01)。
|
| Fig 2 Effect of Rut on expression of Cx43 induced by AngⅡ(x±s, n=3) *P < 0.05 vs control group; #P < 0.05, ##P < 0.01 vs AngⅡ group; ▲▲P < 0.01 vs AngⅡ+Rut (3 μmol·L-1) group |
Fig 3A的Western blot结果显示,Ang Ⅱ孵育细胞4 h可明显增加细胞核中NF-κB p65的水平,胞质中NF-κB p65水平则下降。不同浓度的Rut能剂量依赖性抑制AngⅡ诱导的p65入核,CAPZ可取消Rut这一效应(P<0.05)。免疫细胞化学结果显示,AngⅡ孵育细胞4 h可明显促进NF-κB p65蛋白从细胞质转位到细胞核,Rut(3.0 μmol·L-1)能在一定程度上抑制其入核,该效应可被CAPZ所阻断(Fig 3B)。

|
| Fig 3 Possible mechanism of Rut in down-regulation of Cx43(x±s, n=3) A:Rut inhibited p65 transposition induced by AngⅡ using Western blot; B:Rut inhibited cytoplasm p65 transfer to nucleus induced by AngⅡ using immunocytochemistry.*P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs Ang Ⅱ group; ▲P < 0.05 vs AngⅡ+Rut (3 μmol·L-1) group. |
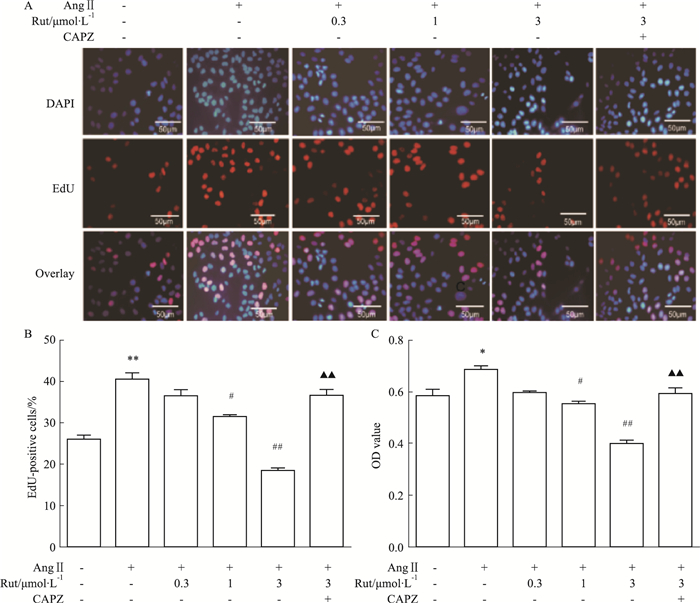
Fig 4的EdU结果显示,AngⅡ可增加VSMCs的EdU阳性细胞百分率(P<0.01),不同浓度的Rut可抑制增殖期阳性细胞数量,该效应可被TRPV1受体阻断剂CAPZ(10 μmol·L-1)阻断(P<0.01)。CCK-8结果显示,AngⅡ孵育细胞24 h可明显促进VSMCs增殖(P<0.05),不同浓度的Rut可剂量依赖性减少AngⅡ诱导的细胞增殖,预先给予CAPZ可取消Rut的这一效应(P<0.01)。
|
| Fig 4 Effects of Rut on proliferation of VSMCs induced by AngⅡ(x±s, n=6) A:The cell proliferation result by EdU staining; B:Analysis of the percentage of EdU-positive cells; C:Cell viability result detected by CCK-8. *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs AngⅡ group; ▲▲P < 0.01 vs AngⅡ+Rut (3 μmol·L-1) group. |
Fig 5的流式细胞周期结果显示,AngⅡ可增加增殖期细胞(S期+G2/M期)的比例(P<0.05)。Rut(3.0 μmol·L-1)可明显降低AngⅡ诱导的增殖期VSMCs比例(P<0.01),该效应可被CAPZ所取消(P<0.05)。Western blot结果显示,AngⅡ可上调细胞周期蛋白Cyclin D1的表达,Rut可明显抑制Ang Ⅱ诱导的Cyclin D1表达上调(P<0.01),CAPZ可取消Rut的这一作用(P<0.01)。

|
| Fig 5 Effect of Rut on VSMCs cell cycle induced by AngⅡ(x±s, n=3) A:Cell cycle distribution detected by flow cytometry; B:Analysis of each phase percentages of cell cycle; C:The expression of cell cycle related protein Cyclin D1 by Western blot. *P < 0.05 vs control group; ##P < 0.01 vs AngⅡ group; ▲P < 0.05, ▲▲P < 0.01 vs AngⅡ+Rut (3 μmol·L-1) group. |
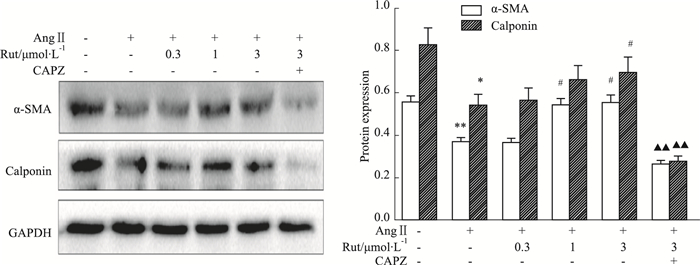
如Fig 6所示,加入AngⅡ孵育48 h后,VSMCs细胞表面收缩型标志蛋白α-SMA和Calponin表达均降低,Rut可部分恢复二者的表达水平,该效应可被CAPZ阻断(P<0.01)。
|
| Fig 6 Effect of Rut on VSMCs phenotype transformation by AngⅡ using Western blot(x±s, n=3) *P < 0.05, **P < 0.01 vs control group; #P < 0.05 vs AngⅡ group; ▲▲P < 0.01 vs AngⅡ+Rut (3 μmol·L-1) group |
Rut是传统降压药吴茱萸的主要有效成分,Qin等[6]在研究Rut的降压机制时发现,Rut可改善高血压导致的阻力血管的重构。最近有研究报道,Rut还可抑制AngⅡ诱导的VSMCs增殖[7],但具体机制未明。Cx43是构成VSMCs间缝隙连接的主要蛋白,参与调控VSMCs功能,被认为是改善血管重构的重要靶点[8-9]。国外学者在培养的人隐静脉平滑肌细胞和大鼠胸主动脉平滑肌细胞均发现,AngⅡ诱导的VMSCs功能改变与上调Cx43表达有关[2, 10]。我们在大鼠胸主动脉VSMCs也证实,AngⅡ (1.0 μmol·L-1)可明显上调Cx43的表达,而不同浓度的Rut均可抑制AngⅡ诱导的Cx43表达增加。这提示Rut可能通过抑制Cx43的表达,改善VSMCs功能。Rut是TRPV1的部分激动剂[11],其主要心血管效应均与激活TRPV1有关[12]。本实验发现,Rut抑制Cx43表达的作用可被TRPV1竞争性阻断剂CAPZ所阻断,提示TRPV1介导了Rut调节Cx43的作用。
Alonso等[2]在培养的大鼠胸主动脉VSMCs中发现,AngⅡ上调Cx43的表达与促进NF-κB亚基p65核转位有关,主要证据如下:大鼠编码Cx43的Gja1基因启动子的-312~-301 bp有NF-κB的结合区,荧光报告基因结果显示,AngⅡ可促进NF-κB和该启动区的结合,而ChIP结果证实,AngⅡ激活启动子的效应可被NF-κB抗体所取消。本实验采用Western blot及免疫细胞化学结果均显示,AngⅡ诱导的VSMCs在4 h即可促进p65由细胞质转移到细胞核,而不同浓度的Rut可抑制AngⅡ诱导的p65核转位,预先给予CAPZ可取消Rut的作用。以上结果提示,Rut激活TRPV1下调Cx43表达的作用,可能与抑制AngⅡ诱导的NF-κB的激活有关。
在人大隐静脉VSMCs的研究中发现,过表达Cx43可明显促进人VSMCs的增殖能力,而敲除Cx43则抑制AngⅡ诱导的VSMCs增殖和细胞周期蛋白Cyclin E的表达上调[10],提示AngⅡ诱导的VSMCs增殖与Cx43表达上调有关。本实验进一步证实,Rut可抑制AngⅡ诱导的VSMCs增殖,表现为逆转AngⅡ诱导的VSMCs内的DNA合成增加及细胞活力升高。细胞周期结果显示,AngⅡ可导致增殖期(S+G2/M期)细胞的比例增加,伴随细胞周期蛋白Cyclin D1水平增加,后者作为细胞周期正性调节因子可促进细胞增殖。而Rut可明显抑制Cyclin D1的表达上调和AngⅡ诱导的细胞周期转换,预先给予CAPZ可阻断Rut的这些抗增殖效应。由此我们推论,Rut可抑制AngⅡ诱导的VSMCs增殖,其机制至少部分与激活TRPV1,抑制有促增殖效应的Cx43的表达有关。
VSMCs表型转换是导致VSMCs功能异常的重要原因,本实验发现,加入AngⅡ孵育后,VSMCs的收缩型标志蛋白α-SMA和Calponin表达降低,说明AngⅡ促进VSMCs由收缩表型转变为合成表型。而Rut可部分恢复两种标志蛋白的表达,其效应被CAPZ所阻断。Rut这种抑制VSMCs表型转换的作用也可能与Cx43有关,已有研究表明Cx43参与调节VSMCs的表型转换[13]。在猪冠状动脉平滑肌中也发现,过表达Cx43可下调收缩型标志蛋白α-SMA和Calponin的表达,敲除Cx43则产生相反的作用[14]。
综上所述,本研究结果表明,Rut通过下调Cx43的表达,抑制AngⅡ诱导的VSMCs增殖和表型转化,其机制涉及TRPV1/NF-κB信号途径。
| [1] | Longchamp A, Allagnat F, Alonso F, et al. Connexin43 inhibition prevents human vein grafts intimal hyperplasia[J]. PLoS One, 2015, 10(9): e0138847. doi:10.1371/journal.pone.0138847 |
| [2] | Alonso F, Krattinger N, Mazzolai L, et al. An angiotensin Ⅱ- and NF-kappaB-dependent mechanism increases connexin 43 in murine arteries targeted by renin-dependent hypertension[J]. Cardiovasc Res, 2010, 87(1): 166-76. doi:10.1093/cvr/cvq031 |
| [3] | Son J K, Chang H W, Jahng Y. Progress in studies on rutaecarpine. Ⅱ.--Synthesis and structure-biological activity relationships[J]. Molecules, 2015, 20(6): 10800-21. doi:10.3390/molecules200610800 |
| [4] | 刘勇, 余艳荣, 彭维杰, 等. 吴茱萸次碱改善溶血性磷脂酰胆碱诱导的内皮细胞缝隙连接细胞间通讯功能障碍[J]. 中国药理学通报, 2013, 29(11): 1514-9. Liu Y, Yu Y R, Peng W J, et al. Rutaecarpine improves dysfunction of gap junctional intercellular communication induced by hemolytic phosphatidylcholine in endothelial cells[J]. Chin Pharmacol Bull, 2013, 29(11): 1514-9. doi:10.3969/j.issn.1001-1978.2013.11.010 |
| [5] | Peng W J, Liu Y, Yu Y R, et al. Rutaecarpine prevented dysfunction of endothelial gap junction induced by Ox-LDL via activation of TRPV1[J]. Eur J Pharmacol, 2015, 756: 8-14. doi:10.1016/j.ejphar.2015.02.051 |
| [6] | Qin X P, Zeng S Y, Tian H H, et al. Involvement of prolylcarboxypeptidase in the effect of rutaecarpine on the regression of mesenteric artery hypertrophy in renovascular hypertensive rats[J]. Clin Exp Pharmacol Physiol, 2009, 36(3): 319-24. doi:10.1111/cep.2009.36.issue-3 |
| [7] | 李艳菊, 张锋, 龚其海, 等. 吴茱萸次碱抑制血管紧张素Ⅱ诱导的大鼠血管平滑肌细胞增殖[J]. 中国结合医学杂志, 2014, 20(9): 682-7. Li Y J, Zhang F, Gong Q H, et al. Rutaecarpine inhibits angiotensin Ⅱ-induced proliferation in rat vascular smooth muscle cells[J]. Chin J Integr Med, 2014, 20(9): 682-7. |
| [8] | Shi Y, Hou X, Zhang X, et al. Inhibition of oxidized-phospholipid-induced vascular smooth muscle cell proliferation by resveratrol is associated with reducing Cx43 phosphorylation[J]. J Agric Food Chem, 2013, 61(44): 10534-41. doi:10.1021/jf4036723 |
| [9] | Lin Y C, Chiang C H, Chang L T, et al. Simvastatin attenuates the additive effects of TNF-alpha and IL-18 on the connexin 43 up-regulation and over-proliferation of cultured aortic smooth muscle cells[J]. Cytokine, 2013, 62(3): 341-51. doi:10.1016/j.cyto.2013.04.003 |
| [10] | Jia G, Cheng G, Gangahar D M, et al. Involvement of connexin 43 in angiotensin Ⅱ-induced migration and proliferation of saphenous vein smooth muscle cells via the MAPK-AP-1 signaling pathway[J]. J Mol Cell Cardiol, 2008, 44(5): 882-90. doi:10.1016/j.yjmcc.2008.03.002 |
| [11] | Wang S, Yamamoto S, Kogure Y, et al. Partial activation and inhibition of TRPV1 channels by evodiamine and rutaecarpine, two major components of the fruits of Evodia rutaecarpa[J]. J Nat Prod, 2016, 79(5): 1225-30. doi:10.1021/acs.jnatprod.5b00599 |
| [12] | Jia S, Hu C. Pharmacological effects of rutaecarpine as a cardiovascular protective agent[J]. Molecules, 2010, 15(3): 1873-81. doi:10.3390/molecules15031873 |
| [13] | Li H, Xiang Y, Fan L J, et al. Myocardin inhibited the gap protein connexin 43 via promoted miR-206 to regulate vascular smooth muscle cell phenotypic switch[J]. Gene, 2017, 616: 22-30. doi:10.1016/j.gene.2017.03.029 |
| [14] | Zhang X, Wang X, Zhou X, et al. Phenotypic transformation of smooth muscle cells from porcine coronary arteries is associated with connexin 43[J]. Mol Med Rep, 2016, 14(1): 41-8. doi:10.3892/mmr.2016.5286 |

