


2. 齐鲁工业大学(山东省科学院), 山东省科学院生物研究所, 山东省生物检测技术工程实验室, 山东省生物传感器重点实验室, 山东省科学院药物筛选重点实验室, 山东 济南 250014
 ,
HAN Li-wen2,
ZHANG Yun2,
HAN Jian2,
HOU Hai-rong2,
WANG Xi-min2,
LIU Ke-chun2,
TIAN Qing-ping1
,
HAN Li-wen2,
ZHANG Yun2,
HAN Jian2,
HOU Hai-rong2,
WANG Xi-min2,
LIU Ke-chun2,
TIAN Qing-ping1
 ,
HE Qiu-xia2
,
HE Qiu-xia2

2. Biology Institute, Qilu University of Technology (Shandong Academy of Sciences), Shandong Provincial Engineering Laboratory for Biological Testing Technology, Key Laboratory for Biosensor of Shandong Province, Key Laboratory for Drug Screening Technology of Shandong Academy of Sciences, Jinan 250014, China
氯氮平是一种非典型抗精神病药物,对于精神分裂症患者具有明显的疗效,并且减少了导致锥体外系运动障碍的倾向。自1961年上市以来,因为副作用,氯氮平一直饱受争议。氯氮平毒性机制研究的结论不一致。最初报道的副作用是粒细胞缺乏症,最近几年集中在心脏毒性。氯氮平引起的心脏毒性报道最多的是心肌炎[1],扩张型心肌病和心包炎也有报道。严重的心脏副作用不仅影响了氯氮平对患者的治疗效果,还限制了其广泛应用。临床数据显示,受感染患者的心内膜心肌活检标本中可以观察到嗜酸性粒细胞和嗜酸性包涵体。因此,很多研究认为,IgE介导的超敏反应是氯氮平心脏毒性的原因。此外,Elman等[2]发现,相比其他抗精神病药物,氯氮平治疗患者血浆的去甲肾上腺素水平升高,这可致左心室功能障碍。其他可能的氯氮平心脏毒性机制包括细胞色素P450 1A2、1A3酶缺乏,钙依赖性离子通道的阻断,以及低硒水平[3]。探索其心脏毒性发生的机制既有利于解释氯氮平产生心肌炎、心包炎的原因,又可为进一步寻找保护心脏损伤的药物提供参考。
斑马鱼是近年来广受关注的整体模式生物,其基因组编码序列与人类基因组的同源性为87%左右。斑马鱼的生物学结构和功能与哺乳动物高度相似,具有繁殖能力强、体积小、成本低、发育周期短、胚胎透明、体外发育等特点,广泛应用于药物活性筛选[4]、模型构建和毒理学[5]评价中。发育早期的斑马鱼胚胎透明,研究人员可以清晰地观察到斑马鱼的心跳以及血液循环,直观评估其心率、收缩性、节律性和形态变化[6]。因此,本研究采用斑马鱼作为模式生物,旨在揭示氯氮平心脏毒性的反应和发生机制,为氯氮平临床安全用药提供实验依据。
1 材料与方法 1.1 试剂与仪器氯氮平(批号076M4128V)、吖啶橙(acridine orange,AO,批号A6014)均购自Sigma-Aldrich公司;PrimeScriptTM RT reagent Kit with gDNA Eraser cDNA合成试剂盒购自TaKaRa公司;SYBR® Green PCR Master Mix荧光定量PCR反应试剂盒购自Vazyme公司;PCR引物由上海捷瑞生物工程有限公司合成。HPG-280BX型光照培养箱(哈尔滨市东联电子技术开发有限公司);斑马鱼养殖饲养设备(北京爱生科技公司);奥林巴斯SZX16型荧光体视显微镜、IX51奥林巴斯倒置显微镜(日本OLYMPUS公司);LightCycler® 96型实时荧光定量PCR仪(瑞士Roche公司)。
1.2 实验动物野生型AB系斑马鱼,由山东省科学院生物研究所药物筛选重点实验室提供,养殖和繁殖方法参照相关文献[7]。将斑马鱼放在水温为28℃的鱼缸中饲养,光照周期为14 h光照和10 h黑暗。成鱼的食物为卤虫的无节幼体,每天喂食两次。日常饲养过程中,♀♂斑马鱼分开喂养,在需要收集胚胎时将♀♂斑马鱼按照1 :2或1 :1的比例放入交配缸中。于次日早上抽去隔板,利用光照刺激交配反射,抽去隔板1~2 h后,收集受精卵,并用胚胎培养水(5 mmol·L-1 NaCl、0.17 mmol·L-1 KCl、0.14 mmol·L-1 CaCl2、0.16 mmol·L-1 MgSO4)清洗3遍,除去斑马鱼排泄物和死卵,健康胚胎放入28.5℃恒温光照培养箱(HPG-280BX型)中继续孵育,在受精24 h后于显微镜下挑选发育正常的胚胎,备用。
1.3 方法 1.3.1 氯氮平的急性毒性检测将发育正常的24 hpf斑马鱼胚胎随机地吸到6孔培养板中,每孔30个,加入不同浓度的氯氮平工作液(12.5、25、37.5、50、62.5、75、80、100 μmol·L-1),同时设置0.1% DMSO的溶剂对照组,实验重复3次。在48、72、96 hpf时分别于倒置荧光显微镜下观察斑马鱼的心率、心包水肿情况,并在SZX16型体式荧光显微镜下对各组进行形态学拍照。
1.3.2 细胞凋亡检测使用AO染色试剂检测氯氮平诱导的心肌细胞凋亡。AO是一种荧光色素染料,能透过细胞膜。正常细胞染色后呈现均一的绿色,凋亡细胞则呈现致密或颗粒状的黄绿色[8]。随机选择15条72 hpf和96 hpf斑马鱼胚胎,加入终浓度为25 mg·L-1的AO溶液,于28℃培养箱中孵育50 min,后用PBS冲洗3遍,在体式荧光显微镜下进行拍照,利用Image-Pro Plus软件统计心脏部位阳性细胞。
1.3.3 RNA提取和实时定量PCR分别在氯氮平处理24、48、72 h时收集鱼卵样本,按照纳米磁珠法RNA提取试剂盒说明书抽提各处理组的总RNA,对与凋亡相关的基因表达进行分析,包括抑制凋亡基因Bcl-2、促凋亡基因Bax、caspase家族(caspase-3和caspase-9)。按照试剂盒说明书进行操作,取1 μg RNA合成cDNA,并进行定量PCR检测,引物序列见Tab 1。以β-actin作为内参,实验数据以2-ΔΔCt方法进行分析。
| Gene | Primer sequence (5′-3′) |
| β-actin | F: AGAGCTATGAGCTGCCTGACG |
| R: CCGCAAGATTCCATACCCA | |
| Bcl-2 | F: TCACTCGTTCAGACCCTCAT |
| R: ACGCTTTCCACGCACAT | |
| Bax | F: GGCTATTTCAACCAGGGTTCC |
| R: TGCGAATCACCAATGCTGT | |
| Caspase-9 | F: CTGAGGCAAGCCATAATCG |
| R: AGAGGACATGGGAATAGCGT | |
| Caspase-3 | F: CCGCTGCCCATCACTA |
| R: ATCCTTTCACGACCATCT |
实验数据均用x±s表示,采用SPSS 23.0统计软件进行单因素方差分析(One-Way ANOVA),以LSD法进行组间的两两比较。
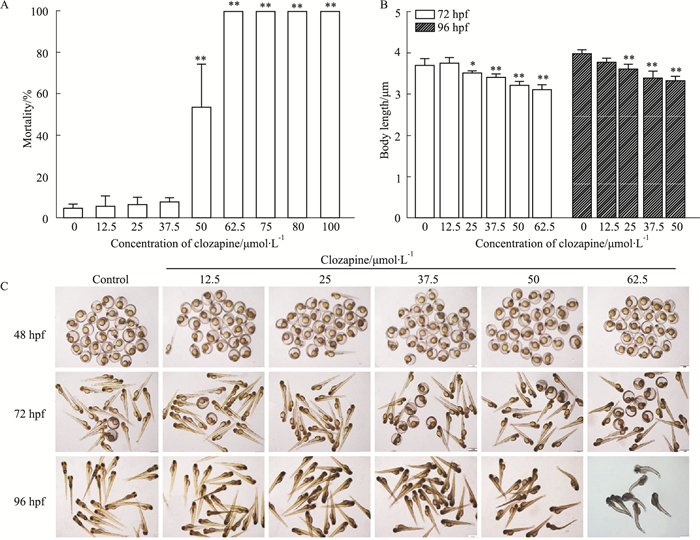
2 结果 2.1 氯氮平对斑马鱼胚胎死亡率及形态学的作用如Fig 1A所示,氯氮平处理72 h后,随着药物浓度的增加,斑马鱼幼鱼的死亡率逐渐增加;62.5 μmol·L-1的氯氮平导致斑马鱼全部死亡。氯氮平处理72 h的LC50值约为50 μmol·L-1。形态学检测表明,氯氮平可剂量依赖地诱导斑马鱼出现体长缩短(Fig 1B)、心包水肿(Fig 1C)等毒性表型。氯氮平处理48 h后,37.5 μmol·L-1及以上浓度的斑马鱼胚胎体长明显缩短,与溶剂对照组相比差异具有显著性(P < 0.01)。
|
| Fig 1 The mortality and morphologic response of zebrafish embryo to clozapine treatment A:The mortality of zebrafish embryos exposed to different concentrations of clozapine at 96 hpf (x±s, n=30);B:Effect of clozapine on the body length of zebrafish embryos(x±s, n=15);C:Effect of clozapine on embryonic morphological changes.*P < 0.05, **P < 0.01 vs control. |
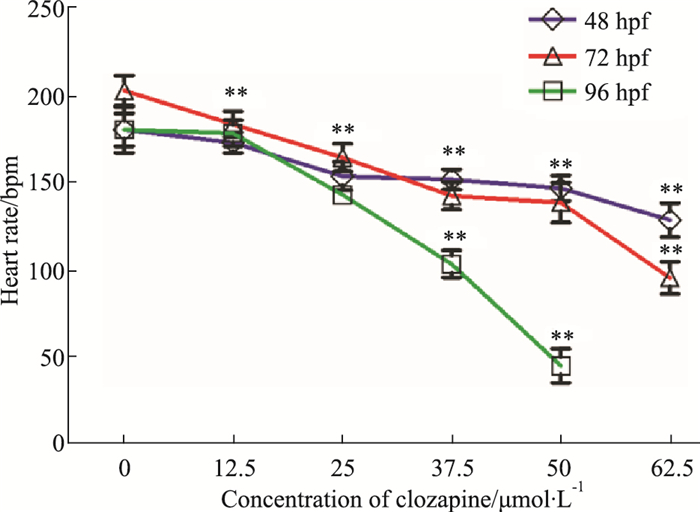
如Fig 2所示,经氯氮平处理24、48、72 h后,暴露于25 μmol·L-1及以上浓度的斑马鱼胚胎的心率明显降低。在72 h时,暴露于50 μmol·L-1浓度氯氮平的斑马鱼每分钟心率值为对照组的25%。
|
| Fig 2 Effect of clozapine on heart rate of zebrafish embryos (x±s, n=15) **P < 0.01 vs control |
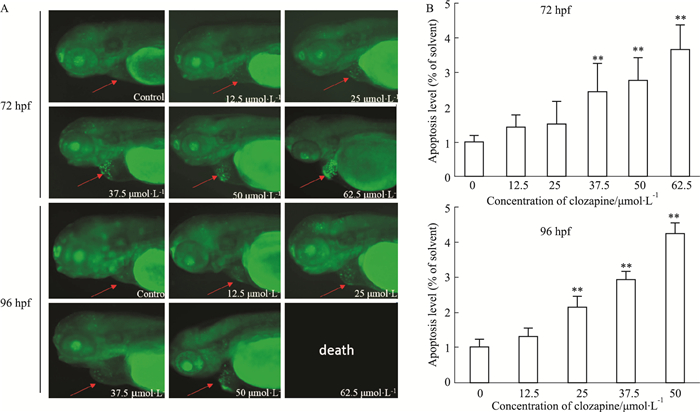
AO染色的结果如Fig 3所示,对照组的斑马鱼心脏部位没有细胞发生凋亡,但暴露于37.5、50、62.5 μmol·L-1的氯氮平后,胚胎心肌细胞开始出现凋亡,凋亡细胞数量增多现象具有剂量依赖性。
|
| Fig 3 Effect of clozapine on apoptosis of cardiomyocyte cell in zebrafish(x±s, n=15) A:Fluorescence photographs of all groups stained with AO; B:The ratio of the number of apoptosis myocardial cells in clozapine exposed groups and the control group. **P < 0.01 vs control. |
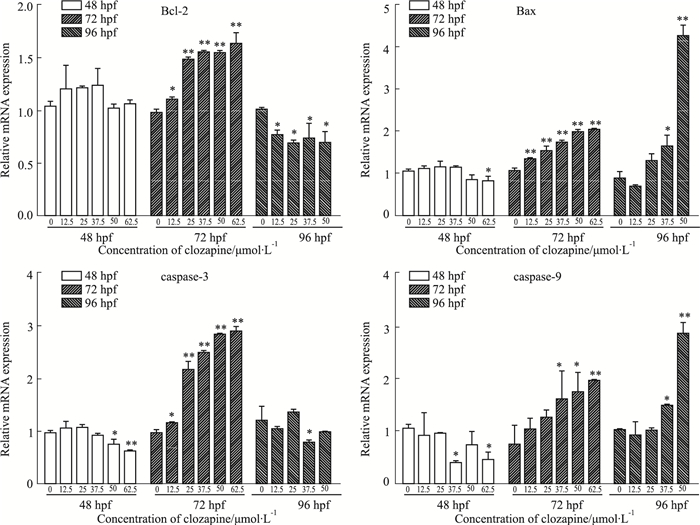
氯氮平处理斑马鱼胚胎24、48、72 h后分别收集胚胎,提取总mRNA,利用qPCR技术检测凋亡相关基因的表达。如Fig 4、Tab 2所示,与对照组相比,经氯氮平处理24 h后,胚胎细胞Bcl-2与Bax表达比值不变;处理48 h后,各组细胞Bax和Bcl-2表达水平均升高,但Bcl-2与Bax的比值不变;72 h后,各组细胞Bcl-2表达水平明显降低,氯氮平(37.5、50 μmol·L-1)处理组细胞Bax表达水平上调,Bcl-2/Bax比值降低。此外,药物处理48 h后,caspase-3和caspase-9的表达水平明显上调;72 h后,caspase-9表达水平仍然升高,而caspase-3逐渐恢复正常。
|
| Fig 4 Effect of clozapine on the mRNA expression of apoptosis-related genes(x±s, n=5) *P < 0.05, **P < 0.01 vs control |
| Concentration of clozapine/μmol·L-1 |
Bcl-2/Bax | ||
| 48 hpf | 72 hpf | 96 hpf | |
| 0 | 0.99±0.010 | 0.93±0.100 | 1.19±0.266 |
| 12.5 | 1.08±0.127 | 0.82±0.024 | 1.10±0.076 |
| 25 | 1.06±0.145 | 0.98±0.101 | 0.53±0.093** |
| 37.5 | 1.09±0.133 | 0.90±0.044 | 0.46±0.161** |
| 50 | 1.21±0.201 | 0.78±0.011 | 0.16±0.015** |
| 62.5 | 1.30±0.108 | 0.80±0.047 | - |
| **P < 0.01 vs control | |||
氯氮平是20世纪60年代末出现的第一种非典型抗精神病药物,其对大脑内5-羟色胺受体和多巴胺受体具有较强的阻滞作用,能缓解患者的幻觉、妄想、兴奋躁动等症状,尤其对难治性精神分裂症具有独特疗效[8]。有文献表明,精神病患者在治疗期间长期服用氯氮平会引起心肌酶水平的变化,其中以肌酸激酶(creatine kinase,CK)升高最为明显[9]。CK相比其他酶对心肌缺血和心内膜下心肌梗死的诊断更灵敏,急性心梗时,血清CK活力明显升高。临床病例报道,患者服用氯氮平第3周后,出现心包、胸膜的渗出性反应,停药后该不良反应消失,排除其他感染性原因后,考虑可能是由患者的个体敏感性引起的,故在临床应用氯氮平时应慎重[10]。
斑马鱼的心脏是第一个发育和发挥功能的器官,于22 h开始跳动,48 h心血管基本结构形成,并表现出一系列复杂的离子通道和代谢过程。斑马鱼胚胎透明,可以在活体上直接观察其心脏的形状、大小,并可记录心率,在心血管毒性评价研究方面优势明显[11]。利用斑马鱼胚胎,研究人员对阿司咪唑的心脏毒性进行了研究,揭示了其潜在的心脏毒性副作用,证明了斑马鱼是一种有效、可靠的可快速检测化合物心脏毒性的模式生物[12]。心率变化是评价心脏毒性的一个重要指标。本实验发现,氯氮平处理后,斑马鱼胚胎心脏功能受损,心率下降明显,而且出现严重的心包水肿,体长缩短的畸形变化,这与文献中抗精神病药物引起心脏毒性的结果一致[13]。
AO染色实验证明,氯氮平诱导了斑马鱼心脏细胞凋亡。定量PCR结果也表明,给药72 h后,斑马鱼胚胎细胞Bcl-2表达降低,Bax表达升高,Bcl-2/Bax比值明显下降。Bcl-2和Bax都属于Bcl-2基因家族,Bcl-2具有抑制心肌细胞凋亡作用,Bax具有促进心肌细胞凋亡作用。当发生凋亡时,Bcl-2/ Bax比值会下降,导致细胞色素C从线粒体释放,进而激活caspase-9和caspase-3,诱导心肌细胞凋亡。本实验中caspase-9的表达也出现升高趋势,而caspase-3表达随作用时间的延长呈现先升高后降低的趋势,这可能与体内存在的代谢补偿机制有关。以上结果表明,氯氮平是通过调控Bcl-2家族基因表达,激活caspase-3和caspase-9基因表达上调而诱导斑马鱼心肌细胞凋亡。氯氮平诱导斑马鱼细胞凋亡致心脏毒性的结果与已有报道一致。据报道,氯氮平处理后的鼠血清CK同工酶和乳酸脱氢酶水平会明显升高,同时TNF-α、MDA、NO、8-羟基脱氧鸟苷、caspase-3、NF-κB的释放量也是增加的,这说明氧化应激、基因损伤和凋亡机制参与到了氯氮平产生心脏毒性的过程[14]。接下来,我们将开展氯氮平导致斑马鱼氧化应激方面的研究。
综上,本实验采用斑马鱼模式生物对氯氮平的不良反应进行了研究,发现氯氮平导致斑马鱼胚胎出现严重的心脏毒性,一些表型如心率下降和水肿与临床表现类似。鉴于氯氮平对于治疗难治性精神失常的明显疗效,临床上仍广泛使用。药物的心脏毒性作用在心电图上会有预示[15],故使用氯氮平时应严密监测患者心电图。通过实时观察服药后的症状,及时通过心电图来预测心脏病变,可以在一定程度上弥补氯氮平的不良反应,继续发挥其治疗精神疾病的优势效果。斑马鱼胚胎的心电图报道很少,在未来研究中,我们拟增加心电图指标,检测药物心脏毒性。利用斑马鱼模型研究氯氮平的毒性反应和毒性机制,可为寻找缓解或者拮抗其副作用的药物,提供实验证据。今后的研究,可从联合用药角度,筛选保持其疗效,同时降低心脏毒性的药物,提高其用药安全性,为氯氮平临床使用提供更多实验证据。
( 致谢: 本实验在山东省科学院生物研究所药物筛选重点实验室完成,感谢本实验的参加人员。)
| [1] | Khan A A, Ashraf A, Baker D, et al. Clozapine and incidence of myocarditis and sudden death-long term Australian experience[J]. Int J Cardiol, 2017, 238: 136-9. doi:10.1016/j.ijcard.2017.03.013 |
| [2] | Elman I, Goldstein D S, Eisenhofer G, et al. Mechanism of peripheral noradrenergic stimulation by clozapine[J]. Neuropsychopharmacology, 1999, 20: 29-34. doi:10.1016/S0893-133X(98)00047-5 |
| [3] | Layland J J, Liew D, Prior D L. Clozapine-induced cardiotoxicity: a clinical update[J]. Med J Aust, 2009, 190(4): 190-2. |
| [4] | 王雪, 刘可春, 王希敏, 等. 大黄酸对马兜铃酸A引起的斑马鱼肾脏损伤的保护作用[J]. 中国药理学通报, 2016, 32(3): 361-5. Wang X, Liu K C, Wang X M, et al. Protective effect of rhein on aristolochic acid-induced renal injury in zebrafish[J]. Chin Pharmacol Bull, 2016, 32(3): 361-5. |
| [5] | 许冰洁, 张立将, 李春启, 等. 斑马鱼胚胎评价5种药物的发育毒性与模型验证[J]. 中国药理学通报, 2016, 32(1): 74-9. Xu B J, Zhang L J, Li C Q, et al. Model validation and evaluation of developmental toxicity of five drugs using zebrafish embryos[J]. Chin Pharmacol Bull, 2016, 32(1): 74-9. |
| [6] | McGrath P, Li C Q. Zebrafish: a predictive model for assessing drug-induced toxicity[J]. Drug Discov Today, 2008, 13(9): 394-401. |
| [7] | Westerfield M, Wegner J, Jegalian B G. Specific activation of mammalian Hox promoters in mosaic transgenic zebrafish[J]. Genes Dev, 1992, 6(4): 591-8. doi:10.1101/gad.6.4.591 |
| [8] | 罗涛, 万普蓉, 张咏梅, 等. 氯氮平急性中毒的临床表现和处理[J]. 临床精神医学杂志, 2017, 27(1): 68-9. Luo T, Wan P R, Zhang Y M, et al. Clinical manifestation and management of acute poisoning by clozapine[J]. J Clin Psychiatry, 2017, 27(1): 68-9. |
| [9] | 张洁, 张宝生, 田韶辉, 等. 长期服用氯氮平对患者心肌酶的影响[J]. 中国民族民间医药, 2014, 23(7): 88-9. Zhang J, Zhang B S, Tian S H, et al. Long-term use of clozapine myocardial enzymes in patients with the result analysis[J]. Chin J Ethnomed Ethnopharm, 2014, 23(7): 88-9. |
| [10] | 赵芳霞, 王怀海, 何宏. 氯氮平致心包与胸腔积液1例[J]. 临床精神医学杂志, 2010, 20(6): 382. Zhao F X, Wang H H, He H. 1 case of pericardial effusion and pleural effusion caused by clozapine[J]. J Clin Psychiatry, 2010, 20(6): 382. |
| [11] | 韩利文, 赵亮, 楚杰, 等. 采用GC-MS代谢组学技术表征阿司咪唑诱导斑马鱼心脏毒性的内源性代谢物[J]. 中国药学杂志, 2015, 50(1): 45-50. Han L W, Zhao L, Chu J, et al. Endogenous metabolites investigation of cadiotoxicity induced by astemizole on zebrafish using GC-MS metabonomics[J]. Chin Pharm J, 2015, 50(1): 45-50. |
| [12] | 吴晓敏, 何秋霞, 韩利文, 等. 阿司咪唑对斑马鱼心脏毒性的初步研究[J]. 中国药理学通报, 2013, 29(9): 1251-4. Wu X M, He Q X, Han L W, et al. Preliminary study of astemizole's cardiotoxicity to zebrafish[J]. Chin Pharmacol Bull, 2013, 29(9): 1251-4. |
| [13] | Lee S H, Kim H R, Han R X, et al. Cardiovascular risk assessment of atypical antipsychotic drugs in a zebrafish model[J]. J Appl Toxicol, 2013, 33(6): 466-70. doi:10.1002/jat.1768 |
| [14] | Abdel-Wahab B A, Metwally M E. Clozapine-induced cardiotoxicity: role of oxidative stress, tumour necrosis factor alpha and NF-κB[J]. Cardiovasc Toxicol, 2015, 15(4): 355-65. doi:10.1007/s12012-014-9304-9 |
| [15] | 郑锡基, 马继红, 赵雪庆, 等. 氯氮平致严重心脏毒性反应2例[J]. 临床精神医学杂志, 2002, 12(1): 62. Zheng X J, Ma J H, Zhao X Q, et al. 2 cases of severe cardiac toxicity induced by clozapine[J]. J Clin Psychiatry, 2002, 12(1): 62. |