


2. 延边大学医学院解剖学教研室,吉林 延吉 133002
 ,
JIANG Jing-zhi2,
YE Jing2,
LI Yan1,
Li Jun-feng2,
YAN Guang-hai2,
LI Liang-chang2,
PIAO Hong-mei1
,
JIANG Jing-zhi2,
YE Jing2,
LI Yan1,
Li Jun-feng2,
YAN Guang-hai2,
LI Liang-chang2,
PIAO Hong-mei1

2. Dept of Anatomy, Yanbian University College of Medicine, Yanji Jilin 133002, China
支气管哮喘是一种常见的呼吸道慢性炎症性疾病[1]。近期研究表明,氧化应激反应在哮喘的发生、发展过程中发挥重要作用[2]。p38丝裂原活化蛋白激酶(p38 MAPK)是丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)家族重要成员之一,在哮喘发生、发展过程中发挥着不可忽视的作用。p38 MAPK受外界刺激后,磷酸化特异性底物引起生物学反应,参与调控炎症反应及氧化应激等[3]。核因子E2相关因子2(nuclear factor erythroid2-related factor 2,Nrf2)作为氧化应激通路中的调节因子之一,发挥调节编码抗氧化蛋白表达、抑制氧化应激反应等重要作用[4]。血红素加氧酶-1(hemeoxygenase1,HO-1)基因是Nrf2的依赖基因,其产物是一种强效的抗氧化剂[5]。p38 MAPK/Nrf2/HO-1通路参与的抗氧化应激途径,为哮喘治疗的研究提供了全新方向。
中药虎杖性味苦寒,归肝胆肺经,具有镇咳、平喘作用。虎杖苷(polydatin,PD)是虎杖的主要化学成分,具有止咳、平喘、祛痰、抗菌、清除自由基等作用[6]。有研究证实,虎杖苷可以通过减少肥大细胞脱颗粒等机制,减轻哮喘小鼠的气道炎症[7]。本研究将从抗氧化等方面探究虎杖苷对哮喘的治疗作用,并探讨其是否通过p38 MAPK/Nrf2/HO-1通路发挥作用。
1 材料与方法 1.1 材料 1.1.1 实验动物♂BALB/c小鼠40只,体质量(20±2)g,清洁级,购自延边大学实验动物中心,合格证号:SCXK(吉)2011-0007。本研究得到延边大学医学院伦理委员会批准,在整个实验中遵守《实验动物管理条例》,做到减轻小鼠痛苦,增加其舒适度。
1.1.2 药物与试剂虎杖苷、卵清蛋白(ovalbumin,OVA)、氢氧化铝粉、β-actin抗体、双氢罗丹明(DHR)-123试剂盒,均购自美国Sigma公司;p38 MAPK、p-p38 MAPK、HO-1、Nrf2抗体、IgG-HRP标记二抗、PCR试剂盒,均购自美国Santa Cruz公司;免疫组化试剂盒、DAB试剂盒及IgE、IL-4、IL-5、IL-13 ELISA试剂盒,均购自北京中杉金桥公司。
1.1.3 仪器雾化器(大连医疗器械厂U219);2135型轮转式切片机(德国徕卡公司);分光光度计(Thermo公司);PCR仪(美国Perkin Elmer Applied Biosystems);酶联免疫检测仪RT-2100C(美国雷杜公司);5415D型低温高速多功能离心机(Eppendorf公司);凝胶成像系统(Flour Chem公司);Western blot转膜仪(Bio-Rad公司)。
1.2 方法 1.2.1 动物分组及模型制备将BALB/c小鼠随机分为4组:生理盐水对照组(SAL)、OVA哮喘组(OVA)、虎杖苷低、高剂量治疗组(PD 30、45 mg·kg-1),每组10只。各组小鼠适应性饲养1周后,SAL组小鼠于d 1、7、14分别腹腔注射0.2 mL生理盐水,其余3组腹腔注射致敏液(OVA 10 μg+氢氧化铝1 mg)0.2 mL致敏。从d 21开始,OVA组、虎杖苷低、高剂量组连续雾化激发7 d。激发液为3% OVA 10 mL,SAL组用等量生理盐水代替。每次激发前1 h,SAL组和OVA组腹腔注射生理盐水0.2 mL;虎杖苷低、高剂量治疗组在激发前7 d开始分别腹腔注射稀释于0.2 mL生理盐水中的30、45 mg·kg-1的虎杖苷,每天1次,连续7 d。
1.2.2 标本收集各组小鼠最后一次雾化吸入24 h后,行无水乙醚麻醉,将麻醉后的小鼠固定在手术板上,颈部常规酒精消毒,纵行切开颈部皮肤,逐层剥离皮下组织至气管充分暴露,在气管上剪一小切口,插入软管,缓慢注入4℃生理盐水0.5 mL后回抽,反复3次,回抽量不少于0.4 mL。收集的肺泡灌洗液(bronchoalveolar lavage fluid,BALF)用高速冷冻台式离心机,以3 000 r·min-1离心5 min,取上清液置于-80℃保存,离心后的沉淀物备用细胞涂片。收集BALF液后,取出小鼠左肺置于甲醛中使其固定,右肺剪碎置于-80℃环境下保存。
1.2.3 肺组织学检查将已经固定好的小鼠左肺进行常规脱水透明、浸蜡、包埋等步骤后,将所得蜡块切成厚度为3~5 μm的切片,并分别进行HE、PAS、Masson染色,每只小鼠随机选3张切片,光镜下观察其组织学变化。
1.2.4 BALF中炎症细胞分类及计数BALF离心后的沉淀物中加入生理盐水,定容至200 μL,混匀后置入细胞涂片离心机,1 000 r·min-1离心10 min,再1 500 r·min-1离心5 min。涂好的细胞涂片进行Diff-Quick染色,在光学显微镜下进行炎症细胞分类及计数。
1.2.5 BALF中总IgE及各细胞因子含量的测定按ELISA试剂盒说明书的步骤,检测BALF中的总IgE及IL-4、IL-5、IL-13的含量。通过使用标准蛋白质生成的标准曲线,计算其浓度。
1.2.6 检测小鼠BALF细胞中活性氧(reactive oxygen species,ROS)含量用PBS洗BALF中的细胞并计数,使用双氢罗丹明(DHR)-123试剂盒检测小鼠BALF细胞中ROS水平,荧光强度(FITC)可代表ROS水平。具体方法依照试剂盒说明书进行。
1.2.7 检测小鼠BALF中的抗氧化酶和MDA依照各个试剂盒说明书的检测方法,检测BALF中超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)活性及丙二醛(malondialdehyde,MDA)含量。将保存在-80℃的BALF取出,冰上复融后,4℃、3 000 r·min-1离心10 min,分别使用试剂盒检测小鼠BALF中SOD、CAT、MDA水平。
1.2.8 免疫组化检测肺组织中HO-1的表达将切好的标本置于60℃烘干机内熔蜡,以增加切片的附着度。然后用二甲苯脱蜡、梯度浓度乙醇脱水,之后置于提取液内,用大功率的微波孵化15 min,缓冲液冷却并清洗,然后用一抗、生物酶标记的二抗孵化。最后,用DAB使切片着色,苏木精复染、脱水,用二甲苯清洗和固定。在400倍放大倍数下,随机选择5个不同的视野观察。
1.2.9 Western blot检测肺组织中p-p38 MAPK、核Nrf2和HO-1表达依照各试剂盒说明书要求,提取小鼠肺组织的总蛋白和核蛋白,将等量的蛋白(30 μg),在10%的SDS-PAGE中以90 V恒压电泳,切取目的条带。300 mA低温条件下转膜。在脱脂奶粉封闭液中常温封闭2 h。分别用小鼠HO-1、Nrf2、β-actin、p38 MAPK、p-p38 MAPK抗体4℃孵育过夜,将膜取出,在TBST中充分洗涤。洗膜后,加入HRP标记的相应二抗,常温孵育1 h。将膜取出,在TBST中洗涤后,使用ECL试剂曝光。底片经扫描仪扫描后,确定目的条带的相对吸光度值。
1.2.10 Real-time PCR法检测肺组织HO-1、Nrf2 mRNA的表达提取总RNA,一步法逆转录扩增,实验方法按Reverse Transcription Kit说明书操作。用SYBR green containing PCR Kit进行Real-time PCR。所用HO-1引物:forward 5′-GATAGAGCGCAACAAGCAGAA-3′,reverse 5′-CAGTGAGGCCCATACCAGAAG-3′;Nrf2引物:forward 5′-GGGCAAGCGACTCATGGTCAT-3′,reverse 5′-AAGCT GCATACAGTCTTCAAA-3′。实验结果分析使用2-△△Ct法。
1.3 统计学方法采用SPSS 13.0统计软件进行分析,计量资料以x±s表示,组间比较采用单因素方差分析。
2 结果 2.1 虎杖苷对肺组织病理学改变的影响Fig 1的肺切片HE染色显示,与SAL组比较,OVA组气道周围有大量炎症细胞浸润。与OVA哮喘组相比,虎杖苷低、高剂量治疗组炎症细胞浸润明显减少,且高剂量组较低剂量组减少更加明显。PAS染色确定虎杖苷是否抑制OVA诱导的气道上皮的黏液分泌增多和杯状细胞的增生,在OVA组中,PAS阳性细胞的百分比明显高于SAL组,但这一增加明显受到虎杖苷的抑制。Masson三联染色验证虎杖苷能否抑制OVA诱导的胶原蛋白沉积,在OVA哮喘组中,胶原蛋白沉积明显较生理盐水对照组增多,而虎杖苷治疗组可抑制OVA诱导的胶原蛋白沉积。

|
| Fig 1 Polydatin affects pathologic changes of lung tissue(×200) |
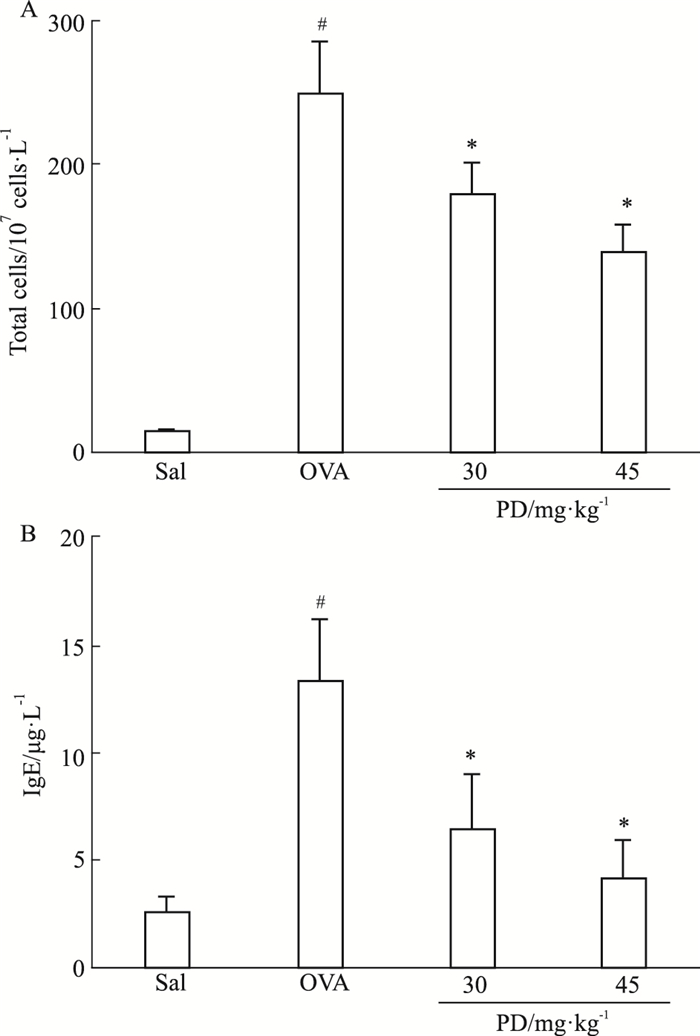
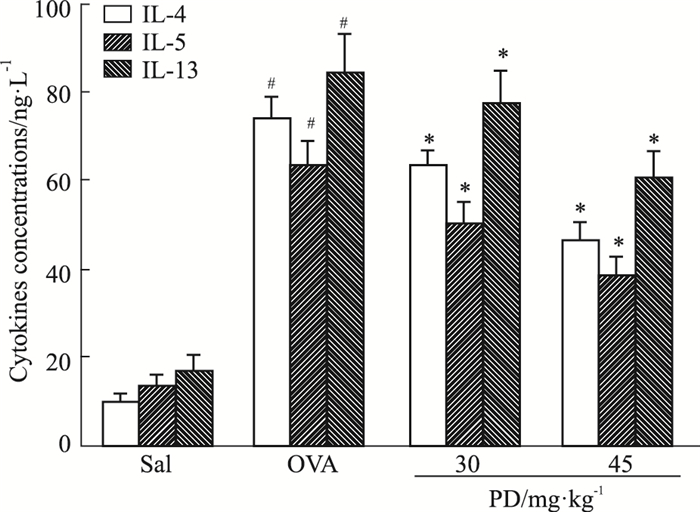
如Fig 2所示,OVA组炎性细胞总数及总IgE浓度明显高于SAL组,虎杖苷治疗抑制了炎性细胞总数和总IgE水平的增加(P < 0.05)。同时,IL-4、IL-5、IL-13的增加也被虎杖苷抑制(P < 0.05),见Fig 3。
|
| Fig 2 Polydatin reduces total number of cells (A) and IgE levels (B) in BALF (x±s, n=10) #P < 0.05 vs SAL; *P < 0.05 vs OVA |
|
| Fig 3 Polydatin reduces concentration of inflammatory cytokines in BALF(x±s, n=10) #P < 0.05 vs SAL; *P < 0.05 vs OVA |
如Tab 1所示,与生理盐水对照组(SAL)相比,OVA哮喘组小鼠BALF中的ROS含量明显升高(P < 0.05),同时BALF中的抗氧化酶SOD、CAT的活性明显降低(P < 0.05),MDA含量升高(P < 0.05);虎杖苷低、高剂量治疗组中的ROS含量明显降低,SOD、CAT的活性明显升高,MDA含量降低(P < 0.05),且高剂量组优于低剂量组。
| Group | ROS/fluorescence intensity | SOD/kU·L-1 | CAT/kU·L-1 | MDA/μmol·g-1 |
| SAL | 51.3±12.1 | 31.0±1.5 | 62.5±5.8 | 7.3±1.8 |
| OVA | 132.5±13.4# | 25.6±2.3# | 50.3±4.7# | 18.2±2.4# |
| PD 30 mg·kg-1 | 82.8±12.9* | 37.1±4.2* | 73.1±4.8* | 13.5±3.2* |
| PD 45 mg·kg-1 | 73.2±10.5* | 44.3±3.2* | 88.5±7.2* | 9.7±2.0* |
| #P < 0.05 vs SAL; *P < 0.05 vs OVA | ||||
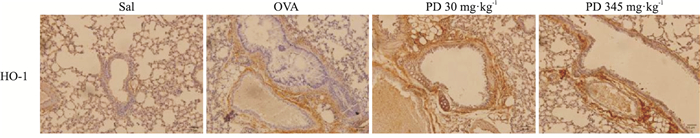
Fig 4的免疫组织化学染色结果表明,与SAL组相比,OVA组HO-1表达减少,虎杖苷治疗组HO-1表达增多。
|
| Fig 4 Polydatin induces expression of HO-1(×200) |
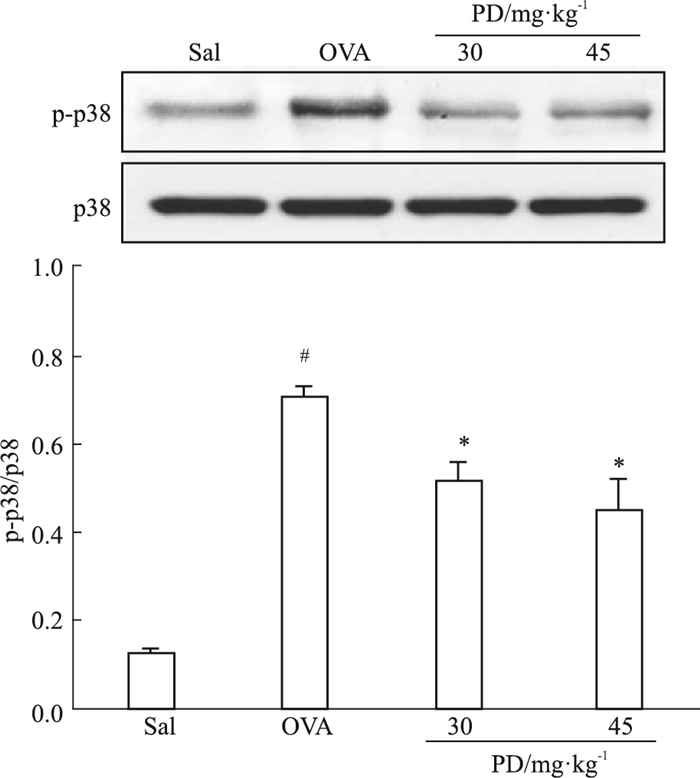
Fig 5的Western blot结果表明,OVA哮喘组p-p38 MAPK水平较生理盐水对照组(SAL)明显升高(P < 0.05),虎杖苷低、高剂量治疗组可减少p-p38 MAPK水平的增加(P < 0.05)。
|
| Fig 5 Polydatin inducing phosphorylation of p38 MAPK #P < 0.05 vs SAL; *P < 0.05 vs OVA |
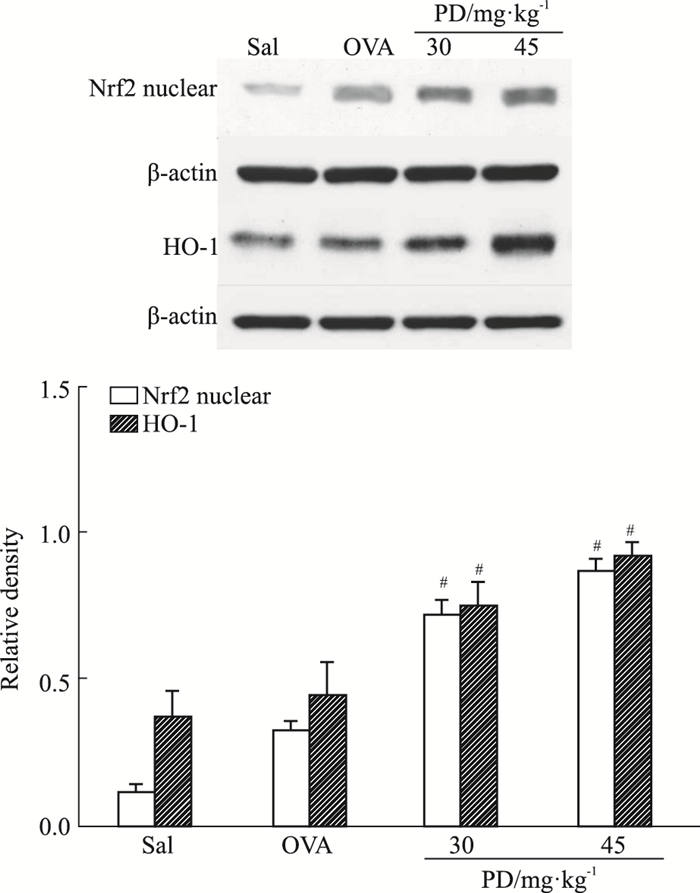
如Fig 6所示,相对于OVA组,虎杖苷治疗组HO-1表达明显增多(P < 0.05)。且核内Nrf2蛋白表达水平明显升高(P < 0.05)。
|
| Fig 6 Polydatin induces expression of HO-1 at protein level and induces Nrf2 into nucleus #P < 0.05 vs OVA |
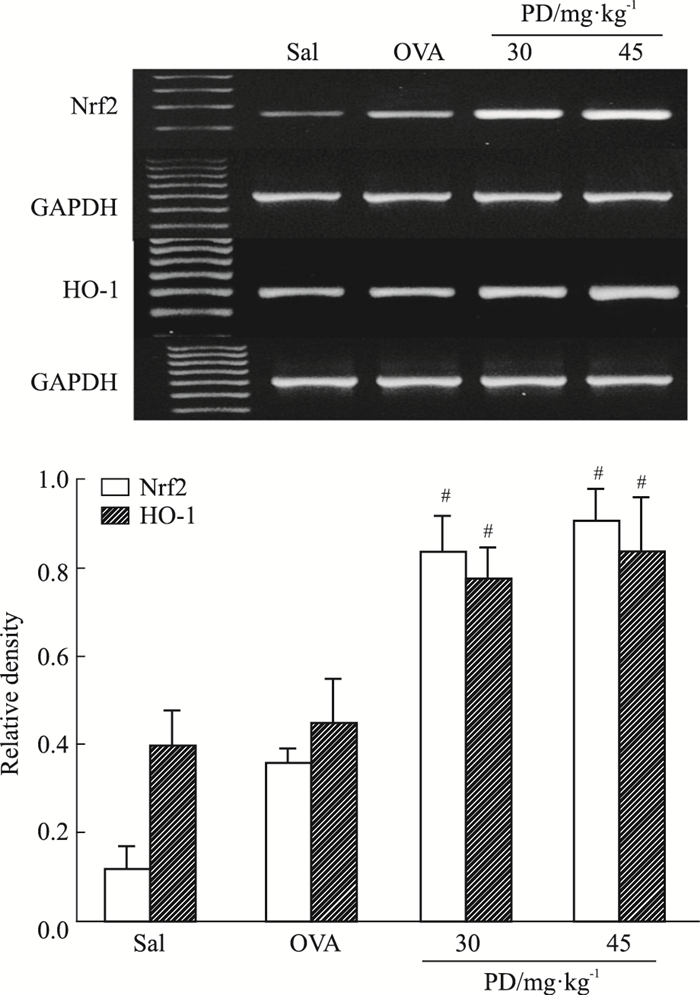
如Fig 7所示,生理盐水对照组(SAL)和OVA哮喘组HO-1、Nrf2的mRNA表达水平较稳定,虎杖苷低、高剂量治疗组HO-1、Nrf2 mRNA表达明显增加(P < 0.05)。
|
| Fig 7 Polydatin induces expression of HO-1 and Nrf2 at mRNA level #P < 0.05 vs OVA |
气道炎症细胞浸润、炎症细胞增多是哮喘的重要特征之一,且其程度和支气管哮喘的严重程度呈明显正相关[8]。本实验HE染色结果表明,经虎杖苷治疗的小鼠炎症细胞浸润程度,以及BALF中的炎症细胞数量均明显降低,且随着剂量的增加疗效更明显。表明虎杖苷可以减少哮喘小鼠气道的炎症细胞增多以及浸润。气道上皮的黏液分泌增多、杯状细胞增生和胶原沉积也是支气管哮喘的重要特征[9]。PAS染色表明,虎杖苷可抑制OVA诱导的气道上皮的黏液分泌增多和杯状细胞的增生;Masson三联染色证明虎杖苷抑制胶原沉积;同时,虎杖苷可减少哮喘小鼠的IgE。以上结果证明虎杖苷抑制OVA诱导的哮喘小鼠模型的气道炎症。
本研究还从氧化应激角度研究了虎杖苷的治疗作用。有大量证据表明[10],ROS在不同种类的肺损伤中发挥重要作用,大量ROS爆发破坏了体内氧化-抗氧化平衡,使机体失去正常调节功能,这与哮喘的发生、发展有着密不可分的关系。虎杖苷减少了BALF的ROS含量。越来越多的证据表明[11],氧化应激与增加的脂质过氧化值有关,加重了气道反应性,同时加重了哮喘模型中炎性介质的过度表达。在本研究中,哮喘小鼠的MDA水平明显增加,这是脂质过氧化作用的最终产物,同时,抗氧化酶SOD和CAT活性降低,虎杖苷明显改善了上述变化。以上结果表明,虎杖苷能减少气道损伤,且其减轻气道炎症的作用可能是通过减少氧化应激实现的。
p38作为MAPK家族的重要的成员之一,受外界刺激后,磷酸化为特异性底物p-p38引起生物学效应,参与调控炎症反应及氧化应激等[12]。本研究证明,虎杖苷可降低p38的磷酸化水平,进而减轻哮喘小鼠的炎症反应。核转录因子Nrf2作为氧化应激通路的调节因子之一,发挥调节编码抗氧化蛋白的表达、抗炎、抗损伤、抑制氧化应激反应等作用,在哮喘治疗中发挥重要作用。本实验结果发现,虎杖苷组小鼠核内Nrf2蛋白的表达明显升高,且虎杖苷促进了Nrf2 mRNA的表达,提示虎杖苷促进了Nrf2的入核作用。应激条件下,HO-1高表达,从而表现出明显的抗氧化作用[13]。本实验结果可见,与OVA哮喘组相比,虎杖苷治疗组的小鼠肺组织HO-1 mRNA及蛋白表达明显增高,表明虎杖苷能诱导HO-1表达。
p38 MAPK/Nrf2/HO-1通路在氧化损伤途径中发挥重要作用。p38 MAPK磷酸化是激活Nrf2的重要途径之一,而被激活的Nrf2的核移位是HO-1活化至关重要的因素。MAPK是参与哮喘的重要信号转导通路之一,在真核细胞内广泛存在,激活后可促进细胞生长发育及分裂凋亡等,并参与到氧化应激反应中。综上所述,本实验结果证实,在OVA诱导的哮喘小鼠模型中,虎杖苷通过激活p38 MAPK/Nrf2信号通路,提高HO-1 mRNA的转录水平,增强HO-1蛋白表达,从而发挥了抗氧化损伤作用,改善了哮喘小鼠的气道炎症。
( 致谢: 本实验在延边大学过敏性疾病研究室完成,感谢各位老师和同学给予的指导和帮助!)
| [1] | 王金磊, 李承德, 孙宏伟, 等. 黄芪多糖抑制NF-κB/MAPK信号通路和改善哮喘大鼠气道炎症的作用[J]. 中国药理学通报, 2016, 32(4): 489-93. Wang J L, Li C D, Sun H W, et al. Astragalus polysaccharide regulates NF-κB/MAPK signaling pathway and attenuates airway inflammation in OVA-induced asthmatic rats[J]. Chin Pharmacol Bull, 2016, 32(4): 489-93. |
| [2] | Saalu L C. The incriminating role of reactive oxygen species in idiopathic male infertility: an evidence based evaluation[J]. Pak J Biol Sci, 2010, 13(9): 413-22. doi:10.3923/pjbs.2010.413.422 |
| [3] | Koh K, Kim J, Jang Y J, et al. Transcription factor Nrf2 suppresses LPS-induced hyperactivation of BV-2 microglial cells[J]. J Neuroimmunol, 2011, 233(1-2): 160-7. doi:10.1016/j.jneuroim.2011.01.004 |
| [4] | 黄娟, 廖君, 彭熙炜, 等. 脑泰方对脑缺血/再灌注大鼠海马区Nrf2、HO-1和膜铁转运辅助蛋白表达的影响[J]. 中国药理学通报, 2017, 33(10): 1467-72. Huang J, Liao J, Peng X W, et al. Effects of Naotai formula on expression of Nrf2, HO-1 and hephaestin in hippocampus of cerebral ischemia/reperfusion rats[J]. Chin Pharmacol Bull, 2017, 33(10): 1467-72. doi:10.3969/j.issn.1001-1978.2017.10.027 |
| [5] | Yang J, Sung J, Kim Y, et al. Inhibitory effects of butein on adipogenesis through upregulation of the Nrf2/HO-1 pathway in 3T3-L1 adipocytes[J]. Prev Nutr Food Sci, 2017, 22(4): 306-11. doi:10.3746/pnf.2017.22.4.306 |
| [6] | Hao J, Chen C, Huang K P, et al. Polydatin improves glucose and lipid metabolism in experimental diabetes through activating the Akt signaling pathway[J]. Eur J Pharmacol, 2014, 745: 152-65. doi:10.1016/j.ejphar.2014.09.047 |
| [7] | 袁美春. 虎杖苷抗过敏性哮喘的作用及机制[D]. 广州: 南方医科大学, 2010. Yuan M C. Effects of polydatin onallergic asthma and the underlying mechanism[D]. Guangzhou: Southern Medical University, 2010. |
| [8] | Park S J, Shin W H, Seo J W, Kim E J. Anthocyanins inhibit airway inflammation and hyperresponsiveness in a murine asthma model[J]. Food Chem Toxicol, 2007, 45(8): 1459-67. doi:10.1016/j.fct.2007.02.013 |
| [9] | Lee M Y, Lee N H, Seo C S, et al. Alpinia katsumadai seed extract attenuate oxidative stress and asthmatic activity in a mouse model of allergic asthma[J]. Food Chem Toxicol, 2010, 48(6): 1746-52. doi:10.1016/j.fct.2010.04.004 |
| [10] | 宋冬梅, 牛英豪, 于磊, 王宝山. 乌司他丁通过Nrf2/HO-1抗氧化途径在OVA诱导的支气管哮喘小鼠中发挥治疗作用[J]. 中国药理学通报, 2014, 30(12): 1713-20. Song D M, Niu Y H, Yu L, Wang B S. Ulinastatin induces Nrf2/HO-1 axis and protects against oxidative stress in ovalbumin-induced murine asthma model[J]. Chin Pharmacol Bull, 2014, 30(12): 1713-20. doi:10.3969/j.issn.1001-1978.2014.12.019 |
| [11] | Shakeri F, Boskabady M H. Anti-inflammatory, antioxidant, and immunomodulatory effects of curcumin in ovalbumin-sensitized rat[J]. Biofactors, 2017, 43(4): 567-76. doi:10.1002/biof.v43.4 |
| [12] | Bhavsar P, Khorasani N, Hew M, et al. Effect of p38 MAPK inhibition on corticosteroid suppression of cytokine release in severe asthma[J]. Eur Respir J, 2010, 35(4): 750-6. doi:10.1183/09031936.00071309 |
| [13] | Wang Z H, Zhang H T, Sun X H, Ren L H. The protective role of vitamin D3 in a murine model of asthma via the suppression of TGF-β/Smad signaling and activation of the Nrf2/HO-1 pathway[J]. Mol Med Rep, 2016, 14(3): 2389-96. doi:10.3892/mmr.2016.5563 |