

心肌纤维化(myocardial fibrosis,MF)是包括高血压、心梗和瓣膜病在内的多种心脏疾病发展到一定程度时所共有的病理改变,是心室重构的主要表现之一[1]。因此,预防和逆转MF和心室重构已成为心血管系统相关疾病研究者们的重点课题。转化生长因子β1(transforming growth factor β1,TGF-β1)是与细胞外基质(extracellular matrixc,ECM)积聚关系非常密切的细胞因子,是促进细胞纤维化的生长元素。Smad3蛋白是TGF-β1信号在胞质内传导的重要分子,与ECM合成及致纤因子分泌等多种生物学行为密切相关[2]。虾青素(astaxanthin,ASTX)隶属胡萝卜素家族叶黄素亚属,存在于大多数甲壳类动物和鲑科鱼类体内[3]。已有研究显示,ASTX能够通过抑制氧化应激和炎症反应,对2型糖尿病和心血管疾病起到抑制作用[4]。此外,Yang等[5]发现,ASTX能够下调高脂喂养的ApoE-/-小鼠血脂水平,增强肝脏内抗氧化酶活性。
本研究探讨ASTX对TGF-β1诱导的心肌成纤维细胞(cardiac fibroblasts,CFs)内活性氧(reactive oxygen spices,ROS)生成和胶原蛋白分泌的影响,以及这种作用与TGF-β1/Smad3信号通路间的关系,旨在探讨ASTX改善心肌纤维化的内在分子机制,为其在临床上用于慢性心力衰竭的治疗提供一定依据。
1 材料与方法 1.1 材料 1.1.1 试剂DMEM高糖培养液(美国Gibco公司);ASTX、胎牛血清、噻唑蓝(MTT)、二甲基亚砜(DMSO)、TGF-β1(美国Sigma公司);实时定量PCR试剂盒及逆转录试剂盒(北京TransGen公司);兔抗大鼠Ⅰ型胶原(college Ⅰ,Col Ⅰ)、Ⅲ型胶原(college Ⅲ,Col Ⅲ)、Smad3、p-Smad3、β-actin多克隆抗体(美国Santa Cruz公司);Smad3-siRNA由南京金丝瑞生物有限公司合成。
1.1.2 仪器iMarkTM酶标仪(美国Bio-Rad公司);超净台(哈尔滨东联电子技术发展有限公司);MCO175型CO2培养箱(日本Sanyo公司);倒置显微镜(日本Olympus公司);CS-15R冷冻离心机(美国Beckman公司);IQ5荧光定量PCR仪(美国ABI公司)。
1.2 CFs的分离与培养无菌条件下,分离2~3 d SD乳鼠左心室,剪碎至1 mm3~2 mm3组织块,消化法进行培养[9]。细胞呈单细胞混悬液时,差速贴壁90 min,去上清,加入15%胎牛血清的DMEM培养基及双抗(0.1 U·L-1的青霉素和0.1 mg·L-1的链霉素),放入37℃、5% CO2细胞培养箱中继续培养,待细胞融合至80%~90%时,用于后续实验。
1.3 MTT法测定不同浓度ASTX对细胞活性的影响将细胞按5×104个每孔的密度接种于96孔板,按照“1.2”项下条件培养24 h后,改用2%低血清培养基培养12 h,将CFs分为空白对照组、ASTX组(5、10、20、40、80、160 μmol·L-1),分别给予相应浓度的ASTX干预24 h后,吸去培养液,每孔加入MTT(5 g·L-1)20 μL,37℃孵育4 h后,弃去上清,每孔加入100 μL DMSO,震荡混匀后,于570 nm处测定吸光度(OD)值。
1.4 DCFH-DA法测定CFs细胞内ROS合成将DCFH溶于10 mmol·L-1甲醇溶液,Hank’s平衡液稀释至20 μmol·L-1待用。CFs分为空白对照组、TGF-β1组、TGF-β1+ASTX(5、10、20 μmol·L-1)组及ASTX组。TGF-β1+ASTX组用ASTX(5、10、20 μmol·L-1)预处理CFs细胞24 h后,加入DCFH孵育1 h,再给予2 mg·L-1 TGF-β1刺激30 min;TGF-β1组仅给予2 mg·L-1 TGF-β1刺激30 min;ASTX组仅给予ASTX 20 μmol·L-1预处理,酶标仪测定各组荧光强度,结果以每微克细胞蛋白中的荧光强度表示。
1.5 qPCR测定Col Ⅰ和Col Ⅲ mRNA表达按“1.2”项所述方法培养细胞,“1.4”项所述方法对各组细胞进行分组及处理后,Transzol试剂盒提取各组细胞总RNA。1%的琼脂糖凝胶电泳鉴定RNA完整性,260 nm处检测RNA的纯度。按照逆转录试剂盒及PCR试剂盒操作步骤进行反转录及实时荧光定量PCR反应。q-PCR引物由上海生物工程有限公司合成,引物序列见Tab 1。PCR扩增条件:95℃预变性5 min,95℃ 15 s,55℃退火15 s,72℃延伸30 s,共计42个循环。使用Bio-Rad IQ7荧光PCR仪自带分析软件对qPCR结果进行分析。
| Gene | Prime sequence | Product length/bp |
| β-actin | 5′-CATTGCTGACAGGATGCAGAAG-3′ | 105 |
| 5′-GAGCCACCAATCCACACAGAGT-3′ | ||
| Col Ⅰ | 5′-CAGGGTTTCAGAGCACCATT -3′ | 159 |
| 5′-CGTTGGGTCATTTCCACAT-3′ | ||
| Col Ⅲ | 5′-GGCTCAAATGGCTCTCCAG -3′ | 112 |
| 5′-GGCTCAAATGGCTCTCCAAG-3′ |
按“1.2”项所述方法培养细胞,“1.4”项所述方法对各组细胞进行分组及处理后,每孔使用150 μL RIPA裂解液提取蛋白。BCA蛋白定量试剂盒测定各组样品蛋白浓度。加入蛋白上样缓冲液并煮沸后,制作12% SDS-PAGE凝胶进行电泳,半干转膜仪转膜。一抗浓度为:Col Ⅰ(1 :250)、Col Ⅲ(1 :400)、Smad(1 :200)、p-Smad3(1 :200)、β-actin(1 :2 000)。以β-actin作为内参。化学发光法检测,Quantity one软件进行图像分析。
1.7 CFs转染Smad3-siRNA后Col Ⅰ、Col Ⅲ mRNA表达检测Smad3-siRNA干扰序列:R:5′-CGCAGAACGUGAACACCAAdTdT-3′,F:3′-dTdTGCGUCUUGCACUUGUGGUU-5′,对Smad3基因进行沉默,按“1.2”项下方法进行培养,待细胞融合率达到80%~90%时转染,Lipofectamine 2 000作为载体,转染过程严格根据试剂盒进行。CFs分为空白对照组、TGF-β1组、TGF-β1+ASTX(20 μmol·L-1)组、TGF-β1-Smad3-siRNA及TGFβ1-Smad3-siRNA-ASTX组,检测各组CFs细胞的Col Ⅰ和Col Ⅲ mRNA表达水平。
1.8 统计学分析使用SPSS 17.0软件进行统计学分析,计量均数用x±s表示,组间比较使用单因素方差分析,多重均数比较使用SNK检验。
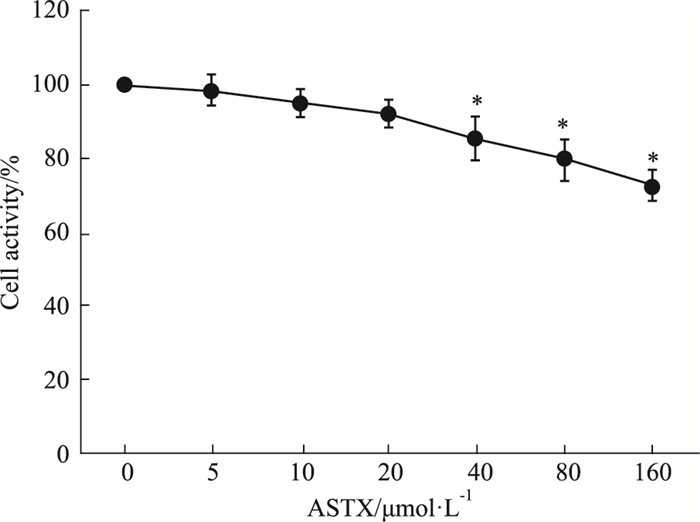
2 结果 2.1 ASTX对CFs活性的影响如Fig 1所示,ASTX在0~20 μmol·L-1范围内,无明显的细胞毒性。因此,后续实验中选择0、5、10、20 μmol·L-1 ASTX用于后续实验。
|
| Fig 1 Effect of different concentrations of ASTX on cell activity (n=8) *P < 0.05 vs control group |
如Fig 2所示,与空白对照组相比,TGF-β1组ROS合成明显增加(P < 0.01);与TGF-β1组比较,TGF-β1+ASTX(5、10、20 μmol·L-1)组ROS合成明显降低(P < 0.01),且降低程度呈剂量依赖性;ASTX组ROS合成无明显变化(P>0.05)。

|
| Fig 2 Effects of different concentrations of ASTX on ROS production of CFs induced by TGF-β1 in CFs (x±s, n=8) ##P < 0.01 vs control group; **P < 0.01 vs TGF-β1 group |
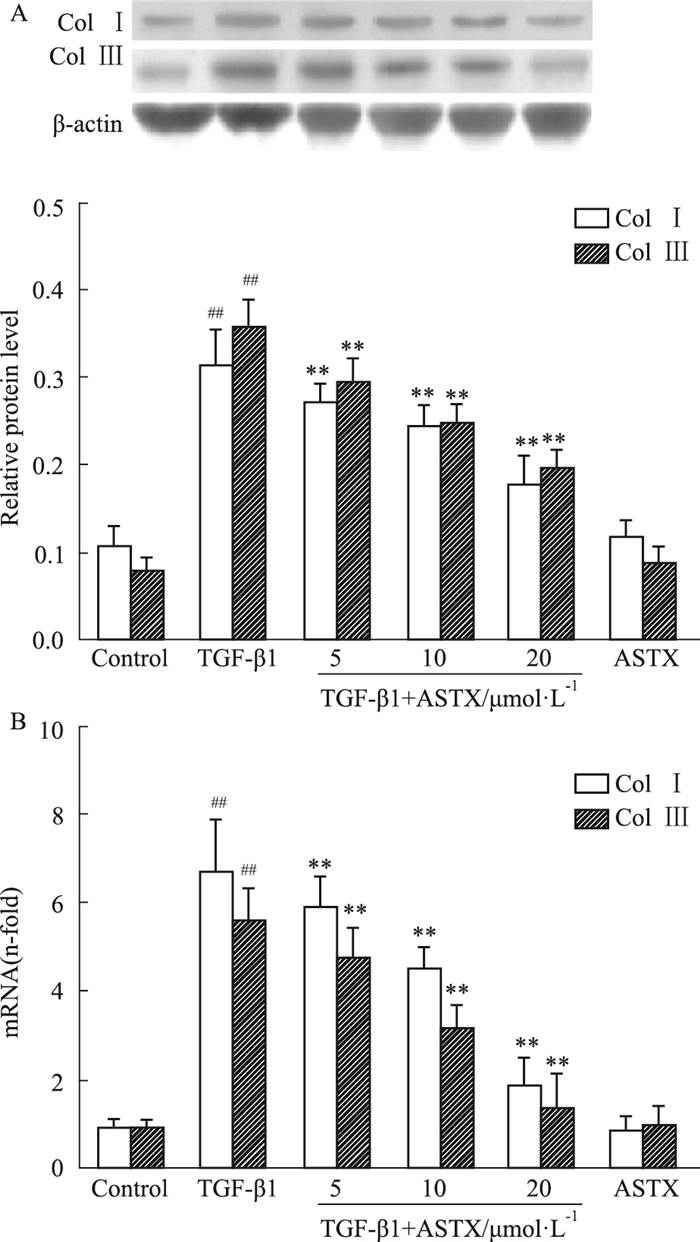
如Fig 3A所示,与空白对照组相比较,TGF-β1组Col Ⅰ和Col Ⅲ蛋白表达明显升高。与TGF-β1组相比较,TGF-β1+ASTX(5、10、20 μmol·L-1)组Col Ⅰ和Col Ⅲ蛋白表达明显下降(P < 0.01),并呈剂量依赖性。ASTX组Col Ⅰ和Col Ⅲ蛋白表达无明显改变(P>0.05)。此外,ASTX亦能够明显抑制TGF-β1诱导的Col Ⅰ和Col Ⅲ mRNA表达(P < 0.01), 见Fig 3B。
|
| Fig 3 Effects of different concentrations of ASTX on Col Ⅰ and Col Ⅲ protein(A) and mRNA (B) expression in CFs induced by TGFβ1 (x±s, n=8) ##P < 0.01 vs control group; **P < 0.01 vs TGF-β1 group |
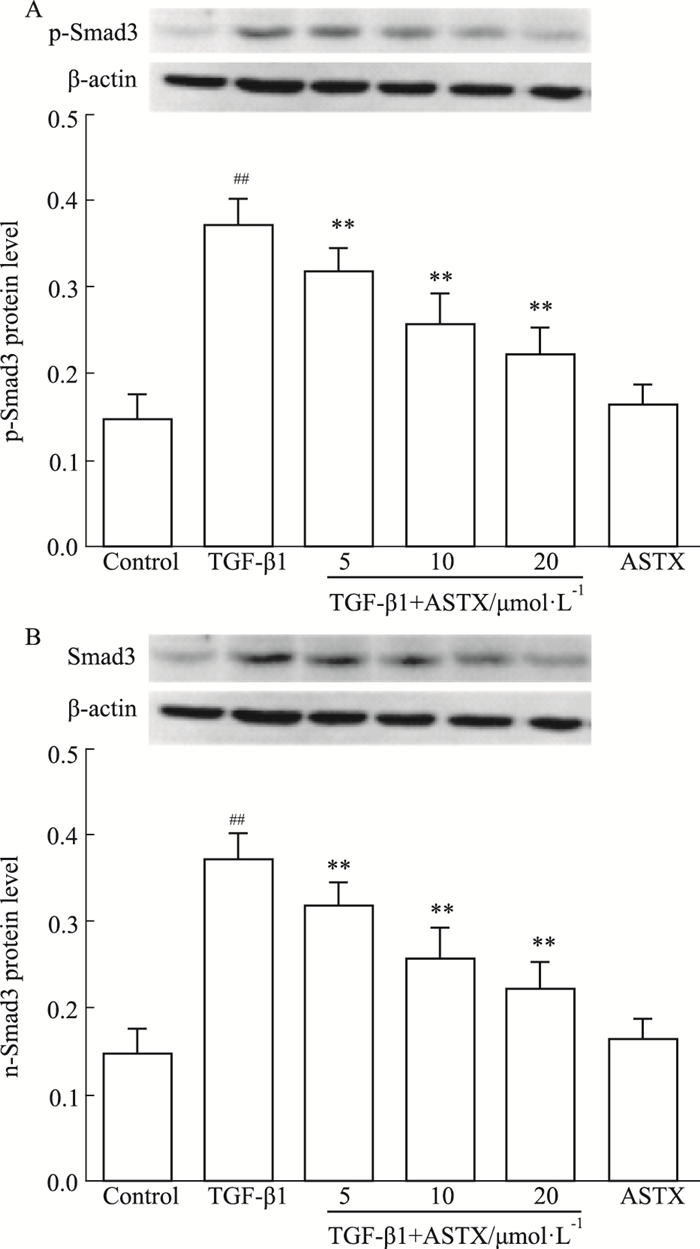
如Fig 4A所示,与空白对照组相比,TGF-β1组Smad3的磷酸化水平明显升高(P < 0.01);与TGF-β1组比较,TGFβ1+ASTX(5、10、20 μmol·L-1)组Smad3的磷酸化水平明显降低(P < 0.01)。此外,与空白对照组相比,TGF-β1组核内的Smad3表达明显升高(P < 0.01);与TGF-β1组比较,TGF-β1+ASTX(5、10、20 μmol·L-1)组核内的Smad3表达明显降低(P < 0.01),见Fig 4 B。
|
| Fig 4 Effects of different concentrations of ASTX on Smad3 phosphorylation(A) and nuclear translocation(B) in CFs cells (x±s, n=8) ##P < 0.01 vs control group; **P < 0.01 vs TGF-β1 group |
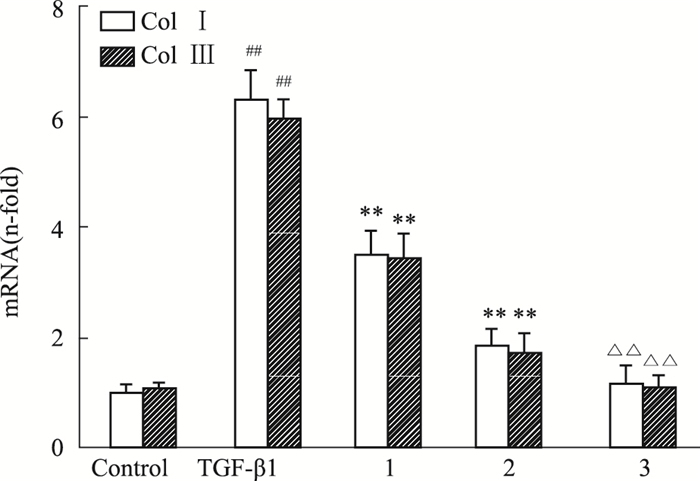
如Fig 5所示,Smad3-siRNA能够明显抑制TGF-β1诱导的CFs细胞Col Ⅰ和Col Ⅲ mRNA表达(P < 0.01)。较单用Smad3-siRNA组相比,Smad3-siRNA联用ASTX(20 μmol·L-1)则能够进一步减少TGF-β1诱导的CFs细胞Col Ⅰ和Col Ⅲ mRNA表达(P < 0.01)。
|
| Fig 5 CFs Col Ⅰ and Col Ⅲ mRNA expression induced by TGF-β1 via activating Smad3 (x±s, n=8) 1:TGF-β1+Smad3-siRNA;2:TGF-β1 +ASTX;3:TGF-β1+Smad3-siRNA+ASTX;##P < 0.01 vs control group; **P < 0.01 vs TGF-β1 group; △△P < 0.01 vs TGF-β1+Smad3-siRNA. |
慢性心力衰竭是常见心脏疾患终末期的共同临床表现,心肌纤维化程度的不断加重是构成慢性心力衰竭的重要病理表现[6]。CFs已被证实能够通过过度增殖、合成胶原蛋白、上调氧化应激反应、分泌纤维化因子、炎症因子和黏附分子等途径,促进心肌纤维化的发展[7]。因此,调节病理状态下的CFs异常生物学行为,极有可能成为抑制心肌纤维化发生、发展的中心环节。
TGF-β1是一种强有力的促纤维化因子,能够明显诱导CFs病理性增殖、表型变化和胶原蛋白合成与分泌[8]。此外,氧化应激导致ROS在CFs内聚集,亦被证实是心肌纤维化的重要促进因素之一。
TGF-β1能够通过上调NOX2和NOX4活性,增强细胞内ROS合成,促进氧化应激反应,加速纤维化进程[9]。本研究结果显示,TGF-β1+ASTX(5、10、20 μmol·L-1)组ROS合成较ASTX未干预组明显降低,提示虾青素干预可以减少TGF-β1诱导的CFs ROS合成,且这种作用呈剂量依赖,这与我们之前的研究结果一致[10]。
新近研究表明,因具有独特的DNA结合和快速激活区域,Smad3在心肌纤维化过程的作用被广泛关注。TGF-β1、血管紧张素Ⅱ(angiotensin Ⅱ,AngⅡ)和压力负荷等常见致心衰因素均能够诱发Smad3的磷酸化激活[11]。此外,有研究表明,抑制TGF-β1/Smad3信号通路激活,能够起到抗心肌纤维化作用[12]。因此,我们亦将研究重点聚焦于Smad3蛋白。本研究结果显示,ASTX能够有效抑制TGF-β1诱导的CFs中Smad3的磷酸化。Smad3磷酸化激活后会发生核转位,因此,我们又测定了核内的Smad3表达,结果显示,ASTX能够明显抑制TGF-β1诱导的CFs Smad3的核转位。
Smad3是TGF-β1信号通路的重要下游分子[13]。为了进一步明确Smad3激活与ASTX抑制TGF-β1诱导的CFs中Col Ⅰ和Col Ⅲ表达之间的关系,我们使用了siRNA对Smad3进行基因沉默。结果提示,Smad3-siRNA能够明显抑制TGF-β1诱导的CFs Col Ⅰ和Col Ⅲ mRNA表达。Smad3-siRNA联用ASTX(20 μmol·L-1)则能够进一步减少TGF-β1诱导的CFs中Col Ⅰ和Col Ⅲ mRNA表达, 产生叠加效果。据此可知,Smad3激活在TGF-β1诱导的CFs Col Ⅰ和Col Ⅲ表达过程中起到重要作用;ASTX抗纤维化作用可能与其抑制Smad3激活相关。结果提示,下调Smad3的磷酸化水平可能是ASTX抑制TGF-β1诱导的CFs Col Ⅰ、Col Ⅲ的mRNA和蛋白生成的中心环节。
综上所述,ASTX能够有效抑制TGF-β1诱导的CFs内ROS、Col Ⅰ和Col Ⅲ生成,可能的机制是下调Smad3磷酸化。
( 致谢: 本课题在郑州大学第一附属医院重点实验室完成,感谢实验的指导老师及各位参与者!)
| [1] | Dzeshka S, Lip Y, Snezhitskiy V, et al. Cardiac fibrosis in patients with atrial fibrillation: mechanisms and clinical implications[J]. J Am Coll Cardiol, 2015, 66(8): 943-59. doi:10.1016/j.jacc.2015.06.1313 |
| [2] | Zhang Y, Zhao N, Wang J K, et al. Telmisartan inhibited angiotensin Ⅱ-induced collagen metabolic imbalance without directly targeting TGF-β1/Smad signaling pathway in cardiac fibroblasts[J]. Minerva Cardioangiol, 2015, 63(6): 507-14. |
| [3] | Higuera-Ciapara I, Félix-Valenzuela L, Goycoolea F M. Astaxanthin: a review of its chemistry and applications[J]. Crit Rev Food Sci Nutr, 2006, 46(2): 185-96. doi:10.1080/10408690590957188 |
| [4] | Uchiyama K, Naito Y, Hasegawa G, et al. Astaxanthin protects beta-cells against glucose toxicity in diabetic db/db mice[J]. Redox Rep, 2002, 7(5): 290-3. doi:10.1179/135100002125000811 |
| [5] | Yang Y E, Min J, Nguyen A, et al. Astaxanthin-Rich extract from the green Alga haematococcus pluvialis lowers plasma lipid concentrations and enhances antioxidant defense in apolipoprotein E knockout mice[J]. J Nutr, 2011, 141(9): 1611-7. doi:10.3945/jn.111.142109 |
| [6] | Lajiness J D, Conway S J. Origin, development, and differentiation of cardiac fibroblasts[J]. J Mol Cell Cardiol, 2014, 70(9): 2-8. |
| [7] | Maclean J, Pasumarthi K B. Signaling mechanisms regulating fibroblast activation, phenoconversion and fibrosis in the heart[J]. Indian J Biochem Biophys, 2014, 51(6): 476-82. |
| [8] | Leask A. Potential therapeutic targets for cardiac fibrosis: TGFbeta, angiotensin, endothelin, CCN2, and PDGF, partners in fibroblast activation[J]. Circ Res, 2010, 106(11): 1675-80. doi:10.1161/CIRCRESAHA.110.217737 |
| [9] | Lu H Y, Tian A J, Wu J M, et al. Danshensu inhibits beta-adrenergic receptors-mediated cardiac fibrosis by ROS/p38 MAPK axis[J]. Biol Pharm Bull, 2014, 37(6): 961-7. doi:10.1248/bpb.b13-00921 |
| [10] | 翟海杰, 孟哲, 陶海龙, 等. 姜黄素对内毒素诱导的血管平滑肌细胞Toll样受体4/NADPH氧化酶/活性氧信号通路及炎症因子释放的影响[J]. 西安交通大学学报, 2015, 36(4): 543-8. Zhai H J, Meng Z, Tao H L, et al. Effect of curcumin on endotoxin-induced Toll-like receptor4/NADPH oxidase/reactive oxygen signaling pathway and release of inflammatory factors in vascular smooth muscle cells[J]. J Xi'an Jiaotong Univ: Med Sci, 2015, 36(4): 543-8. |
| [11] | 刘理静, 于小华, 张平. 白藜芦醇通过TGF-β1/ADAMTS-1信号通路抑制肺纤维化[J]. 中国药理学通报, 2013, 29(3): 425-31. Liu L J, Yu X H, Zhang P. Resveratrol inhibits pulmonary fibrosis through TGF-β1/ ADAMTS-1 signaling pathway[J]. Chin Pharmacol Bull, 2013, 29(3): 425-31. |
| [12] | Liu X E, Gai Y L, Liu F, et al. Trimetazidine inhibits pressure overload-induced cardiac fibrosis through NADPH oxidase-ROS-CTGF pathway[J]. Cardiovasc Res, 2010, 88(1): 150-8. doi:10.1093/cvr/cvq181 |
| [13] | Huang X R, Chung A C, Yang F Y, et al. Smad3 mediates cardiac inflammation and fibrosis in angiotensin Ⅱ-induced hypertensive cardiac remodeling[J]. Hypertension, 2010, 55(5): 1165-71. doi:10.1161/HYPERTENSIONAHA.109.147611 |

