


肝脏缺血/再灌注损伤(ischemia/reperfusion injury, IRI)是指肝脏在缺血一段时间后恢复血液供应,该过程不仅不利于肝功能的恢复,往往造成更严重的肝脏功能障碍。在肝脏IRI进程中,氧化应激反应、炎症反应、肝细胞的凋亡、坏死等都是引起肝损伤的重要原因[1]。沉默信息调节因子1(silent information regulator 1, SIRT1)作为一种广泛存在于人类细胞中的Ⅲ组蛋白去乙酰化酶,通过其去乙酰化作用,调控抑癌因子p53、核因子κB(nuclear factor-κB, NF-κB)、叉头蛋白转录因子(forkhead-box transcription factor, FOXO)等多种因子,发挥各种生物活性[2]。NF-κB作为体内关键的信号分子,精确调控炎症反应,而通过SIRT1的效应,可以降低其亚单位NF-κB p65的表达,抑制下游炎症因子的活性[3]。p53在细胞内主要表现为阻滞细胞周期、促进细胞凋亡等作用,而SIRT1可以降低p53的结合能力,减少细胞凋亡[4]。丹酚酸B(salvianolic acid B, Sal B)是从丹参中提取的高活性、低毒性的水溶性化合物,具有改善心脑血流量、抗氧化、抗炎等生物活性,近年来研究也证明Sal B对心肌梗死有保护作用,且能改善心脑IRI [5]。本研究拟通过建立大鼠肝细胞株BRL-3A的缺氧/复氧(hypoxia/reoxygenation,H/R)模型[6],观察Sal B是否减轻H/R诱导的肝细胞损伤,并初步探讨其潜在机制,为临床治疗肝IRI提供理论依据。
1 材料与方法 1.1 材料 1.1.1 细胞株与试剂大鼠BRL-3A肝细胞株购自武汉Procell公司; Sal B购自上海Winherb医药科技发展有限公司; 胎牛血清(fetal bovine serum,FBS)购自BI公司; DMEM/F12培养基购自Hyclone公司; 丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)试剂盒购自南京建成生物公司; 肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、白细胞介素1β (interleukin 1β,IL-1β) ELISA试剂盒购自Neobioscience公司; 逆转录all in one试剂、SYBR荧光染料、CCK-8试剂购自Biotool公司; TRIzol试剂购自TaKaRa公司; 引物购自上海生工有限公司; RIPA裂解液、BCA蛋白浓度检测试剂盒购自碧云天公司; ECL发光液购自Advansta公司; 兔抗NF-κB p65抗体购自北京中杉金桥生物公司; 兔抗SIRT1、p53、Bax、Bcl-2抗体购自沈阳万类公司; 兔抗β-actin抗体及山羊抗兔IgG购自武汉博士德公司。
1.1.2 仪器3131型三气培养箱(美国Thermo Scientific公司); MSS酶标仪(芬兰雷勃公司); Allegra 64R型超速冷冻离心机(美国Beckman公司); PowerPac 300型电泳仪、CFX96型荧光定量PCR仪(美国Bio-Rad公司); 流式细胞仪(美国BD公司)。
1.2 方法 1.2.1 大鼠BRL-3A肝细胞培养及Sal B药物配制将BRL-3A正常培养在含10% FBS的DMEM/F12培养基中,置于普通的培养箱(37℃、5% CO2、95%空气)中,观察细胞形态。将Sal B溶解在无菌的PBS液中,配成浓度10 μmol·L-1的基础液,封口避光保存于-20℃冰箱,根据实验需要,再用DMEM/F12培养基将基础母液稀释到相应的浓度。
1.2.2 实验分组及H/R模型构建实验分为对照组:正常培养的细胞; 对照处理组:正常培养的细胞中加入实验最适浓度Sal B(0.5 μmol·L-1)干预; 模型组:H/R诱导培养的细胞; 实验处理组:在需要H/R诱导培养的细胞中分别加入0.25、0.5 μmol·L-1 Sal B干预。H/R模型构建:正常条件培养肝细胞生长至融合度70%左右后,改用不含血清的饥饿培养液,置于三气培养箱(37℃、94% N2、1% O2、5% CO2)缺氧培养12 h,再置入普通孵箱培养4 h[6]。在缺氧前2 h加入相应浓度药物干预。
1.2.3 CCK-8检测细胞活力选取状态良好的细胞计数,然后按1.2×104个/孔接种到2块96孔板里,随机将两板分为对照组和H/R组; 对照组设置空白对照及调零组,H/R组设置空白H/R、H/R加药及调零组; 空白对照组正常孵育,空白H/R组缺氧培养12 h后再复氧培养4 h,H/R加药组在不同浓度药物干预2 h后再H/R处理,调零组没有细胞,每组设置3个复孔。接种完毕后,将孔板放入普通培养箱正常培养24 h,再按实验要求药物干预,按需行缺氧/复氧处理,根据说明书,再混入10 μL CCK-8反应液,于正常孵箱中反应90 min,测OD值。
1.2.4 ELISA检测TNF-α和IL-1β水平将细胞接种到2块6孔板中正常培养,待细胞贴壁融合到70%左右,开始药物干预,随机选择1块孔板,设置空白对照组及加入0.5 μmol·L-1药物干预对照组,另一块孔板设置空白H/R组和分别加入0.25、0.5 μmol·L-1药物干预的H/R组。H/R后收集各组细胞液,按说明书要求检测TNF-α和IL-1β水平。
1.2.5 微板法检测ALT和AST水平将细胞接种到2块6孔板中正常培养,随机选择孔板设置分组,按上述方法处理,收集培养液,按试剂盒要求检测ALT、AST水平。
1.2.6 流式细胞术检测细胞凋亡用T25培养瓶正常培养细胞,待贴壁融合70%左右开始药物干预处理细胞,分为对照组、加0.5 μmol·L-1药物干预的对照组、H/R组、加0.25、0.5 μmol·L-1药物干预的H/R组。H/R完成后收集上清,与消化的细胞一起离心,PBS多次冲洗,重复离心步骤,最后收集细胞,按说明操作,检测凋亡。
1.2.7 Western blot检测蛋白表达实验分组和处理方法同上,H/R后提取细胞总蛋白,并用BCA法测定蛋白浓度,绘制标准曲线后,按每孔30 μg计算上样量。浓缩胶80 V电泳,等蛋白预染标记物完全分开后,120 V继续电泳下层胶; 充分分离后,250 mA电转至PVDF膜; 膜在环境温度下用5%的脱脂牛奶于70 r·min-1的摇床上封闭90 min,再孵育一抗(β-actin、SIRT1、p53、Bax、Bcl-2为1 :500,NF-κB p65为1 :800),置于4℃过夜; 隔天将膜夹入TBST中,于110 r·min-1摇床上洗3遍,各10 min,再孵育二抗(1 :5 000),置于37℃培养箱反应1 h,之后再将膜用TBST洗3次; 最后曝光显影,用软件进行蛋白表达量的定量分析。
1.2.8 实时荧光定量PCR检测mRNA表达实验分组和处理方法同上,H/R后用TRIzol法提取各组细胞总RNA,按说明书逆转录为cDNA,并取cDNA行荧光定量PCR,检测SIRT1、NF-κB p65、p53、Bax、Bcl-2的mRNA表达水平,以GADPH作为内参,独立实验,重复3次。PCR反应体系: cDNA 1 μL、SYBR Green 5 μL、上下游引物各0.2 μL、无酶水3.6 μL。引物序列见Tab 1。
| Gene | Forward sequence | Reverse sequence |
| SIRT1 | 5′-TACCCCATGAAGTGCCTCAA-3′ | 5′-CATCGCAGTCTCCAAGAAGC-3′ |
| NF-κB p65 | 5′-TGTTTCCCCTCATCTTTCCCT-3′ | 5′-GCCCTCGCACTTGTAACGG-3′ |
| p53 | 5′-TCACCCTTAAGATCCGTGGG-3′ | 5′-GTAGACTGGCCCTTCTTGGT-3′ |
| Bax | 5′-CGAGTGTCTCAGGCGAATTG-3′ | 5′-CGTCTGCAAACATGTCAGCT-3′ |
| Bcl-2 | 5′-GAGTACCTGAACCGGCATCT-3′ | 5′-ATCAAACAGAGGTCGCATGC-3′ |
| GAPDH | 5′-ACAGCAACAGGGTGGTGGAC-3′ | 5′-TTTGAGGGTGCAGCGAACTT-3′ |
实验至少独立重复3次,应用SPSS 20.0软件进行统计学分析,数据用x±s表示,多样本均数比较采用单因素方差分析,两样本之间比较用t检验。
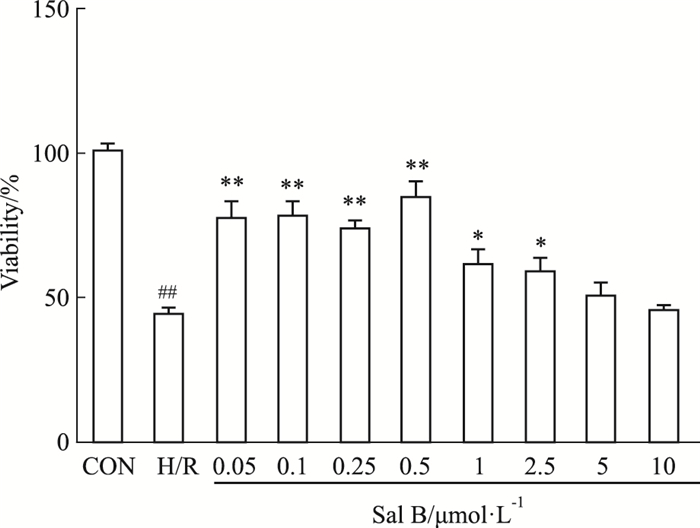
2 结果 2.1 Sal B对H/R后细胞活力的影响在不同浓度Sal B(0.05、0.1、0.25、0.5、1、2.5、5、10 μmol·L-1)预处理后,对细胞行H/R诱导,通过检测分析发现,H/R组与对照组相比,细胞活力明显下降(P < 0.01);0.05、0.1、0.25、0.5、1、2.5 μmol·L-1药物干预后的H/R组与H/R组对比,肝细胞活力升高(P < 0.05,P < 0.01),5、10 μmol·L-1药物干预后的H/R组与H/R组对比,肝细胞活力升高不明显,差异无统计学意义,且0.5 μmol·L-1 Sal B预处理后肝细胞活力提高最明显,所以将该浓度作为后续实验的药物最佳预处理浓度(Fig 1)。
|
| Fig 1 Effect of Sal B on viability of BRL-3A cells induced by H/R CON: Control group; H/R: Hypoxia 12 h/reoxygenation 4 h. ##P < 0.01 vs CON; *P < 0.05, **P < 0.01 vs H/R. |
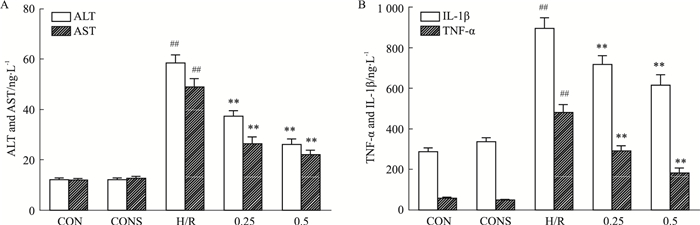
对照组中ALT、AST水平较低,0.5 μmol·L-1 Sal B干预后的对照组中ALT、AST水平变化不大,差异无统计学意义。H/R诱导后,细胞培养液中ALT、AST水平明显上升,预处理后,H/R中ALT、AST水平降低(P < 0.01,Fig 2A)。
|
| Fig 2 Effect of Sal B on levels of ALT, AST, TNF-α and IL-1β in supernatant of BRL-3A cells induced by H/R A:Expression of ALT and AST was detected by microplate assay; B: Levels of TNF-α and IL-1β were determined by ELISA. CON: Control group; CONS: CON+0.5 μmol·L-1 Sal B; H/R: Hypoxia 12 h/reoxygenation 4 h; 0.25: H/R+0.25 μmol·L-1 Sal B; 0.5: H/R+0.5 μmol·L-1 Sal B. ##P < 0.01 vs CON; **P < 0.01 vs H/R. |
药物干预的对照组与空白对照组相比,细胞培养液中TNF-α、IL-1β的分泌变化不明显,H/R诱导的细胞培养液中TNF-α、IL-1β水平明显高于对照组,而药物干预降低了H/R组TNF-α、IL-1β的分泌(P < 0.01,Fig 2B)。
2.4 Sal B降低H/R诱导的肝细胞凋亡率与空白对照比较,药物干预的对照组凋亡率无明显变化,而H/R组细胞凋亡率明显升高(P < 0.01);与H/R组相比,药物干预的H/R组细胞凋亡率降低,差异有统计学意义(P < 0.01), 见Fig 3。

|
| Fig 3 Effect of Sal B on apoptosis in BRL-3A cells induced by H/R ##P < 0.01 vs CON; **P < 0.01 vs H/R |
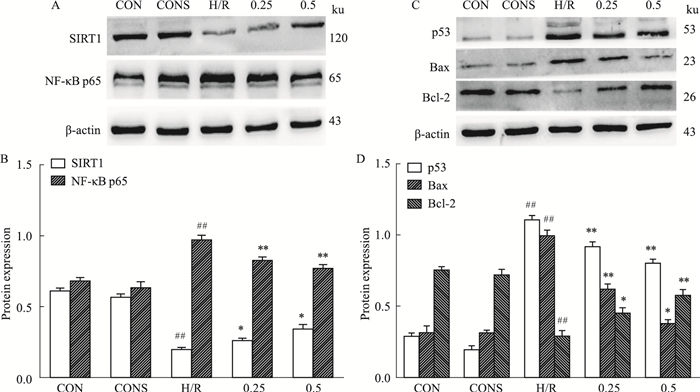
与空白对照相比,H/R组NF-κB p65、p53、Bax蛋白表达上调,SIRT1、Bcl-2蛋白表达降低(P < 0.01);与H/R组相比,Sal B预处理后的H/R组NF-κB p65、p53、Bax表达下调,SIRT1、Bcl-2表达增高(P < 0.05,P < 0.01),见Fig 4。
|
| Fig 4 Effect of Sal B on relative protein expression in BRL-3A cells induced by H/R A, C: Expression of relative protein were detected by Western bolt; B, D: Semi-quantitative analysis of expression of relative protein. ##P < 0.01 vs CON; *P < 0.05, **P < 0.01 vs H/R. |
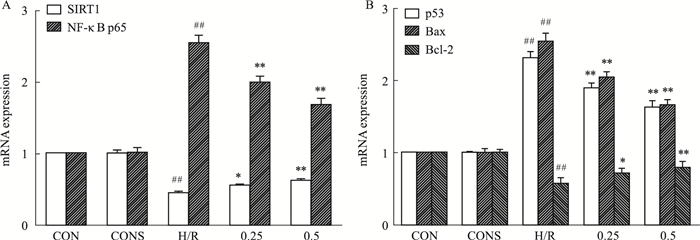
如Fig 5所示,与空白对照相比,H/R组NF-κB p65、p53、Bax的mRNA表达水平明显增高,SIRT1、Bcl-2的mRNA表达水平降低(P < 0.01);与H/R组相比,药物预处理后的H/R组NF-κB p65、p53、Bax的mRNA表达水平降低,SIRT1、Bcl-2的mRNA表达水平增高(P < 0.05,P < 0.01)。
|
| Fig 5 Effect of Sal B on relative mRNA levels in BRL-3A cells induced by H/R A:mRNA expression levels of SIRT1, NF-κB p65; B: mRNA expression levels of p53, Bax, Bcl-2. ##P < 0.01 vs CON; *P < 0.05, **P < 0.01 vs H/R. |
肝IRI作为一个复杂的病理生理过程,在大型的肝脏手术中,尤其是肝移植术中常常是无法避免的。通过了解肝IRI发生的机制发现,炎症反应、肝细胞的凋亡、坏死等都是引起肝损伤的重要原因,因此,控制细胞凋亡和炎症的发生可以减轻IRI[7]。Sal B由于其改善血流量、抗炎、抗氧化等功能,已经应用于大量心脑血管疾病的研究[8]。Wang等[9]发现,Sal B通过调控TLR4/MyD88/TRAF6信号通路,使NF-κB p65的表达降低,减轻了心脏IRI。Li等[10]发现,Sal B通过SIRT1作用,降低乙酰化p53表达,从而对抗乙醇性的急性肝损伤。因此,我们推测Sal B也能够通过减轻炎症及凋亡,缓解肝脏IRI。研究中我们建立了BRL-3A的H/R模型模拟肝脏IRI,用各种浓度的Sal B干预H/R处理的细胞,发现Sal B 0.5 μmol·L-1时,H/R的肝细胞活力最强,且该浓度能明显抑制H/R后的细胞凋亡,降低转氨酶AST、ALT含量,降低TNF-α、IL-1β分泌,表明Sal B能够减少炎性反应和凋亡来保护H/R诱导的肝细胞损伤。这与Lv等[11]通过建立大鼠大脑中动脉闭塞手术模型,验证Sal B作用时所得结果是一致的。
SIRT1作为一种依靠NAD+的Sirtuin蛋白家族中的重要一员,因为其去乙酰化作用,调控p53、NF-κB p65等常见的转录因子,发挥抗炎症反应和抗凋亡的作用[12]。本实验研究证实,不管在蛋白还是mRNA层面,与空白对照相比,H/R诱导后,NF-κB p65、p53、Bax表达明显上调,SIRT1、Bcl-2表达下调; 而Sal B干预后,与H/R组相比,NF-κB p65、p53、Bax表达下调,SIRT1、Bcl-2表达增高。这与Hernández-Jiménez等[13]通过对SIRT1沉默的转基因小鼠脑缺血/再灌注处理后得到的结果一致。Liu等[14]也证实了在H/R条件下,激活SIRT1能降低Bax、p53等的表达。但本实验只在体外进行了验证,未能对相关通路进行更充分的研究,后续实验中我们会加入动物实验,明确Sal B对IRI更加确切的机制。
综上,Sal B能保护H/R诱导的肝细胞损伤,其机制可能与SIRT1/NF-κB/p53通路有关系。
( 致谢: 本实验在重庆医科大学附属第一医院实验研究中心完成,在此感谢在实验中给予指导和帮助的各位老师和同学。)
| [1] | Hu J, Zhu X, Zhang X, et al. Targeting TRAF3 signaling protects against hepatic ischemia/reperfusions injury[J]. J Hepatol, 2016, 64(1): 146-59. doi:10.1016/j.jhep.2015.08.021 |
| [2] | Lin Y, Sheng M, Weng Y, et al. Berberine protects against ischemia/reperfusion injury after orthotopic liver transplantation via activating Sirt1/FoxO3α induced autophagy[J]. Biochem Biophys Res Commun, 2017, 483(2): 885-91. doi:10.1016/j.bbrc.2017.01.028 |
| [3] | Huang W, Shang W, Wang H, et al. Sirt1 overexpression protects murine osteoblasts against TNF-α-induced injury in vitro by suppressing the NF-κB signaling pathway[J]. Acta Pharmacol Sin, 2012, 33(5): 668-74. |
| [4] | Datta G, Fuller B, Davidson B. Molecular mechanisms of liver ischemia reperfusion injury: insights from transgenic knockout models[J]. World J Gastroenterol, 2013, 19(11): 1683-98. doi:10.3748/wjg.v19.i11.1683 |
| [5] | 林超, 刘兆国, 钱星, 等. 丹酚酸B在心血管疾病中药理作用研究进展[J]. 中国药理学通报, 2015, 31(4): 449-51. Lin C, Liu Z G, Qian X, et al. Research progress of salvianolic acid B in cardiovascular diseases[J]. Chin Pharmacol Bull, 2015, 31(4): 449-51. |
| [6] | Wang R, Huang F, Chen Z, et al. Downregulation of connexin 32 attenuates hypoxia/reoxygenation injury in liver cells[J]. J Biochem Mol Toxicol, 2015, 29(4): 189-97. doi:10.1002/jbt.2015.29.issue-4 |
| [7] | He D, Guo Z, Pu J, et al. Resveratrol preconditioning protects hepatocytes against hepatic ischemia reperfusion injury via toll-like receptor 4/nuclear factor-κB signaling pathway in vitro and in vivo[J]. Int Immunopharmacol, 2016, 35: 201-9. doi:10.1016/j.intimp.2016.03.032 |
| [8] | 王新宇, 王曼, 孙帅军, 等. 丹酚酸B保护大鼠缺血心肌与炎症小体NLRP3表达的相关性研究[J]. 中国药理学通报, 2016, 32(10): 1383-8. Wang X Y, Wang M, Sun S J, et al. Protective effects of salvianolic acid B on isoproterenol induced myocardial ischemic rats and its relation with NLRP3 expression[J]. Chin Pharmacol Bull, 2016, 32(10): 1383-8. doi:10.3969/j.issn.1001-1978.2016.10.011 |
| [9] | Wang Y, Chen G, Yu X, et al. Salvianolic acid B ameliorates cerebral ischemia/reperfusion injury through inhibiting TLR4/MyD88 signaling pathway[J]. Inflammation, 2016, 39(4): 1503-13. doi:10.1007/s10753-016-0384-5 |
| [10] | Li M, Lu Y, Hu Y, et al. Salvianolic acid B protects against acute ethanol-induced liver injury through Sirt1-mediated deacetylation of p53 in rats[J]. Toxicol Lett, 2014, 228(2): 67-74. doi:10.1016/j.toxlet.2014.04.011 |
| [11] | Lv H, Wang L, Shen J, et al. Salvianolic acid B attenuates apoptosis and inflammation via Sirt1 activation in experimental stroke rats[J]. Brain Res Bull, 2015, 115: 30-6. doi:10.1016/j.brainresbull.2015.05.002 |
| [12] | Nakazawa H, Chang K, Shinozaki S, et al. Inos as a driver of inflammation and apoptosis in mouse skeletal muscle after burn injury: possible involvement of SIRT1 S-nitrosylation-mediated acetylation of p65 NF-κB and p53[J]. PLoS One, 2017, 12(1): e0170391. doi:10.1371/journal.pone.0170391 |
| [13] | Hernández-Jiménez M, Hurtado O, Cuartero M, et al. Silent information regulator 1 protects the brain against cerebral ischemic damage[J]. Stroke, 2013, 44(8): 2333-7. doi:10.1161/STROKEAHA.113.001715 |
| [14] | Liu L, Wang P, Liu X, et al. Exogenous NAD+ supplementation protects H9c2 cardiac myoblasts against hypoxia/reoxygenation injury via SIRT1-p53 pathway[J]. Fundam Clin Pharmacol, 2014, 28(2): 180-9. doi:10.1111/fcp.2014.28.issue-2 |

