

2. 潍坊医学院药理学教研室,山东省重点应用药理学实验室,山东 潍坊 261053;
3. 广东药科大学中药学院中药药理教研室,广东 广州 510006
2. Dept of Pharmacology, Weifang Medical College, the Key Lab of Applied Pharmacology in Shandong Province, Weifang Shandong 261053, China;
3. Dept of Pharmacology of Chinese Materia Medica, Institute of Traditional Chinese Medicine, Guangdong Pharmaceutical University, Guangzhou Guangdong 510006, China
伴随着糖尿病(diabetes mellitus, DM)发病率的逐年升高,糖尿病肾病已成为导致终末肾病的重要原因之一[1]。目前,糖尿病肾病缺乏有效的特异性治疗,临床常用的西药有血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂等,上述药物虽然在防治糖尿病肾病方面发挥了重要作用,但临床上仍有大量糖尿病患者肾功能逐步恶化,故探索新的对糖尿病引起的肾损伤具有保护作用的药物,是一项重要的医学课题。近年研究显示,TGF-β1/Smads信号通路在糖尿病肾病的发病过程中起重要作用,是糖尿病肾病的一个重要的可干预靶点[2]。课题组前期研究发现,中药黄芪提取物黄芪多糖(astragalus polysaccharide, APS)可减轻糖尿病大鼠早期多尿症状[3]。但APS对糖尿病机体肾脏TGF-β1/Smads信号通路是否具有作用,未见报道。本研究拟就上述问题进行探索,以探讨APS治疗糖尿病肾脏损伤的可能机制。
1 材料与方法 1.1 材料 1.1.1 实验动物Wistar大鼠,♂,体质量(200±20)g,购于山东鲁抗公司,合格证号:SCXK鲁20130001。饲养于(24±2)℃环境,每笼5只,动物适应新实验环境1周后开始实验。
1.1.2 药品与试剂APS纯度为70%(惠州市东方植物保健科技有限公司);链脲佐菌素(streptozotocin, STZ),购自美国Sigma公司;TGF-β1兔抗大鼠一抗、羊抗兔IgG(武汉博士德公司);Smad2、p-Smad2、Smad3、p-Smad3 ELISA试剂盒购自Cell Signaling公司;Smad7、基质金属蛋白酶(matrix metalloproteinase, MMP)2、MMP-9、组织金属蛋白酶抑制因子-1(tissue inhibitor of matrix metalloproteinases 1, TIMP-1)、TIMP-2、肾损伤分子-1(kidney injury molecule-1, KIM-1)、骨桥蛋白(osteopontin, OPN)ELISA试剂盒购于武汉华美公司。
1.1.3 仪器全自动生化分析仪(北京普朗新技术有限公司),eTouch血糖仪(美国强生公司),酶标仪(美国Molecular Devices公司)。
1.2 方法 1.2.1 模型制备及分组选择50只健康Wistar大鼠,参照文献报道[3],每只大鼠腹腔注射55 mg·kg-1 STZ(pH 4.5,现用现配)1次。3 d后用血糖仪检测尾静脉血糖,从中选择随机血糖≥16.7 mmol·L-1的30只大鼠纳入后续实验,并随机分为DM组、APS低、高剂量组,每组10只。另取10只健康Wistar大鼠作为正常组。
1.2.2 药物治疗分组后,APS低、高剂量组大鼠分别给予200、400 mg·kg-1·d-1的APS,灌胃给药,每日1次,连续用药8周。DM组与正常组大鼠给予相同体积的生理盐水。
1.2.3 血糖、血肌酐、尿素氮检测实验结束,称重大鼠,血糖仪测空腹血糖(fasting blood-glucose, FBG)水平。颈总动脉取血,采用全自动生化分析仪检测血肌酐、尿素氮(blood urea nitrogen, BUN)水平。处死大鼠后,取肾脏称重,计算肾重/体重。
1.2.4 Western blot分析实验结束处死大鼠,取部分新鲜的肾组织,提取总蛋白,将40 μg蛋白样品经电泳分离后转移至硝酸纤维素膜,封闭液封闭1 h,一抗(TGF-β1稀释度为1 :1 000;β-actin稀释度为1 :1 000)4℃过夜,洗涤3次,二抗溶液中37℃孵育2 h,显影,定影,采用Image J进行检测分析,蛋白相对表达量=目的蛋白条带灰度/β-actin条带灰度。
1.2.5 ELISA检测代谢笼收集大鼠尿液,ELISA检测尿KIM-1、尿OPN浓度。取部分新鲜的肾组织匀浆,将匀浆液离心后保存上清液。ELISA检测肾组织中Smad2、p-Smad2、Smad3、p-Smad3、Smad7、MMP-2、MMP-9、TIMP-1、TIMP-2水平。
1.2.6 统计学处理实验数据以x±s表示,采用SPSS 19.0统计软件对数据进行单因素方差分析,组间差异比较采用q检验。
2 结果 2.1 APS对大鼠血糖水平的影响如Tab 1所示,与正常组比较,DM组大鼠血糖明显升高(P<0.05)。与DM组比较,APS低、高剂量组大鼠血糖降低(P<0.05),且高剂量组较低剂量组有进一步下降趋势。
| Group | FBG/ng·L-1 | Kidney weight/body weight | KIM-1/ng·L-1 | OPN/ng·L-1 | Creatinine/μmol·L-1 | BUN/mmol·L-1 |
| Normal | 4.67±0.85 | 0.0073±0.0009 | 11.04±3.27 | 14.03±2.35 | 43.71±5.29 | 4.97±0.38 |
| DM | 12.59±1.01# | 0.0150±0.0016# | 67.91±8.21# | 58.53±6.84# | 62.58±4.03# | 7.41±0.54# |
| APS-low | 10.32±0.87* | 0.0118±0.0010* | 49.36±5.83* | 40.19±5.10* | 51.04±4.33* | 6.35±0.42* |
| APS-high | 9.55±0.80 * | 0.0090±0.0008*△ | 34.55±5.16*△ | 27.63±4.82*△ | 49.60±5.19* | 5.96±0.51* |
| #P < 0.05 vs normal; *P < 0.05 vs DM; △P < 0.05 vs APS-low | ||||||
如Tab 1所示,与正常组比较,DM组大鼠肾重/体重、尿KIM-1、尿OPN、血肌酐、血尿素氮浓度明显升高(P<0.05),说明糖尿病引起了大鼠肾脏损伤。与DM组比较,APS低、高剂量组大鼠上述指标水平均明显减低(P<0.05),且高剂量组肾重/体重、尿KIM-1、OPN浓度明显低于低剂量组(P<0.05),说明APS剂量依赖性地改善了糖尿病大鼠的肾脏损伤。
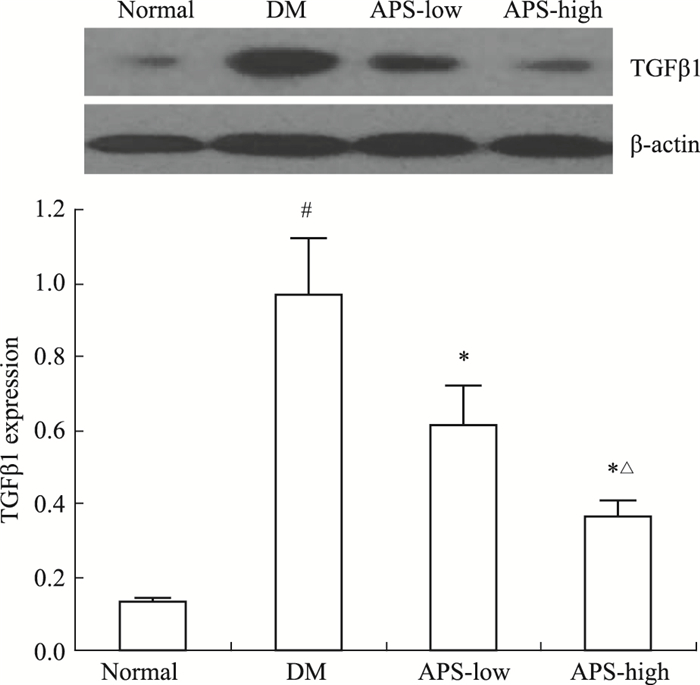
2.3 APS对大鼠肾脏TGF-β1水平的影响如Fig 1 Western blot结果显示,与正常组比较,DM组大鼠肾脏TGF-β1水平明显升高(P<0.05)。与DM组比较,APS低、高剂量组大鼠肾脏TGF-β1水平均明显减低(P<0.05);且高剂量组明显低于低剂量组(P<0.05),说明APS剂量依赖性地抑制了糖尿病大鼠的肾脏TGF-β1表达。
|
| Fig 1 Expression of renal TGF-β1 #P < 0.05 vs normal group; *P < 0.05 vs DM; △P < 0.05 vs APS-low |
如Tab 2所示,与正常组比较,DM组大鼠肾脏Smad2、p-Smad2、Smad3、p-Smad3水平明显升高(P<0.05),而Smad7水平明显降低(P<0.05)。与DM组比较,APS低、高剂量组大鼠肾脏Smad2、p-Smad2、Smad3、p-Smad3水平均明显减低(P<0.05),而Smad7水平明显升高(P<0.05)。且APS高剂量组Smad2、p-Smad2、Smad3、p-Smad3水平低于APS低剂量组(P<0.05),Smad7水平高于APS低剂量组(P<0.05)。
| Group | Smad2/ng·L-1 | p-Smad2/ng·L-1 | Smad3/ng·L-1 | p-Smad3/ng·L-1 | Smad7/ng·L-1 |
| Normal | 34.13±5.68 | 10.46±2.08 | 28.63±4.12 | 9.50±1.48 | 20.37±1.71 |
| DM | 90.96±9.52# | 69.34±9.35# | 83.15±10.71# | 64.04±8.52# | 10.25±1.20# |
| APS-low | 70.01±8.05* | 47.34±6.93* | 64.04±7.82* | 40.18±6.61* | 14.01±1.06* |
| APS-high | 55.27±7.16*△ | 27.06±4.11*△ | 49.11±6.00*△ | 24.52±3.87*△ | 16.95±1.80*△ |
| #P < 0.05 vs normal; *P < 0.05 vs DM; △P < 0.05 vs APS-low | |||||
如Tab 3显示,与正常组比较,DM组大鼠肾脏MMP-2、MMP-9水平明显降低(P<0.05),而TIMP-1、TIMP-2水平明显升高(P<0.05)。与DM组比较,APS低、高剂量组大鼠肾脏MMP-2、MMP-9水平明显升高(P<0.05),而TIMP-1、TIMP-2水平明显减低(P<0.05);且高剂量组变化较低剂量组更为明显(P<0.05)。
| Group | MMP2/ng·L-1 | MMP9/ng·L-1 | TIMP-1/ng·L-1 | TIMP-2/ng·L-1 |
| Normal | 119.88±13.10 | 204.17±16.55 | 12.09±1.14 | 10.22±1.55 |
| DM | 63.16±8.03# | 122.62±11.98# | 79.25±9.08# | 53.25±6.97# |
| APS-low | 80.63±9.41* | 147.00±10.03* | 55.64±8.94* | 38.75±5.31* |
| APS-high | 98.50±8.75*△ | 176.05±13.40*△ | 35.06±5.49*△ | 25.62±4.04*△ |
| #P < 0.05 vs normal; *P < 0.05 vs DM; △P < 0.05 vs APS-low | ||||
糖尿病肾病是糖尿病一种常见的并发症,目前尚缺乏特异性的防治措施。临床上通常在严格控制血糖基础上,应用血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂等加以防治,但上述措施很难完全阻止肾功能恶化。我国传统医学在糖尿病及其并发症的防治上发挥了重要作用,近年研究显示一些中药提取物可部分减轻糖尿病引起的肾损伤[4]。APS是中药黄芪的一种提取物,资料表明,APS可缓解糖尿病动物模型的炎症反应,改善胰岛功能、降低血糖水平,改善糖尿病引起的肝脏、肾脏等脏器损伤,在糖尿病及其多种并发症的防治上显示了较好的疗效[5]。本研究以APS治疗糖尿病大鼠,发现APS可明显降低糖尿病大鼠肾损伤标志物尿KIM-1、OPN、肌酐、尿素氮的水平,表明APS对糖尿病引起的肾损伤有保护作用,这与课题组前期发现相一致[3]。在评价肾功能损伤时,尿KIM-1、尿OPN比肌酐、尿素氮等指标更为敏感,后者通常在肾功能严重下降时才发生明显变化,而尿KIM-1、尿OPN水平在肾脏存在轻微损伤时即发生明显变化,在新近文献中常被用来评价肾脏早期损伤[6]。
糖尿病肾病的发生机制复杂,TGF-β/Smads信号通路的变化被认为与糖尿病肾病关系密切[7]。TGF-β1是TGF-β家族中一个核心成员,具有广泛的生物学效应。如果TGF-β1表达水平过高,在肾脏它可促进成纤维细胞生长、增加细胞外基质含量,引起肾脏硬化。文献显示,糖尿病肾病机体肾脏TGF-β1表达异常升高,而控制其表达水平则有利于改善糖尿病引起的肾损害,是糖尿病肾病一个重要的可干预靶点[8]。本研究显示,糖尿病大鼠肾脏TGF-β1含量较正常大鼠明显升高,这与既往文献报道一致[8]。而经过APS干预,糖尿病大鼠肾脏TGF-β1水平明显下降,且APS疗效呈剂量依赖性,该结果表明APS对TGF-β1信号有抑制作用。在体内,TGF-β1作用的发挥是通过复杂的信号通路实现的,Smad分子是参与TGF-β1信号传导的一族蛋白。Smad家族包括Smad 1、2、3、4、5、6、7、8等,其中Smad2、Smad3被认为在糖尿病肾病发病的过程中起重要作用[9]。TGF-β1与其受体结合后,募集并磷酸化Smad2、Smad3等。作为受体调节型的Smads,Smad2、Smad3被活化后与Smad4结合形成转录复合物,由胞质进入细胞核启动靶基因的转录,最终影响一些参与肾脏损伤的分子的表达。而Smad7被认为是一种抑制型Smad,对TGF-β1信号通路有抑制作用[10]。本研究中,糖尿病大鼠肾脏Smad2、Smad3、p-Smad2、p-Smad3水平较正常大鼠明显增高,而Smad7水平降低。与此类似,其他文献也报道糖尿病机体肾脏等Smads表达发生变化[10-11]。而在本研究中,经过APS干预后,糖尿病大鼠肾脏Smad2、Smad3、p-Smad2、p-Smad3水平明显降低,而Smad7水平明显升高,且APS的作用呈剂量依赖性,说明APS明显抑制了TGF-β1下游分子的Smad2、Smad3的表达及其活化,而同时又增加了抑制型Smad的表达。因TGF-β1/ Smads信号通路在糖尿病肾病的发病中具有重要作用,推断APS对糖尿病大鼠肾脏的保护作用可能与调节其TGF-β1/Smads信号通路有关。除本研究发现APS对糖尿病大鼠肾脏TGF-β1/Smads信号通路具有调节作用外,黄进等[12]研究发现,APS可通过抑制大鼠TGF-β1/Smads信号通路而改善CCl4引起的肝纤维化。此外,尚有研究显示其他一些药物也可通过调节TGF-β1/Smads信号通路,而对糖尿病动物发挥肾脏保护作用[9, 11]。
TGF-β1/Smads信号通路的最终效应是通过调控一些下游分子的表达而实现的。研究显示MMP的表达受到TGF-β的调控[13]。MMP属于Zn2+依赖的中性蛋白酶家族,在肾小球系膜细胞、成纤维细胞等多种细胞均有表达。在肾脏,MMP可降解胶原、分解基质,在防止肾小球硬化方面具有重要作用[14]。既往文献显示,当TGF-β水平增高时,糖尿病机体肾脏MMP表达通常会降低[15]。与此一致,本研究显示糖尿病大鼠肾脏组织中MMP-2、MMP-9水平较正常组大鼠明显降低。此外,TIMP的表达也受到是TGF-β1/Smads信号调控,TIMP具有强烈抑制MMP生物学活性的作用[14]。MMP通常以酶原的形式分泌,需要通过活化后才具有生物学活性,而TIMP可严重干扰MMP的活化过程,抑制MMP生物学活性的发挥。研究显示,TIMP在正常肾组织表达较少,而患有糖尿病肾病时肾脏TIMP表达明显升高。与既往文献报道一致,本研究中DM组大鼠肾脏TIMP-1、TIMP-2表达较正常组大鼠明显升高。然而,经过APS干预后,糖尿病大鼠肾组织中MMP-2、MMP-9水平明显升高,而且TIMP-1、TIMP-2水平则明显降低。该结果表明APS对TGF-β1/Smads信号通路的下游分子的表达具有调节作用。
综上所述,APS对糖尿病引起的肾脏损伤具有保护作用,其保护作用可能与抑制TGF-β1/Smads信号通路有关。
( 致谢: 本实验于山东省重点潍坊医学院应用药理学实验室、山东中医药大学基础医学院完成,向参与本实验的所有实验室研究人员致以感谢!)
| [1] | Prischl F C, Auinger M, Säemann M, et al. Diabetes-related end-stage renal disease in Austria 1965-2013[J]. Nephrol Dial Transplant, 2015, 30(11): 1920-7. doi:10.1093/ndt/gfv113 |
| [2] | 李峥, 王灿, 宋丹青, 等. 小檗碱类似物Y53在STZ诱导的糖尿病C57BL/6J小鼠中抗糖尿病肾病的作用研究[J]. 中国药理学通报, 2016, 32(9): 1236-42. Li Z, Wang C, Song D Q, et al. Study of anti-diabetic nephropathy efficacy of berberine analogue Y53 in STZ-induced diabetic C57BL/6J mice[J]. Chin Pharmacol Bull, 2016, 32(9): 1236-42. |
| [3] | 康白, 毛淑梅, 李承德, 等. 黄芪多糖对糖尿病大鼠早期多尿的保护作用[J]. 中国药理学通报, 2009, 25(11): 1470-3. Kang B, Mao S M, Li C D, et al. Protective action of astragalus polysaccharides on kidney in diabetic rats[J]. Chin Pharmacol Bull, 2009, 25(11): 1470-3. doi:10.3321/j.issn:1001-1978.2009.11.018 |
| [4] | Ho C, Hsu Y C, Lei C C, et al. Curcumin rescues diabetic renal fibrosis by targeting superoxide-mediated Wnt signaling pathways[J]. Am J Med Sci, 2016, 351(3): 286-95. doi:10.1016/j.amjms.2015.12.017 |
| [5] | Cui K, Zhang S, Jiang X, et al. Novel synergic antidiabetic effects of Astragalus polysaccharides combined with Crataegus flavonoids via improvement of islet function and liver metabolism[J]. Mol Med Rep, 2016, 13(6): 4737-44. doi:10.3892/mmr.2016.5140 |
| [6] | Qiu S, Sun G, Zhang Y, et al. Involvement of the NF-κB signaling pathway in the renoprotective effects of isorhamnetin in a type 2 diabetic rat model[J]. Biomed Rep, 2016, 4(5): 628-34. doi:10.3892/br.2016.636 |
| [7] | Nie Y, Li S, Yi Y, et al. Effects of astragalus injection on the TGFβ/Smad pathway in the kidney in type 2 diabetic mice[J]. BMC Complement Altern Med, 2014, 14: 148. doi:10.1186/1472-6882-14-148 |
| [8] | Voelker J, Berg P H, Sheetz M, et al. Anti-TGF-β1 antibody therapy in patients with diabetic nephropathy[J]. J Am Soc Nephrol, 2017, 28(3): 953-62. doi:10.1681/ASN.2015111230 |
| [9] | Al-Onazi A S, Al-Rasheed N M, Attia H A, et al. Ruboxistaurin attenuates diabetic nephropathy via modulation of TGF-β1/Smad and GRAP pathways[J]. J Pharm Pharmacol, 2016, 68(2): 219-32. doi:10.1111/jphp.2016.68.issue-2 |
| [10] | Zhang Y, Wang S, Liu S, et al. Role of Smad signaling in kidney disease[J]. Int Urol Nephrol, 2015, 47(12): 1965-75. doi:10.1007/s11255-015-1115-9 |
| [11] | Wu J S, Shi R, Lu X, et al. Combination of active components of Xiexin decoction ameliorates renal fibrosis through the inhibition of NF-κB and TGF-β1/Smad pathways in db/db diabetic mice[J]. PLoS One, 2015, 10(3): e0122661. doi:10.1371/journal.pone.0122661 |
| [12] | 黄进, 张晨, 詹菲, 等. 黄芪多糖对肝纤维化大鼠TGF-β1/Smads信号通路的影响[J]. 中华中医药杂志, 2015, 30(6): 2184-6. Huang J, Zhang C, Zhan F, et al. Effects of astragalan on liver fiborosis rat in TGFβ1/Smads signal pathway[J]. Chin J Tradit Chin Med Pharm, 2015, 30(6): 2184-6. |
| [13] | 边晓慧. MMPs表达与调控的研究进展[J]. 国外医学·泌尿系统分册, 2004, 24(1): 136-9. Bian X H. Review of the expression and regulation of MMPs[J]. Foreign Med Sci (Urol Nephrol), 2004, 24(1): 136-9. |
| [14] | Wang J, Gao Y, Ma M, et al. Effect of miR-21 on renal fibrosis by regulating MMP-9 and TIMP1 in kk-ay diabetic nephropathy mice[J]. Cell Biochem Biophys, 2013, 67(2): 537-46. doi:10.1007/s12013-013-9539-2 |
| [15] | Dixon A, Maric C. 17beta-Estradiol attenuates diabetic kidney disease by regulating extracellular matrix and transforming growth factor-beta protein expression and signaling[J]. Am J Physiol Renal Physiol, 2007, 293(5): F1678-90. doi:10.1152/ajprenal.00079.2007 |

