


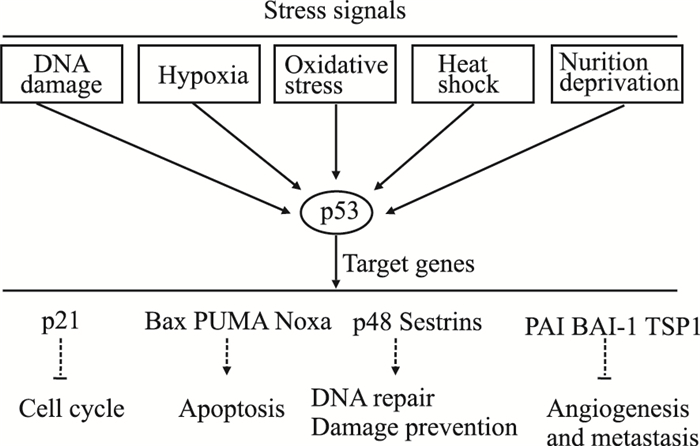
p53蛋白是一个重要的转录因子,通过调节p21、Bax、PTEN、p48、PAI等下游靶基因,阻滞细胞周期,诱导细胞凋亡与衰老、参与DNA损伤修复以及抑制血管生成(Fig 1),阻止肿瘤的发生与发展。突变p53则会缺失正常功能,获得促癌性作用,增强肿瘤的迁移运动和侵袭转移,加速肿瘤细胞出现耐药性,说明突变p53是促癌的一个重要因素,所以p53蛋白可以成为一个治疗肿瘤的药物靶点之一。目前,主要的治疗策略有阻断p53与MDM2相互作用、降解突变p53蛋白、抑制突变p53下游通路、RNA干扰突变p53表达、恢复突变p53构象等[1]。由于p53蛋白空间结构的柔韧性和灵活性,以p53为靶点恢复构象已成为一个研究热点[2],本文将重点阐述恢复突变p53的药物研究进展及其在肿瘤治疗中的作用机制。
|
| Fig 1 p53 signaling pathway |
p53蛋白单体由393个氨基酸残基组成,利用化学交联和质谱技术发现全长p53蛋白四级结构是1个细长的十字形结构,CD区与DNA结合,TAD区、CTD区以及Tet区向四周伸展[3]。p53蛋白核心区域多发生突变,失去DNA结合能力,研究发现四股β片层和五股β片层反平行相间形成的三明治结构支撑着p53核心区域,2个大的环结构(L2/L3)和1个环-片-螺旋结构域(loop-sheet-helix motif,LSH)在β片层骨架结构上共形成DNA结合面,p53蛋白结合靶基因的位置。人类肿瘤中发现突变p53位点多发生在此结合面上,破坏DNA结合的完整结构,改变与DNA的结合能力,失去正常生理功能。
鉴于p53蛋白突变主要发生在DNA核心区域,根据对DNA结合域(DNA binding domain,DBD)结构改变的影响,p53突变可分为3类。Ⅰ类突变是改变DNA接触面上氨基酸残基(Arg273、Arg248),失去与DNA结合能力的DNA接触突变,如R273H、R248Q。R273位点位于LSH二级结构域上,R248位点位于Loop L3上,与DNA磷酸骨架结合,精氨酸残基的胍基与邻近的氨基酸羰基通过疏水键、盐桥接合,稳定DNA结合结构[4]。第273位和第248位精氨酸发生突变后,盐桥和疏水作用减弱,对DNA的亲和力降低甚至丧失。Ⅱ类突变是改变β片层骨架与DNA接触面连接的氨基酸残基(Arg175、Arg249),影响DNA接触面正确定向的突变,如R175H、R249S。R175位点位于Loop L2结构,与锌离子位点邻近,它是连接Loop L2和Loop L3相互作用形成DNA核心区域构象的桥梁,R175的胍基提供疏水力,与Loop L2上的Met237和Loop L3上Ser183、Pro191的羰基相互作用,R175位点突变后,疏水作用消失,Loop L2和Loop L3不再作用,导致p53蛋白核心结构松散,失去功能。R249位点突变也是因为精氨酸突变,疏水力缺失,不能稳定Loop L3结构,DNA结合面改变,影响DBD作用。Ⅲ类突变发生在β片层骨架结构内,改变整个DBD区三级结构,如V143A、Y220C,V143A突变位于β股S3二级结构,Y220C突变位于S7-S8环结构,这两种突变体在37℃下没有蛋白活性,而在30℃和24℃下可以保持野生型或接近野生型的p53构象,激活p53下游靶基因如p21,有温度敏感性[5]。
2 突变p53作为肿瘤药物靶点在抑癌基因中,p53是研究最多的基因之一,其突变多为错义突变,发生在DNA结合区,突变p53蛋白在许多肿瘤细胞中稳定表达,且失去对PUMA、Bcl-2等基因转录激活作用,抑制癌细胞凋亡。Ventura1等[6]在小鼠体内恢复p53活性发现可以抑制肿瘤的生长,证实了重激活p53抗癌治疗的潜力。
人类活性p53蛋白以四聚体的形式存在,通过核心区与四聚体区之间的柔韧连接区将DNA螺旋包裹结合,p53突变后热力学和动力学稳定性下降,蛋白结构不稳定,活性构象改变,失去转录激活能力,但其不会失活,仍保持着构象从非折叠向折叠转换的能力[7]。一般来说,p53蛋白突变多为点突变,所以构象稳定性的改变是微小的,小分子化合物才可以恢复DNA结合表面的结构域。这种突变构象改变的微弱性以及自身结构的可恢复性,为设计小分子化合物恢复p53构象提供了可能性。
3 靶向突变p53药物研究PhiKan083是第一个根据Y220C突变型设计出来的咔唑类化合物(Fig 2A),Tyr220位于β片层与Loop S7/S8连接部位,Y220的侧链可以部分填补p53蛋白表面的结合裂缝,保持蛋白结构稳定,但Y220C突变打开了此结合裂缝,降低了结合表面蛋白的稳定性,改变了其构象失去活性[8]。半胱氨酸打开的这个裂缝成为了亲水性化合物结合位点,PhiKan083的咔唑环可以挤进裂缝,烷基占据裂缝底部,由于表面的结合裂缝是疏水性的,PhiKan083的甲酰胺基团恰好与Asp228主链的羰基疏水键相互作用,重新稳定裂缝,转变突变p53蛋白表面构象,进而恢复了活性。之后发现的PK7088(Fig 2B)和PhiKan083一样具有一个吡唑环结构,不过PK7088与Y220C的体外解离常数为140 μmol·L-1,小于PhiKan083与Y220C的解离常数,所以PK7088可以更好地结合并稳定Y220C突变体[9]。Bauer等[10]合成了含氟的PhiKan083衍生物,即在N-乙烷基上加氟原子,氟原子不仅可以和Leu145、Trp146的羰基相互作用,还可以与Cys220的巯基氢键结合,使氟原子倾向于结合裂缝的底部,产生的这种拉力使氟化的PhiKan083衍生物比PhiKan083对p53Y220C突变体的亲和力提高了5倍,让咔唑环更稳定地挤入裂缝。Wilcken等[11]筛选到二碘代酚系列化合物(Fig 2C),它的亲水性苯环骨架位于Y220C的裂缝中央,其中一个碘原子接近Cys220的硫原子,另一个碘原子与Leu145主链上氧原子共价结合,酚羟基疏水作用于Val147、Asp228,碘原子和酚羟基的共作用使得二碘代酚化合物更稳定有力地结合Y220C突变体。利用计算机分子动态(MD)模拟发现,羟基二苯甲酮类化合物上的羰基氧原子可以与Y220C突变体的Thr150、Thr230、Pro151、Cys220、Cys229氨基氢之间形成氢键(Fig 2D),与Y220C结构对接恢复其突变构象。羟基二苯甲酮类化合物与PhiKan083一样可以作为配体靶向p53突变位点,恢复突变结构,进而重激活转录功能。

|
| Fig 2 Structures of compounds targeted mutant p53 A: Phikan083; B: Phikan073; C: 2-hydroxy-3, 5-benzaldehyde iodide derivative; D: 1-hydroxy-2-methylanthraquinone derivative; E: PRIMA-1; F: PRIMA-1Met; G: MIRA-1; H: STIMA-1; I: WR1065; J: Stictic acid; K: ZMC1. |
最近报道的PRIMA-1Met(ARP-246)在血液恶性肿瘤和前列腺癌的Ⅰ/Ⅱ期临床试验效果良好,在卵巢癌患者中也进行到了Ⅰb/Ⅱ期临床试验[12]。酮类化合物PRIMA-1和PRIMA-1Met(APR-246)可以恢复R175H和R248Q突变体,诱导肿瘤细胞发生凋亡(Fig 2E、2F),作用机制是这两种化合物的分解底物亚甲基奎宁酮(methylene quinuclidinone,MQ)作为烷基配体,共价修饰突变p53核心区域上多个半胱氨酸的巯基,阻止二硫键相互作用引起的p53聚集。MQ也可以与半胱氨酸残基通过氢键疏水键共价结合形成新的DNA接触位点,突变p53直接获得BDB区的结合能力[13]。p53核心区域有10个半胱氨酸残基,MQ具体与哪个位点的半胱氨酸结合目前并不清楚,不过Cys182、Cys229、Cys242和Cys277这4种氨基酸暴露在核心表面,猜测MQ可能与它们结合。p53核心区域有个L1/S3口袋结构,p53二级结构突变多集中在此区域,Cys124、Cys135、Cys141位于L1/S3中心位置。MQ作为烷基化配体与突变p53R273H的Ser116、Gly117直接反应对接L1/S3结构,恢复p53活性[14]。顺丁烯二酰亚胺类似物MIRA(Fig 2G)、喹啉唑衍生物STIMA-1(Fig 2H)和氨磷汀活性代谢物WR1065(Fig 2I)同样作为烷基化配体,与半胱氨酸残基的巯基和赖氨酸残基的氨基反应,恢复R175、R273、G248、V272位点突变。早期研究发现,大部分p53突变体中L1/S3口袋结构是打开的,Cys124突变成Ala124后,在空间上部分阻塞这个开口结构,阻止小分子化合物与L1/S3结构对接,失去对半胱氨酸残基烷基化功能,抑制恢复p53活性,如C124A解除PRIMA-1对p53R175H重激活作用[15]。芳香族有机化合物Stictic acid(Fig 2J)直接与GLn144发生烷基化反应,间接与GLy112、Ser116、Cys124相互作用,这种与氨基酸的多作用力增强了Stictic acid分子与L1/S3结构的对接能力,此外,Stictic acid分子结构比MQ大,使L1/S3结构被迫打开,所以不会被C124A突变抑制功能[15]。
p53蛋白的Arg175侧链胍基可以与Pro191、Met237、Asp184利用疏水力、盐桥相互作用,这种分子布局与锌离子配体中的Cys176、His179、Cys238相邻,精氨酸突变成组氨酸后,失去作用力,降低与锌离子的亲和力,甚至失去锌离子配体,锌离子的缺失会进一步导致p53蛋白热力稳定性下降,增加聚集倾向,此时的p53成为脱辅基蛋白失去功能。前期研究发现[16],MMTV-neu转基因小鼠的乳腺癌肿瘤对阿霉素有耐药性,锌离子联合使用会抑制小鼠体内乳腺癌肿瘤的生长。在SK-BR-3(p53R175H)乳腺癌细胞和U373MG(p53R273H)人胶质瘤细胞中,锌离子会诱导突变型p53R175H/R273H部分转变成有功能活性的野生型p53[17]。锌离子的这种特殊作用引起了研究学者的兴趣,随后筛选得到的缩氧硫脲类化合物NSC319726作为锌离子螯合剂(ZMC1),运送锌离子到p53R175H蛋白(Fig 2K),恢复p53R175H蛋白缺失锌离子状态,重获蛋白活性。缩氧脲类化合物螯合铁离子产生羟基自由基会攻击p53蛋白上半胱氨酸的巯基发生氧化还原反应,影响p53蛋白构象折叠[18]。Blanden等[19]合成了1个ZMC1,螯合锌离子能力比NSC319726强,调控细胞内锌离子浓度,能够为恢复p53R175H构象提供最适锌离子浓度范围。Garufi等[20]利用pAb1620和pAb240抗体免疫荧光实验,发现锌离子姜黄素复合物依赖于锌离子恢复p53R175H、R273H蛋白构象,不过具体分子机制有待进一步研究。最近,Aggarual等[21]在十字花科蔬菜中提取出的苯乙基异硫氰酯(PEITC),可以抑制SK-BR-3(p53R175H)细胞生长,诱导其凋亡。研究发现,ZnCl2可以提高PEITC活性,猜测PEITC可能作为一种锌离子伴侣,恢复p53R175H的构象,其中小分子作用机制有待进一步证明。
目前发现,除了小分子化合物类可以恢复突变p53构象,还有多肽类分子,如多肽46,第1个来自p53-C端区域的人工合成肽(361-382),可以替代突变p53的CTD区,与核心区带电氨基酸结合,改变蛋白构象,恢复R175H和R273H突变体DNA结合功能[22]。另一个多肽小分子CDB3,根据p53结合蛋白53BP2区域(490-498)设计出来的9个多肽物,与核心区上多个位置结合,集中在Loop3和Helix2之间。实验发现,FL-CDB3可以和G245S、R249S结构突变体结合,恢复构象折叠,提高β片层突变I195T与DNA结合的Kd值,恢复p53(R175H、R237H)转录激活功能。CDB3自身与突变p53结合后,p53蛋白会被激活,重新结合的靶基因会占据CDB3位置,进而被释放回细胞,继续靶向其他突变p53[23]。最近发现的两亲性穿透肽p28,一段来自天青蛋白的28个氨基酸序列多肽,可以进入癌细胞,与p53蛋白的DNA结合域结合,恢复突变体活性。p28主要结合位点在非突变Loop L1(氨基酸112-124)和突变Loop L7/L8区域(Y220C、P223L)。两性亲和特性使p28可以改变Loop L1、Loop L7/L8二级结构上疏水氨基酸残疾的疏水性,如Leu114、Cys124,只是调整p53 DBD二级结构,不会改变p53整体构象[24]。多肽小分子虽然可以进入细胞发挥恢复p53功能作用,不过较小分子化合物来说,后期研究进入人类体内很难保持稳定性,发挥作用。
4 总结与展望目前以突变p53为靶点恢复构象的主要有多肽类和小分子化合物,但是大部分小分子化合物是利用细胞和蛋白实验筛选得到,生物学效应研究的较为清楚,对于它们中的大多数,分子化学作用机制仍没有完全理解,这将会成为以后重点研究方向。近几年来,基于蛋白质和细胞筛选体系,虽已有许多p53活化物被发现,但其中大部分不直接和p53蛋白结合,而是抑制p53与MDM2的相互作用,如Nutlin-3[25],或是抑制突变p53分子伴侣进而降解突变p53,如17AAG、SAHA。目前,直接针对p53蛋白结构的药物设计处于初级阶段,p53蛋白突变并不会导致蛋白失去活性,其仍具有热力动力学不稳定的特性,所以小分子化合物可以直接对接p53蛋白,恢复活性构象。了解突变p53蛋白结构是恢复其活性的前提,目前面临最大的挑战是精准地探索出不同p53突变体的结构特征,与此同时,由于个体的差异性,发展先进的诊断方法,确定不同癌症患者突变p53的类型,实现癌症的精准治疗也是必不可少的。
| [1] | Parrales A, Iwakuma T. Targeting oncogenic mutant p53 for cancer therapy[J]. Front Oncol, 2015, 5: 288. |
| [2] | Leelananda S P, Lindert S. Computational methods in drug discovery[J]. Beilstein J Org Chem, 2016, 125: 2694-718. |
| [3] | Demir O, Ieong P U, Amaro R E. Full-length p53 tetramer bound to DNA and its quaternary dynamics[J]. Oncogene, 2017, 36(10): 1451-60. doi:10.1038/onc.2016.321 |
| [4] | Kitayner M, Rozenberg H, Kessler N, et al. Structural basis of DNA recognition by p53 tetramers[J]. Mol Cell, 2006, 22(6): 741-53. doi:10.1016/j.molcel.2006.05.015 |
| [5] | Koulgi S, Achalere A, Sonavane U, et al. Investigating DNA binding and conformational variation in temperature sensitive p53 cancer mutants using QM-MM simulations[J]. PLoS One, 2015, 10(11): e0143065. doi:10.1371/journal.pone.0143065 |
| [6] | Ventura A, Kirsch D G, McLaughlin M E, et al. Restoration of p53 function leads to tumour regression in vivo[J]. Nature, 2007, 445(7128): 661-5. |
| [7] | Friedler A, Veprintsev D B, Hansson L O, et al. Kinetic instability of p53 core domain mutants: implications for rescue by small molecules[J]. J Biol Chem, 2003, 278(26): 24108-12. |
| [8] | Rauf S M, Endou A, Takaba H, et al. Effect of Y220C mutation on p53 and its rescue mechanism: a computer chemistry approach[J]. Protein J, 2013, 32(1): 68-74. doi:10.1007/s10930-012-9458-x |
| [9] | Liu X, Wilcken R, Joerger A C, et al. Small molecule induced reactivation of mutant p53 in cancer cells[J]. Nucleic Acids Res, 2013, 41(12): 6034-44. doi:10.1093/nar/gkt305 |
| [10] | Bauer M R, Jones R N, Baud M G, et al. Harnessing fluorine-sulfur contacts and multipolar interactions for the design of p53 mutant Y220C rescue drugs[J]. ACS Chem Biol, 2016, 11(8): 2265-74. doi:10.1021/acschembio.6b00315 |
| [11] | Wilcken R, Liu X, Zimmermann M O, et al. Halogen-enriched fragment libraries as leads for drug rescue of mutant p53[J]. J Am Chem Soc, 2012, 134(15): 6810-8. doi:10.1021/ja301056a |
| [12] | Bykov V J, Zhang Q, Zhang M, et al. Targeting of mutant p53 and the cellular redox balance by APR-246 as a strategy for efficient cancer therapy[J]. Front Oncol, 2016, 6: 21. |
| [13] | Lambert J M, Gorzov P, Veprintsev D B, et al. PRIMA-1 reactivates mutant p53 by covalent binding to the core domain[J]. Cancer Cell, 2009, 15(5): 376-88. |
| [14] | Omar S I, Tuszynski J. Ranking the binding energies of p53 mutant activators and their ADMET properties[J]. Chem Biol Drug Des, 2015, 86(2): 163-72. doi:10.1111/cbdd.12480 |
| [15] | Wassman C D, Baronio R, Demir O, et al. Computational identification of a transiently open L1/S3 pocket for reactivation of mutant p53[J]. Nat Commun, 2013, 4: 1407. doi:10.1038/ncomms2361 |
| [16] | Margalit O, Simon A J, Yakubov E, et al. Zinc supplementation augments in vivo antitumor effect of chemotherapy by restoring p53 function[J]. Int J Cancer, 2012, 131(4): E562-8. doi:10.1002/ijc.26441 |
| [17] | Puca R, Nardinocchi L, Porru M, et al. Restoring p53 active conformation by zinc increases the response of mutant p53 tumor cells to anticancer drugs[J]. Cell Cycle, 2011, 10(10): 1679-89. |
| [18] | Yu X, Vazquez A, Levine A J, et al. Allele-specific p53 mutant reactivation[J]. Cancer Cell, 2012, 21(5): 614-25. doi:10.1016/j.ccr.2012.03.042 |
| [19] | Blanden A R, Yu X, Wolfe A J, et al. Synthetic metallochaperone ZMC1 rescues mutant p53 conformation by transporting zinc into cells as an ionophore[J]. Mol Pharmacol, 2015, 87(5): 825-31. doi:10.1124/mol.114.097550 |
| [20] | Garufi A, Trisciuoglio D, Porru M, et al. A fluorescent curcumin-based Zn(Ⅱ)-complex reactivates mutant (R175H and R273H) p53 in cancer cells[J]. J Exp Clin Cancer Res, 2013, 32: 72. doi:10.1186/1756-9966-32-72 |
| [21] | Aggarwal M, Saxena R, Sinclair E, et al. Reactivation of mutant p53 by a dietary-related compound phenethyl isothiocyanate inhibits tumor growth[J]. Cell Death Differ, 2016, 23(10): 1615-27. doi:10.1038/cdd.2016.48 |
| [22] | Selivanova G, Ryabchenko L, Jansson E, et al. Reactivation of mutant p53 through interaction of a C-terminal peptide with the core domain[J]. Mol Cell Biol, 1999, 19(5): 3395-402. doi:10.1128/MCB.19.5.3395 |
| [23] | Friedler A, Hansson L O, Veprintsev D B, et al. A peptide that binds and stabilizes p53 core domain: chaperone strategy for rescue of oncogenic mutants[J]. Proc Natl Acad Sci U S A, 2002, 99(2): 937-42. doi:10.1073/pnas.241629998 |
| [24] | Signorelli S, Santini S, Yamada T, et al. Binding of amphipathic cell penetrating peptide p28 to wild type and mutated p53 as studied by raman, atomic force and surface plasmon resonance spectroscopies[J]. Biochim Biophys Acta, 2017, 1861(4): 910-21. |
| [25] | 代晓丽, 刘静, 罗瑛, 等. 靶向作用p53药物的研究进展[J]. 中国药理学通报, 2014, 30(7): 912-6. Dai X L, Liu J, Luo Y, et al. Research progress on drugs targeting p53[J]. Chin Pharmacol Bull, 2014, 30(7): 912-6. |

