


2. 宜春学院化学与生物工程学院药学教研室,江西 宜春 336000;
3. 中山大学附属第一医院麻醉科,广东 广州 510080;
4. 中山大学附属第一医院脊柱外科,广东 广州 510080;
5. 广东省骨科学重点实验室,广东 广州 510080
 ,
YI Zeng-xing2,
LIN Shi-qing3,
WANG Yi-min3,5,
CAI Zhe1,
WEI Ming3,
SUN Lai-bao1,5
,
YI Zeng-xing2,
LIN Shi-qing3,
WANG Yi-min3,5,
CAI Zhe1,
WEI Ming3,
SUN Lai-bao1,5
 ,
ZOU Xue-nong4,5
,
ZOU Xue-nong4,5
2. Dept of Pharmacology, Chemical and Biological Engineering Faculty, Yichun University, Yichun Jiangxi 336000, China;
3. Dept of Anesthesiology, the First Affiliated Hospital of Sun Yat-sen University, Guangzhou 510080, China;
4. Dept of Spine Surgery, the First Affiliated Hospital of Sun Yat-sen University, Guangzhou 510080, China;
5. Guangdong Provincial Key Lab of Orthopedics and Traumatology, Guangzhou 510080, China
慢性腰腿痛是导致劳动力丧失的主要疾病,给社会造成了沉重的经济负担。椎间盘突出髓核的生化致炎特性作用是引起周围神经根炎症,并引起慢性腰腿痛的主要原因,因此也成为当前腰椎间盘突出症发病机制的研究热点。p38促分裂原活化蛋白激酶(p38 mitogen-activated protein kinase, p38 MAPK)、白介素-18(interleukin-18, IL-18)及其受体(interleukin-18 receptor, IL-18R)的激活是导致神经病理性疼痛和炎症性疼痛的关键因素,并且它们之间存在着密切联系[1]。在腰椎间盘突出症导致腰腿痛的发病机制中,它们是否具有类似的效应,目前尚未阐明。临床实践表明,抑制炎症反应是治疗腰腿痛的重要措施。
中药单体蛇床子素(osthole, Ost)又名欧芹酚甲醚或甲基欧芹酚,能有效减轻由椎间盘突出诱发的急、慢性腰腿痛,但具体机制尚不清楚。本课题组前期研究提示,Ost能通过抑制髓核致炎神经根痛大鼠背根神经节内NOS、COX-2、降钙素基因相关肽受体1、3型酸敏感离子通道等的表达,抑制炎性痛的外周敏化,提高大鼠50%机械性撤足阈值(mechanical withdrawl threshold,MWT),从而达到缓解神经根痛觉过敏的作用[2-6],但是它能否抑制炎症在脊髓背角内的中枢敏化效应,值得我们进一步探讨。
1 材料与方法 1.1 实验动物SPF级♂成年SD大鼠156只,体质量(235±15)g,由广东省医学实验动物中心提供,许可证号:SCXK(粤)2013-0002。分笼饲养, 室温(20±2)℃, 维持大鼠12 h/12 h昼夜交替(每天8 :00~20 :00光照)。本实验严格遵守中山大学动物保护和使用的规定。
1.2 试剂与仪器蛇床子素(广州展晨生物科技有限公司),用100 mL·L-1二甲亚砜(DMSO,Sigma,USA)溶解;兔抗鼠IL-18一抗(DF6252,Affinity,USA);兔抗鼠IL-18R一抗(A1414,Santa Cruz, USA);兔抗鼠p-p38 MARK一抗(Thr180,Affinity,USA)。Frey纤毛仪(Stoelting公司,USA);冰冻组织包埋机(美国Thermo公司);倒置荧光显微镜(美国Sakura公司);显微照相系统(日本NIKON公司)。
1.3 动物模型建立、分组及处理 1.3.1 动物模型建立参照文献建立动物模型[6],质量浓度为35 g·L-1的水合氯醛麻醉大鼠(3.5 mL·kg-1,腹腔注射), 固定大鼠,手术区备皮后消毒铺巾,以两侧髂嵴最高点连线中点做30 mm左右正中切口,暴露皮肤组织和肌肉,关节定位后,分别咬除左侧L5下关节突、L6上关节突和L5半椎板,暴露左侧L5背根神经节(dorsal root ganglion, DRG)。从L5半椎板切除处将PE-10导管向头侧硬膜外腔轻柔置入约4 mm,并将其固定于同侧肌肉组织,另一端经皮下隧道从两耳之间引出,回抽无血和脑脊液流出,电凝灼烧封管固定,充分止血后,无菌生理盐水冲洗伤口。消毒鼠尾,20 G针头沿锥体间隙刺取近端2个节段自体髓核组织(约0.4 mg),置于L5 DRG周围。止血充分后逐层缝合伤口,聚维酮碘软膏擦拭缝合皮肤。Sham组取尾部自体髓核组织,但不将其置于L5 DRG部位,其余操作同上。
1.3.2 分组及处理SPF级成年♂SD大鼠156只,分为Blank组(n=36)、假手术组(Sham组,n=36)、模型组(NP组,n=36)、溶剂对照组(DMSO组,n=24)和蛇床子素组(Ost组,n=24)。术后d 2,DMSO组给予100 mL·L-1 DMSO,Ost组给予20 g·L-1蛇床子素,1 min内注射完,注射完毕后用100 mL·L-1 DMSO溶液10 μL冲尽导管内残留药液。将手术日记为d 0,各组大鼠分别于术前1 d(d-1),术后1天(d 1)、2天(d 2)、6天(d 6)、7天(d 7)、12天(d 12)、14天(d 14)、21天(d 21)和28天(d 28)测定50% MWT。给药后5天(d 7)和第12天(d 14)取术侧脊髓背角,用Western blot法检测p38 MAPK、IL-18和IL-18R的蛋白相对浓度。qPCR法测定IL-18 mRNA表达量。
1.4 测定50% MWT建模前,每日9 :00~16 :00将大鼠放于透明有机玻璃箱内自由活动,以适应测试环境,并于术前1 d测定大鼠的基础缩足阈值。术后行为学测试也在该时间段内进行,测试前,大鼠预先在玻璃箱中适应30 min,待其安静后再进行测试。检测50% MWT:大鼠置于玻璃箱内,安静后以不同强度的von Frey纤毛刺激大鼠足心部皮肤,避开肉垫使之稍成S形,持续6 ~ 8 s。若大鼠后肢出现迅速抬起、畏缩、撤回或舔舐足底,则认为是阳性反应。以2 g为初始刺激强度, 当该强度刺激不能引起阳性反应,则给予相邻大一级强度刺激;若有阳性反应则给予相邻小一级强度的刺激,每个强度重复刺激5次,如此连续进行,将出现3次以上阳性反应的最小von Frey纤维强度定为大鼠的50% MWT。相邻2次刺激至少间隔约15 s,每次刺激前大鼠均处于安静状态。
1.5 Western blot法检测p38、IL-18和IL-18R的蛋白相对浓度深麻醉下取出大鼠术侧腰段L4~6脊髓背角,用预冷的PBS缓冲液漂洗2 ~ 3次,去除污血,剪成小块置于匀浆器中。加入10倍于组织体积的组织蛋白提取试剂(使用前数分钟内加入蛋白酶抑制剂),冰浴彻底匀浆。将匀浆液转移至离心管中,振荡。冰浴30 min,期间用移液器反复吹打,确保匀浆液完全裂解,4℃、12 000 r·min-1离心5 min,收集上清。SDS-PAGE电泳,然后转膜,接着用5%脱脂牛奶封闭1 h,除去封闭液,加入兔抗鼠p-p38 MAPK一抗(1:1 000)、兔抗鼠IL-18一抗(1:1 000)、兔抗鼠IL-18R(1:200),4℃孵育过夜。用TBS洗膜3次,每次5 min。再加入稀释好的二抗(1:2 500),室温下孵育30 min。将膜蛋白面侧与新鲜配制的ECL试剂反应后,依次压片、显影、定影。用AlphaEaseFC软件处理系统分析目标条带的光密度值。将每次实验中各样品灰度值与内参β-actin灰度值相除,得到每个样品的蛋白相对含量。
1.6 qPCR法测定IL-18 mRNA表达量取大鼠术侧脊髓背角组织,按TRIzol抽提法提取总RNA,紫外吸收测定法检测RNA浓度和纯度。取适量RNA为模板,逆转录得cDNA,-20℃保存待用。采用Primer 5.0设计基因特异性引物,IL-18引物序列:5′-TGGGATTCGTTGGCTGTT-3′(上游),5′-AGACCACTTTGGCAGACTTCA-3′(下游);内参β-actin引物序列:5′-TGCTATGTTGCCCTAGACTTCG-3′(上游),5′-GTTGGCATAGAGGTCTTTACGG-3′(下游),上述引物均由上海生物工程公司合成。RT-PCR 50 μL反应体系:SYBR Green染料10 μL,上游引物1 μL,下游引物1 μL,dNTP 1 μL,Taq聚合酶2 μL,待测样品cDNA 5 μL,ddH2O 30μL。将配制好的PCR反应溶液置于Real time PCR仪上进行PCR扩增反应。反应条件为:93℃ 2 min预变性,然后93℃变性1 min,退火55 ℃ 1 min,延伸72℃ 1 min,共40个循环,最后72℃ 7 min延伸。运用Bio-Rad CFX 96荧光定量PCR仪配套的Bio-Rad CFX Manager Software1.6数据分析软件进行分析,以IL-18 mRNA/β-actin mRNA的2-ΔΔCt值的比值作为IL-18 mRNA的表达水平。
1.7 统计学方法计量资料以x±s表示。用Levene法检测各组样本方差是否齐性。方差齐性时,50% MWT比较采用Friedman ANOVA方差分析,p-p38、IL-18、IL-18R相对蛋白浓度和IL-18 mRNA含量比较采用One-way ANOVA方差分析,差异有统计学意义时用LSD法行两两比较;方差不齐时,50% MWT比较采用多因素方差分析,p-p38和IL-18 mRNA含量的比较采用Kruskal-Walllis秩和检验,两两比较采用Dunnett T3检验。p-p38 MAPK和IL-18 mRNA的相关性分析采用Speraman秩相关分析法。
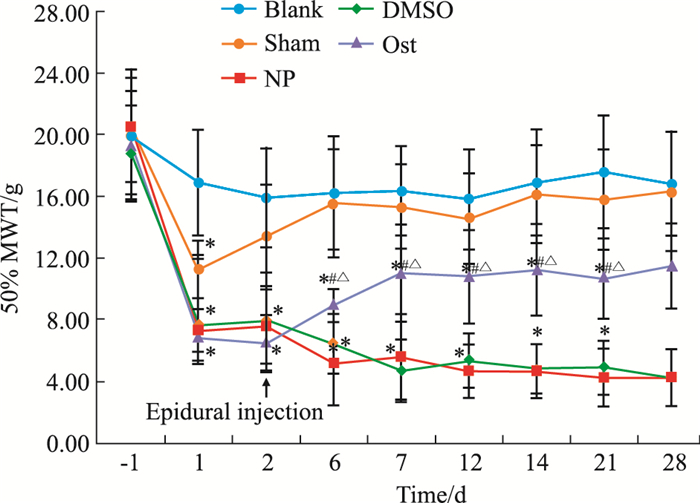
2 结果 2.1 各组大鼠给予Ost前后50% MWT的测试结果各组大鼠术前的50% MWT比较,差异无统计学意义(P>0.05)。与Blank组比较,Sham组大鼠的50% MWT在术后d 1有所下降(P < 0.05),随后逐渐恢复至术前水平;NP组、Ost组和DMSO组大鼠在术后的d 1即出现50% MWT下降(P < 0.05),其中NP组和DMSO组大鼠持续降低至术后28 d,3组大鼠在给Ost前50% MWT无明显差异(P>0.05)。给予相应药物后各个时间点,与DMSO组比较,Ost组50% MWT升高(P < 0.05);DMSO组50% MWT在给药前后无明显变化(P>0.05),与NP组各个时间点相比较,差异无统计学意义(P>0.05),见Fig 1。
|
| Fig 1 Comparison of 50% MWT before and after epidural injection of drug *P < 0.05 vs blank group; #P < 0.05 vs DMSO group; △P < 0.05 vs same group (before application of drug) |
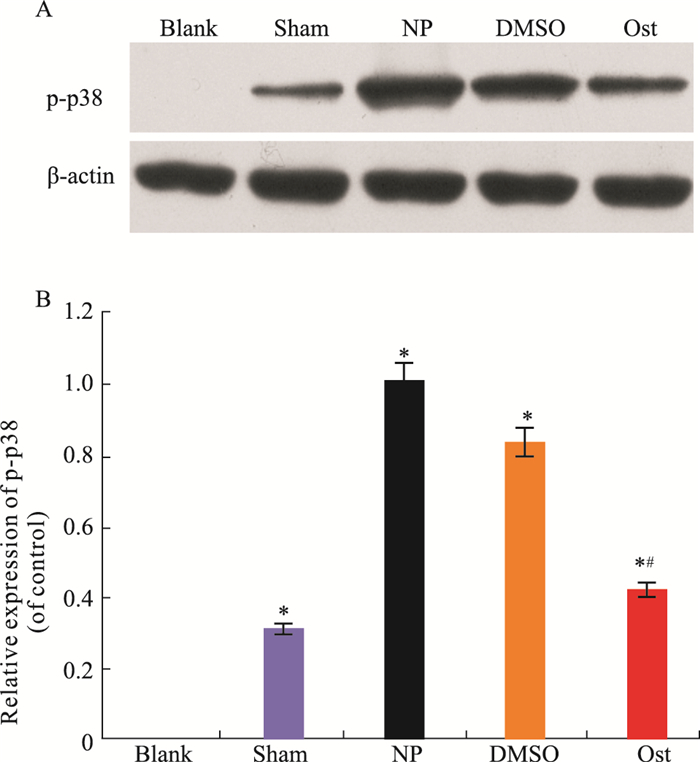
给药后5 d,与Blank组比较,Sham组、NP组、DMSO组和Ost组p-p38蛋白表达升高(P < 0.05)。与DMSO组相比,Ost组p-p38蛋白表达降低(P < 0.05),NP组与DMSO组之间比较,差异无统计学意义(P>0.05),见Fig 2。
|
| Fig 2 Expression of p-p38 in different groups after epidural application of drug A:The expression levels of p-p38 protein in the spinal dorsal horn of rats were analyzed by Western blot; B: Relative expression of p-p38 protein in the spinal dorsal horn of rats. *P < 0.05 vs blank group; #P < 0.05 vs DMSO group |
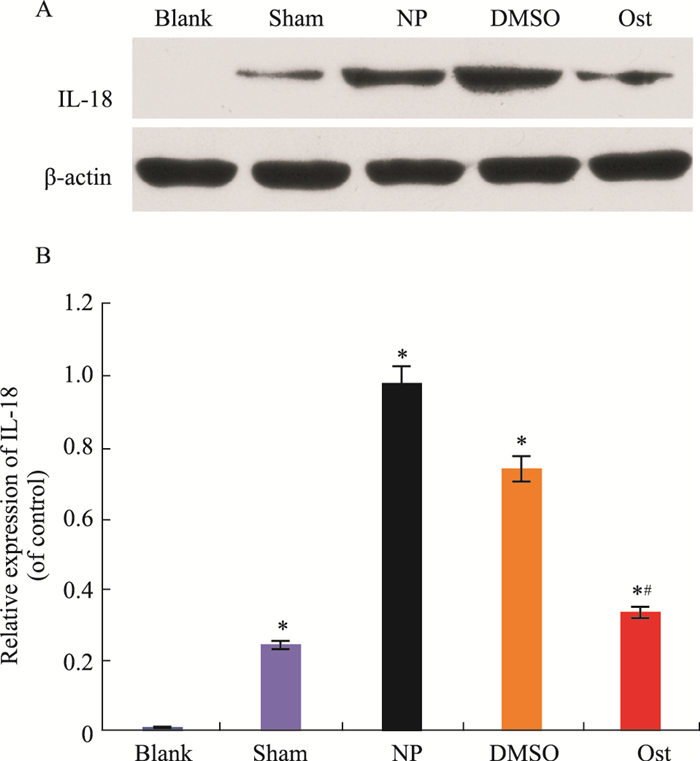
给予Ost后5 d,与Blank组比较,Sham组、NP组、DMSO组、Ost组给药后d 5 IL-18蛋白表达升高(P < 0.05)。与DMSO组相比较,Ost组IL-18蛋白表达降低(P < 0.05),NP组与DMSO组之间比较,差异无统计学意义(P>0.05),见Fig 3。
|
| Fig 3 Expression of IL-18 in different groups after epidural application of drug A:The expression levels of IL-18 protein in the spinal dorsal horn of rats were analyzed by Western blot; B: Relative expression of IL-18 protein in the spinal dorsal horn of rats. *P < 0.05 vs blank group; #P < 0.05 vs DMSO group |
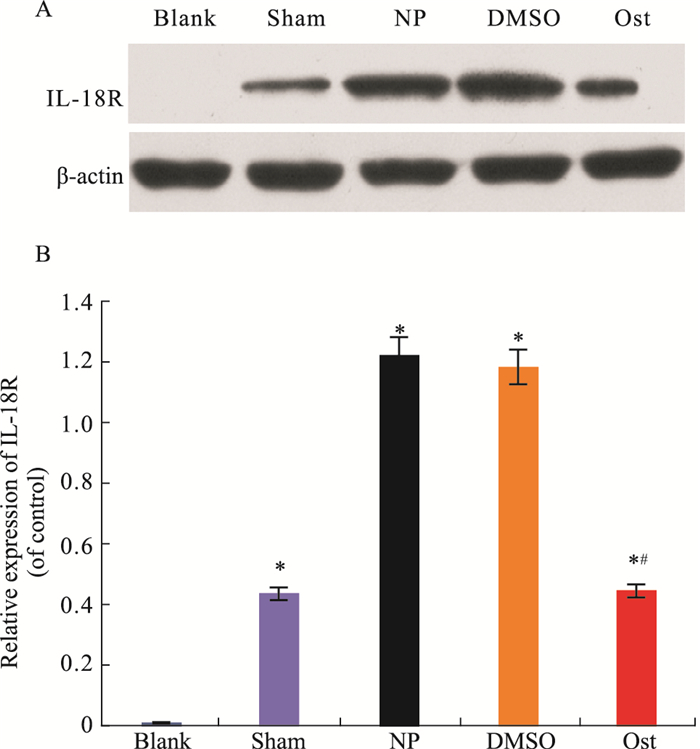
给予Ost后12 d,与Blank组相比,Sham组、NP组、DMSO组、Ost组术后d 14 IL-18蛋白表达升高(P < 0.05)。与DMSO组相比较,Ost组IL-18R蛋白表达降低(P < 0.05),NP组与DMSO组之间比较,差异无统计学意义(P>0.05),见Fig 4。
|
| Fig 4 Expression of IL-18R in different groups after epidural application of drug A:The expression levels of IL-18R protein in the spinal dorsal horn of rats were analyzed by Western blot; B: Relative expression of IL-18R protein in the spinal dorsal horn of rats.*P < 0.05 vs blank group; #P < 0.05 vs DMSO group |
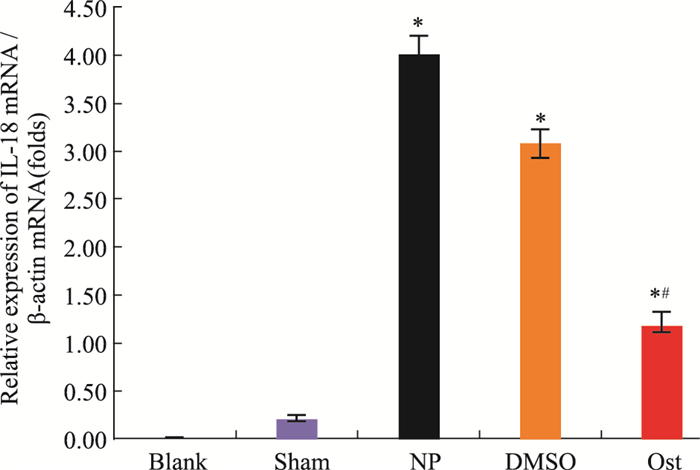
给予Ost后5 d,与Blank组和Sham组相比,NP组、DMSO组、Ost组术后d 7 IL-18 mRNA表达量升高(P < 0.05)。与DMSO组相比较,Ost组IL-18 mRNA表达量降低(P < 0.05),NP组与DMSO组之间比较,差异无统计学意义(P> 0.05),见Fig 5。
|
| Fig 5 Relative expression of IL-18 mRNA in different groups after epidural application of drug *P < 0.05 vs blank group; #P < 0.05 vs DMSO group |
术后d 7将各组大鼠脊髓背角表达的p-p38 MAPK蛋白相对浓度与IL-18 mRNA含量进行Spearman秩相关分析,p-p38 MAPK与IL-18 mRNA秩相关系数R=0.9,提示各组大鼠两者之间的表达呈正相关(P < 0.05)。
3 讨论MAPKs的激活在哺乳动物细胞信号转导中起关键作用,可引发疼痛的外周敏化和中枢敏化,一定程度上加剧了伤害后所导致的痛觉过敏[7],而p38 MAPK信号通路是MAPKs家族中重要的一条分支,一般由细胞应激和促炎因子激活。静脉或鞘内注射p38抑制剂已被证明能有效缓解炎症和关节炎[8]。有研究认为,p38MAPK调控的下游靶基因主要有ICAM-1、IL-1、TNF-α、COX-2等,该通路与腰椎间盘退变和根性症状密切相关[9]。本实验采用我们团队前期成功改良的非压迫性髓核致炎大鼠疼痛的标准化模型[6],检测显示,在建立模型后d 7,NP组大鼠p-p38表达含量上调,这与Seki等[10]研究结果一致,提示了p38的磷酸化激活很可能参与了髓核致炎的致痛过程。而作为IL-1家族成员之一的IL-18,在神经病理性疼痛和腰椎间盘突出诱发坐骨神经痛的发生发展中起重要作用。IL-18致炎效应可能与以下机制有关[11]:①促进淋巴T细胞增殖;②诱发粒-巨噬细胞集落刺激物、IL-8、单核细胞趋化物质-1及巨噬细胞炎症物质-1等;③通过MAPK途径发挥致炎作用。在本实验建立模型后的d 7,NP组大鼠IL-18蛋白及mRNA表达上调,导致大鼠机械性痛阈值下降。表明脊髓背角中的IL-18很有可能参与了髓核致炎神经根疼痛的过程。
在衣原体诱发机体炎症反应的研究中发现,有激活的IL-18与IL-1β表达,而给予p38 MAPK抑制剂后能够明显抑制它们的表达,证明了IL-18与IL-1β是通过激活p38 MAPK通路而发挥致炎作用[12]。在一项神经病理性疼痛模型研究中[13],结扎L5背根神经后可诱发大鼠机械性痛觉过敏,术后d 1开始出现大鼠脊髓背角内IL-18蛋白表达上调,术后d 7 IL-18R蛋白表达升高,其表达的时间与我们结果不同,可能是神经结扎后的炎症反应在更早期即可形成。另外,该模型中,脊髓背角中的p38 MAPK激活诱发了IL-18蛋白表达上调。在给予p38 MAPK通路特异性抑制剂SB203580后,IL-18蛋白明显下降,同时伴有IL-18R蛋白下降,说明IL-18发挥作用可能与p38 MAPK通路表达密切相关。本实验在建立了稳定的髓核致炎疼痛模型后,p-p38和IL-18 mRNA表达明显上调,对p-p38MAPK与IL-18 mRNA表达进行相关性分析,结果显示两者呈正相关关系。因此,IL-18 mRNA与p38 MAPK可能存在上下游信号通路关系。我们推测,在髓核致炎神经根痛大鼠的炎症发生早期,p38 MAPK通路激活后,可通过调控IL-18 mRNA基因表达,产生IL-18炎症介质形成炎症反应,到中晚期出现IL-18R蛋白表达。p38 MAPK信号通路及相关炎症因子IL-18和IL-18R的激活,共同介导了髓核致炎大鼠神经根较长时间的炎性疼痛。
在治疗腰椎间盘突出症的中药中,独活寄生汤具有安全有效的疗效,口服配合中药离子导入治疗腰椎间盘突出症可以有效缓解患者临床症状和体征,明显降低患者体内IL-6、IL-8及TNF-α的表达,从而缓解疼痛[14]。该方剂的主要成分是蛇床子,其主要的药用活性成分是蛇床子素。现代药理学研究发现,其抗炎效果及机制相对广泛[15]:①通过抑制肥大细胞Ca2+通道,减少Ca2+内流,从而减少组织胺释放,稳定其细胞膜而发挥止痒作用;②可直接抑制CNS发挥镇静催眠作用,其本身化学结构具有一定的局麻作用;③增强中枢神经的突触传递,促进学习和记忆;④抗衰老、抗氧化作用。在机械性脑损伤炎症动物模型中,蛇床子素还可以抑制细胞凋亡,减轻炎症反应,从而修复脑损伤等神经系统难治性疾病[16]。除了上述药理学效应,Ost的镇痛作用也非常突出,可明显抑制急性和慢性炎症反应。本课题组前期研究发现,Ost具有明显的抗炎镇痛效应,它能抑制髓核致炎大鼠背神经节内COX-2、CGRPR1、ASIC3的表达,还能通过抑制脊髓背角内ERK通路,降低下游COX-2 mRNA的表达,从而减轻神经元的兴奋性,抑制疼痛的外周敏化和中枢敏化,减弱大鼠的机械性和热觉敏感性刺激[2-6, 17]。本实验中,我们在术后d 2经硬膜外导管给予Ost 1mg/rat,可改善大鼠自身髓核诱发的机械性痛敏;在术后d 7,Ost组大鼠脊髓背角p-p38和IL-18蛋白及IL-18 mRNA均发生下调;在术后d 14,IL-18R蛋白的表达出现下调。我们认为是由于蛇床子素在炎症发生的早期通过下调p-p38和IL-18等炎症介质的表达,从而抑制疼痛的外周敏化,而在炎症发生中晚期下调IL-18R蛋白的表达,进一步阻断了炎症向中枢传递,抑制了炎症的中枢敏化效应。正是由于Ost可在炎症发生的不同时期抑制炎症介质表达,使得术后大鼠的机械性痛敏能得到持续性缓解。
综上所述,脊髓背角p38 MAPK信号相关通路参与了髓核致炎大鼠神经根痛,在疼痛形成早期IL-18为主要炎症参与介质,在中晚期IL-18R为炎症主要参与受体。术后单次硬膜外腔注射Ost可能通过抑制脊髓背角p-p38、IL-18、IL-18R蛋白和IL-18 mRNA的过度表达,从而有效缓解髓核致炎大鼠神经根痛觉过敏。
( 致谢: 本实验研究在广州市中山大学第一附属医院骨科研究所完成,感谢各位老师和实验室同事对本实验的指导和帮助!)
| [1] | Miyoshi K, Obata K, Kondo T, et al. Interleukin-18-mediated microglia/astrocyte interaction in the spinal cord enhances neuropathic pain processing after nerve injury[J]. J Neurosci, 2008, 28(48): 12775-87. doi:10.1523/JNEUROSCI.3512-08.2008 |
| [2] | Wei M, Mo S L, Nabar N R, et al. Modification of rat model of sciatica induced by lumber disc herniation and anti-inflammatory effect of osthole given by epidural catheterization[J]. Pharmacology, 2012, 90(5-6): 251-63. doi:10.1159/000340023 |
| [3] | 吴海璇, 冯璐璐, 徐辉, 等. 蛇床子素对髓核致神经根炎性痛大鼠ERK/MAPK信号通路及COX-2 mRNA表达的影响[J]. 中国药理学通报, 2014, 30(8): 1096-101. Wu H X, Feng L L, Xu H, et al. Effect of osthole on ERK/MAPK signaling pathway and the expression of COX-2 mRNA in the spinal dorsal horn of rats with nucleus pulposus-induced inflammatory radicular pain[J]. Chin Pharmacol Bull, 2014, 30(8): 1096-101. |
| [4] | 吴海璇, 冯璐璐, 贺秋兰, 等. 蛇床子素对髓核致坐骨神经痛大鼠DRG中CGRPR1表达的影响[J]. 中国药理学通报, 2014, 30(1): 49-54. Wu H X, Feng L L, He Q L, et al. Effect of osthole on expression of CGRPR1 in DRG of rats with nucleus pulposus-induced sciatica[J]. Chin Pharmacol Bull, 2014, 30(1): 49-54. |
| [5] | 贺秋兰, 魏明, 李梅娜, 等. 蛇床子素对酸诱发髓核致炎大鼠神经节神经元的膜电位改变抑制的作用[J]. 中国药理学通报, 2010, 26(11): 1459-62. He Q L, Wei M, Li M N, et al. Osthole inhibited the acid-evoked change of membrane potential of rats' dorsal root ganglion neuron following application of nucleus pulposus[J]. Chin Pharmacol Bull, 2010, 26(11): 1459-62. |
| [6] | 魏明, 张劲军, 贺秋兰, 等. 新型腰椎间盘突出致坐骨神经痛大鼠模型及硬膜外腔置管方法的建立[J]. 中国疼痛医学杂志, 2011, 17(12): 744-8. Wei M, Zhang J J, He Q L. Establishment of new rat model for sciatica induced by lumbar disc herniation and new method for epidural catheterization[J]. Chin J Pain Med, 2011, 17(12): 744-8. doi:10.3969/j.issn.1006-9852.2011.12.013 |
| [7] | Obata K, Noguchi K. MAPK activation in nociceptive neurons and pain hypersensitivity[J]. Life Sci, 2004, 74(21): 2643-53. doi:10.1016/j.lfs.2004.01.007 |
| [8] | Kumar S, Boehm J, Lee J C. p38 MAP kinases: key signalling molecules as therapeutic targets for inflammatory diseases[J]. Nat Rev Drug Discov, 2003, 2: 717-26. doi:10.1038/nrd1177 |
| [9] | Ito T, Ohtori S, Inoue G, et al. Glial phosphorylated p38 MAP kinase mediates pain in a rat model of lumbar disc herniation and induces motor dysfunction in a rat model of lumbar spinal canal stenosis[J]. Spine, 2007, 32(2): 159-67. doi:10.1097/01.brs.0000251437.10545.e9 |
| [10] | Seki S, Sekiguchi M, Konno S I. Association between neurotrophic factor expression and pain-related behavior induced by nucleus pulposus applied to rat nerve root[J]. Spine, 2017 Apr 12.[Epub ahead of print] |
| [11] | 颜玮茹, 廖春梅. 白细胞介素-18与神经系统疾病关系的研究进展[J]. 中西医结合心脑血管病杂志, 2016, 14(8): 855-9. Yan W R, Liao C M. Advances in the study of the relationship between interleukin-18 and nervous system diseases[J]. Chin J Integr Med Cardio-Cerebrovasc Dis, 2016, 14(8): 855-9. |
| [12] | Cao W, Zou Y, Su S, et al. Chlamydial plasmid-encoded protein pORF5 induces production of IL-1β and IL-18 via NALP3 inflammasome activation and p38 MAPK pathway[J]. Int J Clin Exp Med, 2015, 8(11): 20368-79. |
| [13] | Porreca F, Ossipov M H, Gebhart G F. Chronic pain and medullary descending facilitation[J]. Trends Neurosci, 2002, 25(6): 319-25. doi:10.1016/S0166-2236(02)02157-4 |
| [14] | 龚晓丽, 郭秀萍, 周涤, 等. 独活寄生汤口服及离子导入治疗腰椎间盘突出症临床研究[J]. 中医学报, 2016, 220(9): 1394-7. Gong X L, Guo X P, Zhou D, et al. Clinical research of Duhuojisheng decoction combined with iontophoresis in treatment of lumbar disc herniation[J]. China J Chin Med, 2016, 220(9): 1394-7. |
| [15] | 孔令雷, 胡金凤, 陈乃宏. 香豆素类化合物药理和毒理作用的研究进展[J]. 中国药理学通报, 2012, 28(2): 165-9. Kong L L, Hu J F, Chen N H. Advances in pharmacology and toxicology of coumarins[J]. Chin Pharmacol Bull, 2012, 28(2): 165-9. |
| [16] | 孔亮, 姚璎珈, 教亚男, 等. 蛇床子素对机械性脑损伤小鼠的抗炎抗凋亡作用研究[J]. 中国药理学通报, 2015, 31(7): 999-1004. Kong L, Yao Y J, Jiao Y N, et al. Anti-apoptosis and anti-inflammatory effect of osthole in mice following stab wound injury[J]. Chin Pharmacol Bull, 2015, 31(7): 999-1004. |
| [17] | Wu H X, Wang Y M, Xu H, et al. Osthole, a coumadin analog from Cnidium monnieri (L.) Cusson, ameliorates nucleus pulposus-induced radicular inflammatory pain by inhibiting the activation of extracellular signal-regulated kinase in rats[J]. Pharmacology, 2017, 100: 74-82. doi:10.1159/000475599 |