

2. 山东省医学科学院药物研究所,山东 济南 250062;
3. 国家卫生部生物技术药物重点实验室,山东 济南 250062;
4. 山东省罕少见病重点实验室,山东 济南 250062
2. Institute of Materia Medica, Shandong Academy of Medical Sciences, Jinan 250062, China;
3. Key Laboratory for Biotech-Drugs Ministry of Health, Jinan 250062, China;
4. Key Laboratory for Rare & Uncommon Diseases of Shandong Province, Jinan 250062, China
近年来,糖尿病(diabetes mellitus,DM)的发病率呈逐年上升趋势,严重威胁着我们的健康以及生命。DM若未得到及时的诊断和治疗,会引发多种并发症[1]。其中,心血管并发症已经成为DM患者发病率及死亡率的主要危险因素[2-3],糖尿病心肌病(diabetic cardiomyopathy,DCM)则被视为DM独立的并发症。DM高血糖状态会促使心血管产生病变,且DCM患者的预后很差,死亡率极高。
研究发现,Wnt/β-catenin经典信号通路对DM的进程起着至关重要的作用,与心脏重构、心肌梗死、心力衰竭、心律失常等病理过程密切相关[4]。糖原合成酶激酶-3β(glycogen synthase kinase-3β,GSK-3β)作为Wnt/β-catenin信号通路重要的一个下游信号分子,调控着糖原的合成,GSK-3β的过表达可能刺激胰岛素抵抗的产生,与DM的发生发展有着密不可分的关系[5]。有研究显示,在DCM的发生发展过程中,Wnt/β-catenin信号通路被激活,进一步促进DCM的发生发展[6]。另有研究显示,抑制GSK-3β后,能够抑制Wnt/β-catenin信号通路的传导,能够对DCM的损伤进行修复[7]。故本实验采用能够对GSK-3β产生抑制作用的合成药物甲异靛(meisoindigo,Me),有文献报道[8],其对GSK-3β有抑制作用,已应用于慢性粒细胞白血病中,但对DCM的作用尚未见报道。本文通过检测Me对Wnt/β-catenin信号通路中相关蛋白表达变化的影响,探讨Me在DCM修复过程中的作用机制,为DCM的诊断治疗提供理论依据。
1 材料与方法 1.1 实验动物及模型建立健康♂SD大鼠60只,SPF级,体质量(170±20)g,购自济南朋悦实验动物有限公司。大鼠经过1周的适应性喂养期,按体重均衡的原则,随机分为正常对照组(A)20只,其中4周、8周正常对照组各10只;DM模型组(B)40只。B组大鼠禁食16 h后,一次性腹腔注射链脲佐菌素(60 mg·kg-1,pH=4.5柠檬酸-柠檬酸三钠缓冲液,4℃配制,现用现配),A组大鼠注射同体积柠檬酸-柠檬酸三钠缓冲液。造模后72 h,尾静脉采血测空腹血糖值(fasting blood glucose, FBG),以FBG≥ 16.7 mmol·L-1,并出现多饮、多食、多尿和体质量下降者为DM模型成功者。B组造模成功组随机分为4周DM模型组、4周Me给药组、8周DM模型组、8周Me给药组,每组10只。给药组20 mg·kg-1灌胃给药,其余组别分别以同体积的蒸馏水灌胃。A、B两组大鼠均以普通饲料和蒸馏水继续饲养。
1.2 试剂链脲佐菌素、戊巴比妥钠(美国Sigma公司);血糖试纸(强生中国医疗器材有限公司);生物素标记山羊抗兔IgG/鼠IgG二抗试剂盒(北京中杉金桥生物技术有限公司);Western blot一抗、二抗去除液、裂解液、BCA蛋白浓度测定试剂盒,均购自碧云天生物技术研究所;ProSieve Color protein markers(美国Lonza Rockland公司);增强型化学发光试剂(美国Millipore公司);单克隆抗体GSK-3β、p-GSK-3β(Ser9)、β-catenin、NF-κB p65、β-actin,均购自美国Cell Signaling Technology公司;Wnt2抗体(美国Epitomics公司);p-NF-κB p65抗体(Ser536,Santa Cruz公司)。
1.3 标本收集各周期末,尾静脉采血测血糖值。大鼠麻醉,仰位固定,开胸,腹主动脉取血,5~10 mL每只,3 000 r·min-1离心10 min,取上清,分装到EP管,-20℃保存待测。迅速取出心脏,用预冷生理盐水洗净,滤纸吸干,沿心室壁剪开,剔除血管、脂肪等非心肌组织,分为左心、右心,分别称取心脏质量(HW)和左心室(含室间隔)质量(LVW),并计算心脏(左心)指数=心脏(左心室)质量(mg)/体质量(g)。将左心分为两部分:一部分用4%多聚甲醛固定,经脱水、透明、包埋,制成心脏组织石蜡块;另一部分置于冻存EP管,液氮保存待测。
1.4 HE染色取正常对照组及各时间点模型组、给药组心肌组织,制作石蜡切片,常规脱蜡至水,苏木精染色10 min,流动的水稍加冲洗,体积分数1%的的盐酸乙醇分化,流动水冲洗数分钟,伊红染色5 min,流动水稍加冲洗,梯度乙醇常规脱水,中性树胶封片。Eclipse TE 2000-S荧光显微镜拍照(日本Nikon),观察心肌组织病理结构的变化。
1.5 免疫组织化学染色取各组石蜡切片常规脱蜡至水,磷酸盐缓冲液(PBS,pH 7.4)洗涤,H2O2溶液封闭30 min,柠檬酸缓冲液(pH 6.0)高压3 min,PBS洗涤后与相应一抗4℃湿盒过夜,次日滴加与辣根过氧物标记的二抗,孵育20 min。二氨基联苯胺(DAB)染色,苏木精对比染色,自来水洗返蓝,梯度乙醇脱水,中性树胶封片,于免疫荧光显微镜下拍照,观察结果。
1.6 Western blot检测取各组别大鼠心肌组织,制备组织匀浆,每20 mg组织加入100~200 μL含1 mmol·L-1 PMSF的裂解液,4℃下14 000×g离心10 min,取上清,分装于EP管,-20℃保存。用BCA蛋白浓度测定试剂盒测定总蛋白浓度。40 μg总蛋白上样量以浓度为10%的凝胶电泳分离。冰浴恒流(300 mA)下湿法转膜2 h,体积分数5%的BSA封闭液室温封闭1 h后,与相应的一抗4℃孵育过夜。TBS-T洗液洗涤,与辣根过氧化物标记的二抗共孵育,增强型化学发光试剂进行显色,并用灰度分析软件定量分析。
1.7 统计学分析数据以x±s表示,应用SPSS 22.0统计软件进行数据分析,组间差异比较采用方差分析及t检验。
2 结果 2.1 DM大鼠模型建立情况实验期间,正常对照组大鼠状态良好、健壮、皮毛柔顺有光泽,自主活动无异常,对外界反应灵敏,无死亡。与正常对照组大鼠相比,DM模型组大鼠逐渐消瘦,精神萎靡,皮毛黯淡无光泽,腥臊臭味加重等;且随着时间的增加,多饮、多食、多尿和消瘦加重,生存状态越来越差。与DM模型组比较,Me给药组大鼠体质量稍有增加,精神较DM模型组略好;随着时间的增加,给药组大鼠体质量增加明显,生存状态明显好转。
2.2 大鼠体质量、空腹血糖值及心脏各指标DM模型组大鼠与正常对照组大鼠比较,空腹血糖值明显升高,体质量明显下降,心脏和左心室质量明显降低(P<0.01)。Tab 1显示,给予大鼠4周Me治疗后,相较于正常对照组,Me组空腹血糖值明显升高,体质量明显下降,心脏和左心室质量明显降低,心脏指数及左心指数升高,大鼠的身体状况并没有向好的趋势发展。由此可见,4周Me给药组相对于DM模型组,疗效并不是很明显,并出现了轻微恶化现象。但随着时间的延长,给药至8周时,Me给药组的体质量、血糖值、心脏指数及左心指数较之DM模型组都有了明显好转(P<0.05)。见Tab 1、2。
| Control | DM | Me | |
| BW/g | 322.2±22.741 | 191.2±34.353** | 150.6±23.597**## |
| FBG/mmol·L-1 | 4.95±0.622 | 28.57±4.481** | 29.55±4.137** |
| HW/g | 0.863±0.063 | 0.519±0.079** | 0.468±0.083 ** |
| LVW/g | 0.696±0.064 | 0.413±0.066** | 0.377±0.066** |
| HW/BW/mg·g-1 | 2.682±0.168 | 2.730±0.164 | 3.097±0.140**## |
| LVW/BW/mg·g-1 | 2.163±0.177 | 2.173±0.186 | 2.496±0.130** |
| BW: Body weight; FBG: Fast blood glucose; HW: Heart weight; LVW: Left ventricular weight. **P < 0.01 vs control; ##P < 0.01 vs DM | |||
| Control | DM | Me | |
| BW/g | 376.2±29.953 | 175.0±38.411 ** | 227.6±48.866**# |
| FBG/mmol·L-1 | 4.98±0.705 | 30.9±3.429** | 13.12±7.700*## |
| HW/g | 1.003±0.096 | 0.513±0.096** | 0.6±0.113 ** |
| LVW/g | 0.822±0.085 | 0.418±0.082** | 0.489±0.094** |
| HW/BW/mg·g-1 | 2.666±0.169 | 2.972±0.322** | 2.656±0.148# |
| LVW/BW/mg·g-1 | 2.184±0.138 | 2.421±0.269* | 2.166±0.153# |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs DM | |||
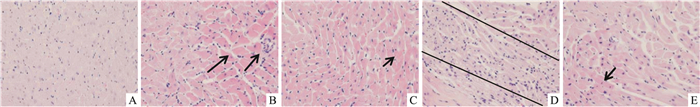
如Fig 1所示,正常对照组大鼠心肌细胞形态正常,排列整齐,细胞核分布均匀,无变形、坏死等变化。DM模型组大鼠心肌细胞中能看到不同程度的病变,心肌细胞明显增大,胞质丰富,排列紊乱,细胞核由正常的圆形或椭圆变为长杆状,且大小不规则,尤其是8周DM模型组的大鼠,局部心肌细胞凝固性坏死,胞质嗜酸性增强,核固缩深染,纤维组织增生,坏死灶内淋巴细胞大量增生。较之DM模型组,Me给药组心肌组织中则偶见心肌细胞点灶状炎症浸润坏死灶,有不同程度的心肌肥大、心肌纤维化等病变缓解的症状。
|
| Fig 1 HE staining of myocardium of DM rats (×400) A:Control group; B:4 wk DM; C:4 wk Me; D:8 wk DM; E:8 wk Me |
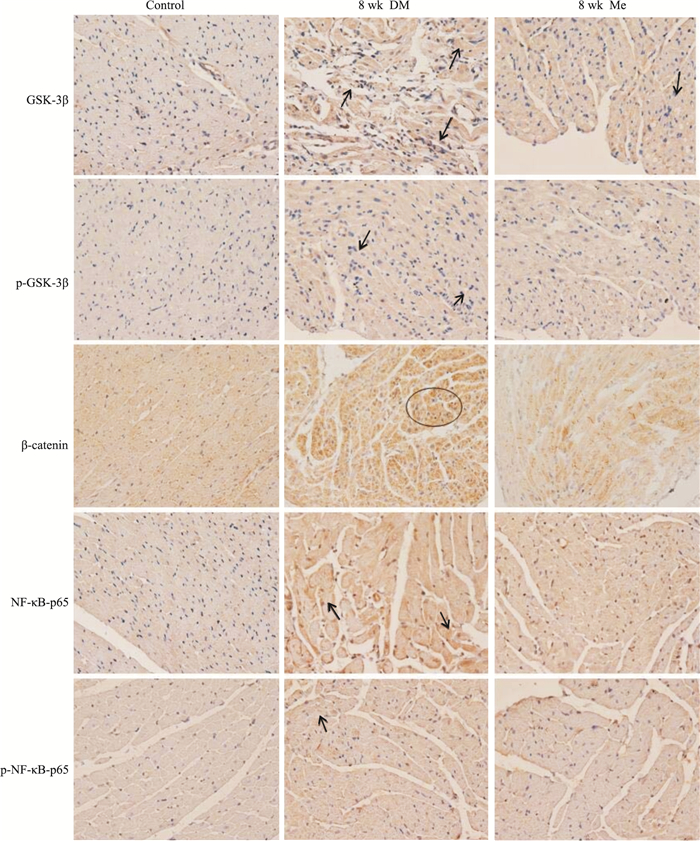
如Fig 2所示,DM模型组中GSK-3β蛋白在心肌中的表达要比正常对照组中略多,颜色较深,尤其是棕黄色的区域,则是表现为蛋白的阳性表达范围,随着时间的延长,8周时DM模型组的阳性表达更为明显;而Me给药组的GSK-3β蛋白阳性表达则比DM模型组的要稍少,细胞质、细胞核均有表达。p-GSK-3β、β-catenin蛋白在DM模型组中的表达,比正常对照组要多,8周DM模型组中p-GSK-3β蛋白表达棕黄色区域更多,阳性表达更加明显;与DM模型组相比,Me给药组中p-GSK-3β蛋白的表达相应减少。NF-κB-p65、p-NF-κB-p65蛋白在DM组中除了有棕黄色阳性表达现象,还出现有染色较深的区域,主要为细胞核表达阳性较正常对照组的表达水平有所增加,在Me给药组中,NF-κB-p65、p-NF-κB-p65蛋白的细胞核表达则有不同程度的减少,细胞质、细胞核表达均匀。
|
| Fig 2 Immunohistochemistry of proteins expression of myocardium in DM rats (×400) |
Western blot结果表明(Fig 3),DM模型组大鼠心肌中GSK-3β以及p-GSK-3β蛋白的表达变化相对于正常对照组以及Me给药组,差异均无显著性(P>0.05),然而DM模型组p-GSK-3β/GSK-3β的值相对于正常组明显升高(P<0.05),且Me给药组明显降低(P<0.05);DM模型组大鼠从4周到8周期间,Wnt2、β-catenin蛋白的表达水平与正常对照组比较明显升高(P<0.05),Me给药至8周时,Wnt2、β-catenin蛋白表达较正常对照组也有明显下降(P<0.01);NF-κB-p65、p-NF-κB-p65蛋白在4周DM模型组大鼠心肌中明显升高(P<0.01),随着时间的延长,到8周时,NF-κB-p65蛋白的表达在Me给药组中较DM模型组明显减少(P<0.01);p-NF-κB-p65蛋白在DM模型组中的表达与正常对照组相比明显上升(P<0.01),Me给药组中p-NF-κB-p65的表达较DM模型组大鼠明显下降(P<0.01)。

|
| Fig 3 The protein levels of GSK-3β, p-GSK-3β, Wnt2, β-catenin, NF-κB-p65, p-NF-κB-p65 in total protein extracts of myocardium from DM rats analyzed by Western blot (x±s, n=10) A: Representative Western blot analysis of the time-dependent changes of protein levels; B: Bar graph of quantification of protein levels(fold of intensity of bands with β-actin). *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs 4 wk DM group |
DM可引起机体多个脏器的损害,其中心肌损伤是1型DM常见的并发症之一。GSK-3是进化保守的丝氨酸/苏氨酸激酶,在多种细胞及生物体内都有表达。在哺乳动物中,GSK-3来自两个紧密相关的由不同的基因编码的亚型GSK-3α、GSK-3β,其中以GSK-3β的作用为主[9]。GSK-3β是调控血糖稳态的重要分子,参与许多DM发生发展的细胞进程,对心肌肥大也有一定影响,抑制GSK-3β能够缓解DM大鼠心肌肥大和心衰的症状[10]。Wnt/β-catenin经典信号通路在DM中的作用研究也越来越广泛。研究发现[11],Wnt/β-catenin通路在1型型糖尿病心肌病大鼠心肌组织中,处于被激活状态,表明Wnt/β-catenin信号通路的激活对糖尿病大鼠心肌损伤起着重要作用。
本实验采用1次性腹腔注射链脲佐菌素的建模方法[1],建立1型糖尿病大鼠模型,与正常对照组比较,DM模型组大鼠空腹血糖值明显升高,并呈现持续的高血糖,体质量明显低于正常对照组,心肌组织中局部心肌细胞凝固性坏死,胞质嗜酸性增强,坏死灶内淋巴细胞大量增生;与DM模型组相比,4周Me给药组,心脏指数、左心指数各项指标都有一定程度的恶化,可能是由于对早期DM模型大鼠给药后,上调了大鼠体内p21蛋白的表达,而p21蛋白表达的升高能够使大鼠体内p65蛋白表达略有上升,使Me给药组大鼠体内Wnt通路愈发处于激活的状态,从而使DM模型组大鼠各项生命指征没有好转的现象[12-13];而给药至8周,DM大鼠的各项指征比DM模型组都有了好转的迹象,HE染色显示其心肌组织中则偶见心肌细胞点灶状炎症浸润坏死灶,有不同程度的心肌肥大、心肌纤维化等病变缓解的症状,表明Me对DM大鼠作用一定时间后,能够通过抑制GSK-3β的表达,抑制Wnt信号通路的传导,对DM大鼠的心肌损伤具有一定的缓解作用。
GSK-3β可调控NF-κB、JNK、MAPK等多条信号通路,对DCM的病理生理过程产生影响。有研究显示[14],对GSK-3β进行抑制,早期能够激活Wnt信号通路,增加β-catenin的表达水平,同时还能够影响NF-κB通路的转导,但β-catenin的表达的升高与NF-κB通路信号的转导之间可能是独立起作用的。另有研究报道[15],有的抑制剂产生抑制GSK-3β的作用,通过抑制GSK-3β的磷酸化,从而抑制β-catenin的表达水平,继而抑制Wnt信号通路的激活及信号转导。本研究Western blot结果表明,Me给药组大鼠体内GSK-3β蛋白总量变化不大,而p-GSK-3β/GSK-3β的值相对于正常组明显升高,说明甲异靛该药对GSK-3β总量及其磷酸化影响不大,而是通过对GSK-3β进行抑制,达到抑制效果的。Western blot结果中,4周和8周DM模型组大鼠心肌中的Wnt2、β-catenin蛋白表达均有升高,特别是到8周时,免疫组化结果也表现为细胞核表达增加,说明Wnt/β-catenin信号通路被激活。而Me给药组4周时,GSK-3β、Wnt2、β-catenin的表达略有升高,这可能是Me对GSK-3β进行抑制之后,在早期会使其内源性抑制剂增加,能够产生激活Wnt信号通路的作用,而随着时间的增加,给药至8周时,这些蛋白的表达明显降低,免疫组化结果显示,细胞核表达减少,细胞核及细胞质表达均匀,表明Wnt/β-catenin信号转导的减少,信号通路受到抑制。对于GSK-3β作用的下游因子NF-κB-p65、p-NF-κB-p65的表达,在4周、8周DM大鼠心肌中表达升高,而在给药组中则明显减少,提示Me对GSK-3β抑制后,能够对NF-κB信号通路也产生影响,主要是通过减少NF-κB-p65蛋白的磷酸化以及减少DM大鼠心肌中NF-κB-p65的总量得以实现。而Wnt/β-catenin及NF-κB两条通路之间是如何在DM大鼠发生发展过程中产生作用的,还有待进一步实验研究。
DCM是DM心血管并发症的主要组成部分,明确其发生发展过程中心肌相关指标的变化,对其尽早诊断治疗有重要作用。本实验发现Me抑制大鼠体内的GSK-3β蛋白的表达,继而对Wnt/β-catenin信号通路进行抑制,并下调其下游相关蛋白因子的表达,参与了DM大鼠心肌损伤的修复过程,揭示了Wnt/β-catenin通路的激活以及NF-κB表达的升高均对DM的发生发展起着至关重要的作用,该结果将为DCM的早期诊断及治疗提供理论依据。
| [1] | Yigitturk G, Acara A C, Erbas O, et al. The antioxidant role of agomelatine and gallic acid on oxidative stress in STZ induced type Ⅰ diabetic rat testes[J]. Biomed Pharmacother, 2017, 87: 240-6. doi:10.1016/j.biopha.2016.12.102 |
| [2] | Elçioǧlu H K, Kabasakal L, Özkan N, et al. A study comparing the effects of rosiglitazone and/or insulin treatments on streptozotocin induced diabetic (type Ⅰ diabetes) rat aorta and cavernous tissues[J]. Eur J Pharmacol, 2011, 660(2-3): 476-84. doi:10.1016/j.ejphar.2011.03.030 |
| [3] | Singh G B, Sharma R, Khullar M. Epigenetics and diabetic cardiomyopathy[J]. Diabetes Res Clin Pract, 2011, 94(1): 14-21. doi:10.1016/j.diabres.2011.05.033 |
| [4] | Dawson K, Aflaki M, Nattel S. Role of the Wnt-Frizzled system in cardiac pathophysiology: a rapidly developing, poorly understood area with enormous potential[J]. J Physiol, 2013, 591(6): 1409-32. doi:10.1113/jphysiol.2012.235382 |
| [5] | Kim J S, Piao S, Lee E, et al. Development of Akt-activated GSK3β inhibitory peptide[J]. Biochem Biophys Res Commun, 2013, 434(4): 735-9. doi:10.1016/j.bbrc.2013.03.103 |
| [6] | 席晓慧, 王福文, 王燕, 等. 早期糖尿病大鼠心肌Wnt/β-catenin信号通路的变化[J]. 中国药理学通报, 2015, 31(3): 363-6. Xi X X, Wang F W, Wang Y, et al. Alteration of Wnt/β-catenin signaling pathway in early diabetic rat myocardium[J]. Chin Pharmacol Bull, 2015, 31(3): 363-6. |
| [7] | Wei H, Qu H, Wang H, et al. 1, 25-Dihydroxyvitamin-D3 prevents the development of diabetic cardiomyopathy in type 1 diabetic rats by enhancing autophagy via inhibiting the β-catenin/TCF4/GSK-3β/mTOR pathway[J]. J Steroid Biochem Mol Biol, 2017, 168: 71-90. doi:10.1016/j.jsbmb.2017.02.007 |
| [8] | Xiao Z, Wang Y, Lu L, et al. Anti-angiogenesis effects of meisoindigo on chronic myelogenous leukemia in vitro[J]. Leuk Res, 2006, 30(1): 54-9. doi:10.1016/j.leukres.2005.05.012 |
| [9] | Doble B W, Patel S, Wood G A, et al. Functional redundancy of GSK-3alpha and GSK-3beta in Wnt/beta-catenin signaling shown by using an allelic series of embryonic stem cell lines[J]. Dev Cell, 2007, 12(6): 957-71. doi:10.1016/j.devcel.2007.04.001 |
| [10] | Kerkela R, Kockeritz L, Macaulay K, et al. Deletion of GSK-3beta in mice leads to hypertrophic cardiomyopathy secondary to cardiomyoblast hyperproliferation[J]. J Clin Invest, 2008, 118(11): 3609-18. doi:10.1172/JCI36245 |
| [11] | Xi X X, Wang Y, Li J, et al. Activation of Wnt/β-catenin/GSK-3β signaling during the development of diabetic cardiomyopahy[J]. Cardiovasc Pathol, 2015, 24(3): 179-86. doi:10.1016/j.carpath.2014.12.002 |
| [12] | Lee C C, Lin C P, Lee Y L, et al. Meisoindigo is a promising agent with in vitro and in vivo activity against human acute myeloid leukemia[J]. Leuk Lymphoma, 2010, 51(5): 897-905. doi:10.3109/10428191003672115 |
| [13] | Zhou Y Q, Li G, Ji Y, et al. Cytoplasmic p21 induced by p65 prevents doxorubicin-induced cell death in pancreatic carcinoma cell line[J]. J Biomed Sci, 2012, 19(1): 15. doi:10.1186/1423-0127-19-15 |
| [14] | Götschel F, Kern C, Lang S, et al. Inhibition of GSK3 differentially modulates NF-κB, CREB, AP-1 and β-catenin signaling in hepatocytes, but fails to promote TNF-α-induced apoptosis[J]. Exp Cell Res, 2008, 314(6): 1351-66. doi:10.1016/j.yexcr.2007.12.015 |
| [15] | Li J, Khavandgar Z, Lin S H, et al. Lithium chloride attenuates BMP-2 signaling and inhibits osteogenic differentiation through a novel Wnt/GSK3-independent mechanism[J]. Bone, 2011, 48(2): 321-31. doi:10.1016/j.bone.2010.09.033 |

