


2. 南京中医药大学 第一临床医学院中医内科学教研室,江苏 南京 210023;
3. 南京中医药大学 医学与生命科学学院分子生物学教研室,江苏 南京 210023;
4. 南京中医药大学 药学院中药炮制学教研室,江苏 南京 210023
 ,
WU Mian-hua2,
JIANG Ze-qun3,
ZHAO Feng-ming3,
LI Li2,
LI Mu-han2,
LU Tu-lin4,
HANG Ai-wu1
,
WU Mian-hua2,
JIANG Ze-qun3,
ZHAO Feng-ming3,
LI Li2,
LI Mu-han2,
LU Tu-lin4,
HANG Ai-wu1

2. First School of Clinical Medicine, Nanjing University of Traditional Chinese Medicine, Nanjing 210023, China;
3. School of Medicine and Life Sciences, Nanjing University of Traditional Chinese Medicine, Nanjing 210023, China;
4. College of Pharmacy, Nanjing University of Traditional Chinese Medicine, Nanjing 210023, China
山茱萸为山茱萸科植物山茱萸(Cornus officinalis Sieb. et Zucc.)的干燥成熟果实,具有补益肝肾、涩精固脱等功效[1]。现代医学研究表明,山茱萸具有抗菌、调节免疫、降血糖、降血脂、抗氧化等作用[2]。环烯醚萜苷类成分是山茱萸中的主要成分之一,在糖尿病降血糖、免疫抑制、抗炎等方面发挥药理作用[3-4],但其在急性肝损伤方面的作用尚未见报道。本实验旨在探讨山茱萸环烯醚萜苷(cornel iridoid glycoside,CIG)对急性肝损伤细胞模型的作用,为山茱萸的临床应用提供实验依据。
在脂多糖(lipopolysaccharide,LPS)诱导的肝损伤模型中,主要是TNF-α为主的炎症因子的过量释放,引发一些列的炎症反应,进而激活某些凋亡通路,导致肝细胞程序性死亡,最终发生肝衰竭[5]。Jesephs等[6]研究证明,在D-半乳糖胺(D-galactosamine, D-GalN)/LPS诱导的肝损伤模型中,TNF-α介导的受体通路主导了模型小鼠的肝脏细胞凋亡,由此可以证明,TNF-α在D-GalN/LPS模型中占有重要地位。因此,对于本实验研究的体外肝细胞损伤模型,为了避免通过LPS诱导产生的TNF-α的不稳定以及无法定量研究等问题,采用D-GalN与TNF-α联合诱导人源性肝细胞L-02损伤作为实验模型进行研究。
1 材料 1.1 细胞株人源性肝细胞(编号BNCC100012, L-02购自中国科学院上海生命科学研究院细胞库。
1.2 药品与试剂DMEM高糖培养基(美国Gibco公司);胎牛血清(美国Hyclone);MTT (美国Amresco);二甲基亚砜(dimethyl sulfoxide, DMSO,广东光华化学有限公司);超氧化物歧化酶(superoxide dismutase, SOD)、丙二醛(malondialdehyde, MDA)、总抗氧化能力(total antioxidant capacity, T-AOC)试剂盒(南京建成生物研究所);兔抗p-PERK、p-eIF-2α、caspase-3抗体(美国Cell Signaling Technology公司);β-actin、HRP标记的羊抗兔IgG(联科生物科技技术有限公司);BCA蛋白定量试剂盒(碧云天生物有限公司)。
1.3 仪器CO2细胞培养箱(日本Sanyo公司);酶联免疫检测仪(美国Bio-Rad公司);CKX-31倒置显微镜(日本Olympus公司)。
2 方法 2.1 环烯醚萜苷的制备采用乙醇加热回流法,进行多次提取。加入80%乙醇加热回流提取,首次加入料液比为1:12的80%乙醇,提取2 h;第2次加入料液比为1:10的80%乙醇,提取1 h;第3次加入料液比为1:8的80%乙醇,提取1 h。合并3次的提取液,旋转蒸发仪进行浓缩,至约每1.2 mL药液含1 g生药,上大孔树脂,吸附12 h,用蒸馏水洗脱,洗至Molish反应为阴性,弃去水洗脱液;用10%乙醇洗脱,流速为1.8 BV/h(1 mL·min-1)收集醇洗脱液,浓缩喷雾干燥,得CIG粉末。取一定量的CIG粉末,加生理盐水配制为1 g·L-1的CIG母液。
2.2 D-GalN/TNF-α损伤L-02细胞模型的建立实验分组为空白组、模型Ⅰ组(D-GalN 0.44 mg·L-1+TNF-α 100 μg·L-1)、模型Ⅱ组(D-GalN 2.2 mg·L-1+TNF-α 100 μg·L-1)、模型Ⅲ组(D-GalN 4.4 mg·L-1+TNF-α 100 μg·L-1)、模型Ⅳ组(D-GalN 22 mg·L-1+TNF-α 100 μg·L-1)、模型Ⅴ组(D-GalN 44 mg·L-1+TNF-α 100 μg·L-1)。取对数生长期的L-02细胞,以5×103/孔接种于96孔板内,37℃、5% CO2培养箱中培养。待细胞完全贴壁后,按照实验分组加入不同的药液,分别观察12、24 h,时间结束后,各孔均加入5 g·L-1的MTT工作液20 μL,4 h后轻轻吸去上清,每孔加入150 μL DMSO工作液,混匀10 min,酶标仪490 nm测定吸光度(optical density, OD)值。根据各组OD值,计算各组细胞相对于正常组的增殖抑制率,相对增殖抑制率=
实验分为对照组、模型组(44 mg·L-1 D-GalN+100 μg·L-1 TNF-α)、CIG高、中、低剂量组(100、20、10 mg·L-1)。对照组即未加任何处理因素,模型组即常规培养24 h后,加入含有D-GalN/ TNF-α的培养液,CIG各组即加入含有不同浓度CIG的培养液作用24 h,然后换成含有D-GalN/ TNF-α的培养液作用12 h。模型组与CIG各剂量组在相同时间点换成含有D-GalN/ TNF-α的培养液,对照组加入等量的磷酸盐缓冲液(phosphate buffer saline, PBS)。
2.3.1 MTT检测CIG对D-GalN/TNF-α损伤肝细胞的保护作用取对数生长期的L-02细胞,以5×103/孔接种于96孔板内,37℃、5% CO2培养箱中培养,待细胞完全贴壁后,按上述实验分组与实验方法进行操作。时间结束后,各孔均加入5 g·L-1的MTT工作液20 μL,4 h后轻轻吸去上清,每孔加入150 μL DMSO工作液,混匀10 min,酶标仪490 nm测定OD值。根据各组OD值,计算各组细胞相对于正常组的凋亡率,相对凋亡率=
取对数生长期的L-02细胞,以1×105/孔接种于6孔板内,37℃、5% CO2培养箱中培养,待细胞完全贴壁后,按上述实验分组与实验方法进行操作。时间结束后弃掉上清,用胰蛋白酶消化、收集细胞,PBS洗涤2次,离心弃掉上清,参照AnnexinⅤ-FITC/PI试剂盒说明书,加入所需试剂,涡旋混匀,避光作用15 min,上流式细胞仪进行检测和数据分析。
2.3.3 T-AOC、SOD、MDA含量检测取对数生长期的L-02细胞,以1×105/孔接种于6孔板内,37℃、5% CO2培养箱中培养,待细胞完全贴壁后,按上述实验分组与实验方法进行操作。时间结束后,取每孔细胞上清液50 μL,按照试剂盒说明书操作,检测T-AOC、SOD、MDA含量。
2.3.4 Ca2+荧光强度检测取对数生长期的L-02细胞,以5×103/孔接种于96孔板内,37℃、5% CO2培养箱中培养,待细胞完全贴壁后,按上述实验方案分组,作用时间结束,按照Fluo 4-AM操作说明书进行操作,检测各组细胞内Ca2+荧光强度。
2.3.5 Western blot检测各蛋白表达按常规方法提取细胞总蛋白,BCA法测定总蛋白质浓度。将各组蛋白与上样缓冲液混匀,95 ℃~100 ℃煮沸变性,取各组细胞的总蛋白50 μg进行SDS-PAGE凝胶电泳,转膜,封闭。按1:1 000浓度稀释一抗,4 ℃摇床孵育过夜,充分洗涤,将HRP结合的二抗按1:5 000浓度室温摇荡孵育1 h,充分洗膜,加ECL发光液,用凝胶成像系统曝光,重复3次。
2.4 统计学处理实验数据采用SPSS 17. 0统计软件进行统计分析,以x±s表示,各组数据采用One-way ANOVA统计学分析,两组间数据比较采用q检验。
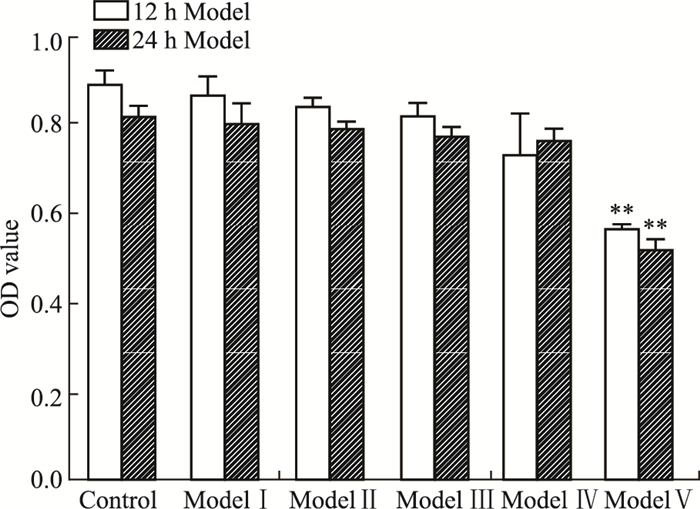
3 结果 3.1 D-GalN/TNF-α损伤L-02细胞模型实验结果如Fig 1所示,作用12、24 h的两组细胞比较,随着D-GalN浓度的依次增加,L-02细胞的生长抑制率也不断增加,在D-GalN 44 mg·L-1时对细胞的抑制率分别达到36%、39%,与对照组比较,差异具有统计学意义(P<0.01)。但是,比较2个时间段的结果发现,细胞的抑制率没有差异。因此,为了缩短实验周期,我们选择TNF-α 100 μg·L-1与D-GalN 44 mg·L-1作为合适的实验造模浓度。
|
| Fig 1 Effects of D-GalN/TNF-α on inhibitory rate of L-02 cells (x±s, n=6) **P < 0.01 vs control group |
Tab 1结果显示,D-GalN和TNF-α联合作用12 h,对L-02细胞的增殖抑制率达到57.8%,与对照组比较,差异有显著性(P<0.01)。加入CIG 100、20、10 mg·L-1预保护的3个组,肝细胞L-02的增殖抑制率分别为36.8%、44.1%、49.3%,与模型组比较差异有显著性(P<0.05)。结果表明,D-GalN和TNF-α联合作用可造成细胞损伤,CIG 10~100 mg·L-1可以降低这种损伤,且呈浓度依赖性。
| Group | OD value | Inhibitory rate/% |
| Control | 1.13±0.04 | - |
| Model | 0.48±0.05** | 57.85 |
| CIG 10 mg·L-1 | 0.58±0.03# | 49.27 |
| CIG 20 mg·L-1 | 0.64±0.04# | 44.08 |
| CIG 100 mg·L-1 | 0.72±0.03## | 36.76 |
| **P < 0.01vs control; #P < 0.05, ##P < 0.01 vs model | ||
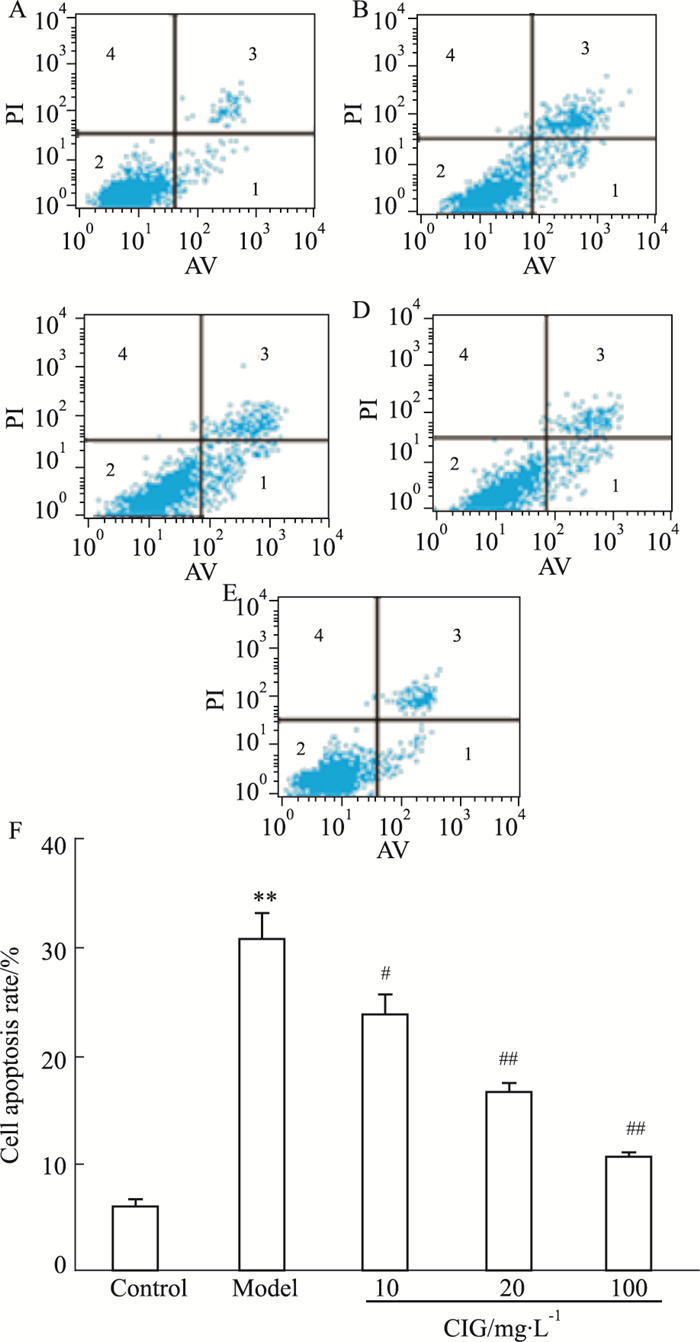
Fig 2结果表明,与模型组比较,CIG 100、20、10 mg·L-1预处理组细胞凋亡率明显降低,差异具有统计学意义。
|
| Fig 2 Effects of CIG on L-02 cell apoptosis rate A: Control group; B: Model group; C: CIG 10 mg·L-1 group; D: CIG 20 mg·L-1 group; E: CIG 100 mg·L-1 group; F: The apoptosis rate of different groups. 1: Early apoptosis; 2: Living cells; 3: Late apoptotic and necrotic cells; 4: Cell debris and loss of cells. **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
Tab 2结果表明,CIG预处理组T-AOC、SOD含量较模型组明显升高,差异具有统计学意义;与模型组比较,CIG高、中剂量预处理24 h,MDA活性明显降低,差异具有统计学意义(P<0.05),低浓度处理组MDA含量降低,但差异不具有统计学意义。
| Group | T-AOC/kU·L-1 | SOD/kU·L-1 | MDA/mmol·L-1 |
| Control | 4.70±0.38 | 54.30±2.36 | 0.422±0.186 |
| Model | 1.24±0.039** | 6.70±0.36** | 1.224±0.365** |
| CIG 10 mg·L-1 | 1.94±0.078# | 14.95±3.55# | 0.872±0.175 |
| CIG 20 mg·L-1 | 2.79±0.038## | 27.22±0.30## | 0.633±0.146# |
| CIG 100 mg·L-1 | 4.37±0.15## | 37.31±0.61## | 0.450±0.064# |
| **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model | |||
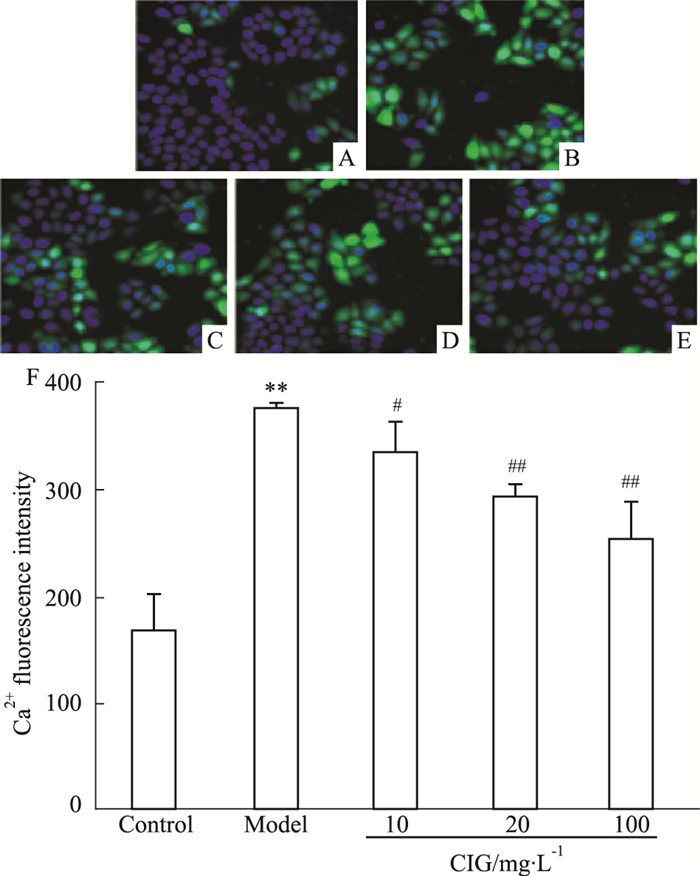
Fig 3结果显示,对照组细胞细胞核清晰,形态完整,偶见少量细胞内Ca2+荧光强度明显;D-GalN/TNF-α损伤组(模型组)细胞内Ca2+荧光强度明显升高,细胞核固缩,形态不清晰,细胞数目明显减少;给予CIG高、中、低浓度组,细胞形态有明显改变,Ca2+荧光强度明显较模型组降低,且各组之间细胞形态差异明显,药效呈依次降低趋势。
|
| Fig 3 Effects of CIG on intracellular Ca2+ content in L-02 cells A: Control group; B: Model group; C: CIG 10 mg·L-1 group; D: CIG 20 mg·L-1 group; E: CIG 100 mg·L-1 group; F: The Ca2+ content of different groups. The blue fluorescence is DAPI stained nuclei, green fluorescence is Ca2+. **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
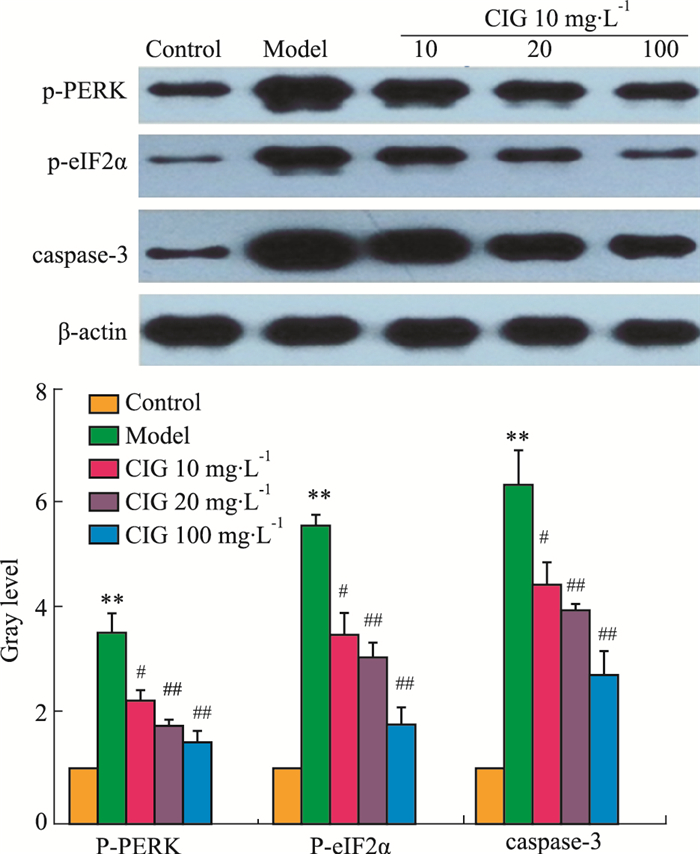
Fig 4 Western blot结果显示,D-GalN/TNF-α损伤肝细胞中磷酸化PERK和eIF2α、凋亡相关蛋白caspase-3的表达明显升高,与对照组比较均具有统计学意义(P<0.05)。CIG低、中、高浓度组均可降低相关蛋白的表达,且呈浓度依赖性。
|
| Fig 4 Effects of CIG on expression of three kinds of protein in injured L-02 cells **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
线粒体、内质网、死亡受体3条调控细胞凋亡信号的通路都与Ca2+有关,最终导致细胞凋亡。大量的活性氧自由基会破坏细胞膜、线粒体、内质网等细胞器,使钙离子重新分配,引起caspase凋亡家族的激活[7]。有研究认为,细胞内钙离子的稳定主要是依靠内质网进行调节,通过内质网释放的Ca2+激活Ca2+/钙调神经磷酸酶,激活Bad蛋白[8]。Fas、TRAILR2、TRAILR1、TNFR1等都属于死亡受体,又是TNF的受体家族,在D-GalN/TNF-α损伤肝细胞模型中,肝细胞局部聚集的TNF-α与细胞膜上的受体结合,使凋亡家族caspase级联反应活化,细胞凋亡反应发生[9]。
肝细胞内质网凋亡通路中最重要的一条就是PERK/eIF-2α-CHOP途径。PERK属于内质网的Ⅰ型膜蛋白,内质网应激发生后PERK/eIF-2α-CHOP途经被激活,磷酸化的eIF-2α诱导下游的转录因子ATF4以及下游的基因表达,促进细胞对内质网应激的适应。活化的ATF4诱导CHOP的表达,CHOP的激活是导致细胞凋亡的最重要途经[10],而且PERK/eIF-2α通路是CHOP蛋白表达所必需的[11]。CHOP被激活后,通过调节参与凋亡途径的蛋白表达发挥作用,抑制抗凋亡基因Bcl-2,激活caspase-3和caspase-9。而caspase-3的表达并不仅仅是被CHOP而激活,Ca2+、氧化应激都导致了caspase家族的激活。因此,降低caspase-3基因的表达,在抗细胞凋亡等方面具有重要的意义。
CIG对D-GalN/TNF-α诱导肝细胞损伤的保护机制研究中,CIG对于提高损伤细胞对氧化应激的耐受力具有积极的影响,可以降低D-GalN/TNF-α损伤导致的细胞内Ca2+含量升高,减轻因钙离子浓度过高引起的细胞器损伤,降低相关凋亡基因的表达,从多方面发挥对损伤细胞的保护作用。
( 致谢: 本实验主要在南京中医药大学基础医学院生物技能实验室完成,感谢席蓓丽老师,段煜、李文婷等同学的帮助,在此致以真诚的感谢。)
| [1] | 国家药典委员会. 中华人民共和国药典[S]]一部. 北京: 中国医药科技出版社, 2010: 26. National pharmacopoeia committee. Pharmacopoeia of the people's republic[S]. the first volume. Beijing: Chinese medical science and technology press, 2010:26. |
| [2] | 于淼, 王晓先, 贾琳. 山茱萸的药理作用研究进展[J]. 东南国防医药, 2010, 12(3): 240-3. Yu M, Wang X X, Jia L. Research on the pharmacological effects of cornus[J]. Southeast Defence Med, 2010, 12(3): 240-3. |
| [3] | 李观林. 山茱萸中环烯醚萜苷类的研究进展[J]. 亚太传统医药, 2014, 10(18): 48-9. Li G L. Research on cornel iridoid glycoside[J]. Asia-Pacific Tradit Med, 2014, 10(18): 48-9. |
| [4] | 沈红胜, 许慧琴, 陆春红. 山茱萸环烯醚萜苷类成分对AGEs诱导HUVEC损伤的保护作用[J]. 中国药理学通报, 2016, 32(8): 1063-7. Shen H S, Xu H Q, Lu C H. Protective effect of loganin and morroniside on HUVEC injury induced by advanced glycation end products[J]. Chin Pharmacol Bull, 2016, 32(8): 1063-7. |
| [5] | Silverstein R. D-galactosamine lethality model: scopeand limitations[J]. J Endotoxin Res, 2004, 10(3): 147-62. |
| [6] | Jesephs M D, Bahjar F R, Fukuzuka K, et al. Lipopolysac-charide and D-galactesamine-induced hepatic injury ismediated by TNF-α and not by Fas ligand[J]. Am J Physiol Regul Integr Comp Physiol, 2000, 278(5): 1196-201. doi:10.1152/ajpregu.2000.278.5.R1196 |
| [7] | Lin H L, Yang J S, Yang J H, et al. The role of Ca2+ on the DADS-induced apoptosis in mouse-rat hybrid retina ganglion cells (N18)[J]. Neurochem Res, 2006, 31(3): 383-93. doi:10.1007/s11064-005-9035-1 |
| [8] | Lamb H K, Mee C, Xu W, et al. The affinity of a major Ca2+ binding site on GRP78 is differentially enhanced by ADP and ATP[J]. J Biol Chem, 2006, 281(13): 8796-805. doi:10.1074/jbc.M503964200 |
| [9] | Muriel P. NF-kappaB in liver diseases:a target for drug therapy[J]. Appl Toxicol, 2009, 29(2): 91-100. doi:10.1002/jat.v29:2 |
| [10] | Oida Y, Shimazawa M, Imaizumi K, et al. Involvement of endoplasmic reticulum stress in the neuronal death induced by transient forebrain ischemia in gerbil[J]. Neuroscience, 2008, 151(1): 111-9. doi:10.1016/j.neuroscience.2007.10.047 |
| [11] | Phal H. Signal transduction from the endoplasmic reticulum to the cell nucleus[J]. Physiol Rev, 1999, 79(3): 683-701. doi:10.1152/physrev.1999.79.3.683 |