

2. 河北医科大学病理学教研室,河北 石家庄 050017
2. Dept of Pathology, Hebei Medical University, Shijiazhuang 050017, China
糖尿病肾病(diabetic nephropathy, DN)是糖尿病最严重的并发症之一,最终引起终末期肾衰竭(end-stage renal disease, ESRD)[1-2]。目前,针对DN的治疗仍以预防为主,临床上尚未研发出治疗DN尤其是抗肾间质纤维化的有效药物。因此,研究DN肾间质纤维化特别是细胞外基质(extracellular matrix, ECM)沉积的发生机制,并寻找潜在的干预靶点,将对DN的防治起到关键作用。硫酯酶超家族成员4(thioesterase superfamily member 4, THEM4)是一种Akt内源性抑制因子[3]。本研究前期从细胞水平上发现重组质粒pYr-ads-4-THEM4的转染能够逆转高糖诱导的人肾小管上皮细胞phospho-Akt(Ser 473)的活化以及胶原的分泌。然而,过表达THEM4能否减轻糖尿病小鼠肾脏ECM沉积还有待进一步证实。因此,本研究通过尾静脉注射将pYr-ads-4-THEM4表达质粒转染至糖尿病小鼠体内,进一步观察THEM4在糖尿病小鼠肾脏中的表达及其对ECM沉积的影响。
1 材料与方法 1.1 试剂pYr-ads-4-THEM4 vector、pYr-adshuttle-4 empty vector均购自长沙赢润生物有限公司;TransIT-EE Hydrodynamic Delivery Solution购自美国Mirus公司;兔抗THEM4单克隆抗体(14692-1-AP)、兔抗β-actin单克隆抗体(20536-1-AP)、兔抗α-SMA单克隆抗体(14295-1-AP)、兔抗纤维黏连蛋白(fibronectin, FN)单克隆抗体(13548-1-AP)、兔抗Ⅲ型胶原蛋白(collagen Ⅲ, Col Ⅲ)单克隆抗体,均购自美国Protein Tech公司;兔抗phospho-Akt (Ser 473)单克隆抗体(#4060)、兔抗Akt单克隆抗体(#4685),均购自美国Cell Signaling公司;兔抗TGF-β1单克隆抗体(#AP12348a)购自ABGENT。
1.2 动物模型及分组体质量20~25 g健康♂CD1小鼠40只,由北京维通利华实验动物技术有限公司提供(合格证编号0126327)。将实验动物随机分为正常对照组(Control组)、糖尿病组(DM组)、糖尿病+THEM4质粒组(DM+THEM4)、糖尿病+空质粒组(DM+V),每组10只。后3组小鼠腹腔注射链脲佐菌素(streptozotocin, STZ, 溶于0.1 mol·L-1枸橼酸盐缓冲液中,pH值4.5,150 mg·kg-1),72 h后尾尖取血,血糖≥16.7 mmol·L-1者确定为DM模型。质粒注射组小鼠在成模4周后,分别给予尾静脉快速注射pYr-ads-4-THEM4质粒或pYr-adshuttle-4空质粒(1 mg·kg-1)。此后每隔7 d注射1次,共注射4次。
1.3 标本收集DM模型建成后,每周测血糖1次,不符合标准者弃去。于质粒注射4周后处死小鼠。在处死前1 d于代谢笼中单独饲养收集24 h尿液,记录尿量。禁食6~8 h,称重后异氟烷吸入麻醉,摘眼球取血,离心分离血清,用于测定血糖、血尿素氮和血肌酐;切取肾脏,取部分肾组织置于4%多聚甲醛(0.01 mol·L-1 PBS配制)固定,用于免疫组化检测,部分肾皮质组织液氮速冻后,保存于-80℃冰箱,用于提取蛋白和RNA。
1.4 血尿生化指标检测每个样本取20 μL血清,采用雷杜RT-9600半自动生化分析仪测定血糖(Glu)、血尿素氮(BUN)及血肌酐(Scr)。同时,每个样本取20 μL尿液测尿蛋白浓度,计算24 h尿蛋白量(Upro)。
1.5 Real-time PCR检测THEM4 mRNA的表达严格按照RNAprep pure动物组织总RNA提取试剂盒(#DP431)说明书提取肾组织RNA,具体步骤参见文献[4]。目的基因的引物序列分别为:小鼠THEM4 sense 5′-CCAGGAGCAGCTAGGAGGTTA-3′,antisense 5′-GTCTGAGGTCCTTAGTCCAGC-3′,扩增片段91 bp;小鼠GAPDH sense 5′-AGGTCGGTGTGAACGGATTTG-3′,antisense 5′-GGGGTCGTTGATGGCAACA-3′,扩增产物95 bp。扩增条件为:预变性95℃ 30 s;95℃ 5 s,55℃ 30 s,72℃ 30 s,扩增40个循环。以GAPDH作为内参照校正,用2-△△Ct法分析基因的相对表达。
1.6 蛋白印迹检测Akt、phospho-Akt(Ser 473)、THEM4、TGF-β1和α-SMA蛋白表达将等量肾组织剪碎后,加入10倍体积的预冷的组织裂解缓冲液,用玻璃研磨器将组织块研碎,冰上裂解30 min,低温高速离心(4℃、12 000 r·min-1、20 min),上清液即为所提取的蛋白溶液。采用考马斯亮蓝试剂法进行蛋白定量。每组样品取50 μg蛋白,进行SDS聚丙烯酰胺凝胶电泳,电泳完毕后,电转移至PVDF膜,5% BSA封闭液37℃封闭1 h,加入抗THEM4、Akt、phospho-Akt(Ser 473)、α-SMA、TGF-β1、β-actin一抗(1:1 000),4℃孵育过夜。经TBST洗涤后,辣根过氧化物酶标记的山羊抗兔IgG(1:5 000稀释),室温孵育2 h。滴加ECL发光试剂于膜上,反应1 min后,OdysseyFC成像系统显影。最后用美国UVP公司LabWorks 4.5软件对Western blot条带进行定量分析,以目的条带和β-actin条带积分光密度值比值作为最终结果。
1.7 免疫组化检测THEM4、phospho-Akt(Ser 473)、FN和Col Ⅲ蛋白表达采用三步法进行免疫组化检测,具体步骤如下:石蜡切片厚4 μm,常规脱蜡至水;0.3%过氧化氢去离子水室温孵育以去除内源性过氧化物酶;pH 6.0枸橼酸抗原修复液进行微波修复;滴加封闭液(10%正常山羊血清),37℃孵育30 min,减少非特异性染色;滴加一抗[THEM4 1:50, phospho-Akt(Ser 473) 1:200, FN 1:100, Col Ⅲ 1:100],4℃过夜;分别滴加生物素化羊抗兔/鼠IgG及辣根过氧化物酶标记的链卵白素工作液,37℃孵育30 min。用新鲜配制的DAB-H2O2液显色,苏木精复染、盐酸酒精分化、氨水返蓝、脱水、透明、封片。免疫组化结果应用Image-Pro Plus(IPP)图文分析软件分析,每个标本切片取10个高倍视野(400倍),综合阳性面积和染色深度计算阳性区域的积分光密度值(integrated optical density, IOD),以各组的均值进行比较。
1.8 统计学处理实验数据以x±s表示,采用SPSS 13.0统计软件进行统计,组间比较采用单因素方差分析(One-Way ANOVA)。
2 结果 2.1 各组小鼠血、尿生化指标检测同正常对照组小鼠相比,糖尿病小鼠血糖、24 h尿蛋白、血肌酐及血尿素氮水平分别上调了4.96、2.59、1.52、7.50倍(P<0.05),经pYr-ads-4-THEM4质粒转染后,血肌酐、血尿素氮及24 h尿蛋白的水平均明显降低(P<0.05),而pYr-adshuttle-4空质粒组上述指标未观察到明显变化(Tab 1)。
| Group | Glu/mmol·L-1 | Upro/mg·(24 h)-1 | Scr/μmol·L-1 | BUN/mmol·L-1 |
| Control | 8.16±0.76 | 0.68±0.17 | 350.33±45.83 | 9.33±1.74 |
| DM | 40.48±1.49* | 1.76±0.38* | 531.83±29.21* | 69.97±5.86* |
| DM+THEM4 | 36.44±1.30* | 0.71±0.29# | 456.50±48.67# | 26.37±1.16*# |
| DM+V | 39.81±1.18* | 1.63±0.60* | 514.33±32.26* | 69.69±7.39* |
| *P < 0.05 vs control; #P < 0.05 vs DM+V | ||||
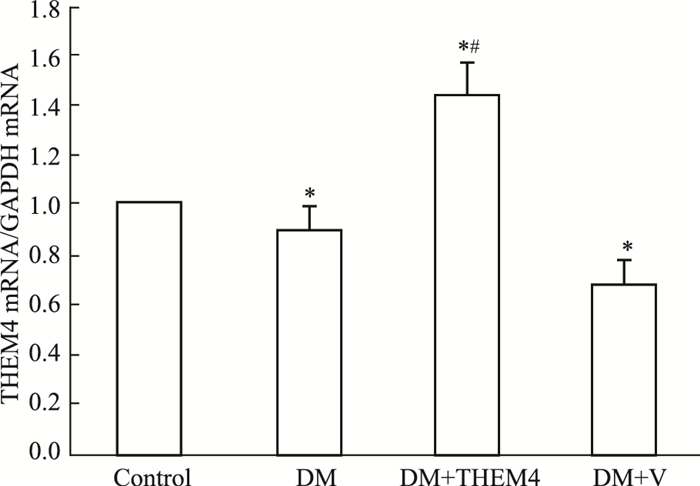
质粒转染后,real-time PCR检测THEM4 mRNA的表达,Fig 1结果显示,糖尿病小鼠肾脏THEM4 mRNA的表达较正常对照组明显降低,经pYr-ads-4-THEM4质粒转染后表达明显上调。Fig 2 Western blot结果显示,pYr-ads-4-THEM4质粒转染组小鼠肾脏THEM4蛋白的表达较pYr-adshuttle-4空质粒组上调了8.84倍。同样地,免疫组化结果发现了类似的现象,THEM4蛋白在正常对照组小鼠有一定量的表达,主要定位于肾小管上皮细胞的胞质,经质粒转染后阳性表达明显增加。IPP软件分析阳性区域IOD值结果显示,与pYr-adshuttle-4空质粒组相比,pYr-ads-4-THEM4质粒转染组小鼠肾脏THEM4蛋白的表达上调了9.43倍(Fig 3、Tab 2)。与THEM4蛋白的表达恰好相反,phospho-Akt (Ser 473)在糖尿病组小鼠肾脏中的表达明显增强,而经pYr-ads-4-THEM4质粒转染后表达受到明显抑制,下调了60.00%。同时免疫组化IPP软件分析阳性区域IOD值结果显示,THEM4质粒转染组phospho-Akt (Ser 473)的表达较空质粒组下降了54.33% (Fig 4、Tab 2)。而总Akt的表达在各组间未见明显差异。
|
| Fig 1 Real-time PCR of THEM4 mRNA with an internal control of GAPDH in mice of four groups *P < 0.05 vs control group; #P < 0.05 vs DM+V group |

|
| Fig 2 THEM4, phospho-Akt (Ser 473) and Akt protein expressions in renal cortex examined by Western blot *P < 0.05 vs control group; #P < 0.05 vs DM+V group |

|
| Fig 3 Immunohistochemical staining for THEM4 in kidneys of mice of four groups (Scale bar: 50 μm) A: Control group; B: DM group; C: DM+ THEM4 group; D: DM+V group. Black arrows show positive signal. |
| Group | THEM4 | phospho-Akt | FN | ColⅢ |
| Control | 36202.00±4306.87 | 42916.33±24570.22 | 42587.54±6874.44 | 63764.67±11519.00 |
| DM | 13831.00±5143.24* | 302573.00±29747.78* | 118326.57±12491.62* | 120616.33±24069.05* |
| DM+THEM4 | 111576.70±8349.97*# | 139787.00±55343.67*# | 57241.68±15473.33*# | 80143.39±10524.29*# |
| DM+V | 10695.67±1139.70* | 306111.30±15049.35* | 117943.52±19732.09* | 134533.06±23712.48* |
| *P < 0.05 vs control; #P < 0.05 vs DM+V | ||||

|
| Fig 4 Immunohistochemical staining for phospho-Akt (Ser 473) in kidneys of mice of four groups (Scale bar: 50 μm) A: Control group; B: DM group; C: DM+ THEM4 group; D: DM+V group. Black arrows show positive signal. |
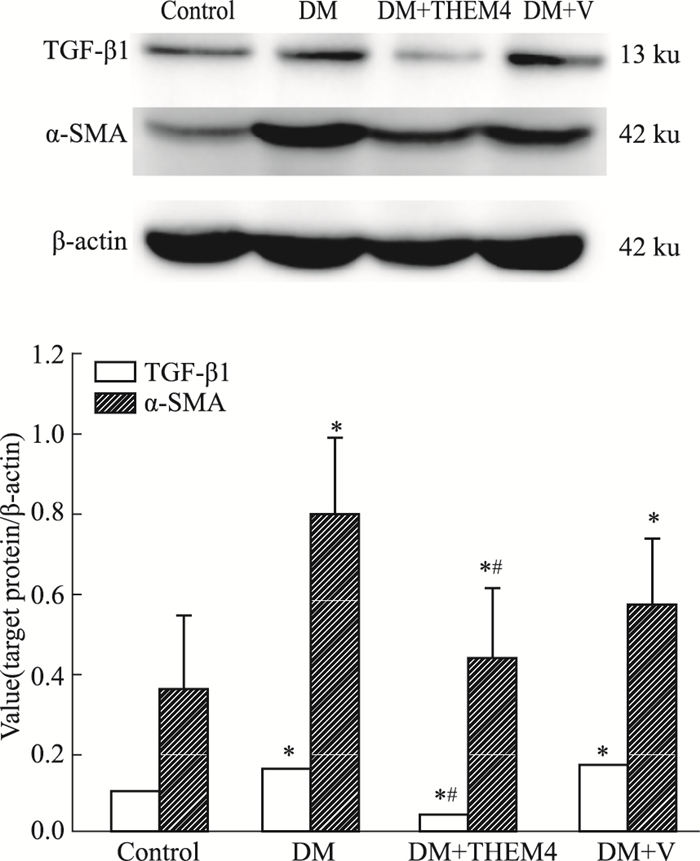
Western blot进一步检测了各组小鼠肾脏α-SMA和TGF-β1蛋白的表达。Fig 5结果显示,糖尿病组小鼠肾脏α-SMA和TGF-β1的表达较正常对照组相比明显上调。而通过尾静脉注射pYr-ads-4-THEM4质粒后,转染组α-SMA和TGF-β1的表达与空质粒组相比分别下调了24.37%和76.50%。
|
| Fig 5 Western blot detection and statistical analyses for TGF-β1 and α-SMA *P < 0.05 vs control group; #P < 0.05 vs DM+V group |
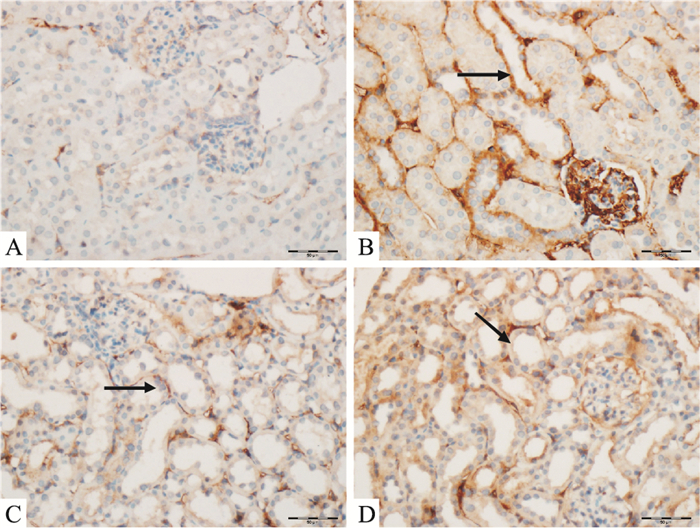
为了进一步观察过表达THEM4对糖尿病小鼠肾脏ECM沉积的影响,应用免疫组化检测了各组小鼠肾脏Col Ⅲ、FN的表达,Fig 6、7结果发现,空质粒组及糖尿病组小鼠肾皮质内二者均出现了明显的阳性信号,主要定位于近端肾小管上皮细胞的间质内,而pYr-ads-4-THEM4质粒组小鼠肾小管上皮细胞间质中Col Ⅲ和FN的表达明显降低,IPP软件分析Col Ⅲ及FN阳性区域IOD值较空质粒组相比分别降低了40.43%及51.47%(Tab 2)。

|
| Fig 6 Immunohistochemical staining for Col Ⅲ in kidneys of mice of four groups (Scale bar: 50 μm) A: Control group; B: DM group; C: DM+ THEM4 group; D: DM+V group. Black arrows show positive signal. |
|
| Fig 7 Immunohistochemical staining for FN in kidneys of mice of four groups (Scale bar: 50 μm) A: Control group; B: DM group; C: DM+ THEM4 group; D: DM+V group. Black arrows show positive signal. |
目前,减少ECM的过度沉积被认为是防治DN尤其是肾小管间质纤维化的一个热点。当肾脏受到长期的炎症介质浸润以及高糖刺激后,会导致肾脏固有细胞发生炎症改变,并激活多种ECM转录蛋白,从而分泌过量的胶原、FN等ECM成分,最终引起肾脏的损伤[5-7]。因此,减少ECM的积聚是延缓DN发生的关键环节。
新近研究发现,G蛋白偶联受体TGR5能够抑制高糖诱导的大鼠肾小球系膜细胞TGF-β1、FN蛋白的表达,减轻DN的ECM沉积[8]。大黄素通过抑制高糖诱导的大鼠肾小球系膜细胞的增殖、FN表达与p38MAPK活化,发挥抗糖尿病肾脏纤维化的作用[9]。本课题组前期也发现,PTEN(Akt的抑制剂之一)通过抑制Akt的活性,下调糖尿病小鼠肾脏结缔组织生长因子(connective tissue growth factor, CTGF)的表达及减少ECM积聚[10]。而THEM4作为Akt另一重要的内源性抑制因子,该基因是位于1号染色体长臂21-24区,与糖尿病、慢性肾脏疾病等代谢性疾病发生相关的基因[11],其是否参与了糖尿病肾脏ECM沉积及其影响如何却尚未见报道。
基因水平的研究是探讨疾病发病机制的重要手段,通过将外源性基因导入体外培养的细胞或者动物模型靶组织中使其过度表达,或通过基因敲除使其有效沉默,从而探讨目的基因在疾病发病过程中的作用及其可能机制,为疾病的靶向治疗提供方向。有学者将携带脂肪因子adipsin的重组腺病毒质粒pAd-adipsin通过尾静脉注射导入2型糖尿病大鼠模型体内,发现能有效改善大鼠的糖、脂质代谢紊乱,对糖尿病的防治具有一定效果[12]。李科军等[13]研究证实,糖尿病小鼠肾皮质中巨噬细胞数量增多并伴随α-SMA、TGF-β1及FN等蛋白表达增强,而通过小鼠尾静脉注射细胞因子信号传导抑制蛋白1(suppressors of cytokine signaling 1, SOCS1)表达质粒后,能明显降低α-SMA、TGF-β1及FN等蛋白的表达,减轻糖尿病小鼠肾小管间质纤维化。另外,有学者通过对糖尿病小鼠尾静脉注射早期生长反应蛋白1(early growth response protein 1, Egr-1)表达质粒后,可引起系膜细胞的增殖及系膜区ECM的积聚;而Egr-1 siRNA质粒的尾静脉注射能有效缓解糖尿病小鼠的上述病变[14]。
本研究同样通过小鼠尾静脉注射,将pYr-ads-4-THEM4质粒转染至糖尿病小鼠体内,发现THEM4 mRNA及蛋白均在质粒转染组小鼠肾脏中高表达,提示质粒转染成功。结果证实过表达THEM4通过抑制phospho-Akt(Ser 473)的活化以及下调α-SMA、TGF-β1、Col Ⅲ、FN等蛋白的表达,减轻糖尿病小鼠ECM的积聚。另外,经THEM4质粒转染后,小鼠血肌酐、血尿素氮以及24 h尿蛋白水平较糖尿病组及空质粒组相比均有所下降,提示THEM4的过表达能够有效改善DM模型小鼠的肾功能,对糖尿病肾损害有一定的防治意义。
本实验首次对THEM4在糖尿病小鼠ECM沉积中的影响进行了研究,通过质粒转染技术使THEM4在糖尿病小鼠体内过表达,并揭示过表达THEM4能够减轻糖尿病小鼠肾脏ECM的沉积。通过本研究能够更加深入地了解糖尿病肾脏ECM沉积的发生发展机制,并为其靶向治疗提供新的理论依据和研究思路。
( 致谢: 本实验于河北医科大学病理学实验室完成,感谢实验室全体老师的帮助。)
| [1] | Cha S A, Yun J S, Lim T S, et al. Severe hypoglycemia and cardiovascular or all-cause mortality in patients with type 2 diabetes[J]. Diabetes Metab J, 2016, 40(3): 202-10. doi:10.4093/dmj.2016.40.3.202 |
| [2] | Wheelock K M, Jaiswal M, Martin C L, et al. Cardiovascular autonomic neuropathy associates with nephropathy lesions in American Indians with type 2 diabetes[J]. J Diabetes Complications, 2016, 30(5): 873-9. doi:10.1016/j.jdiacomp.2016.03.008 |
| [3] | Zhao H, Lim K, Choudry A, et al. Correlation of structure and function in the human hotdog-fold enzyme hTHEM4[J]. Biochemistry, 2012, 51(33): 6490-2. doi:10.1021/bi300968n |
| [4] | 陈宁. C末端调节蛋白在糖尿病肾脏细胞外基质沉积中的作用[D]. 石家庄: 河北医科大学, 2017. Chen N. Roles of Carboxy-terminal modulator protein in extracellular matrix accumulation in diabetic nephropathy[D]. Shijiazhuang:Hebei Medical University, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10089-1017825905.htm |
| [5] | Ahad A, Ahsan H, Mujeeb M, et al. Gallic acid ameliorates renal functions by inhibiting the activation of p38 MAPK in experimentally induced type 2 diabetic rats and cultured rat proximal tubular epithelial cells[J]. Chem Biol Interact, 2015, 240: 292-303. doi:10.1016/j.cbi.2015.08.026 |
| [6] | Yonekura Y, Fujii H, Nakai K, et al. Anti-oxidative effect of the β-blocker carvedilol on diabetic nephropathy in non-obese type 2 diabetic rats[J]. Clin Exp Pharmacol Physiol, 2015, 42(9): 972-8. doi:10.1111/cep.2015.42.issue-9 |
| [7] | Ellein M, Xing C, Amgad Z, et al. The role of Krüppel-like factor 4 in transforming growth factor-β-induced inflammatory and fibrotic responses in human proximal tubule cells[J]. Clin Exp Pharmacol Physiol, 2015, 42(6): 680-6. doi:10.1111/1440-1681.12405 |
| [8] | 熊凤霄, 杨志英, 王少贵, 等. 胆汁酸膜受体TGR5对高糖培养的大鼠肾小球系膜细胞FN、TGF-β1的调控作用[J]. 中国药理学通报, 2016, 32(1): 33-7. Xiong F X, Yang Z Y, Wang S G, et al. Regulatory effects of the bile acid membrane receptor TGR5 on FN and TGF-β1 in rat glomerular mesangial cells cultured under high glucose condition[J]. Chin Pharmacol Bull, 2016, 32(1): 33-7. |
| [9] | 李学娟, 陈泽彬, 魏红, 等. 大黄素对高糖培养的GMC增殖、FN表达及p38MAPK的影响[J]. 中国药理学通报, 2014, 30(2): 233-8. Li X J, Chen Z B, Wei H, et al. Effects of emodin on cell proliferation, FN expression and p38MAPK pathway in rat mesangial cells cultured under high glucose[J]. Chin Pharmacol Bull, 2014, 30(2): 233-8. |
| [10] | Zhu L, Zhao S, Liu S, et al. PTEN regulates renal extracellular matrix deposit via increased CTGF in diabetes mellitus[J]. J Cell Biochem, 2016, 117(5): 1187-98. doi:10.1002/jcb.v117.5 |
| [11] | Lai F N, Zhai H L, Cheng M, et al. Whole-genome scanning for the litter size trait associated genes and SNPs under selection in dairy goat (Capra hircus)[J]. Sci Rep, 2016, 6: 38096. doi:10.1038/srep38096 |
| [12] | 张磊, 周艳, 闫姗姗, 等. Adipsin腺病毒载体构建及对2型糖尿病大鼠的治疗作用[J]. 生物学杂志, 2016, 33(5): 58-62. Zhang L, Zhou Y, Yan S S, et al. Construction of adenovirus vector containing adipsin and its therapy on 2 type diabetes rat model[J]. J Biol, 2016, 33(5): 58-62. |
| [13] | 李科军, 杜云霞, 封晓娟, 等. SOCS1在糖尿病小鼠肾小管间质病变中的作用[J]. 中国细胞生物学学报, 2015, 37(7): 992-7. Li K J, Du Y X, Feng X J, et al. The role of SOCS1 in tubulointerstitium injury of mice with diabetes[J]. Chin J Cell Biol, 2015, 37(7): 992-7. doi:10.11844/cjcb.2015.07.0103 |
| [14] | 刘洁, 张海松, 马永军, 等. Egr-1基因转染对糖尿病小鼠肾脏炎症反应的影响[J]. 中国病理生理杂志, 2015, 31(9): 1688-92. Liu J, Zhang H S, Ma Y J, et al. Effect of Egr-1 gene transfection on renal inflammation in diabetic mice[J]. Chin J Pathophysiol, 2015, 31(9): 1688-92. |

