

2. 河北中医学院河北省心脑血管病中医药防治重点实验室,河北 石家庄 050200
2. Hebei University of Chinese Medicine, Hebei Key Lab of Chinese Medicine Research on Cardio-cerebrovascular Diseases, Shijiazhuang 050200, China
脑血管疾病是危害中老年人健康的常见疾病之一,它具有高发病率、高致残率、高死亡率的特点,给家庭和社会带来了沉重的负担[1]。随着医学水平的不断提高,人们对脑缺血/再灌注损伤的发病机制有了更深入的探索,在治疗脑缺血/再灌注损伤的药物中,传统中药黄芪发挥了巨大的作用。黄芪属豆科草本植物,具有补气固表、敛疮生肌、活血化瘀、消肿止痛的作用[2]。现代研究证实,黄芪不仅可以扩张血管、改善脑血流量,且具有清除氧自由基、提高超氧化物歧化酶活性等多重功效[3-4]。目前,国内应用黄芪与其他药物配伍治疗脑缺血的研究比较常见,而单独应用黄芪的某个单体是一个新的探索。黄芪甲苷作为黄芪皂苷类的单体成分,可抑制缺氧缺糖/复氧复糖PC12细胞凋亡[5],从而发挥神经保护作用。本研究目的在于探讨黄芪甲苷是否具有减轻大鼠局灶性脑缺血/再灌注损伤的作用。
1 材料与方法 1.1 材料 1.1.1 动物健康清洁级SD大鼠40只,♂,体质量(260±20) g,由北京维通利华实验动物技术有限公司提供,许可证号为SCXK(京)2016-0011。
1.1.2 试剂氯化2, 3, 5, 三苯基四氮唑(TTC)购自Biosharp公司;甲苯胺蓝溶液、水合氯醛购自北京索莱宝生物科技有限公司;大脑中动脉阻塞(middle cerebral artery occlusion, MCAO)线栓购自北京西浓生物科技有限公司;黄芪甲苷购自南京森贝伽生物科技有限公司,每瓶100 mg,纯度≥98%,生产批号:170302;其他试剂为国产分析纯。
1.1.3 仪器EG11508型组织包埋机、RM2255型全自动轮转切片机、DM5000B型光学显微镜,均购自德国Leica公司;H-7650型透射电子显微镜购自HITACHI公司。
1.2 方法 1.2.1 动物分组与造模SD大鼠随机分为4组:假手术组(Sham)、脑缺血/再灌注组(I/R)、黄芪甲苷组(AS-Ⅳ)和溶剂对照组(Vehicle)。采用改良线栓法模拟局灶性脑缺血/再灌注损伤:SD大鼠适应性饲养1周,于术前12 h禁食、4 h禁水,经10%水合氯醛腹腔注射麻醉后,将大鼠仰卧位固定到操作台上,备皮消毒,采用颈部正中切口,钝性分离左侧肌肉组织暴露左侧颈总动脉以及颈内、颈外动脉,结扎并离断颈外动脉,选取合适的线栓由颈外动脉残端进入,经颈内动脉到达大脑中动脉并阻塞大脑中动脉[6]。缺血2 h后,缓慢轻柔地拔出线栓直至颈外动脉残端,使颈总、颈内动脉血流通畅,即再灌注开始。再灌注24 h后,挑选模型成功的大鼠处死取材[7]。Sham组线栓由颈外动脉残端插入颈内动脉,但不入颅,除插入深度外,余手术方法与各组相同;AS-Ⅳ组于再灌注的同时腹腔注射黄芪甲苷20 mg·kg-1,黄芪甲苷100 mg溶于二甲基亚砜(DMSO)后经生理盐水稀释配成终浓度为1 g·L-1溶液[8-9];Vehicle组腹腔注射等量等浓度的DMSO生理盐水稀释液。
1.2.2 神经功能学评分术后24 h进行神经功能学评分。Zea Longa评分标准:0分,正常无神经缺损症状;1分,不能完全伸展对侧前爪;2分,行走向对侧转圈;3分,行走向对侧倾倒;4分,不能自发行走,意识丧失。0分、4分或死亡者剔除,1~3分者列为实验对象。
1.2.3 TTC染色测定大鼠脑梗死体积各组于再灌注24 h后断头取脑,取完整的脑组织置于-20℃冰箱内,冷冻15 min后行冠状位切片,每片厚度为2 mm,置于2%的TTC染液中,37℃温箱避光孵育30 min,每隔15 min翻动1次。倾出染液,PBS终止染色,置于4%多聚甲醛固定2 h后拍照,采用Image-Pro Plus 6.0图片分析软件计算脑梗死体积。
1.2.4 尼氏染色观察细胞形态取各组大脑中动脉供血区域的脑组织行冠状位切片(厚3~4 mm),4%多聚甲醛固定,梯度乙醇脱水,二甲苯透明,石蜡包埋,厚度5μm连续冠状切片,二甲苯、梯度乙醇脱蜡至水,浸入甲苯胺蓝1%水溶液染色30 min,蒸馏水洗,体积分数0.95的乙醇分色,无水乙醇脱水,二甲苯透明,中性树胶封片,光学显微镜下观察并拍照。
1.2.5 透射电子显微镜观察细胞超微结构取缺血半暗带部位大小为1 mm×1 mm×1 mm的脑组织数块,PBS清洗后迅速放入预冷的4%戊二醛固定液固定2 h,PBS清洗、1%锇酸后固定2 h,丙酮溶液梯度脱水,Epon812包埋,恒温箱聚合。半薄切片选区后行超薄切片,醋酸铀和柠檬酸铅双重电子染色,透射电子显微镜下观察。
1.3 统计学处理数据以x±s表示,采用SPSS 19.0统计软件进行单因素方差分析,组间两两比较采用SNK-q检验。
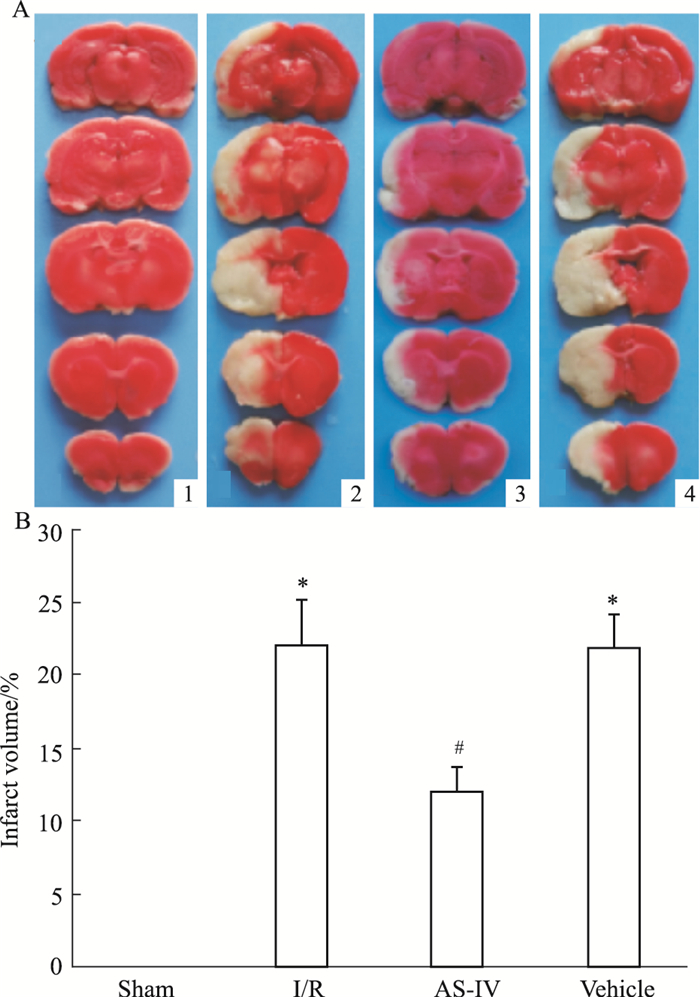
2 结果 2.1 各组大鼠脑梗死体积的变化如Fig 1所示,Sham组未见梗死灶,其他各组均有不同程度的梗死灶形成。与I/R组相比,AS-Ⅳ组脑梗死体积明显缩小(P<0.05),差异有统计学意义;Vehicle组则无明显差异(P>0.05)。
|
| Fig 1 Change of infarct volume with different treatment examined by TTC staining (x±s, n=6) A: Photographs of brain sections with TTC staining; 1: Sham; 2: I/R; 3: AS-Ⅳ; 4: Vehicle; B: Percentage of infarct volume. *P < 0.05 vs sham; #P < 0.05 vs I/R and vehicle. |
如Fig 2所示,Sham组可见细胞排列规整,胞核清晰,尼氏体丰富,染色均匀。I/R组细胞损伤严重,细胞排列紊乱,核固缩深染,核膜模糊不清,尼氏体着色较浅。与I/R组相比,AS-Ⅳ组细胞状态明显好转,细胞形态较完整,尼氏体增多,染色较均匀;Vehicle组细胞形态则无明显变化。

|
| Fig 2 Morphological changes of nerve cells in each group (Nissl staining, ×400) A: Sham; B: I/R; C: AS-Ⅳ; D: Vehicle; E: The average numbers of Nissl-stained cells across five random visual fields per section were used for the statistical analysis(x±s, n=5). *P < 0.05 vs sham; #P < 0.05 vs I/R and vehicle. |
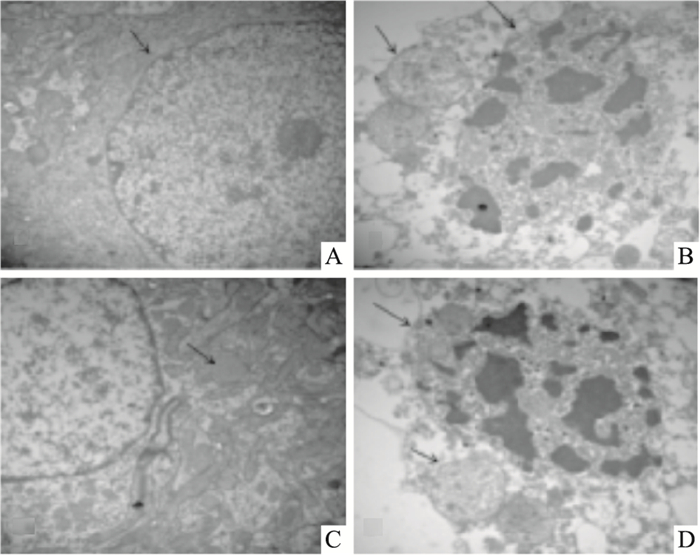
如Fig 3所示,Sham组可见细胞核膜光滑完整,染色质均匀,胞质内各细胞器结构清晰可辨。I/R组可见细胞核膜断裂、溶解,核内异染色质增多,线粒体肿胀,基质密度减低,嵴消失,胞质内空泡形成。与I/R组相比,AS-Ⅳ组细胞状态有所好转,可见细胞核膜较为光滑,染色质均匀,线粒体轻度肿胀变圆;Vehicle组则无明显变化。
|
| Fig 3 Ultrastructure of cells under transmission electron microscope in each group (×20 0000) A:Sham; B:I/R; C:AS-Ⅳ; D:Vehicle |
脑缺血/再灌注损伤的发生是一个非常复杂的病理生理过程,目前研究认为自由基、细胞内钙离子增多以及白细胞的激活是其重要的发病环节[10]。缺血/再灌注导致自由基增多,自由基的化学性质极为活泼,且氧化作用强,可与细胞膜的骨架成分发生反应,从而造成细胞结构损伤以及功能代谢障碍。本实验在透射电镜下观察到,I/R组细胞膜、核膜断裂溶解,细胞肿胀,其原因可能是自由基同膜脂质不饱和脂肪酸相互作用,引发了脂质过氧化反应,造成膜结构和功能的破坏。膜的流动性降低、通透性升高,细胞膜上Na+-ATP酶、Ca2+-ATP酶及Na+/Ca2+交换系统功能异常,将会使细胞内Na+、Ca2+浓度升高,造成细胞肿胀、Ca2+超载。细胞内Ca2+的增加可激活磷脂酶类,促使膜磷脂降解[11],膜结构进一步被破坏。细胞内Ca2+的增加也可激活核酶,引起染色体的损伤,在透射电镜下亦可观察到细胞核内异染色质的增多。缺血/再灌注时,白细胞数量有所增多,以中性粒细胞的增多最为明显,相较于红细胞而言,中性粒细胞体积大、变形能力弱,在一些黏附分子的作用下,中性粒细胞能与受损的血管内皮细胞紧密结合,阻塞微血管,促使无复流现象的发生,加重细胞缺血性损伤[12, 16]。
黄芪是一味传统的补气圣药。始载于《神农本草经》,距今已有2 000多年的历史。研究证实,黄芪具有改善微循环、降低血脂、提高一氧化氮合酶和一氧化氮含量等作用。黄芪甲苷是黄芪三大有效活性成分之一,具有抗氧化、抗病毒、调节免疫力等多种药理活性[13],对缺血器官的保护也有明显的作用[14]。黄芪甲苷可以抑制自由基的生成,减小脂质过氧化物的反应,影响钙泵并调节Ca2+的转运功能,从而缓解钙超载引起的细胞损伤[15]。黄芪甲苷亦可以促进内皮细胞的增殖与迁移,干预炎性细胞黏附,改善血管内皮细胞[16],并且促进骨髓间充质干细胞(bone mesenchymal stem cells, BMSCs)上调血管内皮生长因子(vascular endothelial growth factor, VEGF),促进血管的生成和神经功能的恢复[17]。
本实验采用线栓法模拟脑缺血/再灌注损伤,应用黄芪甲苷分别从脑梗死体积、神经细胞的形态结构等方面进行研究,观察治疗效果。结果显示,Sham组无梗死现象的发生,神经细胞结构清晰完整;I/R组损伤侧出现脑梗死,神经细胞排列紊乱、核固缩,透射电镜下细胞膜、核膜断裂溶解,核内异染色质增多;与I/R组相比,AS-Ⅳ组脑梗死体积缩小,细胞膜、核膜缺损程度降低,细胞的整体状态有所改善。本实验结果表明,黄芪甲苷可以减轻大鼠局灶性脑缺血/再灌注损伤,发挥神经保护作用。然而,目前黄芪甲苷针对脑缺血/再灌注损伤的神经保护作用的探究只是一个初步的认识,脑缺血/再灌注损伤引起的氧化应激反应、炎性因子的介入以及蛋白、基因等方面的变化,尚未进行深入的探讨。本课题组将继续深入研究黄芪甲苷对脑缺血/再灌注损伤的神经保护作用机制。
( 致谢: 本实验在河北省心脑血管病中医药防治重点实验室完成,感谢各位老师和同学的帮助!)
| [1] | Piironen K, Tiainen M, Mustanoja S, et al. Mild hypothermia after intravenous thrombolysis in patients with acute stroke: a randomized controlled trial[J]. Stroke, 2014, 45(2): 486-91. doi:10.1161/STROKEAHA.113.003180 |
| [2] | 国家药典委员会. 中华人民共和国药典(一部) [S]. 北京: 中国医药科技出版社, 2015: 302-3. Chinese pharmacopoeia commission. Pharmacopoeia of the People's Republic of China(a)[S]. Beijing: China Medical Science Press, 2015: 302-3. |
| [3] | 范丽红, 何英, 张平, 等. 黄芪注射液对大鼠早期压疮炎性因子和氧自由基的影响[J]. 解放军护理杂志, 2014, 31(15): 22-4. Fan L H, He Y, Zhang P, et al. Effect of Astragalus Injection on inflammatory factors and oxygen free radicals in rats at early stage[J]. Nursing J Chin PLA, 2014, 31(15): 22-4. |
| [4] | 张小鸿, 徐先祥, 汪宁卿. 黄芪保护血管内皮细胞作用机制研究进展[J]. 中国药学杂志, 2013, 48(18): 1526-30. Zhang X H, Xu X X, Wang N Q. Progress of study on the mechanism of Astragalus membranaceus protecting vascular endothelial cells[J]. Chin Pharm J, 2013, 48(18): 1526-30. |
| [5] | 靳晓飞, 张颖, 周晓红, 等. 黄芪甲苷对缺氧缺糖/复氧复糖PC12细胞凋亡的影响[J]. 中国药理学通报, 2016, 32(10): 1411-5. Jin X F, Zhang Y, Zhou X H, et al. Effects of astragaloside Ⅳ on apoptosis of PC12 cells induced by hypoxia/hypoglycemia and reoxygenation[J]. Chin Pharmacol Bull, 2016, 32(10): 1411-5. doi:10.3969/j.issn.1001-1978.2016.10.016 |
| [6] | Calloni R L, Winkler B C, Ricci G, et al. Transient middle cerebral artery occlusion in rats as an experimental model of brain ischemia[J]. Acta Cir Bra, 2010, 25(5): 428-33. doi:10.1590/S0102-86502010000500008 |
| [7] | Liu J R, Jensen-Kondering U R, Zhou J J, et al. Transient filament occlusion of the middle cerebral artery in rats: does the reperfusion method matter 24 hours after perfusion[J]. BMC Neurosci, 2012, 13(1): 154. doi:10.1186/1471-2202-13-154 |
| [8] | 曲友直, 赵燕玲, 李敏, 等. 黄芪甲苷对脑缺血再灌注后血脑屏障的保护作用及occludin蛋白表达的影响[J]. 卒中与神经疾病, 2010, 17(2): 92-3. Qu Y Y, Zhao Y L, Li M, et al. Protective effect of astragaloside Ⅳ on blood-brain barrier and expression of occludin protein after cerebral ischemia reperfusion[J]. Stroke Nervous Dis, 2010, 17(2): 92-3. |
| [9] | Li M, Qu Y Z, Zhao Z W, et al. Astragaloside Ⅳ protects against focal cerebral ischemia/reperfusion injury correlating to suppression of neutrophils adhesion-related molecules[J]. Neurochem Int, 2012, 60(5): 458-65. doi:10.1016/j.neuint.2012.01.026 |
| [10] | Lewen A, Matz P, Chan P H. Free radical pathways in CNS injury[J]. J Neurotrauma, 2000, 17(10): 871-90. doi:10.1089/neu.2000.17.871 |
| [11] | 叶冬青, 高维娟, 钱涛, 等. 黄芪注射液抑制缺氧缺糖/复氧复糖大鼠海马神经元JNK3的表达[J]. 中国药理学通报, 2010, 26(1): 77-82. Ye D Q, Gao W J, Qian T, et al. Astragalus injection inhibits the expression of JNK3 after hypoxia /hypoglycemia and reoxygenation in hippocampal neurons of rats[J]. Chin Pharmacol Bull, 2010, 26(1): 77-82. |
| [12] | 刘珂, 邱炳勋, 邹利, 等. 黄芪及其有效成分对内皮细胞及其连接的保护作用及机制研究进展[J]. 中草药, 2016, 47(21): 3912-7. Liu K, Qiu B X, Zou L, et al. Research progress in mechanism of Astragali Radix and its active components on endothelial cells and their junction[J]. Chin Tradit Herb Drugs, 2016, 47(21): 3912-7. |
| [13] | 张蔷, 高文远, 满淑丽. 黄芪中有效成分药理活性的研究进展[J]. 中国中药杂志, 2012, 37(21): 3203-7. Zhang Q, Gao W Y, Man S L. Chemical composition and pharmacological activities of Astragali Radix[J]. China J Chin Mater Med, 2012, 37(21): 3203-7. |
| [14] | Qu Y Z, Li M, Zhao Y L, et al. Astragaloside Ⅳ attenuates cerebral ischemia-reperfusion-induced increase in permeability of the blood-brain barrier in rats[J]. Eur J Pharmacol, 2009, 606(1-3): 137-41. doi:10.1016/j.ejphar.2009.01.022 |
| [15] | Jia Y, Zuo D, Li Z, et al. Astragaloside Ⅳ inhibits doxorubicin-induced cardiomyocyte apoptosis mediated by mitochondrial apoptotic pathway via activating the PI3K/Akt pathway[J]. Chem Pharm Bull (Tokyo), 2014, 62(1): 45-53. doi:10.1248/cpb.c13-00556 |
| [16] | Li H B, Ge Y K, Zhang L, et al. Astragaloside Ⅳ improved barrier dysfunction induced by acute high glucose in human umbilical vein endothelial cells[J]. Life Sci, 2006, 79(12): 1186-93. doi:10.1016/j.lfs.2006.03.041 |
| [17] | 王莹, 李文媛, 李明秋, 等. 黄芪皂甙Ⅳ联合骨髓间充质干细胞对脑缺血再灌注大鼠血管生成的影响[J]. 解剖学研究, 2011, 33(5): 323-6. Wang Y, Li W Y, Li M Q, et al. Effects of astragaloside Ⅳ combined with bone mesenchymal stem cell transplantation on angiogenesis after cerebral ischemia-reperfusion in rats[J]. Anatomy Res, 2011, 33(5): 323-6. |

