

2. 山东省肿瘤防治研究院,山东 济南 250117;
3. 山东中医药大学临床医学院,山东 济南 250011
2. Shandong Province Tumor Prevention &Treatment Institution, Jinan 250117, China;
3. School of Medicine, Shandong University of Traditional Chinese Medicine, Jinan 250011, China
糖尿病(diabetes melitus,DM)是由遗传和环境因素使胰岛素分泌不足或胰岛素抵抗而引起的,以血糖升高为特征,严重危害人类健康的慢性代谢综合征[1]。其中,2型糖尿病(T2DM)的特点是高糖血症和高胰岛素血症,其发病率约占糖尿病总数的90%以上。全球共有4.15亿成年人患有糖尿病,即每11个成人中便有1人患有糖尿病[2]。糖尿病患者约2/3死于心脏病和脑中风,其风险比正常人群高2~4倍[1]。其中糖尿病心肌病(diabetic cardiomyopathy, DCM)是糖尿病患者的主要心脏并发症之一,也是糖尿病患者发生心力衰竭的重要原因。糖尿病心肌病的病理改变主要表现为心肌肥厚、心肌细胞凋亡和心肌间质纤维化。
丹酚酸B(salvianolic acid B, Sal B)是从丹参中提取出的药用水溶性成分,现广泛应用于心脑血管疾病[3-5]。文献报道,Sal B能够抑制AngⅡ诱导的心肌细胞肥大[6],降低db/db小鼠的血糖水平[7],但Sal B能否改善糖尿病小鼠心肌肥厚,尚未见报道。过氧化物酶体增殖物激活受体α (peroxisome proliferator-activated receptor α,PPARα)广泛分布于心肌细胞,是生理情况下心肌细胞脂质代谢和能量代谢重要的调控枢纽,参与了糖尿病心肌肥厚的演变过程[8-9]。本研究拟从动物及细胞水平研究Sal B对T2DM模型小鼠心肌肥厚的影响,并从PPARα角度探讨其机制。
1 材料 1.1 实验动物SD大鼠,1~3 d龄,清洁级;C57BL/6J小鼠,5周龄,清洁级。以上动物均由山东大学医学院实验动物中心提供,实验动物许可证号:SCXK(鲁) 2013 0009。
1.2 试剂丹酚酸B购于上海Tauto Biotech公司,HPLC分析示纯度超过98%。DMEM培养基、HBSS(无钙镁)购于美国Gibco公司;Ⅱ型胶原酶购自美国Worthington公司;普通饲料及高脂饲料购于北京华阜康公司;罗氏活力型血糖仪及试纸条购自美国罗氏公司;链脲佐菌素(STZ)、DMSO购于美国Sigma-Aldrich公司;MK-886购自美国Abcam公司;3H-亮氨酸、3H-D-葡萄糖购自美国Perkin Elmer公司;PPARα抗体(货号ab8934)购自美国Abcam公司;GAPDH抗体(货号G9545)购自美国Sigma-Aldrich公司;BCA试剂盒、LDH试剂盒购于碧云天公司。
1.3 仪器石蜡切片机,购自德国Leica公司;Image Proplus 6.0 software购自美国MediaCybernetics公司;生物安全柜、细胞培养箱购自美国Thermo公司;液体闪烁计数仪购自上海核所日环光电仪器有限公司;正置荧光显微镜(Eclipse Ti)购自日本尼康公司;离心机购自德国Eppendorf公司;发光仪及电泳仪购自美国Bio-Rad公司。
2 方法 2.1 动物模型的建立及分组采用高脂饮食喂养联合STZ腹腔注射的方法诱导小鼠产生T2DM表现。适应性饲养1周后,选取110只5周龄的C57BL/6J小鼠,随机分为2组:正常饲养组40只、T2DM造模组70只。正常饲养组采用普通饲料(质量比g%:4.3%脂肪,67.3%碳水化合物以及19.2%蛋白质)喂养4周;T2DM造模组采用高脂饲料(质量比g%:24%脂肪,41%碳水化合物以及24%蛋白质)喂养4周。4周后禁食不禁水12 h,一次性腹腔注射40 mg·kg-1 STZ(溶于0.1 mmol·L-1柠檬酸缓冲液中,pH 4.4,冰浴,现配现用,5 min内用完),继续高脂饲养;正常组注射等体积的柠檬酸缓冲液,继续正常饮食饲养。注射STZ后d 3、7尾静脉采血检测血糖,血糖值连续2次大于11.1 mmol·L-1视为T2DM造模成功。如血糖不合格则再次注射STZ。将存活的正常饲养组小鼠随机分为2组:对照组(18只)、丹酚酸B组(17只);将存活的、成模的T2DM小鼠随机分为2组:T2DM模型组(20只)、T2DM+丹酚酸B组(17只)。之后T2DM+Sal B组和Sal B组采用Sal B 100 mg·kg-1·d-1灌胃8周,对照组及T2DM组使用生理盐水灌胃8周。
2.2 取材称取小鼠体重,0.8%戊巴比妥钠(70 mg·kg-1)腹腔注射麻醉后,仰卧位固定,打开胸腔,将针头插入左心室,生理盐水灌注至肝脏颜色发白,取下心脏称重。取出小鼠胫骨,用游标卡尺测其长度,计算心脏重量(mg)与胫骨长度(mm)的比例。
2.3 石蜡切片麦胚凝集素(WGA)染色心肌组织甲醛固定后脱水,石蜡包埋,0.5 μm切片,脱蜡至水,微波抗原修复15 min,PBS冲洗15 min(每次5 min),滴加5 mg·L-1 WGA染液,置于暗盒内并4℃过夜,d 2冲洗后,抗荧光淬灭封片剂封片,正置荧光显微镜拍片。每组随机选取6只小鼠的心脏,每个心脏选取相同位置的3张切片,每个切片选取6个视野拍照,照片使用Image Proplus 6.0图形分析系统,计算心肌细胞横截面面积。
2.4 乳大鼠心肌细胞的提取及分组该细胞的提取及培养参考文献[10]进行。实验中,使用25.5 mmol·L-1葡萄糖联合0.1 μmol·L-1胰岛素(high glucose and insulin, HGI)诱导乳大鼠心肌细胞的肥大生长。各个实验的具体分组及刺激方法详见图表的图注。
2.5 心肌细胞表面积的测量乳大鼠心肌细胞表面积通过α-辅肌动蛋白(α-actinin)免疫荧光染色测定,基本步骤参考文献[10]。每组细胞随机选择8个视野拍照,使用Image Proplus 6.0 software测量细胞表面积。
2.6 3H-亮氨酸参入率测定采用24孔板培养,以1×105个细胞/孔的密度铺板,心肌细胞贴壁后换液,再培养24 h后无血清饥饿过夜,换用含有相应刺激的无血清培养基继续培养48 h,3H-亮氨酸在细胞培养液中终浓度为1 mCi·L-1。样品制备及检测参考文献[10]。结果以每分钟计数(counts per minute, cpm)表示,参入量反映心肌细胞的蛋白合成速率。
2.7 3H-D-葡萄糖参入率采用3H-D-葡萄糖参入实验评价心肌细胞胰岛素敏感性。培养采用24孔板,以1×105个细胞/孔的密度铺板,心肌细胞贴壁后换液,再培养24 h后无血清饥饿过夜,换用含有相应刺激的培养基,经37℃、5% CO2培养箱中孵育48 h后,加入3H-D-葡萄糖(1.3 mCi·L-1)继续孵育1 h。PBS冰上快速冲洗细胞3次,0.5 mol·L-1 NaOH于37℃裂解细胞30 min,然后加入等体积0.5 mol·L-1 HCl中和。使用BCA测定蛋白浓度。闪烁瓶中加入5 mL闪烁液及细胞裂解物,摇匀,使用液体闪烁计数仪检测。结果以每分钟计数/mg蛋白(CPM·mg-1),反映心肌细胞的3H-D-葡萄糖参入率。然后转换成比值。
2.8 乳酸脱氢酶(LDH)活性检测培养采用24孔板,以1×105个细胞/孔的密度铺板,心肌细胞贴壁后换液,再培养24 h后饥饿过夜,换用含药培养基孵育48 h,将上清吸出。96孔板中每孔加入100 μL上清,然后再加入100 μL LDH试剂,避光室温放置30 min。酶标仪下,490 nm波长处读取吸光度值。
2.9 Western blot检测蛋白的表达Western blot实验所用乳大鼠心肌细胞培养采用6孔板,以5×105个细胞/孔的密度铺板,心肌细胞贴壁后换液,再培养24 h后无血清饥饿过夜,换用含有相应刺激的培养基,经37℃、5% CO2培养箱中孵育48 h。提取乳大鼠心肌细胞或小鼠心脏组织蛋白,BCA试剂盒检测蛋白浓度,加入含有β-巯基乙醇的上样缓冲液,金属浴95℃10 min, 使蛋白变性,-80℃保存。采用SDS-聚丙烯酰胺凝胶电泳法进行电泳,PVDF转膜,5%脱脂牛奶室温封闭1 h, 加入一抗稀释液配置的一抗(GAPDH 1:2 000稀释,PPARα 1:1 000稀释)。摇床4℃封闭过夜,d 2洗膜后加入辣根过氧化物酶标记的二抗(1:30 000稀释)室温孵育1 h,ECL发光液(1:1等比例避光配置,现用现配)显色,Image J图像分析系统对条带进行分析。每组重复3次。
2.10 统计学处理使用SPSS 17.0软件进行数据的处理与分析,以x±s的形式来反映具体数值,多组间数据比较采用单因素方差分析法(one-way ANOVA),组间两两比较采用LSD检验。
3 结果 3.1 丹酚酸B对T2DM模型小鼠心肌肥厚的影响心脏重量/胫骨长度比例、心肌细胞横截面积能够反映小鼠的心肌肥厚程度。如Fig 1所示,与对照组相比,T2DM组小鼠心脏重量与胫骨长度(HW/Tibial length)比值、心肌细胞横截面积明显升高(P<0.01);T2DM+Sal B组该比值明显低于T2DM组(P<0.05);Sal B组与对照组相比差异无统计学意义(P>0.05)。提示糖尿病状态使小鼠产生心肌肥厚,丹酚酸B能够改善T2DM小鼠的心肌肥厚。

|
| Fig 1 Effect of Sal B on heart weight/tibial length(A) and myocardial cross-sectional area(B) in mice with type 2 diabetes melitus **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs T2DM group |
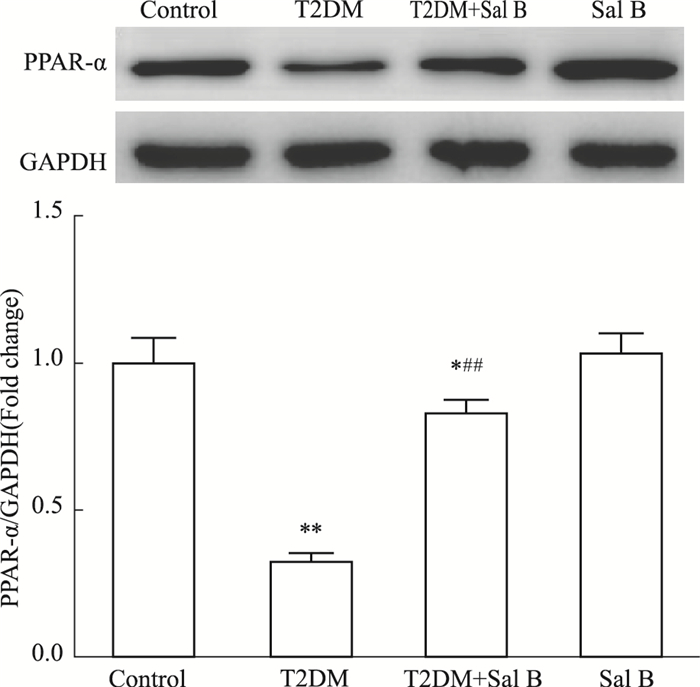
如Fig 2所示,T2DM组PPARα表达水平较对照组明显下降(P<0.01),T2DM+Sal B组PPARα表达较T2DM组上升(P<0.01)。提示丹酚酸B能够改善T2DM引起的小鼠心肌组织PPARα的表达降低。
|
| Fig 2 Effect of Sal B on protein level of PPARα in hearts of mice with type 2 diabetes melitus *P < 0.05, **P < 0.01 vs control group; ##P < 0.01 vs T2DM group |
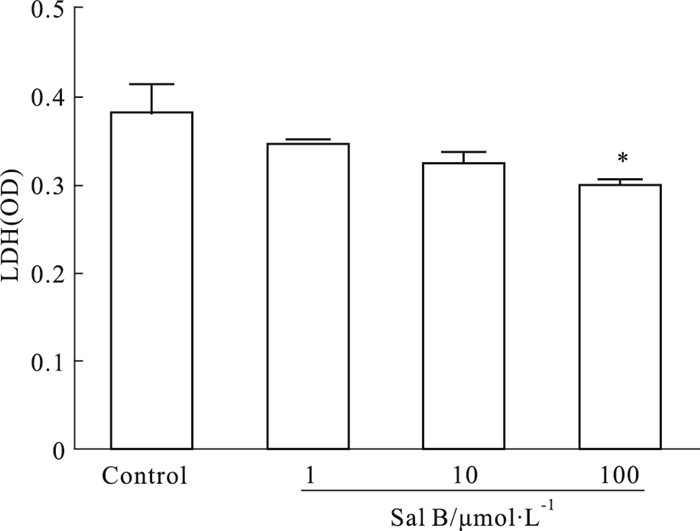
如Fig 3所示,相对于对照组,1~10 μmol·L-1的Sal B没有增加乳大鼠心肌细胞的死亡,100 μmol·L-1的Sal B还能降低无血清培养造成的乳大鼠心肌细胞的死亡(P<0.05)。
|
| Fig 3 Effect of Sal B on viability of NRCMs Neonatal rat cardiomyocytes(NRCMs) were treated with Sal B(1~100 μmol·L-1) for 48 h, then LDH level of the supernatant was measured. *P < 0.05 vs control group. |
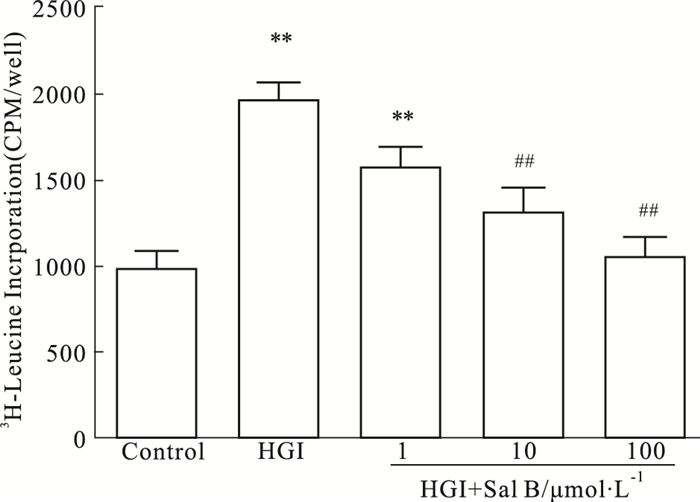
3H-亮氨酸参入率能够反映心肌细胞的蛋白质合成速率,和心肌细胞表面积都是检测心肌细胞肥大的常用指标。Fig 4显示,HGI作用48 h后,心肌细胞3H-亮氨酸参入率明显高于control组(P<0.01)。Sal B干预后,3H-亮氨酸参入率出现不同程度下降,以Sal B 100 μmol·L-1降低最为明显(与HGI组相比P<0.01)。
|
| Fig 4 Effect of Sal B on cardiomyocyte hypertrophy induced by high glucose and high insulin NRCMs were treated with glucose(25.5 mmol·L-1), insulin(0.1 μmol·L-1)and Sal B(1~100 μmol·L-1) for 48 h, then 3H-leucine incorporation of cells was measured. **P < 0.01 vs control group; ##P < 0.01 vs HGI group. |
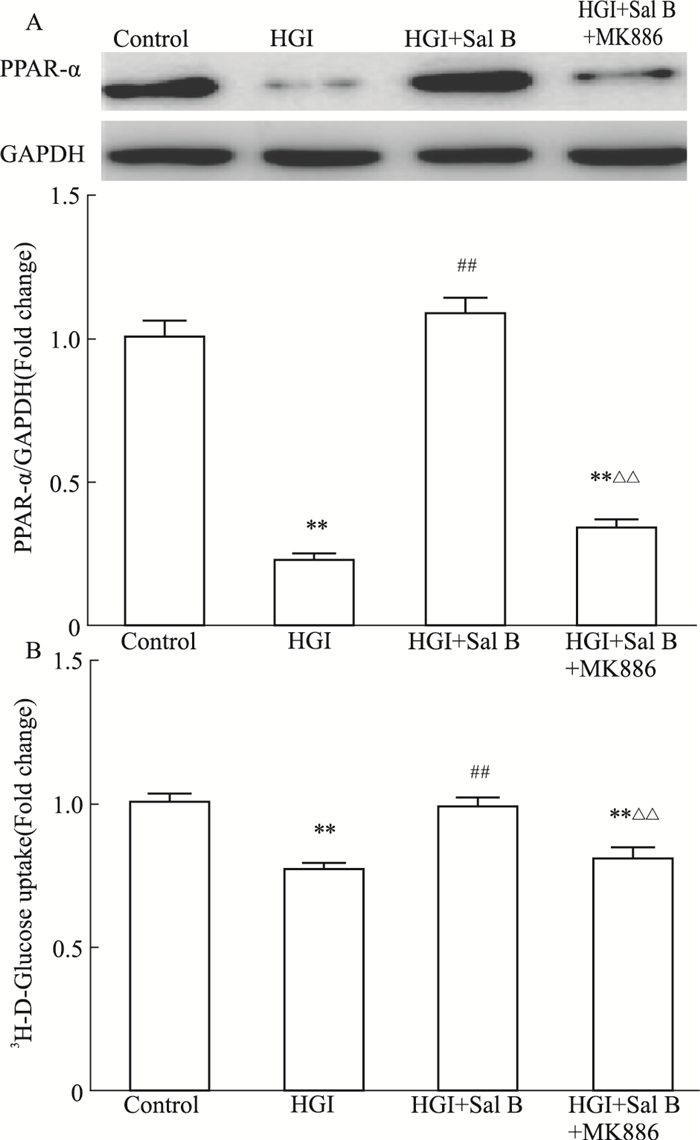
如Fig 5A所示,HGI组PPARα的表达与对照组相比明显下降(P<0.01),Sal B(100 μmol·L-1)能够改善HGI引起的PPARα表达水平下降(P<0.01)。PPARα抑制剂MK886(50 μmol·L-1)干预后,HGI+Sal B+ MK886组PPARα表达较HGI+Sal B组明显下降(P<0.01)。胰岛素抵抗能引起细胞的3H-D-葡萄糖参入率下降。如Fig 5B所示,干预48 h后,HGI组心肌细胞3H-D-葡萄糖参入率与control组相比明显下降(P<0.01);加入100 μmol·L-1 Sal B后,HGI+Sal B组3H-D-葡萄糖参入率较HGI组明显上升(P<0.01);而PPARα抑制剂MK886能够使SalB的上述效应降低(P<0.01)。可见,Sal B能够改善高糖、高胰岛素诱导的乳大鼠心肌细胞胰岛素抵抗状态,其作用是通过激动PPARα发挥的。
|
| Fig 5 Effect of Sal B and MK886 on PPARα expression(A) and 3H-D-glucose incorporation (B) induced by HGI in cardiomyocytes NRCMs were treated with glucose(25.5 mmol·L-1), insulin(0.1 μmol·L-1), Sal B(100 μmol·L-1) and MK886(50 μmol·L-1) for 48 h, then PPARα level and 3H-D-glucose incorporation of cells were measured. **P < 0.01 vs control group; ##P < 0.01 vs HGI group; △△P < 0.01 vs HGI+Sal B group. |
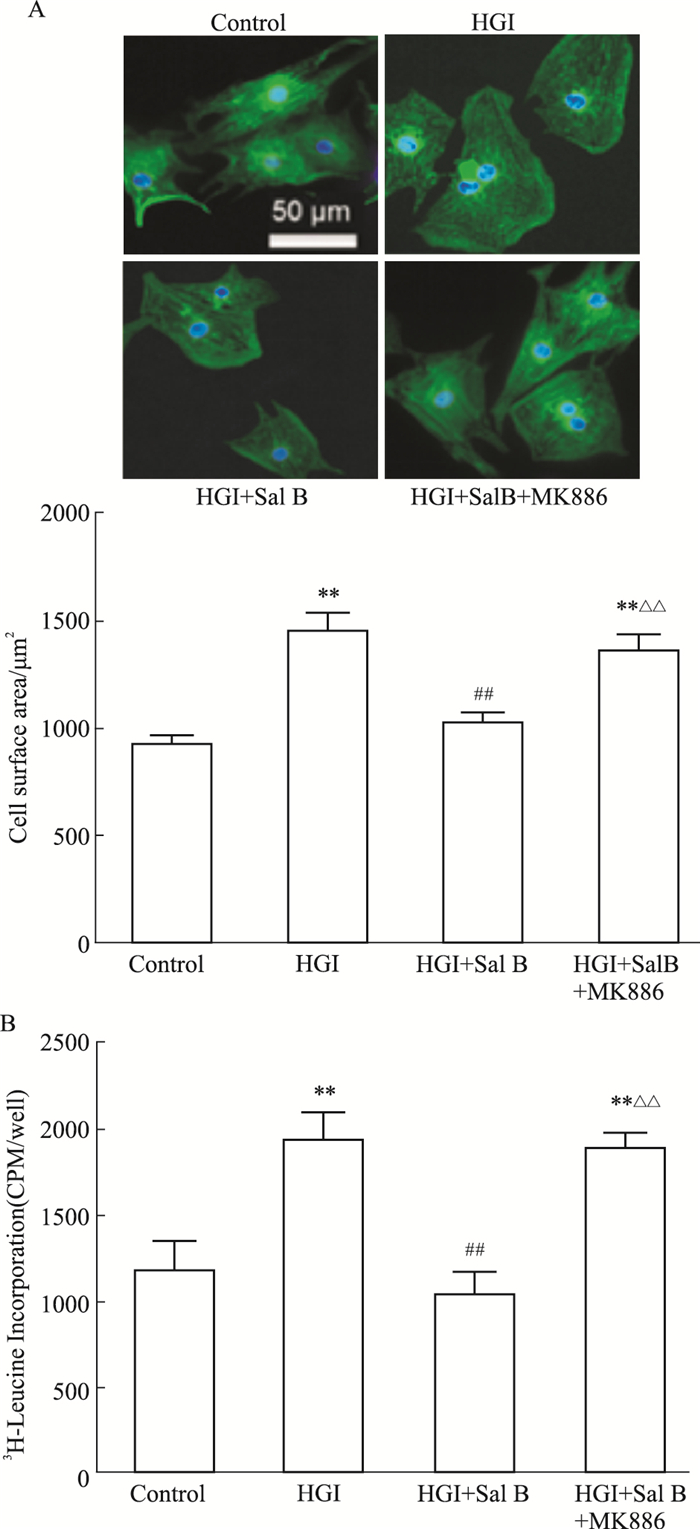
如Fig 6所示,与control组相比,HGI组心肌细胞表面积及亮氨酸参入率明显增加(P<0.01);Sal B(100 μmol·L-1)刺激后,HGI+Sal B组心肌细胞面积及亮氨酸参入率较HGI组相比明显减少(P<0.01);而HGI+Sal B+MK886组心肌细胞面积及亮氨酸参入率明显高于HGI+Sal B组(P<0.01)。说明Sal B可以抑制HGI引起的心肌细胞肥大,而这种作用可被PPARα抑制剂MK886所逆转。
|
| Fig 6 Effect of Sal B and MK886 on cardiomyocyte hypertrophy induced by insulin resistance A: Cell surface area; B: 3H-leucine incorporation. NRCMs were treated with glucose(25.5 mmol·L-1), insulin(0.1 μmol·L-1), Sal B(100 μmol·L-1) and MK886(50 μmol·L-1) for 48 h, then cell surface area and 3H-leucine incorporation were measured. **P < 0.01 vs control group; ##P < 0.01 vs HGI group; △△P < 0.01 vs HGI+Sal B group. |
DCM是T2DM患者常见的心血管系统并发症,以心室肥厚、顺应性降低、峰充盈率减少为主要特点。其中,心肌肥厚是DCM关键的结构改变之一,也是造成病人死亡的病理基础。研究证明,高糖和高胰岛素均可独立参与T2DM患者糖尿病心肌肥厚的形成。此外,T2DM患者多伴有胰岛素抵抗(insulin resistance, IR),IR是引起糖脂代谢紊乱的重要因素,也是T2DM的核心病机[11-12]。
在高脂饮食喂养诱导的肥胖小鼠模型中,Sal B能够抑制PPARγ的表达水平,减轻胰岛素抵抗,调节脂质代谢,减轻小鼠体重[13]。但对糖尿病引起的心肌肥大尚无明确报道。本研究动物实验显示,Sal B能够明显缩小T2DM小鼠心肌细胞横截面面积,降低心脏重量/胫骨长度比值,改善T2DM小鼠的心肌肥厚。在HGI诱导的乳鼠心肌细胞肥大中,Sal B的应用逆转了HGI诱导下3H-D-葡萄糖参入率和3H-亮氨酸参入率的变化,提示Sal B能够改善HGI诱导的心肌细胞胰岛素抵抗和肥大生长。
PPARα是过氧化物酶受体增殖物激活受体(PPARs)成员,也是二型核受体超家族的成员,属于配体激活的核转录因子, 与糖尿病心肌肥厚的发生密切相关[8-9]。本研究中,小鼠心肌组织Western blot结果证实了糖尿病状态下PPARα表达下降,而Sal B的应用使PPARα表达上调,乳大鼠心肌细胞实验结果进一步验证了此结论。我们使用PPARα抑制剂MK886后发现,Sal B改善心肌细胞肥大的作用可被MK886所消除,3H-亮氨酸参入率上升,这表明Sal B对心肌细胞肥大的保护作用与PPARα具有相关性。
综上所述,Sal B能有效改善T2DM模型小鼠的心肌肥厚,其机制可能是通过激活PPARα发挥的。
( 致谢: 实验在山东大学齐鲁医院细胞治疗研究中心完成,感谢实验室老师们的无私帮助!)
| [1] | Deshpande A D, Harris-Hayes M, Schootman M. Epidemiology of diabetes and diabetes-related complications[J]. Phys Ther, 2008, 88(11): 1254-64. doi:10.2522/ptj.20080020 |
| [2] | International Diabetes Federation. IDF Diabetes Atlas. 7th Edition, 2015. Available at http://www.idf.org/. |
| [3] | Lin C, Liu Z, Lu Y, et al. Cardioprotective effect of Salvianolic acid B on acute myocardial infarction by promoting autophagy and neovascularization and inhibiting apoptosis[J]. J Pharm Pharmacol, 2016, 68(7): 941-52. doi:10.1111/jphp.12567 |
| [4] | 陈俞材, 方莲花, 杜冠华. 丹参水溶性化合物抗心肌缺血作用的研究进展[J]. 中国药理学通报, 2015, 31(2): 162-5. Chen Y C, Fang L H, Du G H. Research advances in protective effects of water soluble compounds in alvia miltiorrhiza gainst myocardial ischemia[J]. Chin Pharmacol Bull, 2015, 31(2): 162-5. |
| [5] | 崔国祯, 徐燕玲, 孙安露, 等. 丹参素衍生物对斑马鱼促血管新生作用的研究[J]. 中国药理学通报, 2016, 32(6): 795-800. Cui G Z, Xu Y L, Sun A L, et al. Effect of Danshensu derivative on angiogenesis in zebrafish[J]. Chin Pharmacol Bull, 2016, 32(6): 795-800. |
| [6] | Liu M, Ye J, Gao S, et al. Salvianolic acid B protects cardiomyocytes from angiotensin Ⅱ-induced hypertrophy via inhibition of PARP-1[J]. Biochem Biophys Res Commun, 2014, 444(3): 346-53. doi:10.1016/j.bbrc.2014.01.045 |
| [7] | Huang M Q, Zhou C J, Zhang Y P, et al. Salvianolic acid B ameliorates hyperglycemia and dyslipidemia in db/db mice through the AMPK pathway[J]. CeL Physiol Biochem, 2016, 40(5): 933-43. doi:10.1159/000453151 |
| [8] | Dobrin J S, Lebeche D. Diabetic cardiomyopathy: signaling defects and therapeutic approaches[J]. Expert Rev Cardiovasc Ther, 2010, 8(3): 373-91. doi:10.1586/erc.10.17 |
| [9] | Liu F, Song R, Feng Y, et al. Upregulation of MG53 induces diabetic cardiomyopathy through transcriptional activation of peroxisome proliferation-activated receptor α[J]. Circulation, 2015, 131(9): 795-804. doi:10.1161/CIRCULATIONAHA.114.012285 |
| [10] | Lyu L, Wang H, Li B, et al. A critical role of cardiac fibroblast-derived exosomes in activating renin angiotensin system in cardiomyocytes[J]. J Mol Cell Cardiol, 2015, 89(Pt B): 268-79. |
| [11] | Peng X, Chen R, Wu Y, et al. PPARgamma-PI3K/AKT-NO signal pathway is involved in cardiomyocyte hypertrophy induced by high glucose and insulin[J]. J Diabetes Complications, 2015, 29(6): 755-60. doi:10.1016/j.jdiacomp.2015.04.012 |
| [12] | 吴文君, 汤孙寅炎, 时俊锋, 等. 二甲双胍抑制SREBP-1c改善高脂诱导的骨骼肌胰岛素抵抗[J]. 中国药理学通报, 2016, 32(1): 55-9. Wu W J, Tang-Sun Y Y, Shi J F, et al. Metformin ameliorates PA-induced skeletal muscle insulin resistance by suppressing SREBP-1c[J]. Chin Pharmacol Bull, 2016, 32(1): 55-9. |
| [13] | Wang P, Xu S, Li W, et al. Salvianolic acid B inhibited PPARγ expression and attenuated weight gain in mice with high-fat diet-induced obesity[J]. CeL Physiol Biochem, 2014, 34(2): 288-98. doi:10.1159/000362999 |

