

2. 重庆市南岸区妇幼保健计划生育服务中心药剂科,重庆 400060
2. Dept of Pharmacy, Chongqing Nanan Maternal and Child Health Care and Family Planning Service Center, Chongqing 400060, China
吴茱萸是芸香科植物,具有镇痛、抗炎等作用[1]。吴茱萸碱(evodiamine,ED)是吴茱萸的一种重要生物碱,近年来研究表明,它除了与吴茱萸有相同的作用外,在抑制肿瘤细胞的生长和诱导肿瘤细胞的凋亡等方面也具有突出作用[2-6],作用范围广泛,且具有一定研究开发价值。但由于ED水溶性弱,导致口服吸收差,为此改善其口服吸收,以便更好地发挥其抗肿瘤等作用尤其重要。近年来,微乳液递送系统以其能提高药物的溶解度、改善药物吸收和生物利用度等作用而成为研究热点[7]。ED的微乳液递送技术研究甚少,故本实验将ED制备成吴茱萸碱微乳液(evodiamine microemulsion,EDM),考察其在体外的释放特征,并研究其在大鼠的胃、十二指肠、空肠、回肠和结肠等部位的吸收情况,该实验用HPLC法测定其含量。
1 材料 1.1 动物SD大鼠,♂,体质量(230±20) g,由重庆医科大学实验动物中心提供,许可证号:SCXK-(渝)2012-0001。
1.2 试剂与仪器ED (武汉远城科技发展有限公司,纯度>99%); 油酸乙酯(上海化学试剂二厂,分析纯); 聚氧乙烯蓖麻油(德国BASF公司); 聚乙二醇400(天津精细化工有限公司,分析纯); Krebs-Ringer液(实验室自制,批号:20121113);甲醇(美国新天地科技有限公司,色谱纯); 水为纯化水; 其余试剂为分析纯。1100型高效液相色谱仪(美国Agilent公司)。
2 方法 2.1 EDM的制备称取处方量的ED、油酸乙酯、聚氧乙烯蓖麻油以及聚乙二醇400,磁力搅拌后冷却到室温,滴加处方量的纯化水,搅拌至澄清,即得EDM,测得其平均粒径为26 nm,平均Zeta电位为-15 mV。
2.2 样品的分析 2.2.1 色谱条件色谱柱为Lichrospher C18(250 mm×4.6 mm,5 μm),柱温35℃,检测波长225 nm,流动相为甲醇:水=75 :25,流速1.0 mL·min-1,进样量20 μL。
2.2.2 样品处理将样品液和甲醇以一定体积比混合,涡旋2 min,再于12 000 r·min-1离心10 min,取上清液,即得样品。
2.3 EDM的体外释放动力学将处理好的透析袋的一端结扎,精密量取1.0 mL ED或EDM置透析袋中,紧紧将另一端结扎。将此透析袋浸没到50 mL pH 1.2盐酸溶液和pH 6.8磷酸缓冲液的透析液中,于37℃、100 r·min-1水浴条件下恒温振荡,在不同的时间点取样。考察ED或EDM在pH 1.2盐酸溶液或pH 6.8磷酸缓冲液中的释放行为,于“2.2”项下色谱条件测得含量,对ED和EDM的释放情况作相对因子计算[8],计算其累积释放率,并对其累积释放率和时间进行零级方程、一级方程、Higuchi方程、Hixcon-Crowell方程、Ritger-peppas方程、Weibull方程拟合分析。
2.4 EDM的大鼠胃肠吸收研究 2.4.1 主要溶液配制Krebs-Ringer液参照文献[10]配制方法配制; ED循环液:精密称取10 mg ED,用Krebs-Ringer液稀释并定容至100 mL,即配制成的ED循环液(100 mg·L-1)。同理配制EDM循环液(100 mg·L-1)。
2.4.2 大鼠胃肠吸收实验实验前将6只大鼠随机分成2组,并给予大鼠禁食18 h,不禁水的处理,分别研究ED或EDM在大鼠胃肠的吸收情况。实验时用3.5%的水合氯醛麻醉大鼠,沿腹中线打开腹腔,找到胃并排除内容物后,灌入4 mL ED或EDM,2 h后取出药液并定容至刻度; 然后分别在十二指肠、空肠、回肠、结肠等4段形成回路,除净肠内容物后用Krebs-Ringer液循环,再通入ED或EDM,1 h后取出药液并定容至刻度,得样品,-20℃保存[9-10]。用HPLC测得ED的含量后,计算ED或EDM的吸收速率常数(absorption rate constant,Ka),根据实验后剪下的各肠段的内径和长度,计算二者的有效渗透率(effective permeability,Peff)[11]。
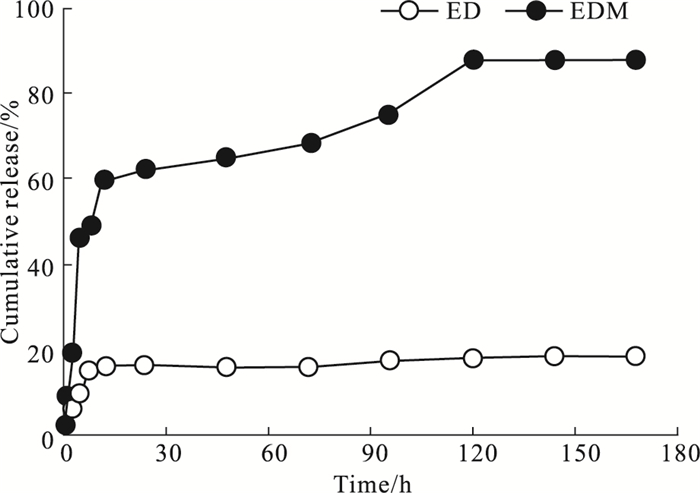
3 结果 3.1 EDM的体外释放动力学根据实验结果,计算得出ED与EDM在pH 1.2盐酸溶液中的相对因子为20.80,在pH 6.8磷酸缓冲液中的18.59,说明二者的释放行为不相似。ED和EDM在pH 1.2盐酸溶液中的释放情况如Fig 1所示,累积释放率分别为(13.98±0.49)%、(64.76±0.73)%,EDM的累积释放率为ED的4.63倍; 在pH 6.8磷酸缓冲液中的释放情况如Fig 2所示,累积释放率分别为(18.34±0.20)%、(91.72±0.51)%,EDM的累积释放率为ED的5.01倍。在pH 1.2盐酸溶液和pH 6.8磷酸缓冲液中,EDM在0~12 h时,累积释放速率一直处于增长状态,于12 h后,累积释放速率开始变缓; 而ED在0~5 h时均处于增长状态,其后一直处于平稳状态。表明将ED制备成EDM后,达到最大累积释放速率的时间相对延长,并且体外释放量明显增加。

|
| Fig 1 Drug release curves of ED and EDM in pH 1.2 HCl dissolution media (x±s, n=3) |
|
| Fig 2 Drug release curves of ED and EDM in pH 6.8 PBS dissolution media (x±s, n=3) |
EDM的累积释放率和时间的各方程拟合情况见Tab 1、2,EDM在pH 1.2盐酸溶液和pH 6.8磷酸缓冲液中的释放与各方程的拟合度均大于0.700,说明拟合效果较好; 在两溶液中的释放与Weibull方程拟合度最高,说明EDM在两溶液中的释放与Weibull方程最符合。
| Fitting models | pH 1.2 HCl dissolution media | |
| Equations | Degrees of fitting | |
| Zero-order equation | Q=0.257t +31.400 | 0.729 |
| First-order equation | ln(1-Q)=-0.004t-0.409 | 0.806 |
| Higuchi equation | lnQ=4.022t1/2+21.150 | 0.840 |
| Hixcon-Crowell equation | (100-Q)1/3 = -0.005t +4.063 | 0.781 |
| Ritger-peppas equation | InQ=0.453lnt +2. 237 | 0.848 |
| Weibull equation | lnln[1/1-Q]=0.533lnt+2.289 | 0.878 |
| Fitting models | pH 6.8 PBS dissolution media | |
| Equations | Degrees of fitting | |
| Zero-order equation | Q=0.400t+33.750 | 0.823 |
| First-order equation | ln(1-Q)=-0.011t-0.410 | 0.940 |
| Higuchi equation | lnQ=5.991t1/2+19.440 | 0.906 |
| Hixcon-Crowell equation | (100-Q)1/3=-0.012t+4.035 | 0.911 |
| Ritger-peppas equation | lnQ=0.479lnt+2.336 | 0.902 |
| Weibull equation | lnln[1/1-Q]=0.627lnt+2.239 | 0.942 |
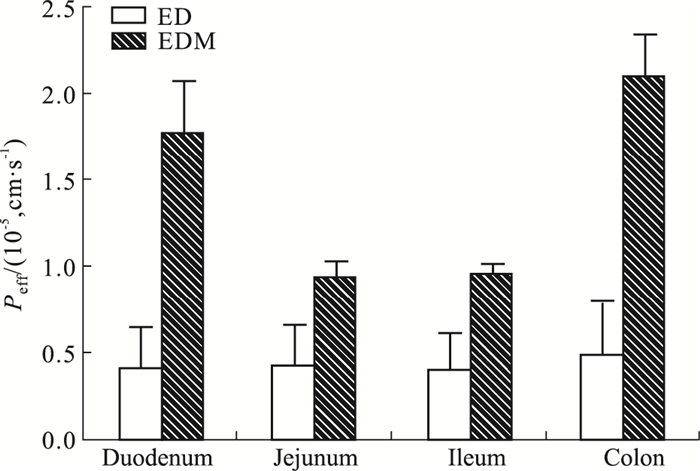
通过实验数据得到ED和EDM在各部位的Ka (Fig 3)和Peff(Fig 4),可得出结果:EDM在十二指肠、空肠、回肠、结肠、胃的Ka分别是ED的2.86、2.66、3.06、4.55、2.62倍,在十二指肠、空肠、回肠、结肠的Peff分别是ED的4.27、2.21、2.38、4.30倍,即EDM在各部位的Ka和Peff均为ED的2倍以上,说明EDM在各部位的吸收远远高于ED,EDM能明显提高ED在大鼠胃肠中的吸收; 且各肠段的Ka均为胃的3倍以上,说明ED在肠段中的吸收远远多于其在胃中吸收。

|
| Fig 3 Absorption rate constant of ED and EDM (x±s, n=3) |
|
| Fig 4 Effective permeability of ED and EDM (x±s, n=3) |
ED作为一种可抗肿瘤的药物被广为使用,但由于存在水溶性差、口服吸收弱等问题,导致生物利用度低,因此提高其口服吸收很有必要。近期研究发现,新兴的微乳液递送系统稳定性好,能有效提高药物的吸收和生物利用度[12-14],在食品、医药和化妆品上都有所应用。但关于ED的微乳液递送系统研究不多,故本实验将ED制备成EDM,研究其体外释放特征和在胃肠吸收情况。
在体外释放研究中,ED与EDM的相对因子均远远小于50,说明了ED与EDM体外释放特征不相似; EDM的体外累积释放率高于ED,在pH 1.2盐酸溶液中增加了3.63倍,在pH 6.8磷酸缓冲液中增加了4.01倍; 且EDM达到最大释放量的时间与ED相比,延长了5 h。说明EDM不仅大大提高了ED的体外释放量,还实现了缓释,延长了作用时间。
在体吸收实验中,EDM与ED相比,胃肠道吸收量明显增长了1倍以上,可能是微乳液递送系统提高了ED与胃肠道的亲和力,提高了ED在胃肠道中的溶解度,促进了胃肠道吸收[7, 14]。综上表明微乳液递送系统不仅延缓了ED吸收,延长其作用时间,也提高了其胃肠吸收,对于改善其口服生物利用度低等问题提供了参考依据。
( 致谢: 本实验在重庆医科大学药学院药物高校工程研究中心完成,真诚感谢实验室的所有老师和同学。)
| [1] | 杨志欣, 孟永海, 王秋红, 等. 吴茱萸药理作用及其物质基础研究概况[J]. 中华中医药学刊, 2011, 29(11): 2415-7. Yang Z X, Meng Y H, Wang Q H, et al. Study of the pharmacological effects and material basis of fructus evodiae[J]. Chin Arch Tradit Chin Med, 2011, 29(11): 2415-7. |
| [2] | Yu H, Jin H W, Gong W Z, et al. Pharmacological actions of multi-target-directed evodiamine[J]. Molecules, 2013, 18(2): 1823-43. |
| [3] | 尹作静, 曹志伟, 闫鑫淼, 等. 黄连素和吴茱萸碱协同抗癌的miRNA网络机制研究[J]. 中国药理学通报, 2017, 33(6): 772-80. Yin Z J, Cao Z W, Yan X M, et al. Study of synergistic mechanism in the combination of berberine and evodiamine from the perspective of miRNA[J]. Chin Pharmacol Bull, 2017, 33(6): 772-80. |
| [4] | 赵绿翠, 廖科, 李科琼, 等. 吴茱萸碱调控人结肠癌HCT-116细胞中JAK2/STAT3信号通路的机制研究[J]. 中国药理学通报, 2015, 31(10): 1394-8. Zhao L C, Liao K, Li K Q, et al. Modulatory effect of evodiamine on JAK2 /STAT3 signal pathway in HCT-116 cells[J]. Chin Pharmacol Bull, 2015, 31(10): 1394-8. doi:10.3969/j.issn.1001-1978.2015.10.014 |
| [5] | 石海莲, 郑沁乐, 吴大正. 吴茱萸碱对肥胖并发血管肥厚的作用研究[J]. 中国药理学通报, 2011, 27(12): 1687-92. Shi H L, Zheng Q L, Wu D Z. The preventive effect of evodiamine on vascular hypertrophy in obese rats[J]. Chin Pharmacol Bull, 2011, 27(12): 1687-92. doi:10.3969/j.issn.1001-1978.2011.12.014 |
| [6] | Lv Y Y, Ding G B, Zhai J H, et al. A superparamagnetic Fe3O4-loaded polymeric nanocarrier for targeted delivery of evodiamine with enhanced antitumor efficac[J]. Colloids Surf B Biointerfaces, 2013, 110(110): 411-8. |
| [7] | 杨鹏飞, 陈卫东. 纳米乳提高难溶性药物生物利用度的研究进展[J]. 中国药学杂志, 2013, 48(15): 1238-44. Yang P F, Chen W D. Research progress of nanoemulsions' applications in improving the bioavailability of poor water-soluble drugs[J]. Chin Pharm J, 2013, 48(15): 1238-44. |
| [8] | 柳珊, 谭群友, 尹华峰, 等. 吴茱萸碱超分子复合物的制备及体外溶出[J]. 中国医院药学杂志, 2012, 32(14): 1088-93. Liu S, Tan Q Y, Yin H F, et al. Process optimization and dissolution kinetics of evodiamine supra-structure complex[J]. Chin J Hosp Pharm, 2012, 32(14): 1088-93. |
| [9] | 周婧婧, 周庆颂, 孙若飞, 等. 不同分子量美沙拉嗪PEG修饰物的大鼠在体肠吸收研究[J]. 中国药理学通报, 2016, 32(10): 1446-51. Zhou J J, Zhou Q S, Sun R F, et al. In situ absorption kinetics of series molecular weight of PEGylated mesalazine in rats[J]. Chin Pharmacol Bull, 2016, 32(10): 1446-51. doi:10.3969/j.issn.1001-1978.2016.10.022 |
| [10] | 袁誉铭, 陈学梁, 陈静, 等. 溴吡斯的明新型纳米乳体外释放和大鼠在体胃肠吸收[J]. 中国药理学通报, 2017, 33(2): 276-9. Yuan Y M, Chen X L, Chen J, et al. In vitro release and gastrointestinal absorption of novel pyridostigmine bromide nanoemulsion[J]. Chin Pharmacol Bull, 2017, 33(2): 276-9. |
| [11] | 罗见春, 何丹, 杨梅, 等. 去甲氧基姜黄素羟丙基-β-环糊精在体肠吸收特征[J]. 第二军医大学学报, 2016, 37(2): 247-50. Luo J C, He D, Yang M, et al. Intestinal absorption characteristics of demethoxycurcumin hydroxypropyl-β-cyclodextrin in rats[J]. Acad J Second Military Med Univ, 2016, 37(2): 247-50. |
| [12] | Laxmi M, Bhardwaj A, Mehta S, et al. Development and characterization of nanoemulsion as carrier for the enhancement of bioavailability of artemether[J]. Artif Cells Nanomed Biotechnol,, 2015, 43(5): 334-44. doi:10.3109/21691401.2014.887018 |
| [13] | Devalapally H, Zhou F, McDade J, et al. Optimization of PEGylated nanoemulsions for improved pharmacokinetics of BCS class Ⅱ compounds[J]. Drug Deliv, 2015, 22(4): 467-74. doi:10.3109/10717544.2013.869275 |
| [14] | 陈风平, 刘晨光. 纳米乳研究进展[J]. 生物技术通报, 2013, 257(12): 43-8. Chen F P, Liu C G. Advances in nanoemulsions research[J]. Biotechnol Bull, 2013, 257(12): 43-8. |

