


2. 北京中医药大学 中医学院,北京 100029;
3. 北京中医药大学 糖尿病研究中心,北京 100029
 ,
MA Ru-feng2,
LIU Hai-xia2,
ZHU Ru-yuan2,
LIU Chen-yue1,
LI Lin2,
CHEN Bei-bei2,
JIA Qiang-qiang2,
GAO Si-hua3,
ZHANG Dong-wei3
,
MA Ru-feng2,
LIU Hai-xia2,
ZHU Ru-yuan2,
LIU Chen-yue1,
LI Lin2,
CHEN Bei-bei2,
JIA Qiang-qiang2,
GAO Si-hua3,
ZHANG Dong-wei3

2. Preclinical Medicine School, Beijing University of Chinese Medicine, Beijing 100029, China;
3. Diabetes Research Center, Beijing University of Chinese Medicine, Beijing 100029, China
骨质疏松症是一种以骨量降低、骨微结构破坏、骨脆性增加、骨强度下降和骨折风险性增加为特征的全身性、代谢性骨骼系统疾病,其最大的风险是骨折,尤其是髋部骨折,其中,近1/3的患者因此残疾和死亡[1]。流行病学调查显示,饮食中脂肪和肉类丰富的西方女性骨质疏松和骨折的发病率明显高于饮食中豆类食品丰富的东方女性[2]。研究也表明,高脂饮食与骨质疏松的发病密切相关。高脂饮食可导致脂质代谢调节紊乱,骨骼微环境改变和炎症增加,促进破骨细胞形成,最终导致骨矿物质密度(bone mineral density, BMD)下降,骨强度下降和骨微观结构恶化[3]。研究发现,♀ SD大鼠用高脂饲料喂养3个月后体内破骨细胞数量超过成骨细胞数量[4]。这说明高脂饮食促进大鼠破骨细胞形成,抑制成骨细胞形成,使大鼠股骨的骨量丢失。同时,高脂饮食使机体抗氧化因子含量降低,炎症递质释放增加,促使小鼠骨质疏松的发生[5]。同时,高脂饮食引起C57BL/6J小鼠下颌骨的骨量丢失[6]。
丹参是一种用于预防和治疗心血管疾病的传统中药。近年来,越来越多的研究表明,以丹酚酸B为代表的水溶性成分具有调节骨代谢的作用,其作用机制可能与Wnt/β-连环蛋白(β-catenin)、细胞外信号调节的蛋白激酶(extracellular signal-regulated protein kinase, ERK)、骨形态发生蛋白(bone morphogenetic protein, BMP)、骨保护素(osteoprotegerin, OPG)/核因子κB受体活化因子配体(receptor activator for nuclear factor-κB ligand, RANKL)/核因子κB受体活化因子(receptor activator of NF-κB, RANK)以及叉头转录因子(Forkhead box O, FoxO)介导的氧化应激等多种信号通路相关[7-8]。我们前期研究也发现,高脂饮食引起小鼠牙槽骨的骨量丢失。而丹酚酸B可以通过改善高脂饮食引起的氧化应激,从而抑制牙槽骨骨量丢失。其可能的机制是丹酚酸B通过调节NADPH氧化酶4(NADPH oxidase 4, Nox4)/核因子κB(nuclear factor kappa B, NF-κB)/组织蛋白酶K(cathepsin K)通路,改善牙槽骨骨量丢失[9]。但是,丹酚酸B对高脂饮食小鼠股骨代谢和骨微结构的影响目前尚不清楚。因此,为了探索丹酚酸B对高脂饮食小鼠股骨代谢作用和可能的作用机制,本研究拟观察丹酚酸B干预治疗高脂饮食的C57BL/6J小鼠12周后,小鼠股骨微结构和生物力学变化,以及其可能对氧化还原通路Nox4-NF-κB-cathepsin K的调节作用。
1 材料与方法 1.1 材料 1.1.1 仪器博勒飞质构仪CT3,美国BROOKFIELD公司; RM2255徕卡轮转式切片机,德国Leica公司; BX53倒置荧光显微镜,日本Olympus公司。
1.1.2 试剂骨组织抗原修复液,购自上海舜百生物科技有限公司; 番红O-固绿购自美国Sigma-Aldrich公司; cathepsin K抗体(ab19027)和NF-κB-p65抗体(ab16502),购自美国Abcam Biocompany公司; Nox4多克隆抗体(NB110-58849),购自美国Novus Biologicals公司; DAB显色液,购自中杉金桥生物科技公司; 高脂饲料(MD12032),包括45%脂肪、20%蛋白质和35%碳水化合物,购于江苏美迪森生物医药有限公司。
1.1.3 实验动物SPF级C57BL/6J ♂小鼠,体质量18~20 g,购自北京华阜康动物科技有限公司。饲养于北京中医药大学科研实验中心清洁级动物实验室,合格证号:SCXK京(2011-0024),室温(20±2)℃,相对湿度(55±5)%,光暗周期12 h/12 h。实验期间,各组小鼠给予自由饮水。
1.2 方法 1.2.1 动物模型的构建同王丽丽等[9]提供的方法,简述如下:将30只C57BL/6J小鼠适应性喂养1周后,随机等分为正常组、高脂组(HFD)和高脂+丹酚酸B(HFD+Sal B)组。高脂+丹酚酸B组每天给予丹酚酸B 125 mg·kg-1·d-1,正常组和高脂组小鼠每天给予等体积的蒸馏水,连续灌胃12周。实验期间,正常组小鼠给予正常饲料饲养,其余两组小鼠均给予高脂饲料饲养。
1.2.2 取材及样品制备连续灌胃12周后,将小鼠用1%戊巴比妥(4 mL·kg-1)腹腔麻醉后,分离股骨。在冰上剥离股骨附着的肌肉组织,将其先置于10%中性福尔马林中固定72 h,再放入15% EDTA钠(pH 7.4)溶液脱钙,脱钙液每2周更换1次,连续脱钙3个月后冲水,包埋,切片备用。
1.2.3 股骨生物力学的测定利用质构仪对各组小鼠股骨进行三点弯曲实验测定骨生物力学性能。实验前,显微镜下观察所有标本,以确保所有测试标本完好无损,并用游标卡尺测量股骨股干的直径。将小鼠股骨置于跨距为7 mm的两个支撑点上,标本的宽面朝上水平放置,按程序使探头缓慢下降,探头的加速度为10 mm·(min2)-1,标本断裂后继续运行2 mm停止。根据探头下降的距离与载荷数据,结合千分尺测量出的骨标本的断端直径生成骨的载荷-变形曲线,计算出最大挠度(maximum load,硬度形变量)和弹性载荷(elastic load,峰值压力)等骨生物力学参数。
1.2.4 股骨HE染色采用组织HE染色方法,简述如下:将股骨石蜡切片(5 μm)常规HE染色,中性树胶封片,倒置显微镜下观察病理变化并拍照。
1.2.5 番红O-固绿染色将股骨石蜡切片脱水,苏木精染色5 min,在1% HCl-乙醇中蘸两下分色,然后依次用0.05%固绿染色5 min,0.1%番红O染色5 min。中性树胶封片,倒置显微镜下观察病理变化并拍照。
1.2.6 免疫组织化学染色将股骨石蜡切片常规脱蜡至水,用抗原修复和山羊血清封闭后,分别滴加一抗NF-κB(1 :50)、Nox4(1 :50)和cathepsin K(1 :50),4℃孵育过夜后,滴加辣根过氧化物酶标记的二抗,DAB显色,苏木精复染,常规脱水、透明、封片。每组选取股骨切片中7个互不重叠的视野,采用Image Pro Plus 6. 0分析软件进行图像分析,测定阳性细胞的平均吸光度,取7个视野平均值进行分析。
1.3 统计学分析所得数据以x±s描述。采用Graph Pad 6.0软件进行数据分析,满足正态分布,方差齐时采用单因素方差分析(ANOVA); 方差不齐时使用Dunnett’s T3检验。不满足正态分布时,则使用非参数检验。
2 结果 2.1 丹酚酸B对高脂饮食小鼠股骨生物力学的影响各组小鼠股骨生物力学检测结果见Tab 1,与正常组小鼠相比,高脂组小鼠股骨的硬度形变量和峰值压力均明显降低(P < 0.05)。给予丹酚酸B治疗12周后,与高脂组小鼠相比,高脂+丹酚酸B组小鼠股骨硬度形变量和峰值压力均明显升高(P < 0.05)。
| Group | Maximum load/mm | Elastic load/kPa |
| Normal | 0.60±0.11 | 10234.00±654.32 |
| HFD | 0.41±0.09# | 7668.57±847.03# |
| HFD+Sal B | 0.60±0.12* | 10233.43±1100.44* |
| #P < 0.05 vs normal; *P < 0.05 vs HFD | ||
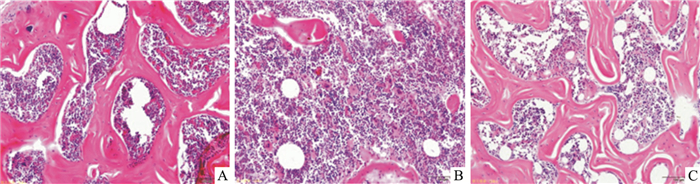
小鼠股骨组织切片HE染色结果见Fig 1。光镜(×200)下观察发现,正常组小鼠股骨骨小梁排列整齐,呈网状,骨微结构完整。与正常组小鼠相比,高脂组小鼠股骨骨小梁结构紊乱、变细、断裂,脂滴增多。与高脂组小鼠相比,高脂+丹酚酸B组小鼠股骨的骨小梁排列相对整齐,骨微结构形态明显改善,骨小梁增粗排列较规则。这说明丹酚酸B能够通过改善高脂饮食引起的骨微结构提高股骨质量。
|
| Fig 1 Effect of Sal B on microstructure alterations in femurs of mice on high fat diet (×200) A: Normal; B: HFD; C: HFD+Sal B |
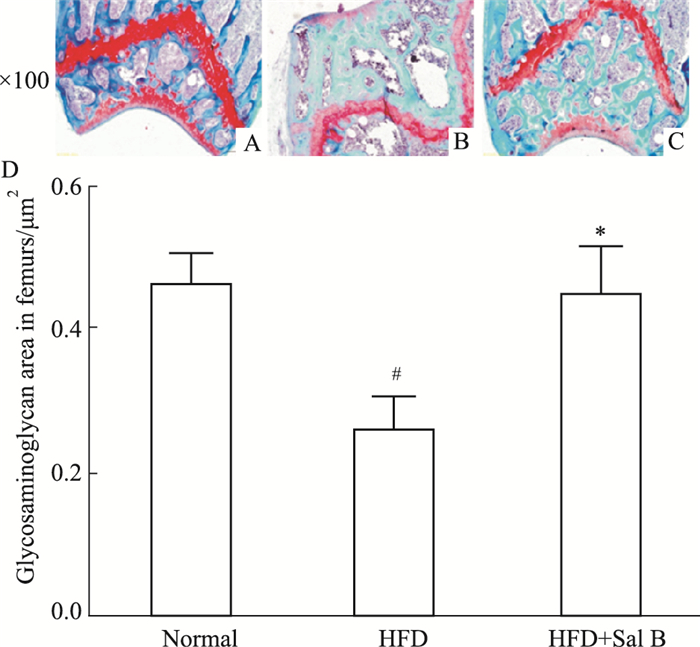
糖氨基葡聚糖(glycosaminoglycan,GAG)是在软骨中发现的天然的碳水化合物,与羟磷灰石结合后促进成骨细胞分化。如Fig 2番红O-固绿染色结果所示,GAG被番红O染成红色。与正常组小鼠相比,高脂饮食小鼠股骨干骺端GAG的面积减少,丹酚酸B干预12周后,GAG的面积明显增加,这提示丹酚酸B有促进成骨细胞分化的作用。
|
| Fig 2 Effect of Sal B on content of glycosaminoglycan (GAG, red color) in femurs of mice on high fat diet (x±s, n=7) A: Normal; B: HFD; C: HFD+Sal B; D: GAG area in femurs. #P < 0.05 vs normal group; *P < 0.05 vs HFD group. |
如Fig 3所示,与正常组小鼠相比,高脂组小鼠股骨小梁表面和骨髓腔中可见Nox4表达增高(P < 0.05)。与高脂组小鼠相比,高脂+丹酚酸B组小鼠股骨中Nox4水平明显降低(P < 0.05)。说明丹酚酸B可抑制高脂饮食引起的小鼠股骨Nox4的高表达。

|
| Fig 3 Effect of Sal B on Nox4 expression in femurs of mice on high fat diet (x±s, n=7) A: Normal; B: HFD; C: HFD+Sal B; D: Nox4 expression in femurs. #P < 0.05 vs normal group; *P < 0.05 vs HFD group. |
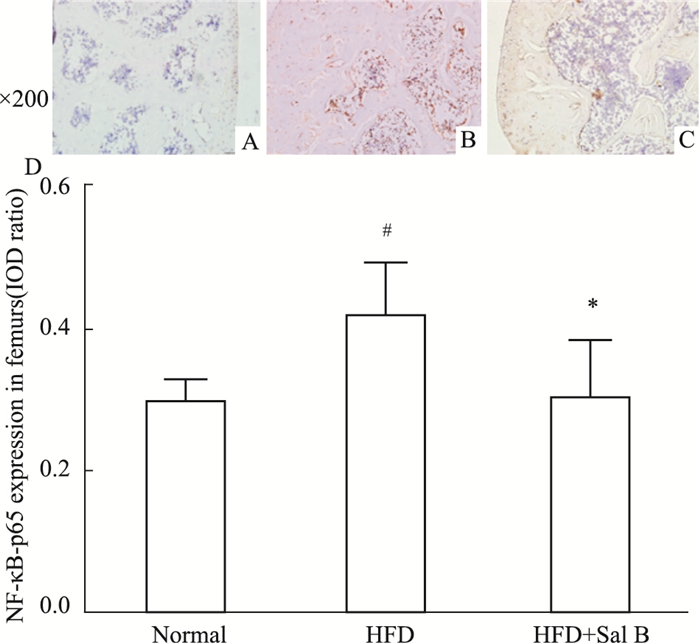
如Fig 4所示,与正常组小鼠相比,高脂组小鼠股骨中骨小梁断裂面以及骨髓腔中可见NF-κB-p65表达明显增高(P < 0.05)。与高脂组小鼠相比,丹酚酸B治疗12周后,小鼠股骨组织中NF-κB-p65的表达明显降低(P < 0.05)。
|
| Fig 4 Effect of Sal B on NF-κB-p65 expression in femurs of mice on high fat diet (x±s, n=7) A: Normal; B: HFD; C: HFD+Sal B; D: NF-κB-p65 expression in femurs. #P < 0.05 vs normal group; *P < 0.05 vs HFD group. |
B对高脂饮食小鼠股骨中cathepsin K表达的影响cathepsin K主要由破骨细胞分泌,被认为是破骨细胞活化和骨吸收的重要指标[10]。如Fig 5免疫组化染色结果所示,与正常组小鼠相比,高脂组小鼠股骨中cathepsin K表达增高(P < 0.05)。丹酚酸B干预12周后,高脂饮食小鼠股骨cathepsin K表达明显下降(P < 0.05)。

|
| Fig 5 Effect of Sal B on cathepsin K expression in femurs of mice on high fat diet (x±s, n=7) #P < 0.05 vs normal group; *P < 0.05 vs HFD group. |
骨质疏松的病理过程包括骨组织微结构的破坏和骨骼脆性的增加。我们之前的研究发现,高脂饮食可以促使小鼠牙槽骨骨质疏松,而丹酚酸B可以明显改善高脂饮食引起的牙槽骨骨微结构破坏和骨密度下降[9]。本研究发现,丹酚酸B可以改善高脂饮食小鼠股骨的微结构。实验中我们采用三点弯曲实验,通过对硬度形变量和峰值压力指标的检测,证明丹酚酸B可以提高高脂饮食小鼠股骨的骨强度。
Nox4主要由破骨细胞分泌,在破骨细胞分化和成熟的过程中表达增多。Nox4的激活能促进破骨细胞分化成熟,从而诱发骨吸收,促进骨质疏松的发生发展。Nox4基因敲除小鼠骨密度升高,破骨细胞数量减少,破骨细胞标志物水平下降。骨质疏松病人骨中的破骨细胞活性增加,Nox4表达增多[11]。研究发现,高脂饮食引起C57BL/6J小鼠Nox4的高表达,进一步导致NF-κB-p65高表达[12-13]。高脂饮食诱导小鼠牙槽骨中Nox4和NF-κB-p65的高表达[9]。本研究也发现,丹酚酸B抑制高脂饮食小鼠股骨中Nox4和NF-κB表达。
骨骼由大约60%的钙羟磷灰石和40%骨基质蛋白构成。其中,主要的蛋白是Ⅰ型胶原蛋白。cathepsin K是由破骨细胞分泌的发挥降解骨基质蛋白最主要的酶,特别是对Ⅰ型胶原蛋白的降解[14]。NF-κB活化后可通过调节NFATc1等基因,促使cathepsin K的高表达,促使骨质疏松的发生[9]。我们前期的研究发现,高脂饮食能诱发小鼠牙槽骨组织的NF-κB的活化和cathepsin K的高表达,引起小鼠股骨微结构破坏[9]。本研究也证明,高脂饮食可以使小鼠股骨组织的NF-κB和cathepsin K表达量上升,引起小鼠股骨强度下降和骨微结构破坏。而给予丹酚酸B干预高脂饮食小鼠12周后,股骨中cathepsin K表达下降,骨微结构改善,骨强度有一定程度的提高。
软骨细胞分泌的细胞外基质主要分为三类:①胶原类:以Ⅱ型胶原为主,是维持组织强度的来源; ②结构糖蛋白:如纤维黏连蛋白; ③蛋白多糖类:主要为GAG,包括硫酸软骨素、硫酸角质素和肝素。其中GAG是软骨的主要细胞外基质,是关节软骨的主要成分之一,占透明软骨干重的20% ~40%[15]。GAG具有促进成骨的作用。研究发现,硫酸软骨素A具有促进兔下颌骨的新骨形成。本研究中我们发现,丹酚酸B可以提高高脂饮食小鼠股骨中GAG的含量。这表明丹酚酸B可以促进成骨细胞的分化,但其作用机制需要进一步的探索。
综上所述,高脂饮食小鼠表现出明显的股骨微结构破坏,骨强度下降。丹酚酸B可通过调节Nox4/NF-κB/cathepsin K信号通路而改善股骨代谢。本研究也首次证明丹酚酸B具有抑制小鼠股骨cathepsin K表达的功能。
( 致谢: 本实验在北京中医药大学糖尿病研究中心进行,对实验中给予指导和帮助的老师和同学表示感谢。)
| [1] | Baccaro L F, Conde D M, Costa-Paiva L, et al. The epidemiology and management of postmenopausal osteoporosis: a viewpoint from Brazil[J]. Clin Interv Aging, 2015, 20(10): 583-91. |
| [2] | Ross P D, Norimatsu H, Davis J W, et al. A comparison of hip fracture incidence among native Japanese, Japanese Americans, and American caucasians[J]. Am J Epidemiol, 1991, 133(8): 801-9. doi:10.1093/oxfordjournals.aje.a115959 |
| [3] | Tian L, Yu X. Fat, sugar, and bone health: a complex relationship[J]. Nutrients, 2017, 9(5): pii: E506. |
| [4] | 梁洁, 宋文琦. 高脂饮食与高植物蛋白饮食结构对雌性大鼠骨细胞的影响[J]. 云南医药, 2016, 37(2): 207-10. Liang J, Song W Q. Effects of high-fat and high plant protein diet on bone cells in female rats[J]. Med Pharm Yunnan, 2016, 37(2): 207-10. |
| [5] | 朱再胜, 戴爽, 吴玲, 等. 高脂饮食诱导肥胖小鼠模型中氧化应激、炎症递质对骨代谢的影响及其可能机制[J]. 温州医科大学学报, 2014, 44(9): 631-6. Zhu Z S, Dai S, Wu L, et al. The effects of inflammatory mediator and oxidative stress on bone metabolism in high fat diet-induced obesity mice and the underlying mechanism[J]. J Wenzhou Med Univ, 2014, 44(9): 631-6. |
| [6] | Fujita Y, Maki K. High-fat diet-induced obesity triggers alveolar bone loss and spontaneous periodontal disease in growing mice[J]. BMC Obes, 2015, 3: 1. doi:10.1186/s40608-016-0082-8 |
| [7] | 李淑惠, 梁燕龙, 杨亚军, 等. 丹参水溶性成分影响骨代谢的机制研究进展[J]. 中国药理学通报, 2016, 32(7): 902-5. Li S H, Liang Y L, Yang Y J, et al. The research progress on the mechanism of bone metabolism affected by the water-soluble components of danshen[J]. Chin Pharmacol Bull, 2016, 32(7): 902-5. |
| [8] | 李近, 杨亚军, 刘钰瑜. Foxos与骨质疏松[J]. 中国药理学通报, 2016, 32(2): 169-71. Li J, Yang Y J, Liu Y Y, et al. Foxos and osteoporosis[J]. Chin Pharmacol Bull, 2016, 32(2): 169-71. |
| [9] | 王丽丽, 马如风, 于娜, 等. 丹酚酸B通过抗氧化作用改善高脂饮食小鼠牙槽骨骨质疏松的实验研究[J]. 中国骨质疏松杂志, 2017, 23(3): 281-5. Wang L L, Ma R F, Yu N, et al. Salvianolic acid B prevents mandibular osteoporosis through anti-oxidation in high fat diet exposed mice[J]. Chin J Osteoporos, 2017, 23(3): 281-5. |
| [10] | Bromme D, Panwar P, Turan S. Cathepsin K osteoporosis trials, pycnodysostosis and mouse deficiency models: commonalities and differences[J]. Expert Opin Drug Discov, 2016, 11(5): 457-72. doi:10.1517/17460441.2016.1160884 |
| [11] | Goettsch C, Babelova A, Trummer O, et al. NADPH oxidase 4 limits bone mass by promoting osteoclastogenesis[J]. Journal Clin Invest, 2013, 123(11): 4731-8. doi:10.1172/JCI67603 |
| [12] | Zhang S Q, Sun Y T, Xu T H, et al. Protective effect of metformin on renal injury of c57bl/6j mouse treated with high fat diet[J]. Die Pharmazie, 2014, 69(12): 904-8. |
| [13] | Anvari E, Wikstrom P, Walum E, et al. The novel NADPH oxidase 4 inhibitor GLX351322 counteracts glucose intolerance in high-fat diet-treated C57BL/6 mice[J]. Free Radic Res, 2015, 49(11): 1308-18. doi:10.3109/10715762.2015.1067697 |
| [14] | Yi C, Hao K Y, Ma T, et al. Inhibition of cathepsin K promotes osseointegration of titanium implants in ovariectomised rats[J]. Sci Rep, 2017, 7: 44682. doi:10.1038/srep44682 |
| [15] | 王传家, 王海鱼, 许红权, 等. bFGF对猪关节软骨细胞合成氨基葡聚糖的作用[J]. 中国美容医学, 2006, 15(7): 782-3. Wang C J, Wang H Y, Xu H Q, et al. Effects of bFGF on glycosaminoglycan of pig chondrocytes in culture[J]. Chin J Aesthetic Med, 2006, 15(7): 782-3. |