

动脉粥样硬化(atherosclerosis,AS)是引起多种心脑血管病变的主要原因,预计到2020年,AS将成为世界首要致死原因[1]。新近研究显示[2],AS是一种炎症性疾病,炎症因子参与了AS的发生及发展过程。血管平滑肌细胞(vascular smooth muscle cells,VSMCs)是动脉壁的重要组成部分,可以在包括内毒素脂多糖(lipopolysaccharide,LPS)以内的多种炎症诱导因子刺激下,分泌大量炎症因子、黏附分子及趋化因子,参与血管壁内的炎症反应[3]。积雪草酸(asiatic acid,AA)是从双子叶伞形科植物积雪草(Centella asiatica)中萃取而来,属于五环三萜酸植物多酚,其结构如Fig 1所示。现代药理学研究表明,AA具有抗炎、抗增殖、抗肿瘤、免疫调节等多种药理学作用[4]。AA可以通过下调TLR4表达,抑制LPS诱导的肺部炎症反应,还被证实具有一定的过氧化物酶体增殖因子活化受体γ(peroxisome proliferators activated receptor γ,PPAR-γ)激活作用[5]。然而,AA是否具有抗AS的心血管保护作用,目前尚未见报道。本文聚焦于AA能否抑制LPS诱导的VSMCs细胞炎症反应,并期望从Toll样受体4(toll-like receptor 4, TLR4)及PPAR-γ表达水平入手,进一步阐明AA抗炎作用的分子机制。

|
| Fig 1 Structural formula of asiatic acid |
SPF级♂ SD大鼠10只,6~8周,购于河南省实验动物中心,许可证号:SYXK(豫)2017-0096。
1.2 试剂DMEM高糖培养液(美国Gibco公司,批号:275639);新鲜胎牛血清(北京TransGen公司, 批号:8131640);积雪草酸标准品(广西博科天然药物有限公司, 批号:20170515, 纯度>96%); PCR试剂盒(北京TransGen公司,批号:20170320);0.25%的胰酶(美国Hyclone公司, 批号:271526);LPS、青霉素、链霉素、GW9662、噻唑蓝,均购于美国Sigma公司; 白细胞介素-6(interleukin, IL-6)、单核细胞趋化蛋白-1(monocyte chemoattractant protein-1, MCP-1)、肿瘤坏死因子(tumor necrosis factor, TNF-α)试剂盒均购于美国R&D公司,批号分别为41230525、39270521、43720425;兔抗大鼠TLR4、PPAR-γ、Histone、β-actin抗体均购自英国Abcam公司,批号分别为3354172、3927129、2765124、4125649;所有PCR引物和TLR4-siRNA由南京金思瑞生物有限公司合成。
1.3 仪器超净台(哈尔滨东联电子技术发展有限公司),MCO175型CO2培养箱(日本Sanyo公司),倒置显微镜(日本Olympus公司),CS-15R冷冻离心机(美国Beckman公司),IQ5荧光定量PCR仪(美国ABI公司)。
2 方法 2.1 原代细胞培养分离8~10周SD大鼠主动脉,去除血管外膜和内膜,充分剪碎至1~2 mm3大小组织块。参照文献[6]所述步骤,使用贴壁法培养VSMCs细胞。将细胞置于10%胎牛血清、100 mg·L-1青霉素、链霉素的高糖DMEM培养基中培养。待细胞融合至80%~90%时,进行后续实验。
2.2 MTT法测定细胞活性“2.1”中细胞培养条件培养24 h,2%的低血清培养基孵育12 h后,将细胞分为8组,分别采用0、5、10、20、30、40、50 μmol·L-1 AA及LPS(500 μg·L-1)干预24 h。吸去培养液,每孔加入MTT(5 g·L-1)20 μL,37℃孵育4 h,弃去上清,每孔加入二甲基亚砜(DMSO)100 μL,微微振荡数次后,在全自动酶标仪上于570 nm处测定各组吸光值。
2.3 TLR-siRNA转染VSMCs细胞将各组细胞以5×105个每孔的密度接种于6孔板中,待生长至70%~80%融合时,换用无血清培养基孵育12 h。转染步骤严格根据说明书进行。将含有100 pmol siRNA的培养液400 μL和含有5 μg脂质体Lip2000的培养液400 μL混合,充分混匀并静置25 min。然后,将此转染混合液加入充分漂洗后的6孔板内,将6孔板置入培养箱中孵育6 h,用含10%胎牛血清、双抗的DMEM高糖培养基继续孵育24 h。荧光显微镜观察转染效果,确定转染成功后,进行后续研究。
2.4 ELISA法测定MCP-1、TNF-α和IL-6水平将各组细胞以5×104个每孔的密度接种于96孔板中,待生长至80%~90%融合时,换用无血清培养基孵育12 h。不同浓度AA(10、20、30 μmol·L-1)预处理2 h,LPS(500 μg·L-1)刺激不同时间后,收集各组细胞上清液。依据操作说明,使用ELISA试剂盒测定MCP-1、TNF-α、IL-6水平。使用自动酶联免疫吸附仪在450 nm处读取数值,绘制MCP-1、TNF-α、IL-6的标准曲线,并依据此计算各实验组结果。
2.5 Real-time PCR法测定MCP-1、TNF-α、IL-6、TLR4、PPAR-γ mRNA的表达将各组细胞以5×105个每孔的密度接种于6孔板中,加入含血清培养基,待细胞密度达到80%~90%融合时,改用无血清培养基孵育12 h。换用不同浓度积雪草酸(10、20、30 μmol·L-1)预处理2 h,再给予LPS(500 μg·L-1)刺激6 h,按照说明书使用TRIzol试剂提取各组总RNA。琼脂糖凝胶电泳鉴定RNA完整性,分光光度计于260 nm处检测RNA的纯度。采用逆转录试剂盒,将各组mRNA反转录为cDNA。所采用的引物序列见Tab 1。扩增条件:95℃预变性5 min,95℃ 15 s,55℃退火15 s,72℃延伸30 s,共计40个循环。使用荧光PCR仪自带分析软件对real-time PCR结果进行分析。
| Gene | Prime sequence | Product length/bp |
| MCP-1 | Forward: 5′-CACGTCGTAGCAAACCACCAA-3′ | 113 |
| Reverse: 5′-GTTGGTTGTCTTTGAGATCCAT-3′ | ||
| TNF-α | Forward: 5′-CACGTCGTAGCAAACCACCAA-3′ | 110 |
| Reverse: 5′-GTTGGTTGTCTTTGAGATCCAT-3′ | ||
| IL-6 | Forward: 5′-TGGTGATAAATCCCGATGAAG-3′ | 676 |
| Reverse: 5′-GGCACTGAAACTCCTGGTCT-3′ | ||
| TLR4 | Forward: 5′-CTTTGAAAATGTAAGGCGGC-3′ | 280 |
| Reverse: 5′-ATGTAGGCAGGTGTGTGGC-3′ | ||
| PPAR-γ | Forward: 5′-GATGACCACTCCCATTCCTTT-3′ | 152 |
| Reverse: 5′-AAACCTGATGGCATTGTGAGA-3′ | ||
| β-actin | Forward: 5′-AATGAGCGGTTCCGATGC-3′ | 143 |
| Reverse: 5′-GGAAGGTGGACAGTGAGGC-3′ |
以5×105个每孔的密度将细胞接种于6孔板中,加入含血清培养基,待细胞密度达到80%~90%融合时,改用无血清培养基孵育12 h后,用含不同浓度AA(10、20、30 μmol·L-1)或TLR4-siRNA、GW9662(10 μmol·L-1)的无血清培养基预处理2 h后,加入LPS(500 μg·L-1)刺激24 h。每孔使用200 μL RIPA裂解液提取蛋白。核内PPAR-γ蛋白使用核蛋白提取试剂盒提取,并采用BCA蛋白定量试剂盒测定各组样品蛋白浓度。加入蛋白上样缓冲液并煮沸,采用10% SDS-PAGE凝胶电泳,半干转膜仪转膜。一抗浓度为TLR4(1 :400)、PPAR-γ(1 :500)、Histone(1 :1 000)、β-actin(1 :2 000)。以β-actin和Histone作为内参照。化学发光法检测,Quantity one软件进行图像分析。
2.7 统计学分析使用SPSS 17.0软件进行统计学分析,计量均数用x±s表示。组间比较使用单因素方差分析,多重均数比较使用SNK检验。
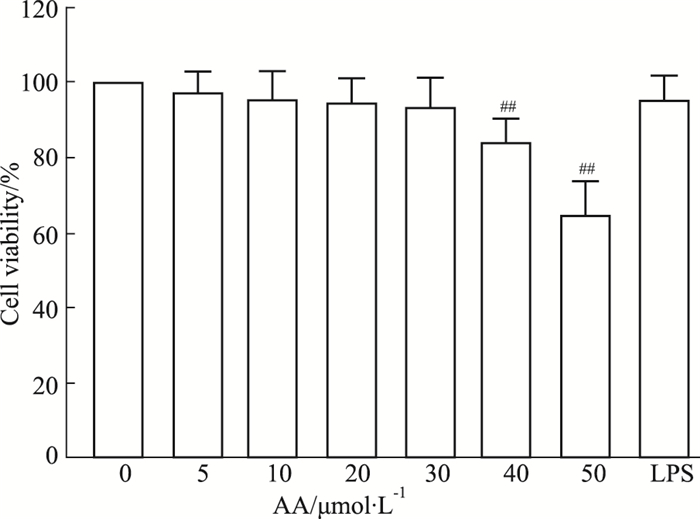
3 结果 3.1 AA对VSMCs细胞活性的影响为排除AA可能的细胞毒性对后续实验结果的影响,使用MTT法测定0~50 μmol·L-1浓度范围内AA和500 μg·L-1的LPS对VSMCs细胞活性的影响。Fig 2结果显示,当AA浓度在0~30 μmol·L-1范围内时,对VSMCs细胞活性无明显影响(P>0.05);当给予细胞500 μg·L-1 LPS刺激24 h,也未产生明显细胞毒性(P>0.05)。故以下实验中,我们选择10、20、30 μmol·L-1 3个浓度AA作为干预条件。
|
| Fig 2 Effect of AA and LPS(500 μg·L-1) on VSMCs viability ##P < 0.01 vs control group |
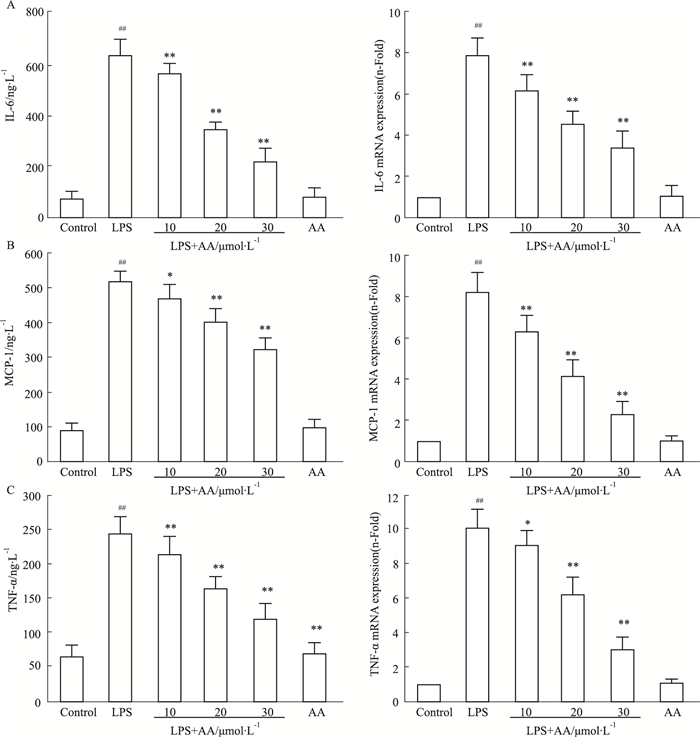
如Fig 3所示,当给予VSMCs细胞500 μg·L-1 LPS刺激24 h后,MCP-1、TNF-α、IL-6蛋白水平明显升高(P < 0.05);AA则能够浓度依赖性地抑制LPS诱导的VSMCs细胞MCP-1、TNF-α、IL-6蛋白合成增加。与之类似,AA亦能够浓度依赖性地抑制LPS诱导的VSMCs细胞MCP-1、TNF-α、IL-6 mRNA合成,当VSMCs细胞与30 μmol·L-1的AA孵育6、24 h,均不影响MCP-1、TNF-α、IL-6 mRNA和蛋白的表达。
|
| Fig 3 Effect of AA on LPS-induced mRNA and protein expression of IL-6(A), MCP-1(B) and TNF-α(C) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs LPS group |
LPS通过与VSMCs表面的CD14结合,进而上调TLR4表达是诱发VSMCs细胞炎症级联反应的关键环节。当给予VSMCs细胞500 μg·L-1 LPS刺激6、24 h后,TLR4 mRNA和蛋白表达水平均明显提高(P < 0.05)。给予细胞不同浓度AA(10、20、30 μmol·L-1)预处理能有效抑制LPS诱导的VSMCs细胞TLR4表达。为了进一步验证AA的抗炎作用与其对TLR4表达下调相关,我们使用TLR4-siRNA对TLR4进行基因沉默。结果显示,TLR4-siRNA能够起到与AA类似的抗炎作用,而联用TLR4-siRNA和AA(30 μmol·L-1)能够进一步降低炎症因子合成。当给予细胞30 μmol·L-1 AA孵育6、24 h,并不影响TLR4 mRNA和蛋白的表达(Fig 4)。

|
| Fig 4 AA inhibited LPS-induced mRNA and protein expression of IL-6, MCP-1 and TNF-α partially dependent on down-regulating TLR4 A: Protein and mRNA expression of TLR4; B: Protein and mRNA expression of IL-6; C: Protein and mRNA expression of MCP-1; D: Protein and mRNA expression of TNF-α. ##P < 0.01 vs control group; **P < 0.01 vs LPS group; △P < 0.05 vs AA group. |
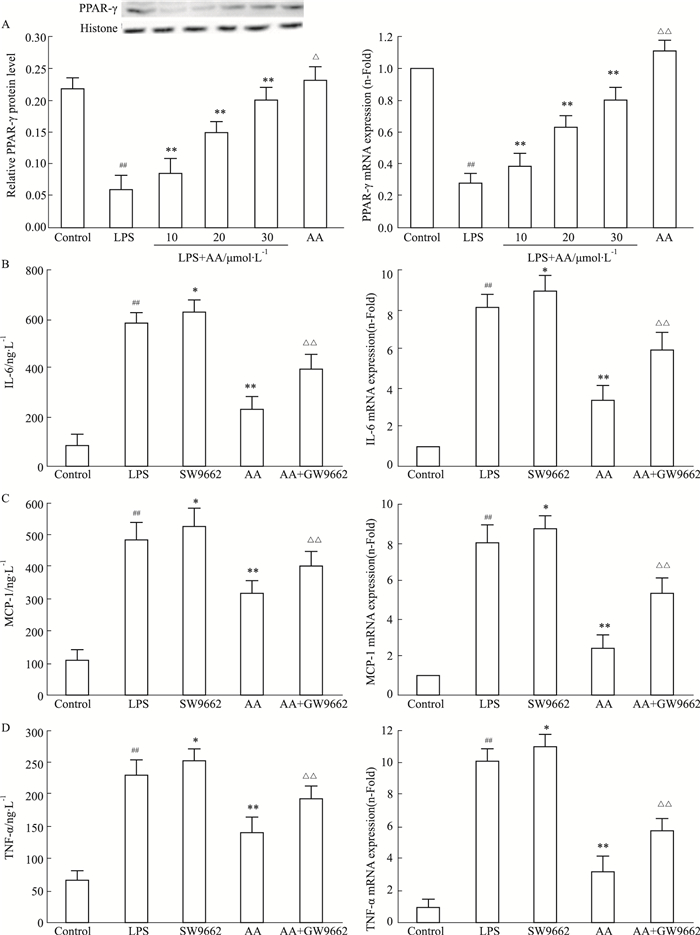
PPAR-γ是LPS诱导的炎症反应的重要负性调节因子。如Fig 5所示,当给予VSMCs细胞500 μg·L-1 LPS刺激6、24 h后,PPAR-γ mRNA和蛋白表达明显降低。给予AA(10、20、30 μmol·L-1)预处理能有效抑制LPS诱导的PPAR-γ活性。当仅给予VSMCs细胞30 μmol·L-1 AA孵育6、24 h后,PPAR-γ mRNA和蛋白表达明显增加。为进一步明确AA抗炎作用与其上调PPAR-γ活性相关,采用PPAR-γ拮抗剂GW9662对细胞进行预处理。结果显示,GW9662能够部分拮抗AA的抗炎作用,提示AA抗炎作用与其上调PPAR-γ活性相关。
|
| Fig 5 AA inhibited LPS-induced mRNA and protein expression of IL-6, MCP-1 and TNF-α partially dependent on up-regulating PPAR-γ A: Protein and mRNA expression of PPAR-γ; B: Protein and mRNA expression of IL-6; C: Protein and mRNA expression of MCP-1; D: Protein and mRNA expression of TNF-α. ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs LPS group; △P < 0.05, △△P < 0.01 vs AA group. |
近年来,长期的低度炎症反应在动脉粥样斑块形成及失稳过程中的作用越来越受到学术界关注。病理性的炎症反应可能通过诱导VSMCs凋亡,加速动脉粥样斑块的形成,并使得稳定性斑块向易损性斑块转变,促进AS的发生和发展[7]。LPS是高效致炎因子,与受体结合后能够诱导内皮细胞、VSMCs、巨噬细胞等大量分泌炎症介质[8]。因此,抑制VSMCs细胞的炎症反应已成为延缓动脉粥样斑块形成的重要治疗靶点。
IL-6能够诱导T细胞活化,增加淋巴因子合成,促进B细胞转化为具有分泌功能的浆细胞,诱导大量特异性抗体生成,目前认为,IL-6主要通过影响细胞免疫过程,参与调节炎症反应,进而促进AS的发生和发展[9]。MCP-1能够诱导循环体系中的巨噬细胞进入内皮下区域,进而加速斑块脂质核心形成速度[10]。TNF-α通过诱导斑块区域VSMCs凋亡、触发血小板黏附和聚集、巨噬细胞趋化和胆固醇沉积等途径,加速动脉粥硬化斑块形成和斑块不稳定,且血清内TNF-α水平和冠脉狭窄程度呈正相关关系[11-12]。因此,抑制IL-6、MCP-1和TNF-α水平病理性升高对减缓AS的发生发展具有重要作用。本研究中,我们发现LPS能够明显诱导VSMCs细胞IL-6、MCP-1、TNF-α mRNA和蛋白合成。AA则能够浓度依赖性抑制LPS诱导的VSMCs细胞IL-6、MCP-1、TNF-α mRNA和蛋白合成增加。据此,可以推测AA能够一定程度抑制LPS诱导的VSMCs细胞炎症反应。
Toll样受体家族成员众多,参与到包括分子模式识别、抗原提呈和信号转导等各种炎症相关免疫应答的多个环节,其中TLR4是Toll样受体家族中的重要一员,也是LPS诱导的炎症反应通路中的关键调节因子,当LPS与细胞膜表面的CD14结合后,使TLR4激活,进而通过Myd88依赖的经典途径或者非经典途径,诱发炎症级联反应,促进多种炎症因子的释放[13]。因此,抑制LPS诱导的TLR4激活可能在抗AS, 保护心血管中起到一定的作用。在本研究中,我们也将AA的抗炎作用聚焦在调节TLR4活性上。研究结果显示,AA能够减少LPS诱导的VSMCs细胞TLR4 mRNA和蛋白表达,并具有浓度依赖性。同时,使用TLR4-siRNA对TLR4进行基因沉默,可以达到与AA相似的抗炎效果;两者同时使用还可以进一步增强对炎症因子释放的抑制作用。由此推测,AA对LPS诱导的VSMCs细胞炎症因子释放的抑制作用可能与其对TLR4表达下调相关。
PPAR-γ是PPAR家族重要成员,活化后与RXR结合,进而调控下游靶基因表达。PPAR-γ已被多项研究证实广泛参与到炎症、细胞增殖、癌细胞侵袭过程的多个环节,且PPAR-γ广泛分布于包括VSMCs在内的多种心血管组织,具有抑制炎症因子释放和VSMCs及心脏成纤维细胞增殖的心血管保护作用[14]。之前的研究显示,AA能够通过上调PPAR-γ活性,抑制LPS诱导的小鼠肺部炎症反应。本研究中,我们发现给予VSMCs细胞LPS刺激后,PPAR-γ的表达明显降低;AA能够浓度依赖性的拮抗LPS诱导的PPAR-γ表达减低。给予VSMCs细胞PPAR-γ拮抗剂GW9662预处理,能够通过抑制PPAR-γ的激活,进而部分抵消AA的抗炎效果。据此可知,AA具有一定的PPAR-γ激活作用,且这种作用参与了AA抑制LPS诱导的VSMCs细胞炎症反应的生理过程。
综上所述,AA能够有效抑制LPS诱导的VSMCs细胞炎症因子释放,其机制可能与下调TLR4表达和上调PPAR-γ活性有关。
| [1] | 李红蓉, 秘红英, 孙颖, 等. 内皮间质分化在动脉粥样硬化中的研究进展[J]. 中国药理学通报, 2017, 10(33): 1338-41. Li H R, Mi H Y, Sun Y, et al. Advances of endothelial stromal differentiation at atherosclerosis[J]. Chin Pharmacol Bull, 2017, 10(33): 1338-41. |
| [2] | 陈燕铭, 熊肇军, 尹琼丽, 等. 2型糖尿病患者血清炎症因子和脂联素水平与动脉粥样硬化的关系[J]. 中国动脉硬化杂志, 2011, 19(10): 842-6. Chen Y M, Xiong Z J, Yin Q L, et al. Relationship between serum inflammatory factors and adiponectin levels in patients with type 2 diabetes mellitus and atherosclerosis[J]. Chin J Arteriosclerosis, 2011, 19(10): 842-6. |
| [3] | Chepelenko G V. Atherosclerosis regulation via media lipid-driven VSMC cholesterol efflux switch[J]. Med Hypotheses, 2015, 84(2): 141-4. doi:10.1016/j.mehy.2014.12.002 |
| [4] | 孟艳秋, 张伟晨, 宁梓廷, 等. 积雪草酸A环开环衍生物的合成及体外抗肿瘤活性研究[J]. 中国新药杂志, 2017, 26(10): 1157-61. Meng Y Q, Zhang W C, Ning X T, et al. Synthesis and in vitro antitumor activity of cycloacyclic A-ring ring-opening derivatives[J]. Chin J New Drugs, 2017, 26(10): 1157-61. |
| [5] | Hao C, Wu B, Hou Z, et al. Asiatic acid inhibits LPS-induced inflammatory response in human gingival fibroblasts[J]. Int Immunopharmacol, 2017, 9(50): 313-8. |
| [6] | 高静, 朱红霞, 王敏哲, 等. VEGF对人血管平滑肌细胞株功能的影响及相关机制[J]. 中国老年学杂志, 2015, 6(35): 3257-9. Gao J, Zhu H X, Wang M Z, et al. Effect of VEGF on the function of human vascular smooth muscle cell line and its related mechanisms[J]. Chin J Gerontol, 2015, 6(35): 3257-9. |
| [7] | Pant S, Deshmukh A, Gurumurthy G S, et al. Inflammation and atherosclerosis-revisited[J]. J Cardiovasc Pharmacol Ther, 2014, 19(2): 170-8. doi:10.1177/1074248413504994 |
| [8] | Li L, He M, Zhou L, et al. A solute carrier family 22 member 3 variant rs3088442 G→A associated with coronary heart disease inhibits lipopolysaccharide-induced inflammatory response[J]. J Biol Chem, 2015, 290(9): 5328-40. doi:10.1074/jbc.M114.584953 |
| [9] | Hartman J, Frishman W H. Inflammation and atherosclerosis: a review of the role of interleukin-6 in the development of atherosclerosis and the potential for targeted drug therapy[J]. Cardiol Rev, 2014, 22(3): 147-51. doi:10.1097/CRD.0000000000000021 |
| [10] | Lin J, Kakkar V, Lu X. Impact of MCP-1 in atherosclerosis[J]. Curr Pharm Des, 2014, 20(28): 4580-8. doi:10.2174/1381612820666140522115801 |
| [11] | Zhang Y, Yang X, Bian F. TNF-α promotes early atherosclerosis by increasing transcytosis of LDL across endothelial cells: crosstalk between NF-κB and PPAR-γ[J]. J Mol Cell Cardiol, 2014, 7(72): 85-94. |
| [12] | Garg P K, McClelland R L, Jenny N S, et al. Lipoprotein-associated phospholipase A2 (Lp-PLA2) and tumor necrosis factor-alpha (TNF-α) and their relation to premature atherosclerosis in β-thalassemia children[J]. Hematology, 2015, 20(4): 228-38. doi:10.1179/1607845414Y.0000000180 |
| [13] | Yang S, Li R, Tang L, et al. TLR4-mediated anti-atherosclerosis mechanisms of angiotensin-converting enzyme inhibitor-fosinopril[J]. Cell Immunol, 2013, 285(2): 38-41. |
| [14] | Zhang Y, Yang X, Bian F, et al. TNF-α promotes early atherosclerosis by increasing transcytosis of LDL across endothelial cells: crosstalk between NF-κB and PPAR-γ[J]. J Mol Cell Cardiol, 2014, 7(72): 85-94. |
文章信息
-
文章历史
- 收稿日期: 2017-09-12
- 修回日期: 2017-11-20
- 网络出版时间: 2017-12-14

