

2. 中国中医科学院西苑医院临床药理中心,北京 100091;
3. 甘肃中医药大学附属医院,甘肃 兰州 730000;
4. 中国中医科学院西苑医院急诊科,北京 100091
2. Center of Clinical Pharmacology, Xiyuan Hospital, China Academy of Chinese Medical Sciences, Beijing 100091, China;
3. Affiliated Hospital of Gansu College of Traditional Chinese Medicine, Lanzhou 730000, China;
4. Dept of Emergency, Xiyuan Hospital, China Academy of Chinese Medical Sciences, Beijing 100091, China
糖尿病血管并发症是引起患者高致残率和高致死率的主要原因[1]。慢性稳定性高血糖和波动性高血糖是糖尿病患者高血糖的两种主要表现形式。研究表明,高血糖可诱导血管内皮损伤,且以波动高糖损伤为重,同时高血糖通过多种机制导致血小板黏附、聚集和释放功能失调,进而引发过度活化状态[2-3]。基于血小板活化在动脉血栓形成的重要作用,阿司匹林已成为糖尿病患者预防心血管病变的推荐药物[4]。然而,目前尚缺乏关于波动性高血糖对内皮损伤过程中血小板活化程度影响的相关研究,同时,阿司匹林对此过程具有怎样的影响亦未可知。基于此,本研究通过体外构建人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)血糖波动模型以及波动高糖诱导HUVECs损伤培养液和健康人血小板共孵育体系,体内构建2型糖尿病(type 2 diabetes mellitus,T2DM)大鼠血糖波动模型,观察阿司匹林对波动高糖诱导内皮损伤过程中血小板活化的影响。
1 材料与方法 1.1 实验动物与药物清洁级♂ SD大鼠,体质量170 g~190 g,购自中国食品药品检定研究院,许可证编号:SCXK(京)2009-0017。动物饲料购自北京华富康饲料公司,高糖高脂饲料:猪油20%(W/W)、蔗糖10%(W/W)、胆固醇1.25%(W/W)、胆酸盐0.25%(W/W)、普通饲料68.5%。高升糖指数(glucose index,GI)饲料:每公斤饲料含糯玉米淀粉(蜡质玉米淀粉)542 g、凝胶20 g、酪蛋白200 g、蔗糖85 g、豆油56 g、麦麸50 g、DL-蛋氨酸2 g、维生素混合物10 g、矿物质混合物35 g。低升糖指数(GI)饲料配方:每公斤饲料含高直链玉米淀粉542 g、凝胶20 g、酪蛋白200 g、蔗糖85 g、豆油56 g、麦麸50 g、DL-蛋氨酸2 g、维生素混合物10 g、矿物质混合物35 g。阿司匹林(acetylsalicylic acid,ASA,批号:BJ10194)购自拜耳医药保健有限公司。
1.2 HUVECs的培养与分组无菌条件下取健康产妇正常分娩的新生儿脐带,HUVECs的分离、培养和鉴定参照Jaffe等[5]的方法。所用实验细胞均为第3-5代细胞。实验分为4组:正常低糖(N)组:持续低糖型DMEM全培养基培养; 稳定性高糖(W)组:持续高糖型DMEM全培养基培养; 波动性高糖(B)组:高糖型DMEM全培养基/低糖型DMEM全培养基培养,每24 h更换1次; 波动性高糖组+阿司匹林(ASA)组:波动性高糖组进行阿司匹林(1 mmol·L-1)干预,阿司匹林剂量是应用细胞计数试剂盒测得的半数致死量。培养8 d,收集各组培养上清液,置于-80℃冰箱中储存备用。
1.3 健康人血小板采集健康志愿者15例,年龄20~45岁,近2周未发生炎症性疾病,未服用任何药物。于清晨进食前,将收集所得的健康人枸橼酸钠抗凝(1 :9)血提取富血小板血浆(platelet rich plasma,PRP)、贫血小板血浆(platelet poor plasma,PPP),用PPP调整PRP至2.0×1011~3.0×1011·L-1备用。
1.4 细胞培养上清液诱导人血小板聚集实验将N组、W组和B组培养8 d收集到的细胞上清液,进行编号分别为①、②、③。将收集到的健康人PRP加入刺激剂(正常低糖组、稳定性高糖组和波动性高糖组分别加①、②、③号上清液、阿司匹林干预组加③号上清液)10 μL进行温育处理。应用血小板聚集仪进入测试状态,在窗口读取血小板最大聚集率。
1.5 动物模型制备与分组60只SD大鼠经普通饲料适应性喂养2周后,随机抽取10只作为正常对照组(N组)。对余下50只进行定时高糖高脂饲料喂食4周,给予1次性经腹腔注射链脲佐菌素(30 mg·kg-1),3 d后测定模型大鼠空腹和餐后2 h血糖,以空腹血糖大于11.1 mmol·L-1且餐后血糖不大于33.3 mmol·L-1做为入组标准,成功纳入2型糖尿病大鼠32只分为:稳定高糖组(W组,11只):每日定时喂食低GI饲料; 波动高糖组(B组,11只):每日定时喂食高GI饲料; 波动高糖+阿司匹林组(ASA组,10只):根据《中药药理研究方法学》实验动物与人按体表面积比等效剂量换算表,换算阿司匹林用药剂量[6]。即每日定时喂食高GI饲料,并按60 mg·kg-1·d-1灌服阿司匹林混悬液。正常组(N组,10只):每日定时喂食基础饲料,并灌服等体积蒸馏水。各组干预6周后,大鼠腹主动脉采血,5 mL促凝血分离血清,用于生化指标、内皮损伤指标检测; 采集1 mL 3.8%枸橼酸钠(pH 7.4)1 :9抗凝血取材,用于流式细胞术检测。
1.6 检测指标 1.6.1 大鼠体重和血清生化指标的测定采用己糖激酶法测定大鼠空腹血糖(fasting plasma glucose,FPG),采用酶法测定血清总胆固醇(total cholesterol,TC)和甘油三酯(triglycerides,TG),采用酶联免疫吸附实验(ELISA)法测定空腹胰岛素(fasting insulin,FINS)水平。
1.6.2 内皮损伤指标检测大鼠腹主动脉采血,5 mL促凝血分离血清,采用ELISA法检测细胞培养上清液和大鼠血清可溶性E-选择素(sE-selectin)和血管性假性血友病因子(von Willebrand factor,vWF)水平。
1.6.3 大鼠血小板膜蛋白CD62p水平测定流式细胞术检测血小板膜蛋白CD62p表达,于采血2 h内完成检测。
1.6.4 血小板聚集率测定应用血小板聚集仪进行测定,读取血小板最大聚集率。
1.7 统计学分析实验数据均采用SPSS 13.0软件进行处理。所有资料以x±s表示,多组间比较用单因素方差分析。
2 结果 2.1 各组大鼠体质量及血糖、血脂水平如Tab 1所示,与N组相比,W组和B组糖尿病大鼠血清FPG、TC、TG均明显升高(P < 0.01),大鼠体质量和FINS明显降低(P < 0.01),但W组和B组比较,差异无统计学意义(P>0.05)。与B组相比,阿司匹林对大鼠体质量、血糖、血脂水平无明显作用。
| Group | Weight/ g | FPG/mmol • L-1 | FINS/g • L-1 | TC/mmol • L -1 | TG/mmol • L -1 |
| N | 556.00 ±40.06 | 5. 97 ±102 | 1.24 ±0.36 | 1.32 ±0.20 | 1.02±0.41 |
| W | 438.25 ±39.46** | 18.55 ±3.66** | 0.56±0.13** | 2.15 ±0.38** | 2. 00 ± 0.39** |
| B | 415.13 ±66.36** | 18.08 ±4.14** | 0.55 ±0.14** | 2.48 ±0.50** | 2.31 ± 0.45** |
| ASA | 415.71 ±15.43 ** | 19.00 ±2.83** | 0.68 ±0.40** | 2.43 ±0.62** | 2. 09 ±0.37** |
| N:normal glucose; W: steady high glucose; B: fluctuant high glucose; ASA: aspirin group. **P < 0.01 vs N group | |||||
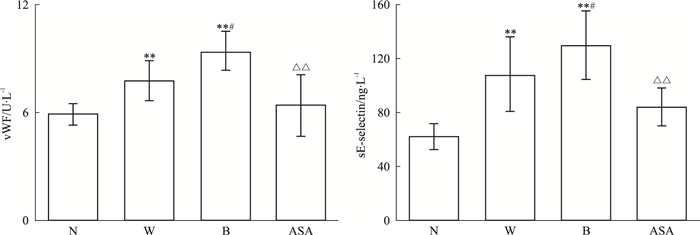
如Fig 1所示,与N组相比,W组和B组细胞上清vWF和sE-selectin含量明显增多(P < 0.01),且B组与W组之间差异具有显著性(P < 0.05);ASA干预后,细胞上清vWF和sE-selectin含量均明显下降(P < 0.01)。
|
| Fig 1 Effects of aspirin on levels of vWF, sE-selectin in HUVECs with high glucose fluctuation N:normal glucose; W: steady high glucose; B: fluctuant high glucose; ASA: aspirin group. **P < 0.01 vs N group; #P < 0.05 vs W group; △△P < 0.01 vs B group |
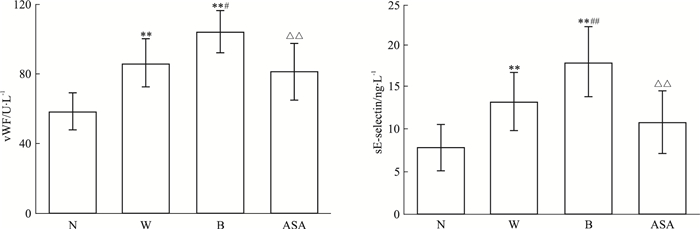
与N组相比,W组和B组T2DM大鼠血清vWF、sE-selectin水平均明显升高(P < 0.01),且B组更加明显(P < 0.05,P < 0.01);与B组相比,ASA组大鼠血清vWF、sE-selectin水平明显降低(P < 0.01)。见Fig 2。
|
| Fig 2 Effects of aspirin on serum vWF, sE-selectin of T2DM rats with high glucose fluctuation N:normal glucose; W: steady high glucose; B: fluctuant high glucose; ASA: aspirin group. **P < 0.01 vs N group; #P < 0.05, ##P < 0.01 vs W group; △△P < 0.01 vs B group |
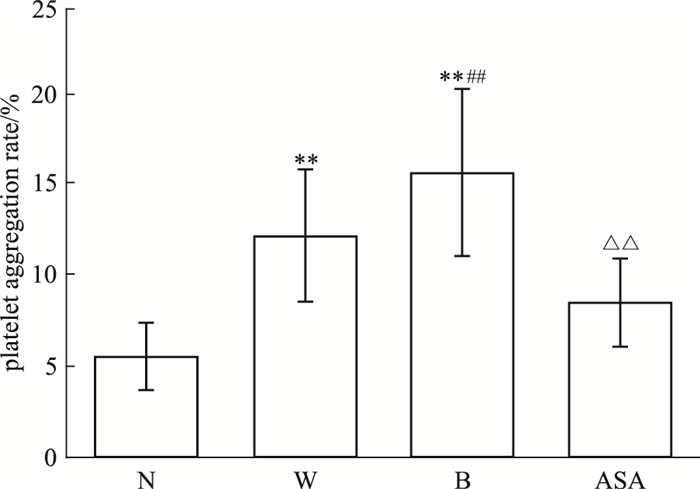
如Fig 3所示,与N组相比,W组和B组健康人外周血血小板最大聚集率均明显增高(P < 0.01),且B组与W组之间差异有显著性(P < 0.01);运用ASA药物预处理15 min后,波动性高糖诱导的血小板最大聚集率明显降低(P < 0.01)。
|
| Fig 3 Effects of aspirin on platelet maximumaggregation rate in HUVECs with high glucose fluctuation N:normal glucose; W: steady high glucose; B: fluctuant high glucose; ASA: aspirin group. **P < 0.01 vs N group; ##P < 0.01 vs W group; △△P < 0.01 vs B group |
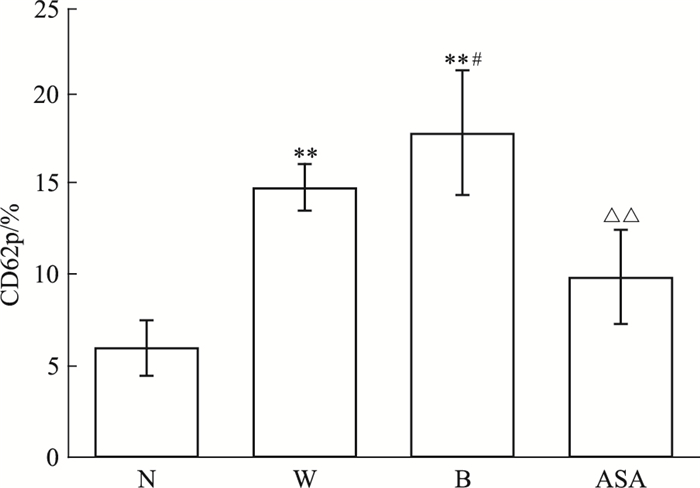
与N组相比,W组和B组大鼠血小板膜蛋白CD62p表达均明显增多(P < 0.01),且B组与W组之间差异有显著性(P < 0.05);应用ASA干预后,大鼠血小板膜蛋白CD62p表达明显下降(P < 0.01)。见Fig 4。
|
| Fig 4 Effects of aspirin on platelet membrane proteinlevel of CD62p in T2DM rats with high glucose fluctuation N:normal glucose; W: steady high glucose; B: fluctuant high glucose; ASA: aspirin group. **P < 0.01 vs N group; #P < 0.05 vs W group; △△P < 0.01 vs B group |
血小板的高活性状态是糖尿病血管病变的一个重要因素[7]。血小板活化、黏附、聚集于血管内皮损伤部位,释放生长因子,促进平滑肌增殖,导致动脉粥样硬化,引起糖尿病大血管病变; 血小板的高黏附、高聚集状态造成微循环淤滞,导致组织缺氧,又可引起糖尿病的微血管病变[8]。因此,在T2DM早期有效抗血小板活化治疗对于预防糖尿病血管病变的发生、发展具有积极的临床意义。血糖波动性在糖尿病血管损伤中的作用已经为大家所公认,然而其在促进血小板活化中所发挥的作用尚不明确。
vWF是血管内皮功能异常的特异性表达分子。同时,vWF还具有明显诱导血小板聚集的功能[9]。E-selectin是唯一仅限于活化的内皮细胞表面表达的黏附分子,是内皮细胞活化的一个重要标志[10]。CD62p是血小板活化的特异标志物[11],当血小板受到各种刺激时,才会大量表达于血小板膜表面,进而介导黏附反应,参与血栓形成过程和炎症反应的发生。本研究结果表明,稳定高糖和波动高糖均可诱导HUVECs中vWF和sE-selectin水平升高,且以波动组更为明显。进一步我们应用波动高糖和稳定高糖诱导HUVECs损伤上清液温浴健康人血小板,结果发现,二者均能明显诱导血小板聚集,且以波动组诱导的血小板聚集率升高明显。同时,体内实验研究也发现,在构建的T2DM血糖波动大鼠中出现了明显的血管内皮细胞损伤,同时大鼠血小板膜蛋白CD62p表达明显升高,表明其存在更为明显的血小板活化状态。
阿司匹林是临床常用药物,其治疗作用随剂量而有差异,具有良好的解热、镇痛、抗炎以及抑制血小板聚集等作用[12]。随着对该药研究的深入,近年来又发现了阿司匹林的一些新应用,包括心脑血管病、肿瘤、阿尔茨海默病、预防流产等。阿司匹林可通过抑制血小板活化聚集、抗炎、抗氧化等机制,延缓动脉粥样硬化的进程,因而也成为糖尿病患者心脑血管事件一、二级预防的基石[13]。本研究对其在血糖波动状态下的血管内皮功能及血小板活化状态的影响进行了研究。结果显示,阿司匹林不仅能够有效保护波动高糖所诱导的HUVECs和T2DM大鼠血管内皮细胞损伤,而且能有效抑制波动高糖诱导内皮损伤过程中所出现的血小板聚集和活化,提示阿司匹林在糖尿病预防中具有保护内皮和抗血小板活化的双重效应,但其确切的作用机制仍有待我们进行深入研究。
( 致谢: 本研究在中国中医科学院西苑医院心血管实验中心完成,感谢实验中心杨琳和缪宇老师给予的支持,感谢血液科实验室许勇钢老师在血小板膜蛋白CD62p检测中给予的帮助。)
| [1] | Rask-Madsen C, King G L. Vascular complications of diabetes: mechanisms of injury and protective factors[J]. Cell Metab, 2013, 17(1): 20-33. doi:10.1016/j.cmet.2012.11.012 |
| [2] | Linden M D, Tran H, Woods R, et al. High platelet reactivity and antiplatelet therapy resistance[J]. Semin Thromb Hemost, 2012, 38(2): 200-12. doi:10.1055/s-0032-1301417 |
| [3] | Tang W H, Stitham J, Gleim S, et al. Glucose and collagen regulate human platelet activity through aldose reductase induction of thromboxane[J]. J Clin Invest, 2011, 121(11): 4462-76. doi:10.1172/JCI59291 |
| [4] | Basevi V, Di Mario S, Morciano C, et al. Comment on: American Diabetes Association. Standards of medical care in diabetes-2011. Diabetes Care 2011;34(Suppl. 1):S11-S61[J]. Diabetes Care, 2011, 34(5): e53. |
| [5] | Jaffe E A, Nachman R L, Becker C G, et al. Culture of human endothelial cells derived from umbilical veins.Identification by morphologic and immunologic criteria[J]. J Clin Invest, 1973, 52(11): 2745-56. doi:10.1172/JCI107470 |
| [6] | 陈奇. 中药药理研究方法学[M]. 北京: 人民卫生出版社, 1993: 1103. Chen Q. Research methodology of traditional Chinese medicine pharmacology[M]. Beijing: People′s Medical Publishing House, 1993: 1103. |
| [7] | Ravindran R, Krishnan L K. Increased platelet cholesterol and decreased percentage volume of platelets as a secondary risk factor for coronary artery disease[J]. Pathophysiol Haemost Thromb, 2007, 36(1): 45-51. doi:10.1159/000112639 |
| [8] | Schäfer A, Bauersachs J. Endothelial dysfunction, impaired endogenous platelet inhibition and platelet activation in diabetes and atherosclerosis[J]. Curr Vasc Pharmacol, 2008, 6(1): 52-60. doi:10.2174/157016108783331295 |
| [9] | Colwell J A, Nesto R W. The platelets in diabetes: focus on prevention of ischemic events[J]. Diabetes Care, 2003, 26(7): 2181-8. doi:10.2337/diacare.26.7.2181 |
| [10] | Nadar S, Blann A D, Lip G Y. Endothelial dysfunction: methods of assessment and application to hypertension[J]. Curr Pharm Des, 2004, 10(29): 3591-5. doi:10.2174/1381612043382765 |
| [11] | Ferroni P, Martini F, Riondino S, et al. Soluble P-selectin as a marker of in vivo platelet activation[J]. Clin Chim Acta, 2009, 399(1-2): 88-91. doi:10.1016/j.cca.2008.09.018 |
| [12] | 李才正, 苗佳. 阿司匹林的临床应用进展[J]. 华西医学, 2012, 27(7): 988-91. Li C Z, Miao J. Clinical application progress of aspirin[J]. West China Med J, 2012, 27(7): 988-91. |
| [13] | 郎艳松, 秘红英, 刘红利, 等. 通心络联合阿托伐他汀、阿司匹林对家兔动脉粥样硬化早期血管外膜滋养血管新生的干预作用[J]. 中国药理学通报, 2015, 31(1): 71-6. Lang Y S, Mi H Y, Liu H L, et al. Interventional effects of Tongxinluo combined with atorvastatin and aspirin(ATS) on the angiogenesis of vasa vasorum in the early stage of atherosclerosis[J]. Chin Pharmacol Bull, 2015, 31(1): 71-6. |

