




肝细胞癌(hepatocellular carcinoma,HCC)是我国常见的恶性肿瘤之一,一般由慢性肝炎-肝纤维化-肝硬化-HCC的顺序逐渐演变而来。由于HCC的发病机制尚不明确,目前仍缺少有效的防治措施。HCC的中药治疗是其防治的重要研究方向。丹参是治疗肝纤维化最常用的中药之一,丹酚酸B(salvianolic acid B,Sal B)是其水溶性提取物之一。通过双盲双模拟临床观察与治疗前后肝组织病理活检,证实Sal B能有效逆转慢性乙型肝炎-肝纤维化[1]。Sal B通过抑制肝星状细胞(hepatic stellate cell,HSC)活化,减少胶原纤维的沉积而发挥抗肝纤维化作用。有研究报道,Sal B高浓度可抑制肝癌HepG2细胞的增殖[2],促进其凋亡[3]。
转化生长因子-β1(transforming grow factor beta 1,TGF-β1)是一种重要的细胞生长和分化调节因子,其介导的TGF-β1/Smad信号转导通路在肝纤维化-HCC的发生、发展中发挥重要作用[4-5]。研究表明,Smad3不同位点磷酸化在HCC的发生发展中发挥不同的效应,其C-末端活化形式pSmad3C,靶向下游基因p21,介导肿瘤抑制信号,而其连接区活化形式pSmad3L,靶向下游基因纤溶酶原激活物抑制剂-1(plasminogen activator inhibitor 1,PAI-1)及c-Myc,介导促纤维化-癌变信号[6]。我们推测,Sal B可能通过干预pSmad3C/pSmad3L而发挥抗肝纤维化-HCC作用。因此,本研究建立二乙基亚硝胺(diethylnitrosamine, DEN)诱导的小鼠肝纤维化-HCC模型,观察Sal B对小鼠肝纤维化-HCC进程的影响,并探讨Sal B经由pSmad3C/p21、pSmad3L/PAI-1/c-Myc信号的调控机制。
1 材料与方法 1.1 药品与试剂DEN(0.95 kg·L-1)购于美国Sigma公司;Sal B(纯度≥95%, 批号:PS12091001)、秋水仙碱(colchicine,Col)(纯度≥98%,批号:PS08092201),购自成都普思生物科技股份有限公司。Western blot及IP细胞裂解液、PMSF购自上海碧云天生物技术有限公司;兔抗pSmad3L(linker-phosphorylated Smad3)多克隆抗体由日本关西医科大学松崎教授惠赠;兔抗pSmad3C(C-terminally phosphorylated Smad3)单克隆抗体购自Cell Signaling Technology公司;兔抗PAI-1(PA5-27216)多克隆抗体购自Thermo Fisher Scientific公司;兔抗c-Myc(ab32072)单克隆抗体购自Abcam公司;小鼠抗p21单克隆抗体(556430)购自BD Biosciences公司;小鼠抗GAPDH单克隆抗体、辣根过氧化物酶标记山羊抗兔IgG、辣根过氧化物酶标记山羊抗小鼠lgG,均购自北京中杉金桥;苦味酸、品红,购自西陇化工股份有限公司。
1.2 DEN诱导小鼠肝纤维化-HCC模型建立及SalB干预♂昆明系小鼠,体质量(20±2)g,SPF级,安徽医科大学实验动物中心提供,许可证号:scxk(皖)2011-002。100只♂小鼠,随机分成5组:正常对照组、模型组、Sal B低剂量(15 mg·kg-1)组、Sal B高剂量(30 mg·kg-1)组、阳性药物Col(0.2 mg·kg-1)组,每组20只。正常对照组小鼠腹腔注射无菌生理盐水,其余组小鼠给予1.0% DEN溶液(无菌生理盐水配置)诱导肝纤维化-HCC模型,按体质量10 mL·kg-1给药,每周1次,连续16周。于造模当天开始,Sal B组小鼠分别给予15、30 mg·kg-1·d-1 Sal B灌胃,阳性药物组小鼠给予0.2 mg·kg-1·d-1 Col灌胃,正常对照组小鼠给予相应溶媒灌胃,持续给药至16周末。于第12周末处死小鼠5只,16周末处死小鼠8只,取材,进行组织固定、病理检测或蛋白表达检测。
1.3 检测指标 1.3.1 一般状况实验过程中定期观察记录小鼠进食状况、体重变化、活动情况及外表征象。
1.3.2 肝脏指数小鼠处死后,切取全部肝脏,生理盐水清洗血迹,滤纸吸干,称取肝脏重量(Wl)、体质量(Wb),计算肝脏指数(Wl/Wb)×100%。
1.3.3 病理观察切取肝脏左叶,4%多聚甲醛溶液固定48 h,脱水,常规石蜡包埋,4 μm切片,烤片;梯度酒精脱蜡,水化,苏木精-伊红(hematoxylin-eosin,HE)染色。常规脱水,透明,干燥,中性树胶封片。按照标准操作规范,使用数字扫描仪显微镜随机拍摄肝细胞团显微照片5张,由病理医师阅片、诊断和评价,确定肝脏病变程度。
1.3.4 Van Gieson(VG)染色配制VG染液:A液,1%酸性品红水溶液;B液,苦味酸饱和水溶液,临用前按A :B=1 :9的比例混合。石蜡切片常规脱蜡至水,蒸馏水洗,用滤纸吸干水分,VG染液染色5 min左右,95%酒精分化,无水乙醇脱水,二甲苯透明,中性树胶封片,显微镜下观察胶原纤维分布情况。
1.4 Western blot法检测pSmad3C、pSmad3L、p21、PAI-1、c-Myc蛋白表达常规方法提取小鼠肝组织中细胞总蛋白,十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)电泳、转膜,5%脱脂奶粉封闭,分别以小鼠抗GAPDH、兔抗pSmad3C、兔抗pSmad3L、小鼠抗p21、兔抗PAI-1、兔抗c-Myc抗体4℃孵育过夜,TBST洗膜3次,每次10 min,继而以相应的辣根过氧化物酶标记lgG常温孵育90 min,TBST洗膜3次,每次10 min,ECL法曝光显影。采用Image J软件对Western blot检测结果进行灰度分析,分析结果以目的蛋白与内参蛋白GAPDH条带的比值表示。
1.5 统计学处理计量资料用x±s表示,采用SPSS16.0软件对定量资料进行统计学分析,多组均数之间两两比较采用单因素方差分析。
2 结果 2.1 Sal B可改善DEN诱导的肝纤维化-HCC小鼠的一般状况正常组小鼠饮食好,活泼好动,反应灵活,背毛柔顺有光泽,体重明显增加;模型组小鼠在诱癌初期,食欲良好,体重未减轻,12周后,模型组小鼠出现皮毛枯槁无光泽、食欲不振、活动减少等表现,体重逐渐减轻;和模型组比较,Sal B组症状改善,食欲增加,精神状况较好。DEN诱导小鼠肝纤维化-HCC过程中,部分小鼠因耐受能力较差,出现灌药后死亡等,至DEN诱癌第16周取材时统计,各组小鼠死亡率分别为正常对照组(0/20,0.0%)、模型组(7/20,35.0%)、Sal B低剂量组(5/20,25.0%)、Sal B高剂量组(3/20,15.0%)、Col组(6/20,30.0%)。
2.2 Sal B对DEN诱导的肝纤维化期小鼠体质量与肝脏系数的影响与正常组相比,12周末时,模型组小鼠体质量、肝重与肝脏系数明显降低;与模型组比较,Sal B组小鼠体质量与肝重有增加的趋势,肝脏系数无明显变化(Tab 1)。
| Group | Dose/mg • kg-1 | Body weight/g | Liver weight/g | Liver index/% |
| Control | - | 55.0 ±3.406 | 2. 829 ±0.187 | 5.156 ±0.367 |
| Model | - | 27.2±2.638## | 0.851 ±0.188## | 3.103 ±0.445## |
| Sal B | 15 | 28.6 ±3.666 | 0.887±0.172 | 3.080±0.233 |
| Sal B | 30 | 27.4±1.019 | 0.805±0.077 | 2.937±0.265 |
| Co | 0.2 | 27. 8 ±0.980 | 0.889±0.152 | 3.188±0.481 |
| ##P < 0.01 vs control | ||||
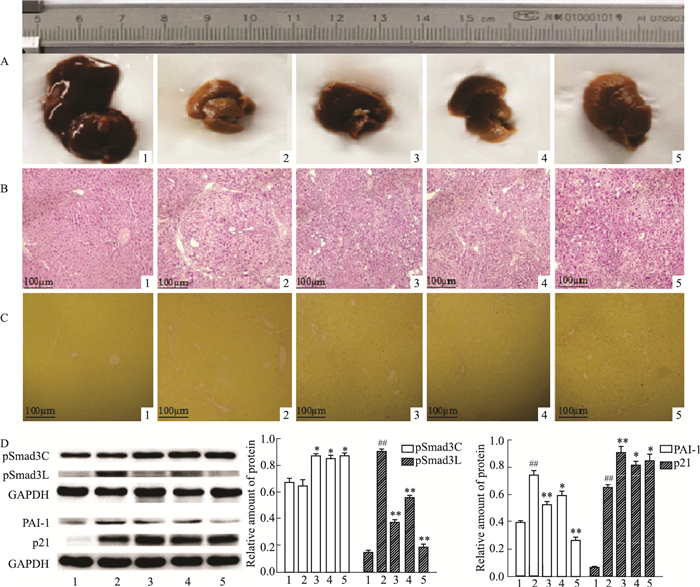
Fig 1A小鼠肝脏大体可见,正常组小鼠肝脏表面光滑,边缘锐利,质地柔软;12周末模型组小鼠肝脏表面粗糙,边缘变钝;与模型组比较,Sal B组小鼠肝脏表面较光滑,质地较柔软,症状改善。
|
| Fig 1 Effects of Sal B on hepatic fibrosis induced by DEN in mice (HE, × 100; VG, × 100) A: General appearance of liver; B: HE staining of liver tissue; C: VG staining of liver tissue; D: Protein expression detected by Western blot. 1: Control; 2: Model; 3: Sal B 15 mg·kg-1; 4: Sal B 30 mg·kg-1; 5: Col. ##P<0.01 vs control; *P<0.05, **P<0.01 vs model. |
如Fig 1B、1C所示,第12周时,光镜所见,正常组小鼠肝小叶结构完整,有肝小叶和汇管区,VG阳性胶原纤维仅局限于门管区和小叶间静脉周围;模型组肝组织炎性细胞浸润,胶原纤维增生,大量胶原纤维分隔肝小叶结构形成假小叶结构;Sal B组炎细胞浸润、胶原纤维增生均轻于模型组,未形成假小叶结构。Sal B组小鼠肝组织病变程度减轻。提示第12周为纤维化病变期,Sal B具有抗肝纤维化的作用。
2.5 Sal B对DEN诱导的肝纤维化期小鼠肝组织中pSmad3C、pSmad3L、PAI-1、p21蛋白表达的影响Fig 1D Western blot结果显示,12周时,正常肝组织中pSmad3C、pSmad3L、PAI-1蛋白表达均较少,p21蛋白几乎不表达;与正常组相比,模型组肝组织中pSmad3C蛋白无明显变化,p21蛋白表达增多,pSmad3L和PAI-1蛋白表达明显增多;与模型组比较,Sal B组肝组织中pSmad3C、p21蛋白水平明显升高,pSmad3L、PAI-1蛋白水平明显降低。提示Sal B抗小鼠肝纤维化时,升高pSmad3C、p21蛋白,降低pSmad3L和PAI-1蛋白的表达。
2.6 Sal B对DEN诱导的小鼠HCC癌前阶段体质量与肝脏系数的影响16周末时,与正常组相比,模型组小鼠体质量、肝重与肝脏系数明显减少;与模型组比较,Sal B组小鼠体质量、肝重与肝脏系数明显增加, 差异均具有统计学意义(Tab 2)。
| Group | Dose/mg·kg-1 | Body weight/g | Liver weight/g | Liver index/% |
| Contol | - | 53.25 ±4.576 | 2.385 ±0.187 | 4.492±0.336 |
| Model | - | 26.63 ±2.342## | 0.866 ±0.142## | 3.241 ±0.385## |
| SalB | 15 | 29.50 ±2.646* | 1.155 ±0.290* | 3.869 ±0.643* |
| Sal B | 30 | 28.25 ±1.920 | 1.103 ±0.232* | 3.881 ±0.650* |
| Co | 0.2 | 29.71 ±2.249 | 1.193 ±0.217* | 4.015 ±0.642* |
| ##P < 0.01 vs control; *P < 0.05 vs model | ||||
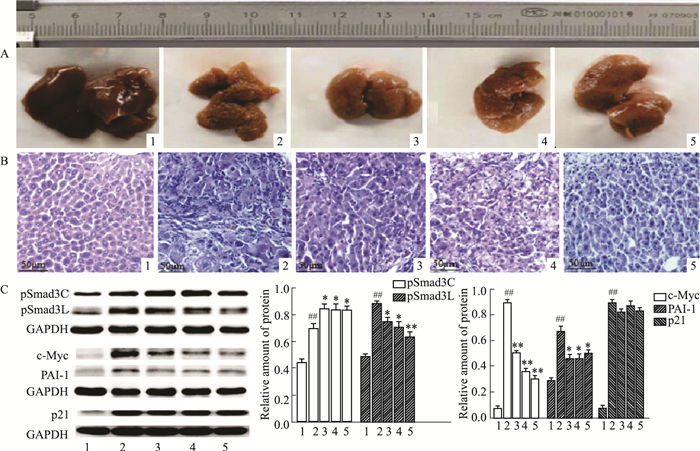
由小鼠肝脏大体所见,正常组小鼠肝脏表面光滑,边缘锐利,质地柔软;16周末,模型组肝脏表面粗糙,出现大量弥漫性结节,质地坚硬;与模型组比较,Sal B组小鼠肝脏结节少,质地柔软,症状改善(Fig 2A)。
|
| Fig 2 Effects of Sal B on precancerous lesion of hepatocellular carcinoma induced by DEN in mice (HE, × 100) A: General appearance of liver; B: HE staining of of liver tissue; C: Protein expression detected by Western blot. 1: Control; 2: Model; 3: Sal B 15 mg·kg-1; 4: Sal B 30 mg·kg-1; 5: Col. ##P<0.01 vs control; *P<0.05, **P<0.01 vs model. |
如Fig 2B所示,16周时光镜下所见,正常组肝组织细胞围绕中央静脉呈放射状有序排列,相邻肝板吻合连接成网状,肝细胞核圆,位于细胞中央,着色较浅,肝细胞无明显变性与坏死;模型组肝小叶结构紊乱,肝细胞坏死发生在肝小叶内、累及肝细胞点状坏死,坏死灶原有细胞消失,代以浸润的淋巴细胞。增生肝细胞具有癌细胞样异型性,表现为细胞体积变大,且大小不一致,同时,肝细胞核体积变大,染色变深,分裂相增多;Sal B组肝细胞坏死、炎细胞浸润、纤维组织增生、细胞核异型性均轻于模型组。提示16周为癌前病变期。12周、16周Sal B组小鼠肝组织病变程度均明显减轻。Sal B延缓DEN诱导的小鼠肝纤维化-HCC进程。
2.9 Sal B对DEN诱导的HCC癌前病变期小鼠肝组织中pSmad3C、pSmad3L、c-Myc、PAI-1、p21蛋白表达的影响Fig 2C Western blot结果显示,16周末,正常肝组织中pSmad3C、pSmad3L、PAI-1表达均较少,c-Myc、p21蛋白几乎不表达;与正常组相比,模型组肝组织中pSmad3C、P21蛋白表达增多,pSmad3L、c-Myc、PAI-1蛋白表达明显增多;与模型组比较,Sal B组肝组织中pSmad3C蛋白水平明显升高,p21蛋白水平几乎无变化,pSmad3L、c-Myc、PAI-1蛋白水平明显降低。提示Sal B延缓小鼠肝纤维化-HCC进程时,升高pSmad3C蛋白水平,降低pSmad3L、PAI-1、c-Myc蛋白的表达。
3 讨论DEN作为N-亚硝基类物质的一种,是遗传毒性致癌物,其诱导HCC发生,一般经过慢性肝炎-肝纤维化-肝硬化-癌前病变-HCC等病变过程,与人类肝癌发病进程相似[7]。小鼠具有可基因干预发现靶点的优势,DEN诱发小鼠肝脏癌前病变被用于预防肝癌药物筛选的理想动物模型[8-9]。本实验采用DEN腹腔注射给药,实验结果表明,DEN能够成功诱导小鼠肝纤维化、肝脏癌前病变模型。小鼠出现一般状态不良、体质量与肝脏重量降低、肝系数下降,炎细胞浸润、肝细胞变性、胶原纤维增生,12周末出现假小叶结构,16周末增生肝细胞核异型性明显,分别具备肝纤维化、HCC癌前病变的基本特征。
丹参为唇形科鼠尾草属植物丹参的根,其味苦,微寒,归心、肝经,具有活血祛瘀、通经止痛、清心除烦、凉血消痛的功效。近年来,丹参、丹参复方制剂及丹参有效成分在慢性肝病治疗,尤其是抗肝纤维化中得到广泛应用,其中丹参有效成分研究进展迅速。Sal B是丹参中含量最高的活性成分[10],也是水溶性成分中研究最多的成分之一。Sal B可抑制和减轻四氯化碳(carbon tetrachloride,CCl4)、二甲基亚硝胺(dimethylnitrosamine,DMN)、TGF-β1诱导的大鼠肝纤维化。临床试验也显示,Sal B可明显逆转乙肝患者的肝纤维化。本次实验中,DEN诱导的小鼠肝纤维化阶段,与模型组比较,Sal B组炎性细胞浸润,纤维增生明显减轻。DEN诱导的小鼠肝癌癌前阶段,Sal B组小鼠体质量、肝重、肝脏系数明显增加,肝细胞坏死、细胞异型性均轻于模型组。表明Sal B具有抗DEN诱导小鼠肝纤维化-HCC的作用,可以延缓小鼠肝纤维化-HCC疾病进程,对小鼠肝纤维化和肝癌前病变具有防治作用。
体内外实验表明,Sal B抗肝纤维化作用可能与TGF-β1/Smad信号转导通路有关。Sal B可抑制HSC中TGF-β1表达及其激酶的活性,抑制胞内Smad2、Smad3的表达,Smad2的磷酸化及核转位[11-12]。近年研究表明,TGF-β1/Smad信号转导通路在HCC的发生、发展过程中具有双重作用。目前认为,这种双重作用与Smad3的C末端和L区磷酸化有关。在肝纤维化过程中,TGF-β1一方面通过TGF-β1/TβRI/pSmad3C/p21抑制肝纤维化的发生;另一方面,通过TGF-β1/MAPK/pSmad3L/PAI-1使得Smad3连接区磷酸化[13-14],促进胶原等细胞外基质(extracellular matrix,ECM)合成,同时促进下游靶基因PAI-1表达增强,抑制ECM降解,导致ECM过度堆积。本实验结果表明,正常小鼠肝脏中pSmad3C/p21与pSmad3L、PAI-1蛋白表达均较少,DEN组中pSmad3C p21表达无明显变化,pSmad3L和PAI-1表达明显增多,Sal B组pSmad3C与p21表达明显多于DEN组,pSmad3L和PAI-1表达明显少于DEN组。因此,Sal B可能一方面通过TGF-β1/TβRI,促进pSmad3C表达,进而激活其下游p21蛋白表达,抑制肝纤维化。同时,通过TGF-β1/JNK通路下调pSmad3L及其下游靶基因PAI-1的表达,减少肝组织中ECM的合成,进而延缓肝纤维化。
在HCC癌前阶段,TGF-β1与Ⅰ型受体结合,促使Smad3C磷酸化,pSmad3C促使p21表达增多,传递肿瘤抑制信号。p21抑制受损DNA的复制和积累,从而抑制细胞的生长和分裂,促进细胞凋亡。炎症因子激活JNK通路,促进pSmad3L表达,进而激活癌基因c-Myc表达,促使细胞增殖异常、细胞浸润而发生癌变,同时诱导PAI-1表达增多,促进肿瘤细胞浸润、转移,活化间充质细胞的ECM合成传递致瘤信号[15-16]。本实验结果表明,正常小鼠肝脏中pSmad3C、p21、pSmad3L、PAI-1、c-Myc蛋白表达均较少,DEN组pSmad3C表达无明显变化,p21、pSmad3L、PAI-1、c-Myc表达明显增多,Sal B组pSmad3L、PAI-1、c-Myc表达明显少于DEN组,pSmad3C表达多于DEN组,p21表达无明显变化。因此,Sal B的抗HCC作用可能主要通过抑制pSmad3L的表达,进而抑制其下游靶基因c-Myc和PAI-1表达,来阻碍HCC的发生发展。
综上,DEN诱导肝纤维化-HCC进程中,Sal B可能通过增强pSmad3C/p21介导的抑癌信号而减弱pSmad3L/PAI-1/c-Myc介导的促纤维化-癌变信号,阻碍肝纤维化-肝癌进程。
( 致谢: 本实验病理检测部分得到安徽省立医院病理科郭真理医师指导分析,在此由衷地表示感谢。)
| [1] | Liu P, Hu Y Y, Liu C, et al. Clinical observation of salvianolic acid B in treatment of liver fibrosis in chronic hepatitis B[J]. World J Gastroenterol, 2002, 8(4): 679-85. doi:10.3748/wjg.v8.i4.679 |
| [2] | Wang Q L, Wu Q, Tao Y Y, et al. Salvianolic acid B modulates the expression of drug-metabolizing enzymes in HepG2 cells[J]. Hepatobiliary Pancreat Dis Int, 2011, 10(5): 502-8. doi:10.1016/S1499-3872(11)60085-4 |
| [3] | 李艳, 张端莲, 王兰, 等. Sal B对肝癌细胞株HepG2的促凋亡作用[J]. 中国组织化学与细胞化学杂志, 2012, 21(1): 9-13. Li Y, Zhang R L, Wang L, et al. Sal B promotes apoptosis of human liver cancer cell line HepG2[J]. Chin J Histochem Cytochem, 2012, 21(1): 9-13. |
| [4] | Yoshida K, Murata M, Yamaguchi T, Matsuzaki K. TGF-β/Smad signaling during hepatic fibro-carcinogenesis[J]. Int J Oncol, 2014, 45(4): 1363-71. doi:10.3892/ijo.2014.2552 |
| [5] | Hu X P, Rui W J, Wu C, et al. Compound Astragalus and Salvia miltiorrhiza extracts suppress hepatocarcinogenesis by modulating transforming growth factor-β/Smad signaling[J]. J Gastroenterol Hepatol, 2014, 29(6): 1284-91. doi:10.1111/jgh.2014.29.issue-6 |
| [6] | 吴佳俊, 江宇峰, 伍超, 等. Smad3 WT、Smad3 EPSM、Smad3 3S-A 3种质粒稳转HepG2细胞株的建立与功能研究[J]. 中国药理学通报, 2016, 32(6): 825-31. Wu J J, Jiang Y F, Wu C, et al. Construction and functional study of three plasmids including Smad3 WT, Smad3 EPSM and Smad3 3S-A stably transfected HepG2 cell lines[J]. Chin Pharmacol Bull, 2016, 32(6): 825-31. |
| [7] | Lee J S, Chu I S, Mikaelyan A, et al. Application of comparative functional genomics to identify best-fit mouse models to study human cancer[J]. Nat Genet, 2004, 36(12): 1306-11. doi:10.1038/ng1481 |
| [8] | Tolba R, Kraus T, Liedtke C, et al. Diethylnitrosamine (DEN)-induced carcinogenic liver injury in mice[J]. Lab Anim, 2015, 49(1 Suppl): 59-69. |
| [9] | Sharma S, Gao P, Steele V E. Quantitative morphometry of respiratory tract epithelial cells as a tool for testing chemopreventive agent efficacy[J]. Anticancer Res, 2010, 30(3): 737-42. |
| [10] | Cheng T O. Cardiovascular effects of Danshen[J]. Int J Cardiol, 2007, 121(1): 9-22. doi:10.1016/j.ijcard.2007.01.004 |
| [11] | Liu C, Gaca M D, Swenson E S, et al. Smads 2 and 3 are differentially activated by transforming growth factor-beta (TGF-beta) in quiescent and activated hepatic stellate cells. Constitutive nuclear localization of Smads in activated cells is TGF-beta-independent[J]. J Biol Chem, 2003, 278(13): 11721-8. doi:10.1074/jbc.M207728200 |
| [12] | 刘成海, 刘平, 胡义扬, 朱大元. 丹酚酸B盐对转化生长因子-β1刺激肝星状细胞活化与胞内信号转导的作用[J]. 中华医学杂志, 2002, 82(18): 1267-72. Liu C H, Liu P, Hu Y Y, Zhu D Y. Effects of salvianolic acid-B on TGF-β1 stimulated hepatic stellate cell activation and its intracellula[J]. Natl Med J China, 2002, 82(18): 1267-72. doi:10.3760/j:issn:0376-2491.2002.18.014 |
| [13] | Yoshida K, Matsuzaki K, Mori S, et al. Transforming growth factor-beta and platelet-derived growth factor signal via c-Jun N-terminal kinase-dependent Smad2/3 phosphorylation in rat hepatic stellate cells after acute liver injury[J]. Am J Pathol, 2005, 166(4): 1029-39. doi:10.1016/S0002-9440(10)62324-3 |
| [14] | Urukawa F, Matsuzaki K, Mori S, et al. p38 MAPK mediates fibrogenic signal through Smad3 phosphorylation in rat myofibroblasts[J]. Hepatology, 2003, 38(4): 879-89. doi:10.1002/(ISSN)1527-3350 |
| [15] | Matsuzaki K, Kitano C, Murata M, et al. Smad2 and Smad3 phosphorylated at both linker and COOH-terminal regions transmit malignant TGF-beta signal in later stages of human colorectal cancer[J]. Cancer Res, 2009, 69(13): 5321-30. doi:10.1158/0008-5472.CAN-08-4203 |
| [16] | 芮文娟, 何淑芳, 黄先甲, 等. DEN诱导大鼠肝纤维化-肝癌过程中pSmad3L和PAI-1蛋白的表达[J]. 中国药理学通报, 2012, 28(10): 1393-7. Rui W J, He S F, Huang X J, et al. Expression of pSmad3L and PAI-1 during the process of DEN-induced hepatic fibrosis-carcinoma in rats[J]. Chin Pharmacol Bull, 2012, 28(10): 1393-7. |