


2. 重庆医科大学 重庆市生物化学与分子药理学重点实验室,重庆 400016
 ,
REN Wen-yan1,2,
LIAO Yun-peng1,2,
WANG Han1,2,
ZHU Jia-hui1,2,
HU Ying1,2,
LI Fu-shu1,2,
ZHOU Ya1,2,
HE Bai-cheng1,2
,
REN Wen-yan1,2,
LIAO Yun-peng1,2,
WANG Han1,2,
ZHU Jia-hui1,2,
HU Ying1,2,
LI Fu-shu1,2,
ZHOU Ya1,2,
HE Bai-cheng1,2

2. Chongqing Key Lab of Biochemistry and Molecular Pharmacology, School of Pharmacy, Chongqing Medical University, Chongqing 400016, China
汉防己甲素(tetrandrine,Tet)是一种双苄基异喹啉类生物碱,主要从多年生藤本防己科植物汉防己的块根中提取。Tet作为一种钙通道阻滞剂,具有多种药理作用,已在临床应用多年,主要用于治疗矽肺、自身免疫性疾病、炎症性肺部疾病、心血管疾病等。近年来研究表明,Tet对肝癌、结肠癌、前列腺癌等多种肿瘤细胞具有增殖抑制和促进凋亡的作用[1-3],并且对结肠癌还具有一定的预防作用[4]。除此之外,Tet对乳腺癌细胞也具有抑制增殖和促进凋亡的作用,机制可能与抑制PKC-α和逆转耐药等有关[5-6],但具体分子机制仍不十分清楚。
胰岛素样生长因子(insulin-like growth factors, IGFs)是一类与胰岛素具有高度同源序列的蛋白,IGFs与其受体结合后参与调节多种生理过程。IGFs信号受到胰岛素样生长因子结合蛋白(IGF binding proteins, IGFBPs)的调节。因此,当IGF信号异常时,可使细胞的多种生物学过程发生异常,最终导致肿瘤发生。其中,胰岛素生长因子结合蛋白5(IGFBP-5)表达异常与多种肿瘤有关。文献报道,乳胰癌的发生也与IGF信号异常有关[7]。课题组前期研究表明,Tet通过促进IGFBP-5表达抑制结肠癌细胞增殖,但Tet对乳腺癌的作用是否与IGFBP-5有关,目前还不清楚。因此,本研究选用人乳腺癌MCF-7细胞,分析Tet对乳腺癌的增殖抑制作用,并探讨IGFBP-5与Tet抑制乳腺癌细胞增殖作用的可能关系。
1 材料 1.1 细胞株及细胞培养人乳腺癌MCF-7细胞购自ATCC(American Type Culture Collection),用含10%胎牛血清,1%双抗(100 kU·L-1青霉素和100 mg·L-1链霉素)的DMEM培养基(高糖)培养。培养条件为37℃、5% CO2,待细胞生长至对数生长期时用0.25%胰酶消化传代。
1.2 试剂汉防己甲素购自Sigma-Aldrich公司;实验所用IGFBP-5、p53等一抗均购自Santa Cruz Biotechnology公司;CCK-8试剂盒购自上海七海复泰生物科技有限公司;Annexin V-FITC/PI试剂盒购自南京凯基生物科技有限公司。
1.3 仪器细胞培养箱(Thermo)、酶标仪(基因公司)、倒置显微镜(Nikon公司)、定量PCR仪(Bio-Rad)、流式细胞仪(BD公司)、电泳仪(北京六一)等。
2 方法 2.1 重组腺病毒的构建采用AdEasy系统构建IGFBP-5过表达和沉默IGFBP-5的siRNA片段重组腺病毒。过表达IGFBP-5(AdIGFBP-5)及沉默IGFBP-5(AdsiIGFBP-5)的重组腺病毒均由美国芝加哥大学何通川教授提供。仅表达绿色荧光蛋白(green fluorescent protein, GFP)的重组腺病毒(AdGFP)用作载体对照。
2.2 实验设计及分组按实验要求,将细胞分为对照组和实验组。采用二甲基亚砜(dimethyl sulphoxide,DMSO)溶解Tet,实验组细胞采用不同浓度Tet或Tet合并相应重组腺病进行处理,对照组细胞则用相同体积的DMSO和(或)GFP重组腺病毒进行处理。
2.3 CCK-8法检测细胞增殖将生长良好的MCF-7细胞消化后,接种到96孔板中,每孔2 000个细胞。待细胞贴壁后,按实验设计加入不同浓度的Tet(1、2、3、4、5 μmol·L-1)。分别于24、48、72 h后进行检测,每孔加入10 μL CCK-8试剂,放入孵箱孵育2 h后,用酶标仪在450 nm处测定吸光值,并绘制增殖曲线。每组实验重复3次。
2.4 流式细胞术检测细胞周期和凋亡将生长状态良好的MCF-7细胞均匀种于6孔板,待细胞贴壁后,用不同浓度的Tet(1、2、4 μmol·L-1)或同体积DMSO进行处理。48 h后收集细胞,按试剂盒说明书进行操作,然后上机检测进行周期分析。对细胞进行凋亡分析时,利用不含EDTA的胰酶消化并收集细胞,按试剂盒操作说明进行实验,然后通过流式细胞仪检测,进行凋亡分析。每组实验重复3次。
2.5 总RNA的提取与real-timePCR检测将生长状态良好的MCF-7细胞消化后,接种到T25培养瓶,等细胞贴壁后加入不同浓度的Tet(1、2、4 μmol·L-1)或同体积DMSO进行处理。利用TRIzol法提取总RNA,然后通过逆转录反应制备cDNA。最后通过real-time PCR检测目的基因mRNA表达水平变化情况。所用引物如下:GAPDH上游引物5′-CAACGAATTTGGCTACAGCA-3′, 下游引物5′-AGGGGAGATTCAGTGTGGTG-3′;IGFBP-5上游引物5′-CGTTTCAGCCCTCATTTAATTC-3′,下游引物5′-CAG TTTTCCCAGAATGAGGAAG-3′。每组实验重复3次。
2.6 Western blot实验将生长状态良好的MCF-7细胞消化后均匀种于6孔板,用不同浓度Tet(1、2、4 μmol·L-1)或同体积DMSO对细胞进行处理。按实验设计,在相应时间点提取各组总蛋白,按常规方法进行Western blot实验操作。最后,采用ECL试剂盒对目的条带进行显影并采集图像。每组实验重复3次。
2.7 统计学分析采用SPSS 11.0软件进行统计学分析,实验数据以x±s表示。数据用单因素分析,利用SNK检验法进行组间比较。
3 结果 3.1 Tet对MCF-7乳腺癌细胞生长的影响Fig 1A结果显示,不同浓度的Tet(1、2、3、4、5 μmol·L-1)在体外对乳腺癌MCF-7细胞的增殖有明显抑制作用,并呈现一定的时间和浓度依赖性。2 μmol·L-1 Tet在48 h时,即可明显诱导生长抑制。Fig 1B周期分析结果显示,Tet明显增加G1期细胞比例,降低S期细胞比例。Fig 1C的Western blot结果显示,Tet呈浓度依赖性降低PCNA蛋白水平。以上结果提示,Tet对乳腺癌细胞MCF-7的增殖有明显抑制作用。

|
| Fig 1 Effects of Tet on proliferation of MCF-7 cells A:CCK-8 assay results showed the anti-proliferation effect of Tet in MCF-7 cells (*P < 0.05, **P < 0.01 vs control). B: Cell cycle analysis results showed the cell cycle arrest effect of Tet in MCF-7 cells. C: Western blot assay results showed the effect of Tet on the level of PCNA in MCF-7 cells |
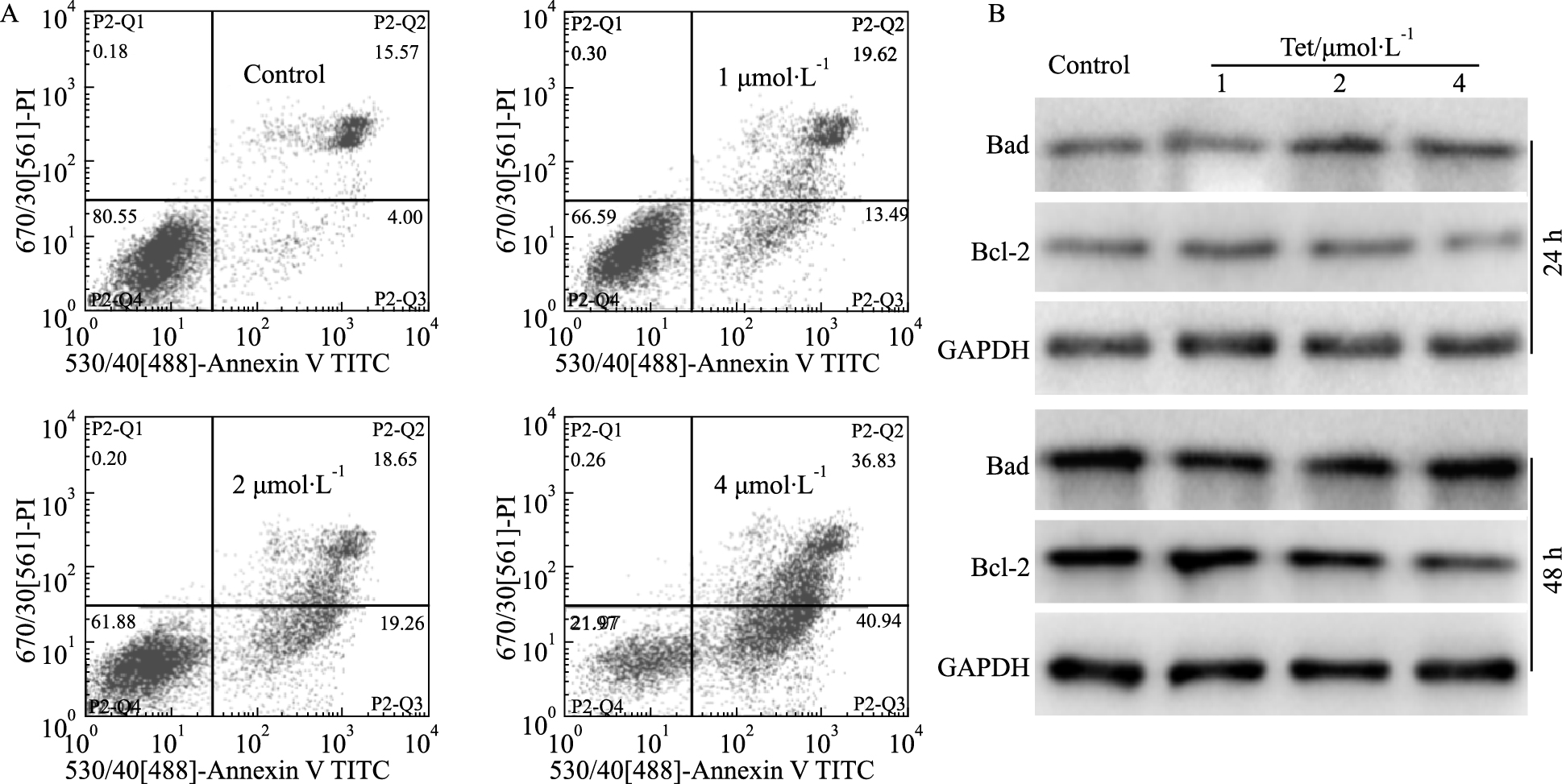
Fig 2A流式分析结果显示,Tet呈浓度依赖性增加MCF-7细胞的凋亡比例。Fig 2B Western blot结果显示,Tet升高Bad的蛋白水平,降低Bcl-2的蛋白水平。结果表明,Tet对乳腺癌MCF-7细胞的凋亡具有促进作用。
|
| Fig 2 Effects of Tet on apoptosis in MCF-7 cells A:Flow cytometric analysis results showed the effect of Tet on apoptosis in MCF-7 cells. B:Western blot assay results showed the effect of Tet on the level of Bad and Bcl-2 in MCF-7 cells. |
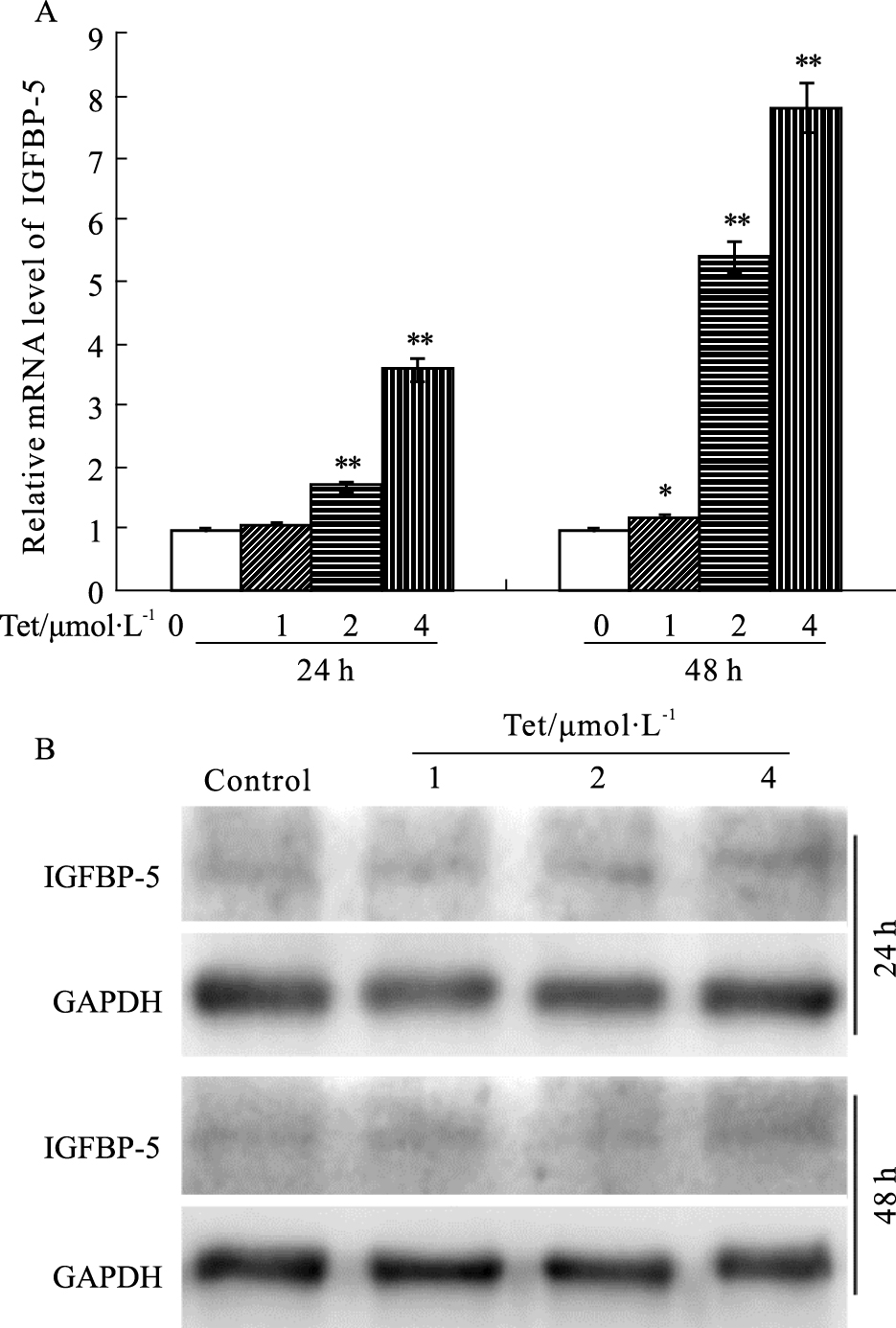
IGFs信号异常是肿瘤发生的重要原因之一。IGFBP-5对IGFs信号具有抑制作用,但IGFBP-5与乳腺癌的确切关系目前尚不十分清楚。因此,本研究拟分析Tet抑制乳腺癌MCF-7细胞增殖的作用是否与IGFBP-5有关。Fig 3A real-time PCR分析结果显示,Tet明显增加IGFBP-5的mRNA表达水平。Fig 3B Western blot结果也显示,Tet可增加IGFBP-5的蛋白水平。结果提示,Tet抑制MCF-7细胞增殖的作用可能与其上调IGFBP-5表达有关。
|
| Fig 3 Effects of Tet on IGFBP-5 in MCF-7 cells A:Real-time PCR assay results showed the effect of Tet on the expression of IGFBP-5 in MCF-7 cells (*P < 0.05, **P < 0.01 vs control). B:Western blot assay results showed the effect of Tet on the level of IGFBP-5 in MCF-7 cells. |
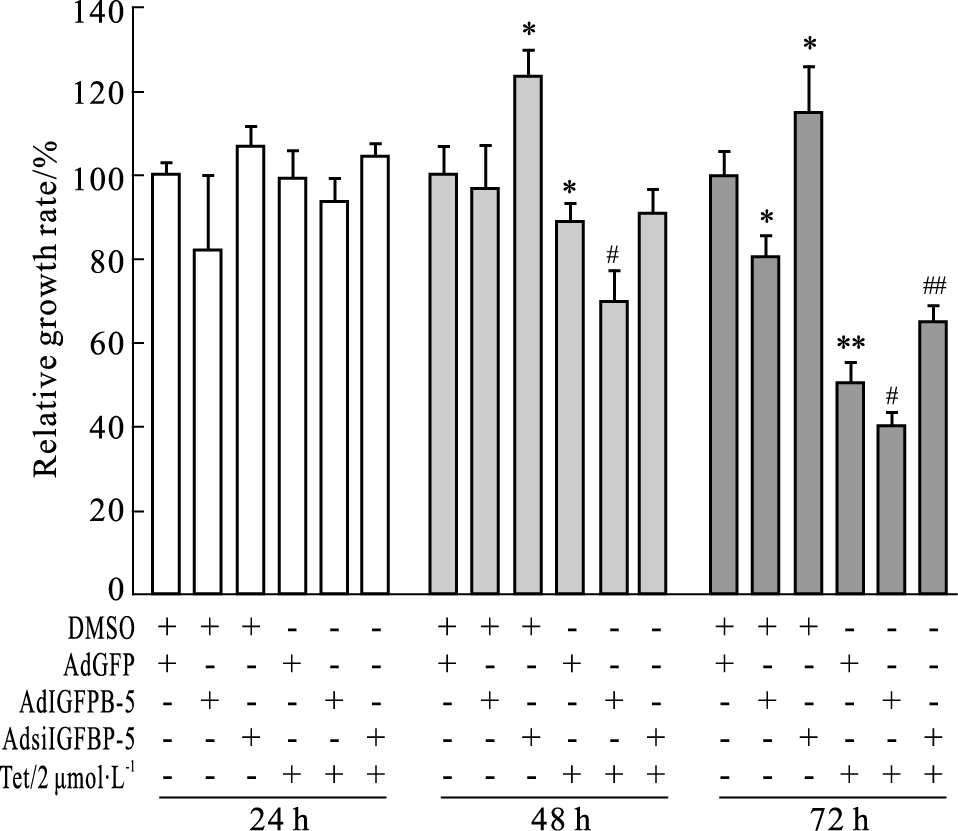
由于Tet在MCF-7细胞中明显促进IGFBP-5表达,提示Tet对MCF-7细胞的增殖抑制作用可能与IGFBP-5有关。Fig 4 CCK-8检测结果显示,高表达IGFBP-5能抑制MCF-7细胞增殖,并明显增强Tet对该细胞增殖的抑制作用;沉默IGFBP-5能促进MCF-7细胞增殖,同时减弱Tet对MCF-7细胞的增殖抑制作用。结果提示,IGFBP-5与Tet抑制MCF-7细胞增殖有关,但具体分子机制尚不清楚。
|
| Fig 4 Effects of IGFBP-5 on the anti-proliferation effect of Tet in MCF-7 cells CCK-8 assay results showed the effect of over-expression or knockdown IGFBP-5 on Tet-induced proliferation inhibition effect in MCF-7 cells (*P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs group treated with Tet alone). |
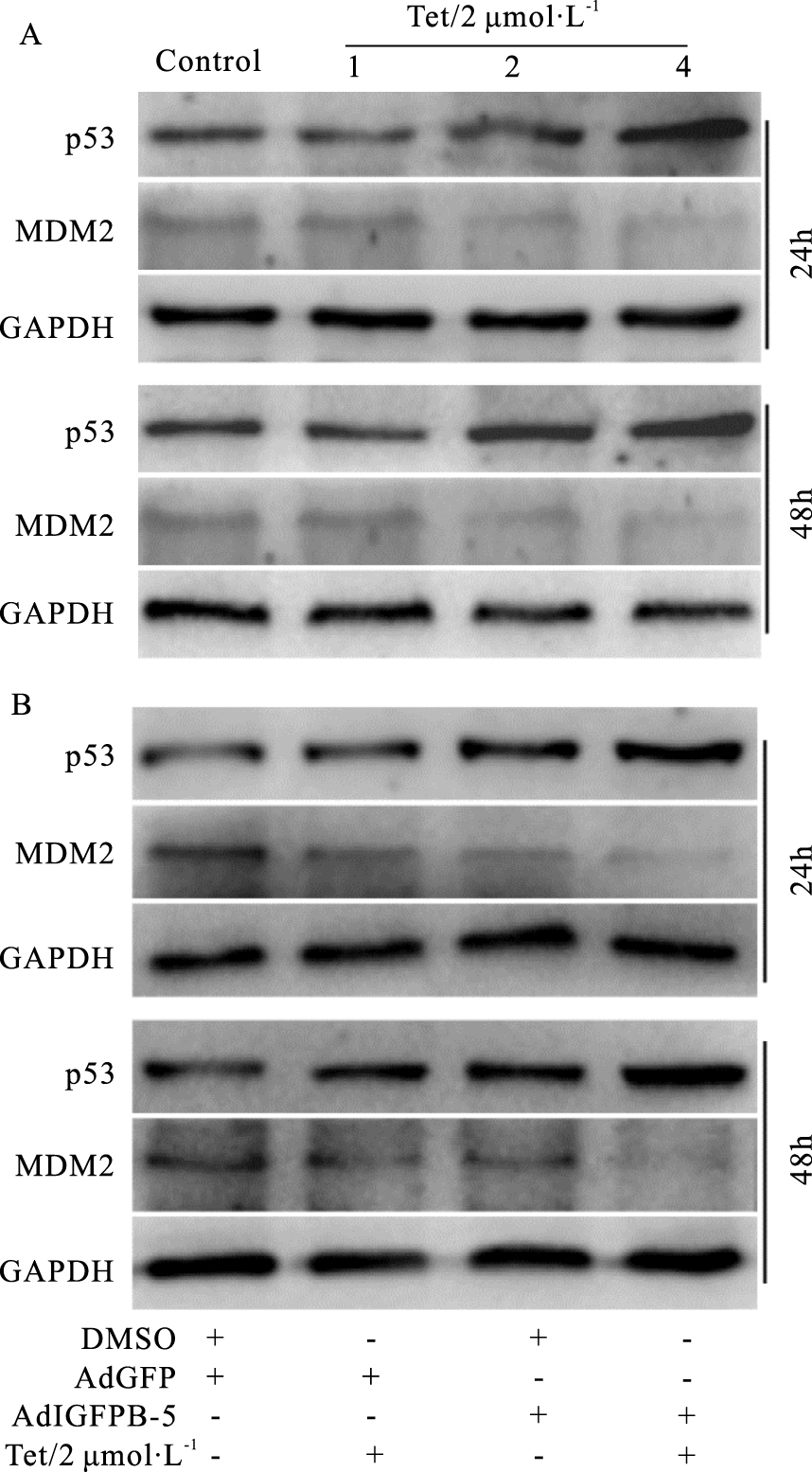
p53作为重要的肿瘤抑制因子,是抗肿瘤药物的重要靶点之一。因此,Tet对MCF-7细胞的增殖抑制作用可能也与p53有关。Western blot分析结果显示,Tet明显增加p53的蛋白水平,同时降低MDM2的水平(Fig 5A)。提示Tet抑制MCF-7细胞增殖可能与增加p53信号的功能有关,但Tet调节p53的机制尚不清楚。进一步分析结果表明,高表达IGFBP-5能增强Tet对p53表达的促进和对MDM2表达的抑制作用(Fig 5B)。以上实验结果提示,Tet对MCF-7细胞的增殖抑制作用可能与其上调IGFBP-5表达,进而增强p53信号的功能有关。
|
| Fig 5 Effects of Tet and/or IGFBP-5 on p53 and MDM2 in MCF-7 cells A: Western blot assay results showed the effect of Tet on the level of p53 and MDM2 in MCF-7 cells. B: Western blot assay results showed the effect of Tet and/or over-expression of IGFBP-5 on the level of p53 and MDM2 in MCF-7 cells. |
乳腺癌是最常见的侵袭性肿瘤之一,严重威胁女性健康。乳腺癌的治疗包括手术、放疗、化疗、靶向治疗等。近年来,乳腺癌的发生呈上升趋势,但随着早期筛查和诊断技术的发展,乳腺癌的治愈率有较大的提高。尽管如此,乳腺癌的预后仍不乐观,如何有效改善乳腺癌的预后仍面临巨大的挑战[8]。天然药物在肿瘤治疗的过程中发挥着重要作用,越来越多从天然药物来源的单体化合物被证明具有较好的抗肿瘤作用。本研究发现,Tet能明显抑制乳腺癌MCF-7细胞增殖,这种作用可能与Tet通过促进IGFBP-5表达而增强p53信号的功能有关。
Tet是从防己科植物粉防己干燥根中提取的一种二苄基异喹啉类生物碱。Tet因具有多种药理作用,在临床上可用于关节炎、神经痛、消化系统疾病的治疗[9]。研究表明,Tet还具有抗肿瘤作用,对多种肿瘤细胞具有明显增殖抑制和促进凋亡作用,如结肠癌、肝癌等[1-3]。本研究结果也显示,Tet对乳腺癌MCF-7细胞的增殖具有明显抑制作用,并能诱导其凋亡。因此,Tet可能对乳腺癌具有潜在的治疗效果。研究表明,Tet抗肿瘤作用的机制可能与抑制Wnt/β-catenin信号或促进p53表达等有关[2, 10]。但到目前为止,Tet抗肿瘤作用的确切机制仍不十分清楚。
IGFs信号对细胞增殖、分化和凋亡具有重要调节作用。因此,IGFs信号与胚胎及个体发育,以及肿瘤发生过程密切相关。该信号主要包括2种多肽生长因子配体(IGF-1和IGF-2),与IGFs结合的2种受体(IGF-1受体和IGF-2受体),7种能与IGFs结合的蛋白(IGFBP1-7),以及一系列参与降解IGFBPs的蛋白酶,该信号异常与多种肿瘤密切相关[11]。IGFBP-5作为一种IGFs结合蛋白,对IGF信号具有调控作用。研究表明,IGFBP-5表达异常与多种肿瘤的发生有关,如骨肉瘤、肝癌、乳腺癌等[12-13]。IGFBP-5对部分肿瘤细胞生长具有抑制作用,但对另外的一些肿瘤细胞生长具有促进作用。因此,IGFBP-5对肿瘤细胞生长的影响具有双向作用,原因可能与肿瘤细胞的微环境、细胞种类以及IGFBP-5各结构域的功能状态有关[14]。本研究发现,Tet能抑制乳腺癌MCF-7细胞增殖,同时上调IGFBP-5表达;高表达IGFBP-5增强Tet对MCF-7细胞增殖的抑制作用,而沉默IGFBP-5则减弱Tet对MCF-7细胞增殖的抑制作用。提示Tet对MCF-7细胞的增殖抑制作用可能与上凋IGFBP-5表达有关,但具体机制尚不清楚。
作为一种重要的肿瘤抑制因子,p53突变或表达异常与多种肿瘤的发生有关。对于p53水平较低的乳腺癌,可通过促进p53表达或抑制其降解,从而增强p53信号的功能而抑制肿瘤生长。文献报道,LQFM064能通过p53途径抑制MCF-7细胞增殖[15]。因此,p53可作为治疗某些类型乳腺癌的靶点。Tet对MCF-7乳腺癌细胞具有明显增殖抑制作用,而这种作用与上调IGFBP-5有关。提示,在MCF-7细胞中IGFBP-5表达水平增加可能与p53有关。本研究结果显示,Tet在MCF-7细胞中明显增加p53蛋白水平,降低MDM2的蛋白水平;高表达IGFBP-5增加p53水平,降低MDM2的水平;高表达IGFBP-5合并Tet则明显增加Tet对p53表达的促进和对MDM2表达的抑制作用。以上结果表明,IGFBP-5对MCF-7细胞增殖的抑制作用可能与其上调p53表达有关。
综上所述,本研究表明Tet能抑制乳腺癌MCF-7细胞增殖,这种作用可能与Tet通过上调IGFBP-5表达,进而增强p53信号的功能有关。但Tet调节IGFBP-5表达及IGFBP-5调节p53的机制尚需进一步深入研究。
| [1] | Lan J, Wang N, Lou H, et al. Design and synthesis of novel tetrandrine derivatives as potential anti-tumor agents against human hepatocellular carcinoma[J]. Eur J Med Chem, 2017, 127: 554-66. doi:10.1016/j.ejmech.2017.01.008 |
| [2] | He B C, Gao J L, Zhang B Q, et al. Tetrandrine inhibits Wnt/β-catenin signaling and suppresses tumor growth of human colorectal cancer[J]. Mol Pharmacol, 2011, 79(2): 211-9. doi:10.1124/mol.110.068668 |
| [3] | 任文艳, 陈前昭, 周林云, 等. 汉防已甲素抑制人结肠癌细胞增殖与TGF-1的关联机制研究[J]. 中国药理学通报, 2017, 33(9): 1227-33. Ren W Y, Chen Q Z, Zhou L Y, et al. Study on the relationship between the anti-proliferation effect of tetrandrine and TGF-β1 in human colon cancer cells[J]. Chin Pharmacol Bull, 2017, 33(9): 1227-33. |
| [4] | 王东旭, 袁霜雪, 伍秋香, 等. 胰岛素样生长因子结合蛋白5与汉防己甲素抑制人结肠癌细胞增殖的关系研究[J]. 中国药理学通报, 2015, 31(10): 1403-8. Wang D X, Yuan S X, Wu Q X, et al. Study on the relationship between insulin-like growth factor binding protein 5 and the anti-proliferation effect of tetrandrine in human colon cancer cells[J]. Chin Pharmacol Bull, 2015, 31(10): 1403-8. doi:10.3969/j.issn.1001-1978.2015.10.016 |
| [5] | Wong V K W, Zeng W, Chen J, et al. Tetrandrine, an activator of autophagy, induces autophagic cell death via PKC-α inhibition and mTOR-dependent mechanisms[J]. Front Pharmacol, 2017, 8: 351. doi:10.3389/fphar.2017.00351 |
| [6] | Cao X, Luo J, Gong T, et al. Coencapsulated doxorubicin and bromotetrandrine lipid nanoemulsions in reversing multidrug resistance in breast cancer in vitro and in vivo[J]. Mol Pharm, 2015, 12(1): 274-86. doi:10.1021/mp500637b |
| [7] | McKeown B T, Hurta R A. Magnolol affects expression of IGF-1 and associated binding proteins in human prostate cancer cells in vitro[J]. Anticancer Res, 2014, 34(11): 6333-8. |
| [8] | Rubovszky G, Horváth Z. Recent advances in the neoadjuvant treatment of breast cancer[J]. J Breast Cancer, 2017, 20(2): 119-31. doi:10.4048/jbc.2017.20.2.119 |
| [9] | Bhagya N, Chandrashekar K R. Tetrandrine--a molecule of wide bioactivity[J]. Phytochemistry, 2016, 125: 5-13. doi:10.1016/j.phytochem.2016.02.005 |
| [10] | Meng L H, Zhang H, Hayward L, et al. Tetrandrine induces early G1 arrest in human colon carcinoma cells by down-regulating the activity and inducing the degradation of G1-S-specific cyclin-dependent kinases and by inducing p53 and p21Cip1[J]. Cancer Res, 2004, 64(24): 9086-92. doi:10.1158/0008-5472.CAN-04-0313 |
| [11] | Kasprzak A, Kwasniewski W, Adamek A, et al. Insulin-like growth factor (IGF) axis in cancerogenesis[J]. Mutat Res, 2017, 772: 78-104. doi:10.1016/j.mrrev.2016.08.007 |
| [12] | Su Y, Wagner E R, Luo Q, et al. Insulin-like growth factor binding protein 5 suppresses tumor growth and metastasis of human osteosarcoma[J]. Oncogene, 2011, 30(37): 3907-17. doi:10.1038/onc.2011.97 |
| [13] | Ghoussaini M, Edwards S L, Michailidou K, et al. Evidence that breast cancer risk at the 2q35 locus is mediated through IGFBP5 regulation[J]. Nat Commun, 2014, 4: 4999. doi:10.1038/ncomms5999 |
| [14] | Luther G A, Lamplot J, Chen X, et al. IGFBP5 domains exert distinct inhibitory effects on the tumorigenicity and metastasis of human osteosarcoma[J]. Cancer Lett, 2013, 336(1): 222-30. doi:10.1016/j.canlet.2013.05.002 |
| [15] | Cabral B L S, da Silva A C G, deÁvila R I, et al. A novel chalcone derivative, LQFM064, induces breast cancer cells death via p53, p21, KIT and PDGFRA[J]. Eur J Pharm Sci, 2017, 107: 1-15. doi:10.1016/j.ejps.2017.06.018 |