

神经病理性疼痛(neuropathic pain,NPP)是由外周或中枢神经系统的直接损伤和功能紊乱所致的病理性疼痛。例如三叉神经痛、带状疱疹后神经痛、糖尿病性神经痛及各种损伤以及手术所致的神经痛。临床表现为自发性疼痛[1]、痛觉过敏、异常疼痛以及感觉异常。NNP目前的发病机制尚不明确,但广泛认同的机制为沿感觉神经纤维的脉冲产生异常(受伤的和相邻非受伤的感觉神经元可以产生并扩布它们的兴奋性变化,产生类似起搏器样电位,随之发生异位自发性放电)。NPP的发病率呈逐年上升的趋势,寻找新型高效的治疗措施是目前神经科学领域的热点[2]。背根神经节(dorsal root ganglia,DRG)在躯体痛觉感受的传递过程中起着非常重要的作用。它是初级传入神经元细胞的聚集处,是痛觉传向中枢的第一站,也是机体内外环境链接的纽带[3]。阻断疼痛在DRG的传递可能是发展新型镇痛药物的一个靶点,然而,目前这方面的研究尚少。
阿霉素(doxorubicin,DOX)是临床常用的抗恶性肿瘤药物,然而,DOX具有广泛的细胞毒性和神经毒性作用。如大鼠腹腔注射DOX,可产生类似局麻样作用,使动物的外周神经痛觉减退,高剂量可使动物的运动功能丧失[4]。进一步的研究发现,将DOX注射于外周神经干内,利用其逆行性轴浆运输和特异性聚集于感觉神经元的特性,可用于外周神经病理性疼痛和肌痉挛的治疗,疗效确切可靠[5]。此外,有研究将DOX应用于颈椎和胸椎旁神经阻滞治疗顽固性带状疱疹后遗症和癌性疼痛,均取得较为满意的结果,且未发现有运动神经的损伤[6]。目前,“影像引导下阿霉素背根神经节介入治疗神经病理性疼痛”技术在临床已广泛应用,但对于其导致神经损伤进而治疗NPP的分子机制尚不清楚[7]。本研究采用结扎大鼠右侧坐骨神经建立大鼠慢性神经病理性疼痛模型,观察静脉给予临床常用剂量的DOX对疼痛的治疗作用及其在DRG的聚集情况,并从DRG细胞的超微结构及凋亡蛋白的角度对其机制进行初步分析。该研究可初步探明DOX治疗NPP的分子机制,为临床该药物的合理应用提供实验依据。
1 材料与方法 1.1 实验动物清洁级成年♂ SD大鼠60只,体质量200~220 g, 由河北医科大学实验动物中心提供,动物合格证号:1503127,动物使用许可证号:SCXK(冀)2013-2-001。
1.2 药物、试剂与仪器阿霉素(海正辉瑞制药有限公司);FCS(冰冻切片化合物,德国Leica公司);β-actin一抗(Santa Cruz公司);Bax、Bcl-2抗体(美国Abcam公司);PKCɑ、PKCδ、PKCε抗体(美国BD公司);兔及鼠荧光二抗(美国Rockland公司);凝胶配制试剂盒(上海碧云天生物技术有限公司)。电泳及转膜装置(北京君意东方电泳设备公司);紫外可见分光光度计(美国NanoDrop公司);Odyssey双色红外激光成像系统(Gene Company Limited);研究级荧光显微镜(日本Olympus公司);热痛仪(泰盟科技有限公司);冰冻切片机(德国Leica公司)。
1.3 大鼠坐骨神经慢性缩窄性损伤(chronicconstriction injury of sciatic nerve,CCI)模型的建立及实验分组将60只大鼠随机分为4组:A组(假手术组,Sham)、B组(CCI手术模型组,Model)、C组(假手术+阿霉素5 mg·kg-1组,Sham+DOX)、D组(CCI手术模型+阿霉素5 mg·kg-1组,Model+DOX),每组均15只。大鼠CCI手术模型参照Bagriyanik等[8]方法结扎右侧坐骨神经制得,假手术组仅暴露但不结扎。分别在手术后d 1、3、5、7采用Von Frey纤维刺痛针法测定大鼠的机械痛阈值,采用热痛仪测定大鼠的热痛阈值。在手术后d 8,C组和D组均尾静脉注射DOX(5 mg·kg-1),其余2组给予等量生理盐水。给药后d 1、3、6分别采用同法测定大鼠的机械痛及热痛阈值,观察DOX对动物痛觉行为的影响。
1.4 行为学测试 1.4.1 机械刺激缩爪阈值测试用标准Von Frey纤维针刺激小鼠右爪的掌心,从克数最小的纤维针开始,将纤维针抵住掌心并使之微微弯曲,以小鼠突然抬足或添足现象为出现疼痛反应(阳性)。间隔5~10 min,重复测试5次,其中出现3次相同结果(阳性或阴性)为判定标准。记录出现回缩反应时所使用纤维针的克数作为机械缩爪反应的阈值。
1.4.2 热刺激爪缩回潜伏时间用热痛仪的红外聚光灯照射大鼠右侧后足足底。记录大鼠足爪回缩时间。连续3次,每次间隔5~10 min,取其平均值作为其热痛阈值。
1.5 背根神经节的提取在行为学检测结束后,也就是手术后d 15提取各组大鼠的DRG神经节。将大鼠腰部棘突向下各数1段关节处剪断,剪掉棘突两侧的肌肉组织和肋骨,将腰4、5段脊椎取出。沿椎管将脊椎剪开,取出L4-5 DRG。
1.6 DRG样本的处理 1.6.1 冰冻切片的制备每组随机提取3只大鼠右侧L4-5 DRG。将L4-5 DRG用0.67 mol·L-1多聚甲醛固定24 h。0.88 mol·L-1蔗糖溶液脱水12 h。PBS缓冲液漂洗3次,每次10 min,之后包埋于冰冻切片化合物中4℃过夜。d 2转移到-80℃冰箱中速冻。将速冻后的DRG取出,用冰冻切片机进行切片,切片厚度为6 μm。荧光显微镜下观察DOX荧光的分布情况。
1.6.2 石蜡切片的制备及HE染色每组随机提取3只大鼠右侧L4-5 DRG。放入3.33 mol·L-1甲醛溶液,固定24~72 h。常规梯度乙醇脱水、二甲苯透明、浸蜡、包埋。采用冰冻切片机连续冠状切片,切片厚5 μm。苏木精-伊红(HE)染色,光学显微镜下观察细胞的形态。
1.6.3 电镜切片的制备每组随机提取3只大鼠右侧L4-5 DRG。将DRG组织块置于0.25 mol·L-1戊二醛中,进行前固定,4℃冰箱放置2~4 h。磷酸缓冲液清洗3次,每次10~15 min。1%四氧化锇中后固定1~2 h,4℃冰箱保存。再次用磷酸缓冲液清洗3次,每次10~15 min。梯度丙酮脱水,每种浓度处理10~15 min,然后再用17.24 mol·L-1的丙酮脱水2次,每次10~15 min。包埋剂将样品包埋于胶囊或包埋板里。经聚合后,用超薄切片机将样品切成厚约50 nm的超薄切片,经醋酸铀和柠檬酸铅等进行电子染色,透射电镜观察照相。
1.6.4 DRG组织蛋白的提取将DRG组织用磷酸盐缓冲液漂洗10 min,重复3次。单个DRG加入400 μL RIPA裂解液和4 μL苯甲基磺酰氟(PMSF),高通量组织研磨机中将DRG破碎。4℃裂解40 min。4℃,12 000 r·min-1离心30 min,取上清,-80℃保存。
1.7 Western blot检测对提取的DRG组织蛋白用ND-2000C紫外可见分光光度计进行蛋白定量,蛋白变性后-80℃冰箱保存。SDS-PAGE方法分离蛋白。将蛋白转移到PVDF膜上,转印完毕后,将PVDF膜浸泡于50 g·L-1脱脂奶粉溶液中封闭(室温摇床上摇动2 ~ 3 h)。4℃孵育一抗过夜,次日TBST洗膜3次,每次10 min。避光室温孵育二抗2 h,TBST洗膜3次,每次10 min。条带用Odyssey双色红外激光成像系统扫描并分析。
1.8 统计学处理数据用SPSS 19.0软件分析处理,首先将数据进行正态分布及方差齐性检验,呈正态分布的实验数据以x±s表示,计量资料比较采用方差分析,进行组间比较,SNK检验进行两组比较。
2 结果 2.1 DOX在DRG中的荧光表达在激发光源波长为488 nm的氩离子激光下,DOX组出现明显的红色荧光,而对照组未见明显的荧光(Fig 1)。

|
| Fig 1 Fluorescence imaging of DOX in DRG A: Sham (×100); B: Sham (×200); C: Sham+DOX (×100); D: Sham+DOX (×200) |
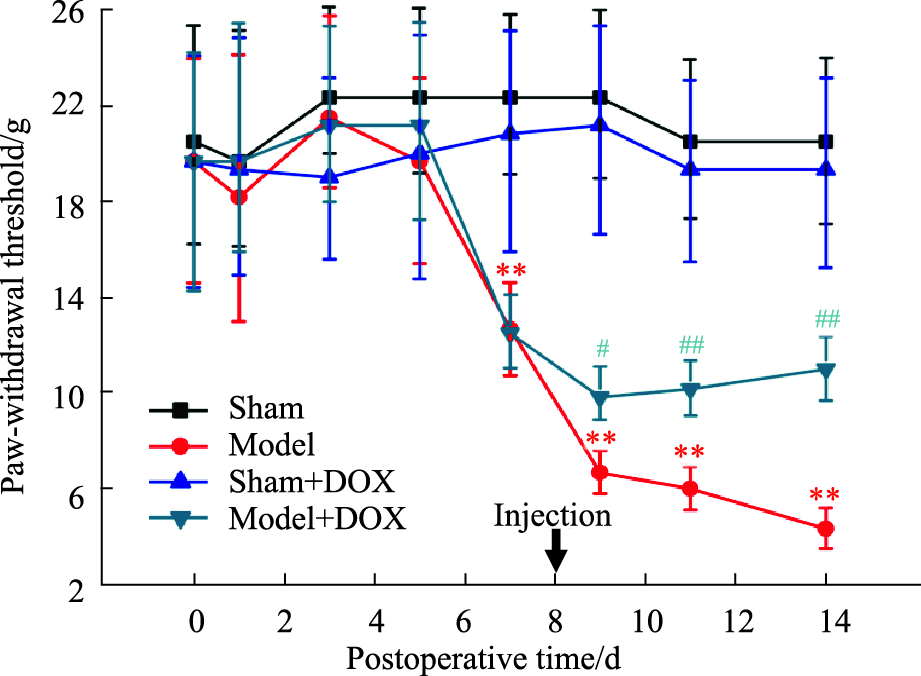
与Sham组相比,Sham+DOX组在整个实验期间机械痛域值和热痛阈值均未见明显改变, 而Model组大鼠于术后d 7对机械性疼痛和热痛的敏感性均增加,表现为痛阈值的降低,并且在之后的观察期持续存在(P<0.01或P<0.05),提示CCI模型的成功建立。手术后d 8给予DOX,与Model组相比,Model+DOX组在给药后的d 1、3、6,大鼠的机械痛阈值和热痛阈值均明显回升(P<0.01或P<0.05),见Fig 2、3。
|
| Fig 2 Effect of DOX on mechanical pain threshold in CCI model rats (n=15) **P < 0.01 vs Sham group; #P < 0.05, ##P < 0.01 vs Model group |

|
| Fig 3 Effect of DOX on heat pain threshold in CCI model rats (n=15) *P < 0.05, **P < 0.01 vs Sham group; ##P < 0.01 vs Model group |
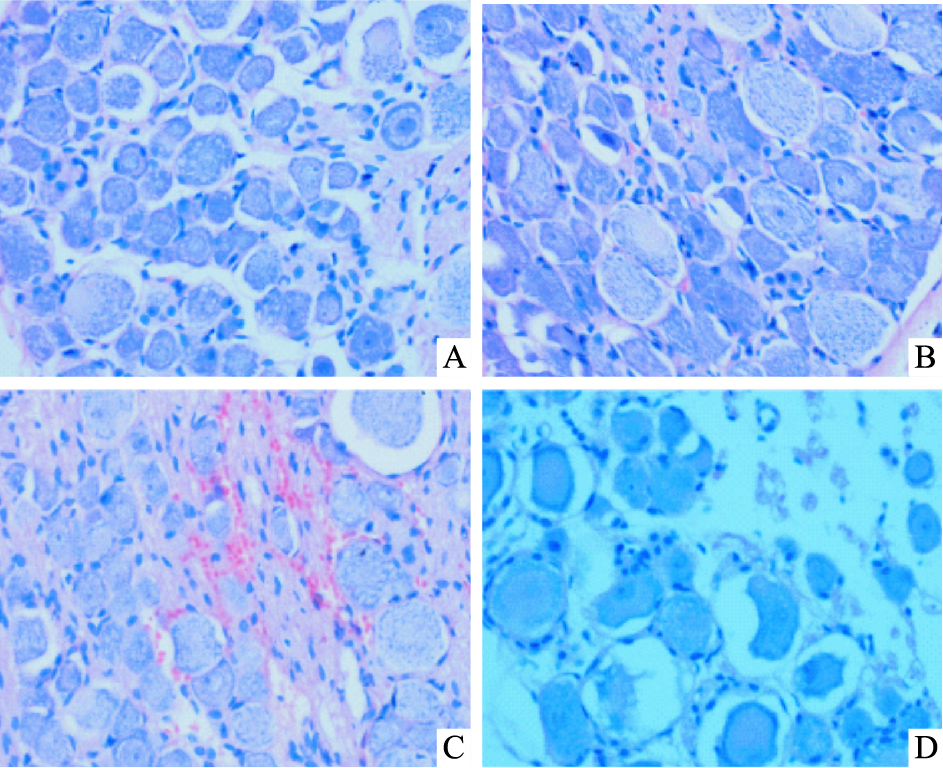
如Fig 4所示,Sham组细胞形态完整,排列整齐;Model组细胞轻度肿胀,排列整齐;Sham+DOX组细胞间质炎细胞浸润,胞质皱缩,部分细胞可见核固缩或核溶解;Model+DOX组胞质严重皱缩,部分细胞可见核固缩或核溶解。
|
| Fig 4 Effects of DOX on DRG cell morphology in CCI model rats under light microscope (×400) A: Sham; B:Model; C: Sham+DOX; D: Model+DOX |
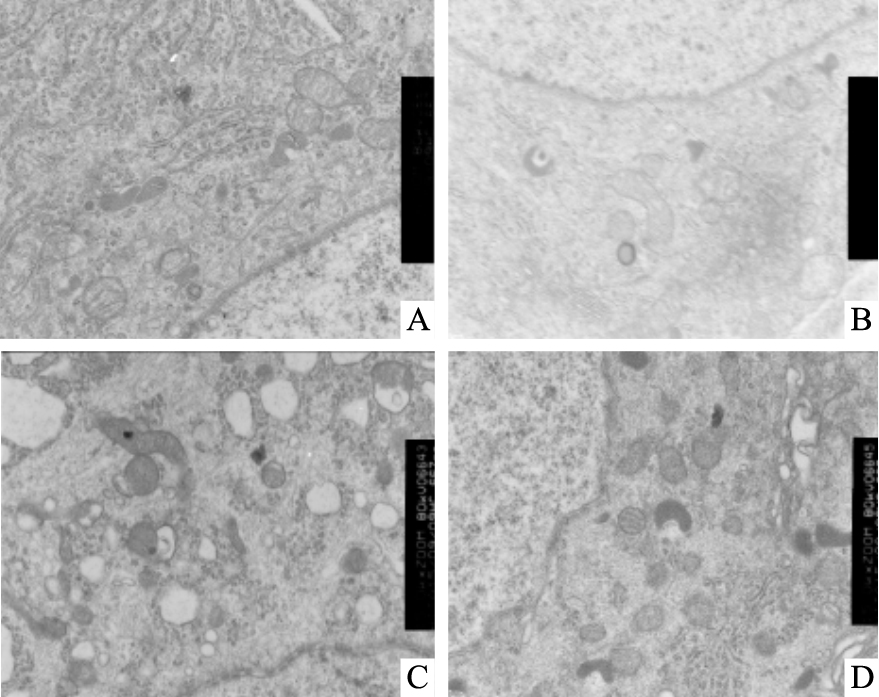
如Fig 5所示,Sham和Model组细胞的核膜完整,未发现固缩现象;Sham+DOX组细胞核膜弯曲,不规则变形,出现核固缩现象,线粒体结构致密、空泡化,线粒体内部丝样化结构增多,内质网扩张;Model+DOX组细胞的核膜弯曲,有核固缩现象,线粒体嵴和膜融合或消失,排列紊乱,有的空泡形成,内质网扩张。
|
| Fig 5 Effect of DOX on DRG cell ultrastucture in CCI rats under electron microscopy(×15 000) A: Sham; B: Model; C: Sham+DOX; D: Model+DOX |
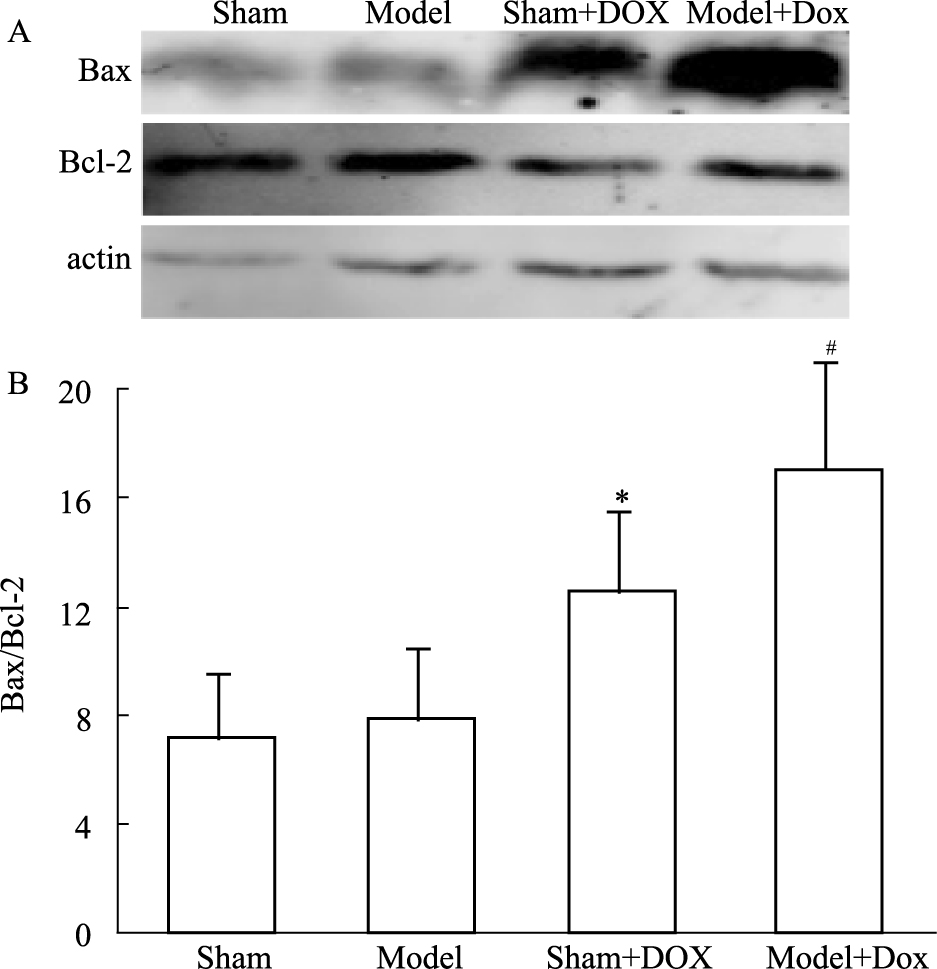
Fig 6 Western blot结果显示,与Sham组相比较,Model组Bax/Bcl-2未见明显变化,而Sham+DOX组Bax/Bcl-2明显升高(P<0.05或P<0.01)。相较于Model组,Model+DOX组的Bax/Bcl-2值明显增高(P<0.05)。
|
| Fig 6 Effect of DOX on Bax/Bcl-2 in CCI model rats(n=6) A: Western blot results; B: Bax/Bcl-2 gray value. *P < 0.05 vs Sham group; #P < 0.05 vs Model group |
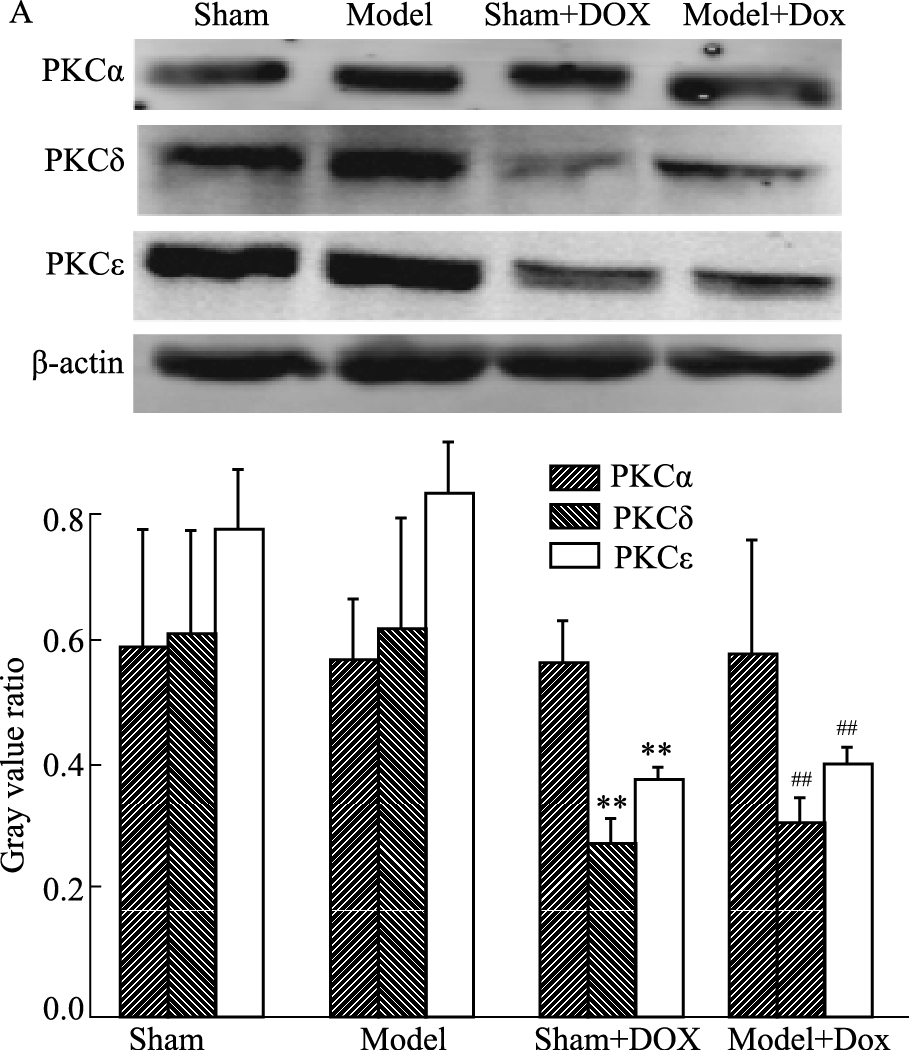
如Fig 7所示,PKCɑ在4组中的表达无明显变化。与Sham组相比,Model组的PKCδ和PKCε的表达无明显变化,而Sham+DOX组的表达量则明显降低(P<0.01)。相较于Model组,Model+DOX组PKCδ和PKCε的蛋白表达量明显下降(P<0.01)。
|
| Fig 7 Effect of DOX on expressions of PKCɑ, PKCδ, PKCε protein in CCI model rats(n=6) A: Western blot results; B: PKCα/β-actin, PKCδ/β-actin and PKCε/β-actin gray value. **P < 0.01 vs Sham group; ##P < 0.01 vs Model group. |
近年来,国内外学者深入研究了DOX对外周感觉神经节细胞的毒性作用,发现DOX可被神经元轴突末梢吸收,并通过轴浆逆向转运到神经元的胞体,起到化学切除神经节的作用。DOX可进入神经节细胞导致核孔及核孔复合体(nuclearpore complex, NPC)亚细胞结构的改变。当DOX进入神经核之后,一方面核孔发生变化,这是引起感觉神经节细胞退化的主要原因;另一方面,NPC亚细胞结构改变影响到细胞核及核仁的功能,进而引起蛋白质合成功能障碍,最终导致感觉神经节细胞死亡[9]。但目前关于DOX神经毒性机制方面的基础研究尚少。
对DRG组织的荧光分析表明,阿霉素可聚集于DRG。这可能和阿霉素可破坏感觉神经节周围毛细血管,使其渗透性增加有关。周围神经系统微血管及神经束膜是外界物质进入的屏障,外周感觉神经节的血管渗透性很高,DOX可轻易通过血-神经屏障进入并损害神经节细胞[10]。我们的结果也提示,DOX有快速逆行性轴浆运输的特性,静脉注射可逆向转运至神经元胞体,损害胞体的正常结构,这一结果和文献报道的一致[11]。这种破坏作用使神经细胞与其支配的靶细胞之间的信息传递和功能调控能力逐渐丧失。同时影响神经细胞代谢,导致神经细胞变性坏死[12]。临床上,DOX这种治疗NPP的自杀性轴浆运输作用称为“逆行性感觉神经节切除术”。有研究发现,阿霉素单次静脉注射5 mg·kg-1,背根神经节细胞即出现明显的组织形态学改变,而单次剂量达到10 mg·kg-1可能会出现明显的临床外周神经系统损伤症状[13]。为了保证达到镇痛效果的同时,对神经造成最小的伤害,本实验选用的尾静脉注射的剂量为5 mg·kg-1。
对凋亡蛋白的分析表明,阿霉素可导致DRG组织Bax/Bcl-2的升高,提示阿霉素可诱导细胞凋亡,同样的结果在心肌细胞也得到证实。这可能与阿霉素可增加DRG组织凋亡蛋白p53和Bax的表达,增加神经细胞肿瘤坏死因子-α(TNF-α)的水平,导致神经细胞损伤有关。PKC是一类丝氨酸/苏氨酸蛋白激酶,在细胞的信号转导过程中起着重要的作用,与细胞的增殖、分化、凋亡密切相关。PKC分为传统PKC(conventional PKC, cPKC,α、βI、βⅡ、γ)、新型PKC(novel PKC, nPKC, δ、ε、η、θ)和不典型PKC(aPKC, ξ、λ)。其中,PKCα、PKCδ及PKCε在神经细胞中均有表达。研究发现,PKC抑制剂可促进TNF和其受体的结合,进而诱导细胞凋亡,提示在TNF介导的细胞凋亡中PKC是一个负调控因子[14-15]。在本研究中,我们发现,DOX可下调PKCδ和PKCε的表达,而对PKCα未见明显影响,提示PKC对凋亡蛋白的调节具有亚型特异性。我们的实验也提示,DOX有类似于PKC抑制剂的作用,可明显减少PKCδ和PKCε的表达。
综上所述,DOX静脉给药可蓄积于DRG组织中,明显减轻CCI大鼠的疼痛反应,这一作用与其可降低PKCδ、PKCε的蛋白表达,诱导DRG凋亡有关。
| [1] | Galuppo M, Giacoppo S, Bramanti P, et al. Use of natural compounds in the management of diabetic peripheral neuropathy[J]. Molecules, 2014, 19(3): 2877-95. doi:10.3390/molecules19032877 |
| [2] | Li C X, Ma G Y, Guo M F, et al. Sialic acid accelerates the electrophoretic velocity of injured dorsal root ganglion neurons[J]. Neural Regen Res, 2015, 10(6): 972-5. doi:10.4103/1673-5374.158364 |
| [3] | Liu S, Shi Q, Zhu Q, et al. P2X7 receptor of rat dorsal root ganglia is involved in the effect of moxibustion on visceral hyperalgesia[J]. Purinergic Signal, 2015, 11(2): 161-9. doi:10.1007/s11302-014-9439-y |
| [4] | Matouk A I, Taye A, Heeba G H, et al. Quercetin augments the protective effect of losartan against chronic doxorubicin cardiotoxicity in rats[J]. Environ Toxicol Pharmacol, 2013, 36(2): 443-50. doi:10.1016/j.etap.2013.05.006 |
| [5] | Sturgeon K, Schadler K, Muthukumaran G, et al. Concomitant low-dose doxorubicin treatment and exercise[J]. Am J Physiol Regul Integr Comp Physiol, 2014, 307(6): 685-92. doi:10.1152/ajpregu.00082.2014 |
| [6] | Ammar A S, Mahmoud K M. Does the addition of magnesium to bupivacaine improve postoperative analgesia of ultrasound-guided thoracic paravertebral block in patients undergoing thoracic surgery[J]. J Anesth, 2014, 28(1): 58-63. doi:10.1007/s00540-013-1659-8 |
| [7] | Naik A K, Latham J R, Obradovic A, et al. Dorsal root ganglion application of muscimol prevents hyperalgesia and stimulates myelin protein expression after sciatic nerve injury in rats[J]. Anesth Analg, 2012, 114(3): 674-82. doi:10.1213/ANE.0b013e31823fad7e |
| [8] | Bagriyanik H A, Ersoy N, Cetinkaya C, et al. The effects of resveratrol on chronic constriction injury of sciatic nerve in rats[J]. Neurosci Lett, 2014, 561: 123-7. doi:10.1016/j.neulet.2013.12.056 |
| [9] | Purdie L, Alexander C, Spain S G, et al. Influence of polymer size on uptake and cytotoxicity of doxorubicin-loaded DNA-PEG conjugates[J]. Bioconjug Chem, 2016, 27(5): 1244-52. doi:10.1021/acs.bioconjchem.6b00085 |
| [10] | Chun-jing H, yi-ran L, hao-xiong N. Effects of dorsal root ganglion destruction by adriamycin in patients with postherpetic neuralgia[J]. Acta Cir Bras, 2012, 27(6): 404-9. doi:10.1590/S0102-86502012000600008 |
| [11] | Kaminskas L M, McLeod V M, Kelly B D, et al. Doxorubicin-conjugated PEGylated dendrimers show similar tumoricidal activity but lower systemic toxicity when compared to PEGylated liposome and solution formulations in mouse and rat tumor models[J]. Mol Pharm, 2012, 9(3): 422-32. doi:10.1021/mp200522d |
| [12] | Hassan M, Selim ovic D, Hanning M, et al. Endoplasmic reticulum stress-mediated pathways to both apoptosis and autophagy: significance for melanoma treatment[J]. World J Exp Med, 2015, 5(4): 206-17. doi:10.5493/wjem.v5.i4.206 |
| [13] | 杨宇, 刘庆. 阿霉素治疗神经病理性疼痛的进展[J]. 海南医学, 2008, 19(10): 133-4. Yang Y, Liu Q. The progress of doxorubicin in the treatment of neuropathic pain[J]. Hainan Med, 2008, 19(10): 133-4. doi:10.3969/j.issn.1003-6350.2008.10.087 |
| [14] | 汤雷, 胥甜甜, 易小清, 等. PKCε信号通路介导的葛根素抗心肌细胞缺氧/复氧损伤作用[J]. 中国药理学通报, 2014, 30(1): 77-81. Tang L, Xu T T, Yi X Q, et al. PKCε signaling pathway mediated by puerarin anti-cardiomyocyte hypoxia/reoxygenation injury[J]. Chin Pharmacol Bull, 2014, 30(1): 77-81. |
| [15] | Morioka N, Yoshida Y, Nakamura Y, et al. The regulation of exon-specific brain-derived neurotrophic factor mRNA expression by protein kinase C in rat cultured dorsal root ganglion neurons[J]. Brain Res, 2013, 1509: 20-31. doi:10.1016/j.brainres.2013.03.015 |

