2. 南京中医药大学第三附属医院 检验科、江苏 南京 210001;
3. 南京中医药大学第三附属医院 中心实验室,江苏 南京 210001;
4. 南京中医药大学 药学院,江苏 南京 210023;
5. 南京中医药大学 第一临床医学院,江苏 南京 210023
 ,
ZHANG Hui2,
TAN Yan-yan1,
ZHU Wei-na3,
LI Zhi-wei4,
LU Wei5,
LI Rui-ying5,
ZHAO Min5,
DING Yang5,
LI Meng5,
HUANG Shi-cai5,
DING Yi-jiang1
,
ZHANG Hui2,
TAN Yan-yan1,
ZHU Wei-na3,
LI Zhi-wei4,
LU Wei5,
LI Rui-ying5,
ZHAO Min5,
DING Yang5,
LI Meng5,
HUANG Shi-cai5,
DING Yi-jiang1
 ,
ZHANG Su-min1
,
ZHANG Su-min1

2. Clinical Laboratory, the Third Affiliated Hospital of Nanjing University of Chinese Medicine, Nanjing 210001, China;
3. Central Laboratory, the Third Affiliated Hospital of Nanjing University of Chinese Medicine, Nanjing 210001, China;
4. School of Pharmacy, Nanjing University of Chinese Medicine, Nanjing University of Chinese Medicine, Nanjing 210023, China;
5. the First Clinical Medical College, Nanjing University of Chinese Medicine, Nanjing 210023, China
丁氏溃结灌肠液为国家级非物质文化遗产“丁氏中医诊疗法”第八代传人丁泽民教授的经典方,具有清热利湿解毒、活血化瘀、怯腐生肌之功效,以中医治法理论为依据,药物组成主要包括金银花、地榆、白及、珠黄散(乳香、珍珠粉、轻粉等)[1-2],针对不同溃疡性结肠炎(ulcerative colitis,UC)患者、不同发病特点均可进行治疗,其在全国肛肠中心运用于临床50余年,有极好的疗效。前期的研究发现,丁氏溃结灌肠液有着良好的疗效[3-4],并且揭示了其有可能治疗的靶点和炎症因子相关,具有较好的抗炎、修复黏膜和促进溃疡愈合的作用[5]。但缺乏完善的中医理论的科学内涵研究,从而限制了其推广应用,进一步的研究希望通过高密度、高通量、高特异性的蛋白芯片技术在动物实验层面,全面考察丁氏溃结灌肠液通过改善哪些差异性靶点的表达而起作用。
1 材料与方法 1.1 实验动物健康SD大鼠,20只,SPF级,体质量180~220 g,♀♂各半,浙江省实验动物中心提供,动物合格证号:SCXK(浙)2014-0001。
1.2 药物与试剂硫酸葡聚糖钠(dextran sulfate sodium, DSS)购自美国MP公司,批号:MP16011090;ELISA试剂盒购自Multisciences公司,批号:237450922;GSR-CAA-67试剂盒购自RayBiotech公司,药物为南京市中医院院内制剂丁氏溃结灌肠液(处方包括:金银花120 g、地榆120 g、白及40 g、复方珠黄散20 g),苏药制字:Z040001781;美沙拉秦灌肠液由德国Falk公司生产60 g/4 g,批号:H20100253。
1.3 方法 1.3.1 造模与分组20只SD大鼠随机选取5只大鼠作为空白对照组,其余15只大鼠通过DSS法建立急性期溃疡性结肠炎的大鼠模型。将DSS用蒸馏水配制成3.5%的溶液,造模组大鼠自由饮用,现喝现配,连饮7 d,空白对照组大鼠饮用纯水。造模组大鼠出现腹泻、便血、体重下降等症状,说明模型复制成功。造模成功后,将UC模型大鼠随机分为3组,分别为模型组、美沙拉秦灌肠液组和溃结灌肠液组,每组5只。停饮DSS,各组饮水恢复正常,开始灌肠给药。按非标准体重动物的校正系数表,人与大鼠换算系数为6.17,折算大鼠用药量为6 g·kg-1灌肠,美沙拉秦灌肠液组予美沙拉秦灌肠液2.4 g·kg-1灌肠,灌肠量均10mL·kg-1。模型组大鼠给予等剂量生理盐水灌肠,空白对照组自由喂养,不予灌肠处理。灌肠3 d后,除空白对照组外,其余各组复饮4% DSS 5 d,同时继续灌肠治疗,7 d后停饮DSS,恢复正常饮水,再继续灌肠治疗6 d,按照标准操作流程将大鼠处死后,取20个肠道组织样本,采用RayBiotech试剂盒进行检测。
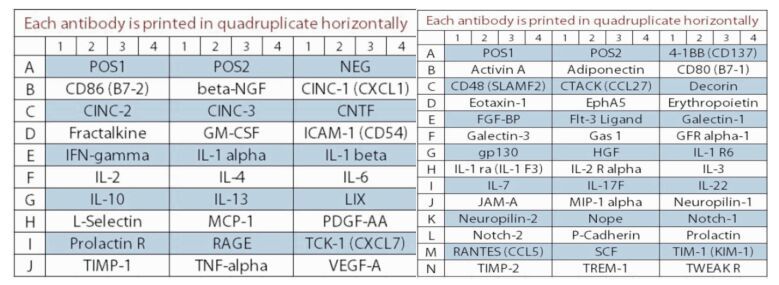
1.3.2 采用GSR-CAA-67蛋白芯片技术结合数据分析软件进行数据分析 1.3.2.1 芯片检测原理及指标
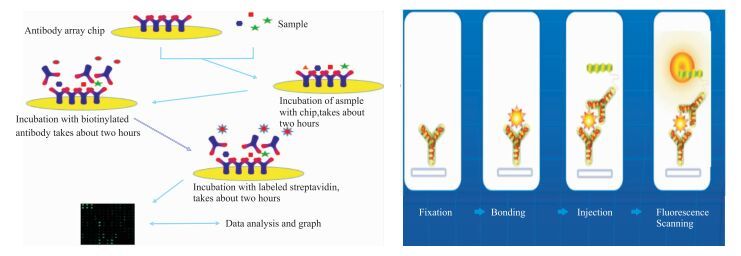
|
| Fig 1 Detection principle of protein array |
① 组织裂解:按100 mg组织加入500 μL裂解液,冰上裂解;在冰上用高速分散切割机进行破碎组织,离心取上清。② 芯片操作流程:每个孔中加100 μL的样品稀释液,添加100 μL的标准液和样品到孔中,在摇床4℃过夜孵育。使用Thermo Scientific Wellwash Versa芯片洗板机清洗玻片。检测抗体混合物的孵育Cy3-链霉亲和素的孵育,采用激光扫描仪例如Inno Scan300扫描信号,采用Cy3或者绿色通道(激发频率=532nm)。
1.4 统计学方法采用SPSS23.0软件,计量资料以x±s表示,进行正态分布检验和方差齐性检验后,多组间比较采用单因素方差分析,两组间比较采用t检验。
2 结果通过GSR-CAA-67芯片筛查共验证B7-2、β-NGF、CINC-1、CINC-2、CINC-3、CNTF、Fractalkine、GM-CSF、ICAM-1、IFN-γ、IL-1α、IL-1β、IL-2、IL-4、IL-6、IL-10、IL-13、LIX、L-Selectin、MCP-1、PDGF-AA、Prolactin R、RAGE、TCK-1、TIMP-1、TNF-α、VEGF、4-1BB、Activin A、Adiponectin、B7-1、CD48、CTACK、Decorin、Eotaxin、EphA5、Erythropoietin、FGF-BP、Flt-3L、Galectin-1、Galectin-3、Gas 1、GFR alpha-1、gp130、HGF、IL-1 R6、IL-1 rα、IL-2 Rα、IL-3、IL-7、IL-17F、IL-22、JAM-A、MIP-1α、Neuropilin-1、Neuropilin-2、Nope、Notch-1、Notch-2、P-Cadherin、Prolactin、RANTES、SCF、TIM-1、TIMP-2、TREM-1、TWEAK R共67种蛋白,其中筛选出8种在模型组与空白对照组之间差异有统计学意义的蛋白(Tab 2、Fig 2)。
| Difference protein | Control | Model | Ding’s herb enema prescription | Mesalazine |
| IL-6 | 551.9±141.4 | 1239.7±244.5* | 562.4±265.5△△ | 871.9 ±125.1△ |
| TNF-α | 2201±332.2 | 3075.9±145.2* | 2542±373.1△ | 2683.8±425 |
| IFN-γ | 3004.5±135.2 | 3417.8±57.2* | 3457.8±438.5 | 3482.3±421.0 |
| IL-22 | 236.7±97.7 | 500.7±242.1* | 147.9±133.6△ | 507.0±109.2 |
| TIMP-1 | 1171.2±230.9 | 3522.9±750.1* | 2015.6±811.8△ | 1576.1±402.6△△ |
| TIMP-2 | 156.7±25.9 | 300.4±63.1** | 203.2±120.9 | 273.3±97.8 |
| Erythropoietin | 972.8±112.1 | 1149.9±119.9* | 1019.1±205.8 | 1138.5±280.5 |
| TIM-1 | 771.5±246.1 | 1277.9±335.8* | 929.2±271.7 | 1251.2±314.5 |
| *P<0.05, **P<0.01 vs control; △P<0.05, △△P<0.01 vs model | ||||
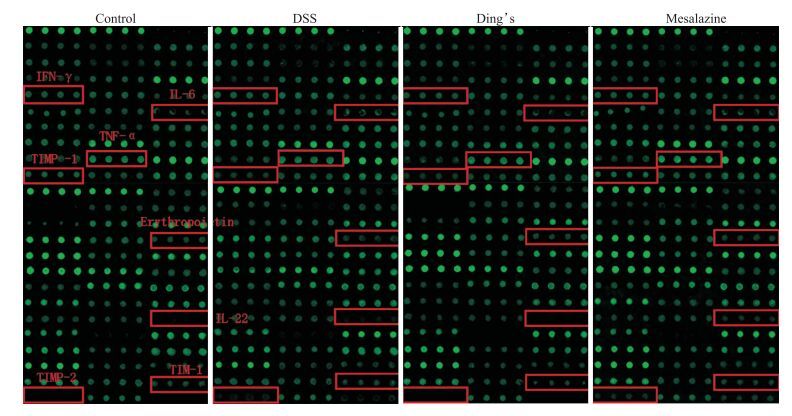
|
| 图 2 Fluorescence signal intensity picture |
针对8种差异蛋白进行统计及作图,Fig 3显示,模型组与空白对照组比较,有4种蛋白IFN-γ、EPO、TIMP-2和TIM-1差异均有统计学意义(P<0.05),而丁氏溃结灌肠液及美沙拉秦组与模型组比较没有明显的变化(P>0.05),提示两种药物对上述靶点没有改善作用。Fig 4结果显示,模型组和空白组与对照组比较,有另外4种蛋白IL-6、TIMP-1、TNF-α和IL-22差异亦有统计学意义(P<0.05),丁氏溃结灌肠液与美沙拉秦均对IL-6、TIMP-1蛋白表达有明显抑制作用(P<0.05),此外,丁氏溃结灌肠液对TNF-α、IL-22蛋白表达也有明显抑制作用(P<0.05),美沙拉秦组则没有类似作用(P<0.05)。

|
| Fig 3 Tendency of differences in protein(IFN-γ, erythropoietin, TIM-1, TIMP-2) *P < 0.05, **P < 0.01 vs control |

|
| Fig 4 Tendency of differences in protein(IL-6, TIMP-1, TNF-α, IL-22) *P < 0.05, **P < 0.01 vs control; △P < 0.05, △△P < 0.01 vs model |
丁氏溃结灌肠液是国家非物质文化遗产丁氏诊疗法所涉及方药的重要组成部分,本课题组长期开展此复方的临床研究,取得了较满意的结果。发现治疗后UC患者的脓血便、黏液便和溃疡病变均明显改善。与阳性药物对比,患者在大便次数、Sourtherland DAI评分、有效率方面的差异有统计学意义,说明丁氏溃结灌肠液在疗效上不劣于阳性药,可为临床提供一种副作用小、安全可靠的补充治疗方法。鉴于丁氏溃结灌肠液在UC的治疗上取得了明显的疗效,课题组跟踪南京中医院治疗UC处方中发现此制剂使用量极大,近5年的年用量均在万瓶以上,且呈逐年增加之势,经济效益明显,其确切的疗效深受广大患者的认同,下一步需要对其治疗机制进行科学研究。高密度、高通量、高特异性的蛋白芯片技术在生物标志物的筛查、疾病机制探究等方面应用广泛,能避免盲目挑选细胞因子,省时省力并节省宝贵的样品。本课题组希望通过此技术全面考察丁氏溃结灌肠液是通过改善哪些蛋白靶点的表达从而发挥作用。
UC患者具有慢性复发和迁延难愈的特点,其慢性非特异性炎症引发了机体对结肠壁反复的修复,细胞外基质(extracellular matrix,ECM)合成分泌增加,降解减少,在组织内过度沉积,导致原有正常结构和组织形态改变,肠道缩短,肠纤维化形成[6]。长期严重的组织纤维化,将导致大量的组织细胞被胶原纤维与ECM所替代,从而引发脏器功能下降,并引起肠腔狭窄和肠壁顺从性丧失,患者腹痛、腹泻等症状加重,既然肠纤维化是UC发病过程中常见的严重并发症,其发生发展是个复杂多变的过程,针对于此的治疗非常重要。UC的治疗主要应用柳氮磺胺吡啶(SASP)、肿瘤坏死因子-α(TNF-α)抗体和白细胞介素-10 (IL-10) 等,均对于纤维化无能为力。肠纤维化的形成与ECM合成增加的病理改变、肠道肌层的过度生长密切相关,而基质金属蛋白酶(matrix metalloproteinases, MMPs)/基质金属蛋白酶组织抑制物(tissue inhibitors of metalloproteinases, TIMPs)平衡对维持ECM的正常代谢至关重要。研究发现,MMPs可降解过多生成的ECM,TIMPs则导致ECM降解异常,因此,MMPs与TIMPs的失衡则导致肠纤维化[7]。己发现的TIMPs酶有4种,TIMP-1 (28 ku)广泛存在于组织和体液中,能被多种细胞因子诱导产生,在肠纤维化的发生中起着重要作用。本实验中,DSS造模后TIMP-1表达明显上升,MMPs活性被抑制,进一步导致肠道纤维化的发生,而中药可能是通过抑制TIMP-1 mRNA及蛋白表达而降低对MMPs的抑制,有利于MMPs对ECM的降解,阻止肠纤维化的发生,从而达到治疗的目的,可以弥补通过改善纤维化的过程治疗UC的空白。
UC的发生与感染、环境、免疫以及遗传等多种因素有关,但具体机制尚不清楚,有报道,免疫调节机制中炎症细胞因子在UC的发病中可能发挥重要作用[8]。促炎细胞因子如TNF-α、IL-6等的过度产生和抑炎因子如IL-22等生成不足,IL-22又具有双向作用,在某些环境下表现出抗炎活性,而在另一些环境中可表现为放大炎症反应,炎症细胞因子导致肠道内环境紊乱是促使UC发生的重要环节[9]。TNF-α是炎症性肠病,特别是溃疡性结肠炎病理进程中的关键细胞因子,通过表达黏附分子、成纤维增殖因子、凝血因子以及启动细胞毒性、凋亡和急性期反应等过程发挥作用。IL-6是一种免疫调节细胞因子,在炎症反应中启动了细胞表面信号复合体(包括IL-6、sIL-6R及共享信号受体gp130) 发挥作用。亦有研究表明,中药的提取物可减轻DSS诱导的小鼠体重下降,改变肠损伤程度,其机制与降低TNF-α、IL-6水平有关[10]。在UC发病机制及随后的UC相关结肠肿瘤形成中,IL-6主要通过STAT3信号通路发挥重要作用[11]。IL-22/JAK-STAT通路也是UC发病机制中的重要信号通路,STAT3的磷酸化是IL-22在上皮细胞屏障表面介导效应的基本途径。已经证实了在口服葡聚糖硫酸钠诱导结肠炎肠上皮细胞,STAT3活化更依赖IL-22[12]。也有研究发现,IL-22/STAT3信号通路与UC及其致癌作用相关,IL-22及受体在UC及不典型增生患者结肠黏膜中表达升高,并且使STAT3磷酸化[13]。本实验中,模型组和空白对照组相比,炎症细胞因子IL-6、TNF-α、IL-22差异均有统计学意义,丁氏溃结灌肠液对IL-6、TNF-α、IL-22的异常表达均有抑制作用,表明丁氏溃结灌肠液可通过改善肠道炎症反应起到治疗UC的作用。
总之,本研究初步发现国家级非物质文化遗产丁氏溃结灌肠液可能通过改善肠道炎症反应及肠纤维化,达到治疗UC的目的,进一步的研究将对可能机制进行实验验证及深入探讨。
| [1] | 蒋庆林, 夏崇才. 溃结灌肠颗粒制备工艺优选研究[J]. 亚太传统医药, 2015, 11(21): 20-1. Jiang Q L, Xia C C. Optimization of preparation process of Ding's herb enema prescription[J]. Asia-Pacific Tradit Med, 2015, 11(21): 20-1. |
| [2] | 国家药典委员会. 中国药典[M]. 北京: 中国医药科技出版社, 2010. Commossion C P. Pharmacopoeia of the People's Republic of China[M]. Beijing: China Medical Science Press, 2010. |
| [3] | 李睿瑛, 赵敏, 张亚杰, 等. 丁氏溃结灌肠液对DSS诱导的溃疡性结肠炎大鼠肠道屏障的保护作用[J]. 江苏中医药, 2016, 48(11): 79-82. Li R Y, Zhao M, Zhang Y J, et al. Protection of Ding's herb enema prescription on DSS induced ulcerative colitis rat intestinal barrier[J]. Jiangsu J TCM, 2016, 48(11): 79-82. |
| [4] | 赵敏, 李睿瑛, 张亚杰, 等. 丁氏溃结灌肠液改善DSS诱导大鼠肠道炎症反应的机制研究[J]. 时珍国医国药, 2017, 28(1): 95-7. Zhao M, Li R Y, Zhang Y J, et al. Ding's herb enema prescription improve DSS induced rat intestinal inflammatory reaction mechanism[J]. Lishizhen Med Mater Med Res, 2017, 28(1): 95-7. |
| [5] | 张苏闽, 刘轩良. 溃结灌肠液对溃疡性结肠炎模型大鼠结肠组织中set9及血清TNF-α的影响[J]. 山东中医药大学学报, 2014, 38(5): 477-9. Zhang S M, Liu X L. Effect of Ding's herb enema prescription in TNF-α of serum and set9 of colon tissueon on ulcerative colitis model rats[J]. J Shandong Univ, 2014, 38(5): 477-9. |
| [6] | Lawrance I C, Maxwell L, Doe W. Altered response of intestinal mucosal fibroblasts to profibrogenic cytokines in inflammatory bowel disease[J]. Inflamm Bowel Dis, 2001, 7(3): 226-36. doi:10.1097/00054725-200108000-00008 |
| [7] | Lohr K, Sardana H, Lee S, et al. Extracellular matrix protein lumican regulates inflammation in a mouse model of colitis[J]. Inflamm Bowel Dis, 2012, 18(1): 143-51. doi:10.1002/ibd.21713 |
| [8] | Pedersen J, Coskun M, Soendergaard C, et al. Inflammatory pathways of importance for management of inflammatory bowel disease[J]. Wold J Gastroenterol, 2014, 20(1): 64-77. |
| [9] | Pichai M V, Ferguson L R. Potential prospects of nanomedicine for targeted therapeutics in inflammatory bowel diseases[J]. World J Gastroenterol, 2012, 18(23): 2895-901. doi:10.3748/wjg.v18.i23.2895 |
| [10] | 孙阿宁, 任改艳, 邓超, 等. 牡荆素减轻小鼠溃疡性结肠炎的药效作用及机制研究[J]. 中国药理学通报, 2014, 30(12): 1677-81. Sun A N, Ren G Y, Deng C, et al. Effects and mechanism of alleviation of Vitexin on ulcerative colitis in mice[J]. Chin Pharmacol Bull, 2014, 30(12): 1677-81. doi:10.3969/j.issn.1001-1978.2014.12.012 |
| [11] | Li Y, de Haar C, Chen M, et al. Disease-related expression of the IL-6 /STAT3 /SOCS3 signalling pathway in ulcerative colitis and ulcerative colitis-related carcinogenesis[J]. Gut, 2010, 59(2): 227-35. doi:10.1136/gut.2009.184176 |
| [12] | Pickert G, Neufert C, Leppkes M, et al. STAT3 links IL-22 signaling in intestinal epithelial cells to mucosal wound healing[J]. J Exp Med, 2009, 206(1): 1465-72. |
| [13] | Yu L Z, Wang H Y, Yang S P, et al. Expression of interleukin-22/STAT3 signaling pathway in ulcerative colitis and related carcinogenesis[J]. World J Gastroenterol, 2013, 19(1): 2638-49. |