


2. 南昌大学 第二附属医院江西省分子医学重点实验室,江西 南昌 330006
2. Jiangxi Provincial Key Lab of MolecularMedicine, the Second Affiliated Hospital to Nanchang University, Nanchang 330006, China
近年来,铁过载诱发细胞、组织损伤逐步引起人们的注意。研究发现,铁在体内具有很强的氧化活性,机体铁过载时可导致活性氧(reactive oxygen species, ROS)的产生[1-2]。血管内皮细胞对ROS极为敏感,是铁过载损伤的主要靶细胞之一[3]。血管内皮细胞产生非对称性二甲基精氨酸(asymmetric dimethylarginine, ADMA)与细胞内ROS生成互为因果,调控内皮细胞功能,与多种血管内皮功能失调性疾病高度相关,是一种心血管疾病危险因子[4]。ADMA在铁过载引起的血管内皮细胞损伤中的作用及其机制尚未见报道。本文选用人脐静脉血管内皮细胞(human umbilical vein endothelial cells, HUVECs),以梯度右旋糖酐铁(iron dextran)确认造成铁过载损伤,分别检测HUVECs细胞内ADMA含量、内皮型一氧化氮合酶(endothelial nitric oxide synthase, eNOS)表达、二甲基精氨酸二甲基氨基水解酶Ⅱ(dimethylarginine dimethylaminohydrolaseⅡ, DDAHⅡ)活性等及其相应的细胞线粒体功能;加用ADMA生理性对抗剂L-精氨酸(L-Arg)[5],探讨铁过载对HUVECs细胞线粒体的损伤作用及其机制。
1 材料与方法 1.1 药品与试剂右旋糖酐铁(Iron)、右旋糖酐(Dex)、L-Arg:Sigma公司;eNOS、β-actin抗体及相应二抗:Santa Cruz公司;蛋白提取试剂盒:北京普利来公司;胎牛血清、MEM培养基:Gibco BRL公司;ROS检测试剂盒、线粒体分离试剂盒:Sigma-Aldrich公司;线粒体膜电位检测试剂盒、细胞凋亡检测试剂盒:BD公司产品;增强化学发光印迹试剂、硝酸纤维素膜:Amersham, UK;MTT、HEPES、PMSF、亮肽素、丙烯酰胺、SDS、亚甲基双丙烯酰胺、过硫酸铵、TEMED、EDTA和DTT:Sigma公司;其他试剂均为分析纯。
1.2 细胞系及培养HUVECs购自中国科学院细胞库。HUVECs细胞培养于含10% FBS的DMEM培养基中,置于37℃ CO2培养箱培养。细胞生长接近融合状态(70%~80%)时,备用。
1.3 实验分组① 正常对照(Ctrl)组:取正常培养HUVECs细胞,常规培养24 h;② Iron组:取正常培养HUVECs细胞,加入终浓度分别为30、15、7.5、3.75、1.875 μmol·L-1右旋糖酐铁,孵育24 h;③ Dex组:取正常培养HUVECs细胞,加入终浓度分别为30、15、7.5、3.75、1.875 μmol·L-1右旋糖酐,孵育24 h;④ L-Arg组:取正常培养HUVECs细胞,加入终浓度为7.5 μmol ·L-1右旋糖酐铁,以及终浓度为1 mmol ·L-1 L-Arg孵育24 h。
1.4 MTT比色法检测细胞存活率胰酶消化收集细胞,以每孔104个细胞接种96孔培养板。细胞融合达70%~80%后,弃培养基;加入MTT溶液(5 g·L-1溶于PBS)每孔20 μL,37℃孵育4 h;弃上清液,每孔加DMSO 150 μL,振荡10 min。酶联免疫检测仪在490 nm波长处测定其OD值。细胞存活率/% = (实验组光吸收值/对照组光吸收值) ×100%。
1.5 HPLC法检测细胞培养液ADMA含量[6]实验结束后,取细胞培养液0.5 mL,加5-磺基水杨酸沉淀蛋白,离心10 min后,取上清液上样,激发波长338 nm,发射波长425 nm检测ADMA含量。
1.6 细胞DDAHⅡ活性测定[6]采用间接法检测。冰浴下将细胞裂解液分为2份,分别加入终浓度为500 μmol·L-1 ADMA;一份立即加入30% 5-磺基水杨酸灭活DDAHⅡ;另一份37℃孵育2 h后,再加入30% 5-磺基水杨酸灭活DDAHⅡ。用HPLC法测定2份的ADMA水平,其ADMA差值反映DDAHⅡ活性。
1.7 Western blot法检测细胞eNOS表达实验结束后,按试剂盒方法提取细胞总蛋白;BCA法蛋白定量后行SDS-PAGE电泳(12%分离胶);湿转PVDF膜、封闭;eNOS抗体(1:500) 或β-actin抗体(1:500) 孵育,4℃过夜。洗膜后以1:2 000二抗孵育1 h后,ECL化学发光法检测。X线片扫描后,用Quantity One图形分析软件分析,以β-actin相应条带的密度标化相应组的eNOS条带密度。
1.8 生化检测实验结束后,各组分别取培养液200 μL,Beckman生化自动分析仪测定乳酸脱氢酶(lactate dehydrogenase, LDH)活性;消化收集且反复冻融破碎细胞,离心后取上清液,按试剂盒说明书测定细胞内一氧化氮(nitric oxide, NO)及丙二醛(malondialdehyde, MDA)含量。
1.9 流式细胞术测定细胞内ROS含量[7]实验结束后,4℃预冷PBS洗涤2~3次细胞;加入含0.02%乙二胺四乙酸(elhylene diamine tetraacetic acid, EDTA)的0.25%胰蛋白酶消化收集细胞,用10 μmol·L-1 DCFH-DA溶液500 μL重悬细胞,37℃孵育30 min;800×g、5 min离心,弃上清,预冷PBS洗涤2~3次细胞,制成108 ·L-1的悬液,立即以488 nm为激发波长,以530 nm为发射波长行流式细胞仪检测,以不加DCFH-DA的1管为阴性对照。
1.10 流式细胞术测定细胞线粒体膜电位[7]实验结束后,4℃预冷磷酸盐缓冲液(phosphate buffer, PBS)洗涤2~3次细胞;加入含0.02% EDTA的0.25%胰蛋白酶消化收集细胞,用10 μmol·L-1 JC-1溶液200 μL重悬细胞,37℃孵育20 min;800×g、5 min离心,弃上清,预冷PBS洗涤2~3次细胞,制成109 ·L-1的悬液,立即行流式细胞仪检测,分别以488 nm为激发光波长,527 nm和590 nm为发射光波长测绿色和红色荧光强度,以各组红/绿荧光强度的比值反映线粒体膜电位水平。
1.11 线粒体通透性转运孔(mitochondrial permeability transition pore, mPTP)开放测定以线粒体肿胀实验揭示mPTP开放情况[8]。实验结束后,4℃预冷PBS洗涤2~3次细胞;按试剂盒说明书分离、纯化线粒体;线粒体蛋白终浓度为0.5 g·L-1,25℃、pH 7.4;1 min后加入150 μmol·L-1 CaCl2,分光光度仪检测线粒体在520 nm处的吸光度(OD520)在l min内的变化,持续检测20 min。
1.12 细胞凋亡检测[8]采用AnnexinV/PI凋亡检测试剂盒及流式细胞仪检测。实验结束后,4℃预冷PBS洗涤2~3次细胞;用不含EDTA的胰蛋白酶消化、收集细胞;用预冷PBS洗2次后,用1×Binding buffer重悬细胞,细胞密度约为5×109 ·L-1;分别加入5 μL Annexin V-FITC和5 μL PI;重悬后,室温避光孵育15 min,加入500 μL Binding buffer,立即以激发光488 nm、发射光578 nm行流式细胞仪检测,各组阳性细胞百分率用于表示细胞凋亡状况。
1.13 数据处理应用SPSS11.5统计软件行组间方差分析,各实验组数据均以x±s表示。
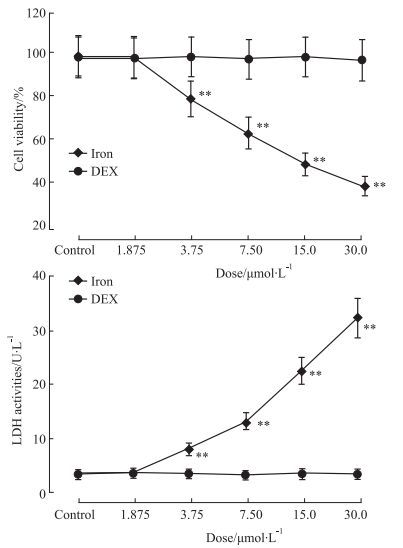
2 结果 2.1 右旋糖酐铁对HUVECs细胞存活率以及培养液LDH活性的影响MTT结果显示(Fig 1),经不同浓度右旋糖酐铁处理48 h后,细胞存活率降低、培养液LDH活性增加(P<0.01),3.75~30 μmol·L-1区间呈明显的剂量依赖性;而同步进行的、对应浓度的右旋糖酐处理的HUVECs细胞存活率和培养液LDH活性均无改变(P>0.05),表明相应剂量的右旋糖酐铁造成的HUVECs细胞损伤,源于Fe2+毒性,与渗透压改变等因素无关。鉴于7.5 μmol·L-1位于右旋糖酐铁处理剂量区间中段,本文后续实验中凡涉及右旋糖酐铁处理的终浓度均为7.5 μmol·L-1。
|
| Fig 1 Effects of iron dextran on cell viability (A) and LDH activity(B) of HUVECs (x±s, n=8) **P < 0.01 vs prior dosage |
Western blot结果显示(Fig 2),与对照组相比,Iron组细胞eNOS蛋白表达明显下调(P<0.01);而1 mmol·L-1 L-Arg可明显减弱右旋糖酐铁下调细胞eNOS表达的作用。

|
| Fig 2 Iron overload down-regulated eNOS expression in HUVECs(x±s, n=8) **P < 0.01 vs Control; ##P < 0.01 vs Iron |
如Tab 1所示,Iron组细胞DDAHⅡ活性明显降低,MDA含量升高(P<0.01),培养液中ADMA含量明显增加(P<0.01),NO含量减少(P<0.01);而1 mmol ·L-1 L-Arg可明显逆转右旋糖酐铁的相关作用。
| Group | ADMA/μmol·L-1 | NO/μmol·L-1 | DDAHⅡactivity/% | MDA/μmol·L-1 |
| Control | 0.48±0.03 | 80.26±6.85 | 98.03±8.51 | 3.08±0.28 |
| Iron 7.5 μmol·L-1 | 2.31±0.35** | 39.53±5.66** | 47.24±6.08** | 5.82±0.63** |
| L-Arg 1 mmol·L-1 | 1.16±0.21## | 64.08±7.01## | 76.85±8.58## | 3.42±0.42## |
| **P<0.01 vs Control; ##P<0.01 vs Iron. | ||||
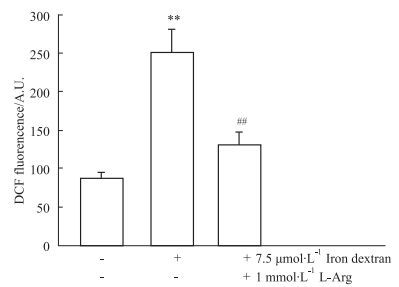
如Fig 3所示,HUVECs经右旋糖酐铁处理后,ROS生成明显增加(P<0.01);而1 mmol ·L-1 L-Arg处理后,细胞ROS生成明显降低(P<0.01),提示L-Arg可减轻铁过载引起的ROS爆发。
|
| Fig 3 Iron overload induced ROS generation in HUVECs(x±s, n=8) **P < 0.01 vs Control; ##P < 0.01 vs Iron |
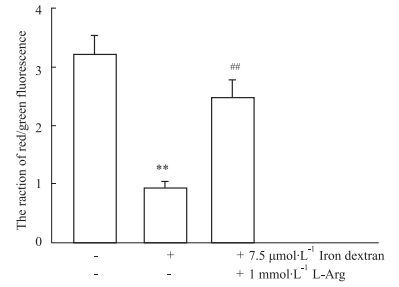
如Fig 4所示,HUVECs经右旋糖酐铁处理后,线体粒膜电位明显减小(P<0.01);而1 mmol·L-1 L-Arg处理后,线粒体膜电位明显恢复(P<0.01),表明L-Arg可稳定线体粒膜电位。
|
| Fig 4 Iron overload loss of mitochondria membrane potential in HUVECs(x±s, n=8) **P < 0.01 vs Control; ##P < 0.01 vs Iron |
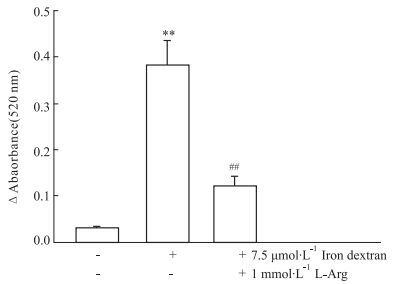
如Fig 5所示,HUVECs经右旋糖酐铁处理后,其线体粒受到CaCl2刺激后极易肿胀(P<0.01),即线体粒的mPTP易于开放;而1 mmol·L-1 L-Arg处理后,线粒体对CaCl2刺激明显耐受(P<0.01),表明L-Arg可使mPTP关闭。
|
| Fig 5 Iron overload opened mitochondrial permeability transition pores in HUVECs (x±s, n=8) **P < 0.01 vs Control; ##P < 0.01 vs Iron |
如Fig 6所示,HUVECs经右旋糖酐铁处理后,其阳性细胞百分率明显高于对照组(P<0.01);与之相比,1 mmol·L-1 L-Arg处理后,细胞凋亡率明显降低(P<0.01)。

|
| Fig 6 Iron overload induced apoptosis in HUVECs(x±s, n=8) **P < 0.01 vs Control; ##P < 0.01 vs Iron |
自然界的铁离子有高铁(Fe3+)与亚铁(Fe2+)之分,研究发现,仅有Fe2+可被机体吸收,服用Fe3+制剂必须还原成Fe2+。铁是一切生物体所必需的微量元素,它参与细胞的增殖和分化,通过催化氧化-还原反应参与电子传递、细胞呼吸、能量代谢、解毒、DNA合成、酶促反应等许多重要生理过程[9]。然而,铁又是一把双刃剑,铁缺乏是全球最常见的公共营养问题——贫血,过量的铁同样也会对机体产生毒性作用,诱导体内生成过多自由基可导致多种疾病[1-2]。Fe2+具有很强的氧化活性,机体一旦摄入过量的铁,就会有铁游离出来,迅速氧化机体内结合不稳的生物分子,并产生大量的自由基如O2-、OH-、H2O2等,攻击、损伤血管内皮细胞等靶细胞,诱发相关疾病的发生、发展[3, 10]。本实验证实,在3.75~30 μmol·L-1剂量区间,右旋糖酐铁处理24 h可造成HUVECs细胞存活率明显下降,培养液中LDH活性明显增加,且呈明显的剂量依赖性,表明过多的铁离子确实会损伤HUVECs细胞。
研究表明[4-6, 11],L-Arg与ADMA可竞争性抑制eNOS,影响NO生成,调控血管内皮细胞功能以及血管张力。ADMA由内皮细胞产生,被DDAHⅡ降解、失活。DDAHⅡ对细胞内ROS增加极为敏感而使活性降低,使得ADMA堆积。ADMA不仅与L-Arg竞争eNOS,使NO生成减少,影响内皮细胞功能以及血管张力,且可通过“NOS脱偶联”机制,即eNOS不能催化L-Arg的双电子氧化生成NO,反而产生超氧离子(更多ROS生成),而对DDAHⅡ产生更为强大的抑制,形成恶性循环,最终导致血管内皮细胞功能衰竭。本实验首次发现,7.5 μmol·L-1右旋糖酐铁处理24 h可使HUVECs细胞eNOS表达下调、DDAHⅡ活性降低、MDA含量增加,而培养液中ADMA含量明显增加、NO含量明显减少(由于未能检测p-eNOS变化,难以确认NO含量改变与eNOS表达下调间的因果关系);而用1 mmol·L-1 L-Arg同步处理后,铁离子的上述作用明显减弱,表明铁过载造成的HUVECs细胞损伤与eNOS有关,也很可能有ADMA/DDAHⅡ的参与。
近年来发现,线粒体不仅控制细胞的能量代谢,而且在维持细胞钙稳态、调节细胞凋亡或坏死等过程中起着决定性作用[12]。某些触发因素使得部分线粒体产生、释放ROS,通过“活性氧引起的活性氧释放”(ROS-induced ROS-release, RIRR)机制,正反馈性诱发周边正常线粒体产生、释放大量的ROS,即导致ROS爆发;引起线粒体膜电位振荡,mPTP的开放,导致外膜破裂及线粒体不可逆损伤;随之基质肿胀,外膜破裂,细胞色素C等凋亡信号分子释放,导致细胞凋亡或死亡[3, 13]。本实验首次发现,7.5 μmol·L-1右旋糖酐铁处理48 h可使HUVECs细胞ROS生成明显增加,线粒体膜电位减小,mPTP的开放,细胞凋亡明显增加;而用1 mmol·L-1 L-Arg同步处理后,铁离子的上述作用明显减弱,表明铁过载成的HUVECs细胞损伤与其线粒体功能衰竭有关。
综上所述,铁过载可引起HUVECs细胞ROS形成,可能在eNOS以及ADMA/NO/ DDAHⅡ参与下,使得ROS恶性生成,进而激活RIRR机制,诱发mPTP过度开放,最终导致内皮细胞功能衰竭。
| [1] | Galaris D, Pantopoulos K. Oxidative stress and iron homeostasis: mechanistic and health aspects[J]. Crit Rev Clin Lab Sci, 2008, 45(1): 1-23. doi:10.1080/10408360701713104 |
| [2] | Liu D, He H, Yin D, et al. Mechanism of chronic dietary iron overloadinduced liver damage in mice[J]. Mol Med Rep, 2013, 7(4): 1173-9. doi:10.3892/mmr.2013.1316 |
| [3] | Mak I T, Chmielinska J J, Nedelec L, et al. D-propranolol attenuates lysosomal iron accumulation and oxidative injury in endothelial cells[J]. J Pharmacol Exp Ther, 2006, 317(2): 522-8. doi:10.1124/jpet.105.097709 |
| [4] | Siekmeier R, Grammer T, März W. Roles of oxidants, nitric oxide, and asymmetric dimethylarginine in endothelial function[J]. J Cardiovasc Pharmacol Ther, 2008, 13(1): 279-97. |
| [5] | Mangoni A A. The emerging role of symmetric dimethylarginine in vascular disease[J]. Adv Clin Chem, 2009, 48: 73-94. doi:10.1016/S0065-2423(09)48003-X |
| [6] | Yuan Q, Peng J, Liu S Y, et al. Inhibitory effect of resveratrol derivative BTM-0512 on high glucose-induced cell senescence involves dimethylaminohydrolase/asymmetric dimethylarginine pathway[J]. Clin Exp Pharmacol Physiol, 2010, 37(5-6): 630-5. doi:10.1111/cep.2010.37.issue-5-6 |
| [7] | 周敏, 游嘉振, 何欢, 等. Bcl-2介导的芹菜素抗心肌细胞缺氧/复氧损伤作用[J]. 中国药理学通报, 2015, 31(1): 122-7. Zhou M, You J Z, He H, et al. Role of Bcl-2 signal pathway in apigenin preconditioning against cardiomyocytes anoxia/reoxygenation injury[J]. Chin Pharmacol Bull, 2015, 31(1): 122-7. |
| [8] | 刘丹, 彭易安, 刘卓琦, 等. Bcl-2/Bad/mPTP通路介导14-3-3γ对抗脂多糖所致心肌损伤[J]. 中国药理学通报, 2013, 29(1): 48-52. Liu D, Peng Y A, Liu Z Q, et al. Bcl-2/Bad/mPTP pathway mediates 14-3-3γ protecting against LPS-induced myocardial injury[J]. Chin Pharmacol Bull, 2013, 29(1): 48-52. |
| [9] | Muñoz M, Villar I, García-Erce J A. An update on iron physiology[J]. World J Gastroenterol, 2009, 15(37): 4617-26. doi:10.3748/wjg.15.4617 |
| [10] | Lawen A, Lane D J. Mammalian iron homeostasis in health and disease: uptake, storage, transport, and molecular mechanisms of action[J]. Antioxid Redox Signal, 2013, 18(18): 2473-507. doi:10.1089/ars.2011.4271 |
| [11] | 呼晓雷, 周继朋, 陈小平. AGXT2与ADMA代谢及心脑血管疾病的研究进展[J]. 中国药理学通报, 2015, 31(5): 601-5. Hu X L, Zhou J P, Chen X P. Role of AGXT2 in ADMA metabolism and the development of cardiovascular and cerebrovascular diseases[J]. Chin Pharmacol Bull, 2015, 31(5): 601-5. |
| [12] | Levi S, Rovida E. The role of iron in mitochondrial function[J]. Biochim Biophys Acta, 2009, 1790(7): 629-36. doi:10.1016/j.bbagen.2008.09.008 |
| [13] | Zinkevich N S, Gutterman D D. ROS-induced ROS release in vascular biology: redox-redox signaling[J]. Am J Physiol Heart Circ Physiol, 2011, 301(3): H647-53. doi:10.1152/ajpheart.01271.2010 |

