


2. 广东工业大学环境科学与工程学院,广东 广州 510006;
3. 广东药科大学附属第一医院重症医学科,广东 广州 510080
2. School of Environmental Science and Engineering, Guangdong University of Technology, Guangzhou 510006, China;
3. Intensive Care Unit, the First Affiliated Hospital of Guangdong Pharmaceutical University, Guangzhou 510080, China
脓毒症是机体对病原体感染的免疫应答紊乱而导致危及生命的多器官功能障碍[1]。若感染未能有效控制,可发展为脓毒症休克和多器官功能衰竭(multiple organ dysfunction syndrome, MODS)[2]。脓毒症的发病机制涉及到复杂的全身系统性炎症反应及宿主对不同感染病原体及其毒素的异常反应等多个方面[3-5]。中性粒细胞作为固有免疫重要成员,在机体抗病原体感染中发挥重要作用。现已知,在严重脓毒症患者中, 中性粒细胞向感染部位趋化功能降低,导致不能及时控制感染的恶化。
黄芪甲苷(astragaloside Ⅳ, AS-Ⅳ)作为中药黄芪的主要活性成分,具有多种药理作用,如抗糖尿病、心血管疾病、糖尿病肾病等[6]。AS-Ⅳ参与抗菌作用逐渐得以认识,但其具体的作用机制尚未清楚。本文通过建立盲肠末端结扎穿孔(cecal ligation and puncture, CLP)诱导脓毒症小鼠模型,探讨AS-Ⅳ在重症细菌感染中的免疫保护作用,为研究其免疫调节机制及中药靶向药物研发提供实验依据。
1 材料与方法 1.1 材料 1.1.1 实验动物SPF级C57BL/6近交系小鼠,♂,体质量(20±2) g,6~8周龄,购自广东省医学实验动物中心,许可证号:SCXK(粤)2008-0002。所有动物实验均严格遵守广东药科大学动物伦理保护指导进行。
1.1.2 药物与试剂AS-Ⅳ分析标准品(纯度≥98%,阿拉丁公司);Percoll(美国Sigma);anti-CXCR2-Alexa Fluor 647、PE anti-mouse CD11b、FITC anti-mouse Ly-6G(美国Biolegend);RPMI 1640培养基、胎牛血清(美国Gibco)。
1.1.3 仪器台式高速冷冻离心机(型号:5810R,德国Eppendorf);细胞培养箱(型号:3110,美国Thermo);流式细胞仪FACS CALIBUR(美国BD)。
1.2 方法 1.2.1 CLP诱导脓毒症模型的建立与给药♂ SPF级C57BL/6小鼠随机分为3组:Sham组、CLP组、CLP+AS-Ⅳ组,每组均为10只。造模术前2 d,灌胃给予AS-Ⅳ(10 mg·kg-1),对照组给予等剂量生理盐水。按照Miyaji等[7]方法建立CLP模型。Sham组小鼠,除盲肠不结扎和穿刺外,其余操作与手术组相同。术后密切观察小鼠状态,记录小鼠存活情况。
1.2.2 脏器组织HE染色无菌操作,摘取小鼠肺、肝脏、肾脏,多聚甲醛固定后,石蜡切片,进行HE染色[8]。
1.2.3 血液、腹腔液和脏器细菌负荷量的测定CLP组和CLP+AS-Ⅳ组小鼠眼眶取血,收集血液样品,用生理盐水稀释后,在血平板上涂布;将2 mL无菌磷酸盐缓冲盐水(PBS)注入腹腔,收集腹腔灌洗液,倍比稀释后在血平板上涂布;摘取小鼠肺、肝、肾脏匀浆,倍比稀释后,在血平板上涂布。37℃孵育24 h后,计数菌落,并以每毫升(CFU·mL-1)的菌落形成单位表达。
1.2.4 流式细胞术检测中性粒细胞表面趋化因子受体CXCR2(CXC chemokine receptor 2, CXCR2) 表达取100 μL小鼠外周血,加入anti-CXCR2、anti-CD11b、anti-mouse Ly-6G抗体,避光孵育30 min;裂解红细胞,staining buffer洗涤后,加400 μL staining buffer重悬中性粒细胞,将细胞悬液转移至流式管中,流式细胞仪检测中性粒细胞表面CXCR2表达。
1.2.5 中性粒细胞的分离纯化参照文献[9],采用Percoll密度梯度离心分离小鼠外周血和腹腔灌洗液的中性粒细胞。制备78%、69%和52% Percoll密度梯度,外周血加至Percoll液面,1 200×g离心30 min;在69%~78%界面部分收集中性粒细胞。
1.2.6 中性粒细胞趋化功能中性粒细胞分为3组:PBS对照组、LPS组、LPS+AS-Ⅳ组,每组含5×105个细胞。AS-Ⅳ(30 mg·L-1)预处理1 h后,加入LPS(1 mg·L-1)继续培养1 h;随后将中性粒细胞转移至Transwell小室,下室加入含30 μg·L-1巨噬细胞炎性蛋白-2(macrophage inflammatory protein-2,MIP2) 的RPMI 1640培养基,培养1 h;Transwell趋化膜经多聚甲醛固定,结晶紫染色后,显微镜观察迁移的中性粒细胞数目。
1.2.7 中性粒细胞体外杀伤功能AS-Ⅳ(30 mg·L-1)加至1×106中性粒细胞悬液,预孵育1 h;E.coli浓度调整为2.5×1010 CFU·L-1,加10% FBS孵育30 min;按细胞:细菌=10:1比例进行混合培养,37℃孵育2 h;倍比稀释,涂布LB平板,37℃过夜培养,进行细菌总数测定。
1.2.8 统计学分析实验数据使用Sigmaplot软件处理,结果以x±s表示。样本两两间比较运用t检验或One-Way ANOVA方差分析。
2 结果 2.1 AS-Ⅳ对脓毒症小鼠存活率的影响假手术组小鼠饮食活动正常;CLP小鼠出现活动减少,精神萎靡,肛周有粪便黏连等系列症状,而AS-Ⅳ组小鼠从饮食、精神状态等方面均明显改善。如Fig 1所示,经AS-Ⅳ治疗的脓毒血症小鼠存活率较对照组小鼠明显上升,70 h后对照组存活率仅为30%,而AS-Ⅳ组小鼠仍有60%存活。

|
| Fig 1 Survival curve of mice after CLP (n=10) *P < 0.05 vs CLP group |
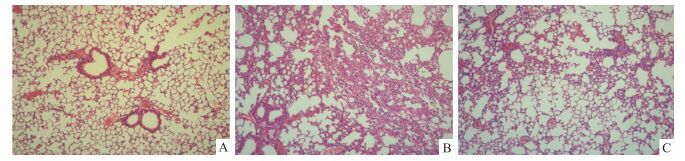
CLP小鼠24 h后取肝、肺、肾进行组织病理学检测。CLP小鼠各器官有不同程度的损伤,其中肺组织的病理损伤最为明显。光镜下观察Sham组肺组织结构完整、肺泡腔清晰且肺泡壁无充血,肺间质较少炎细胞浸润;CLP组肺泡壁弥漫性增厚合并部分肺泡壁破坏,较多炎细胞浸润、部分肺泡出血和结构破坏;CLP+AS-Ⅳ组病理改变较CLP组明显减轻(Fig 2)。
|
| Fig 2 Changes of pulmonary pathology in mice after CLP A: Sham group; B: CLP group; C: CLP+ AS-Ⅳ group |
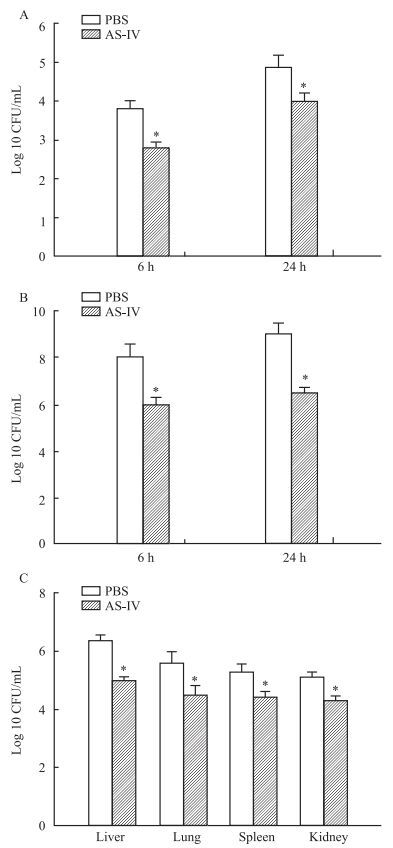
盲肠结扎穿孔后,肠道内的细菌流出,造成腹腔感染,且细菌入血造成全身感染。在感染后6、24 h,经AS-Ⅳ预处理的小鼠腹腔液和血液中细菌数量明显减少。同时,在感染24 h后,AS-Ⅳ预处理的小鼠肝、肺、肾等脏器中细菌数量也明显降低,差异有显著性(P<0.05),见Fig 3。
|
| Fig 3 Bacterial loads in blood, peritoneal fluid and organelle after CLP in septic mice(x±s, n=5) Bacterial loads in blood (A) and peritoneal fluid (B) at 6 and 24 h after CLP; C: Bacterial loads in different organs at 24 h after CLP. *P < 0.05 vs PBS-treated group. |
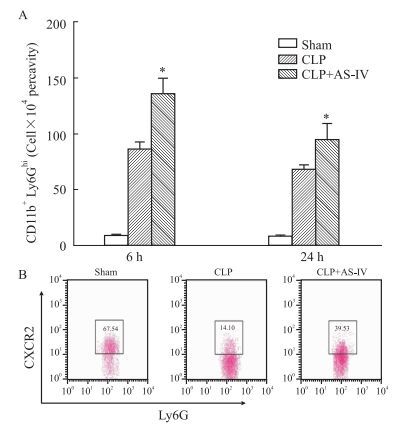
相比于CLP组,CLP+AS-Ⅳ组小鼠腹腔灌洗液中的中性粒细胞(CD11b+Ly6Ghi)的数量明显升高(P<0.05,Fig 4A)。Sham组小鼠中性粒细胞趋化因子受体CXCR2表达为67.54%,CLP组小鼠为14.10%,而AS-Ⅳ处理后,CXCR2表达为39.53%。结果显示,CLP组小鼠中性粒细胞趋化因子受体CXCR2表达明显降低,而AS-Ⅳ预处理后可抑制CXCR2表达下调(Fig 4B)。
|
| Fig 4 Number of CD11b+Ly6Ghi neutrophils and CXCR2 expression in peritoneal fluid A: The number of CD11b+Ly6Ghi neutrophils at 6 and 24 h after CLP; B: CXCR2 expression on the cell surface of neutrophils. *P < 0.05 vs CLP group |
Fig 5体外实验显示,在静息状态中性粒细胞表面趋化因子受体CXCR2呈高水平表达。在LPS刺激时,中性粒细胞表面CXCR2表达降低,AS-Ⅳ处理后阻止LPS介导的中性粒细胞表面CXCR2下调。

|
| Fig 5 Effects of AS-Ⅳ on neutrophil chemotaxis(n=5) Neutrophil surface CXCR2 expression (A) and chemotaxis to CXCL2 (B) were determined. *P < 0.05 vs LPS group |
如Fig 6所示,中性粒细胞经AS-Ⅳ预处理,随后加入E.coli孵育2 h后,中性粒细胞对E.coli的杀菌作用明显增强(P<0.05)。

|
| Fig 6 Effects of AS-Ⅳ on bactericidal ability of neutrophils(n=4) *P < 0.05 vs PBS-treated group |
脓毒症病因机制复杂,可由任何部位的感染引起,其综合征是机体免疫应答失调引起,包括早期不受控制的全身性炎症和晚期免疫抑制状态延长[10]。脓毒血症诱导的免疫功能障碍主要特征为抗炎/促炎因子失衡、巨噬细胞提呈抗原功能受损、淋巴细胞快速凋亡及中性粒细胞向感染部位趋化能力降低,导致不能及时控制感染的恶化[11]。中性粒细胞在外周血液中含量最为丰富,在固有免疫中起重要作用。中性粒细胞在激活后,通过吞噬、杀伤病原微生物并释放可溶性介质,诱导单核细胞进一步募集到炎症部位发挥作用。中性粒细胞数量受到严密调控,趋化因子及其受体在中性粒细胞释放与骨髓滞留平衡中发挥关键性调节作用。中性粒细胞表面主要趋化因子受体有CXCR2和CXCR4,当骨髓内皮细胞产生的CXCL1、CXCL2与相应受体CXCR2结合,中性粒细胞从骨髓进入血液循环。中性粒细胞到达感染部位后,识别病原微生物并将其摄入胞内,通过脱颗粒和“呼吸爆发”等方式杀灭病原体[12-13]。
临床和动物研究结果表明AS-Ⅳ黄芪甲苷能上调LPS致急性肺损伤(acute lung injury,ALI)大鼠支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)中中性粒细胞数,并增强水通道蛋白(aquaporins 5, AQP5) 蛋白的表达,对肺部感染有保护作用[14]。在急性大肠杆菌腹腔感染小鼠模型中,我们首次证实AS-Ⅳ预处理可增加体内细菌清除率,提高小鼠存活率[15]。本研究发现,AS-Ⅳ明显延长脓毒症小鼠存活时间,其抗菌作用与阻止细菌感染所致中性粒细胞表面CXCR2表达下调,从而增加中性粒细胞趋化能力相关。AS-Ⅳ处理后,CLP小鼠外周血、腹腔液及脏器中细菌负荷量均明显减少,与上调中性粒细胞吞噬杀菌能力相关,可潜在解释AS-Ⅳ在脓毒症小鼠中的免疫保护作用,但其具体杀菌机制还有待进一步研究。
( 致谢: 本实验于广东药科大学广东省生物活性药物研究重点实验室完成,感谢所有老师和同学的帮助和支持!)
| [1] | 张利鹏, 赵焱, 刘国娟, 等. 乌司他丁通过干预p38MAPK/ERK信号通路减轻脓毒症性肺损伤[J]. 中国药理学通报, 2016, 32(9): 1311-6. Zhang L P, Zhao Y, Liu G J, et al. Ulinastatin attenuates lipopolysaccharide-induced acute lung injury by intervening p38MAPK/ERK signaling pathway[J]. Chin Pharmacol Bull, 2016, 32(9): 1311-6. |
| [2] | Shankar-Hari M, Phillips G S, Levy M L, et al. Developing a new definition and assessing new clinical criteria for septic shock:for the Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)[J]. JAMA, 2016, 315(8): 775-87. doi:10.1001/jama.2016.0289 |
| [3] | Seymour C W, Liu V X, Iwashyna T J, et al. Assessment of clinical criteria for sepsis:for the Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)[J]. JAMA, 2016, 315(8): 762-74. doi:10.1001/jama.2016.0288 |
| [4] | Kaukonen K M, Bailey M, Pilcher D, et al. Systemic inflammatory response syndrome criteria in defining severe sepsis[J]. N Engl J Med, 2015, 372(17): 1629-38. doi:10.1056/NEJMoa1415236 |
| [5] | Rhodes A, Evans L E, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsisand septic shock: 2016[J]. Intensive Care Med, 2017, 43(3): 304-77. doi:10.1007/s00134-017-4683-6 |
| [6] | 靳晓飞, 张颖, 周晓红, 等. 黄芪甲苷对缺氧缺糖/复氧复糖PC12细胞凋亡的影响[J]. 中国药理学通报, 2016, 32(10): 1411-5. Jin X F, Zhang Y, Zhou X H, et al. Effects of astragaloside Ⅳ on apoptosis of PC12 cells induced by hypoxia/hypoglycemia and reoxygenation[J]. Chin Pharmacol Bull, 2016, 32(10): 1411-5. doi:10.3969/j.issn.1001-1978.2016.10.016 |
| [7] | Miyaji T, Hu X, Yuen P S, et al. Ethyl pyruvate decreases sepsis-induced acute renal failure and multiple organ damage in aged mice[J]. Kidney Int, 2003, 64(5): 1620-31. doi:10.1046/j.1523-1755.2003.00268.x |
| [8] | 许力, 吴珊, 杨清海, 等. 免疫组化技术(六)[J]. 诊断病理学杂志, 2010, 17(1): 79. Xu L, Wu S, Yang Q H, et al. Immunohistochemistry (6)[J]. Chin J Diagn Pathol, 2010, 17(1): 79. |
| [9] | Alves-Filho J C, Freitas A, Souto F O, et al. Regulation of chemokine receptor by Toll-like receptor 2 is critical to neutrophil migration and resistance to polymicrobial sepsis[J]. Proc Natl Acad Sci USA, 2009, 106(10): 4018-23. doi:10.1073/pnas.0900196106 |
| [10] | Jung Y, Jerng U, Lee S. A systematic review of anticancer effects of Radix Astragali[J]. Chin J Integr Med, 2016, 22(3): 225-36. doi:10.1007/s11655-015-2324-x |
| [11] | Fu X, Song B, Tian G W, Li J L. The effects of the water-extraction of Astragali Radix and Lycopi herba on the pathway of TGF-smads-UPP in a rat model of diabetic nephropathy[J]. Pharmacogn Mag, 2014, 10(40): 491-6. doi:10.4103/0973-1296.141773 |
| [12] | Kolaczkowska E, Kubes P. Neutrophil recruitment and function in health and inflammation[J]. Nat Rev Immunol, 2013, 13: 159-75. doi:10.1038/nri3399 |
| [13] | Garg A D, Vandenberk L, Fang S, et al. Pathogen response-like recruitment and activation of neutrophils by sterile immunogenic dying cells drives neutrophil-mediated residual cell killing[J]. Cell Death Differ, 2017, 24(5): 832-43. doi:10.1038/cdd.2017.15 |
| [14] | 赵建军, 张建勇, 陈玲. 黄芪甲苷对急性肺损伤大鼠肺水通道蛋白5表达的影响[J]. 中国医院药学杂志, 2013, 33(5): 385-9. Zhao J J, Zhang J Y, Chen L. Influence of astragaloside on aquaporin 5 in rats with acute lung injury[J]. Chin Hosp Pharm J, 2013, 33(5): 385-9. |
| [15] | Huang P, Lu X, Yuan B, et al. Astragaloside IV alleviates E. coli-caused peritonitis via upregulation of neutrophil influx to the site of infection[J]. Int Immunopharmacol, 2016, 39: 377-82. doi:10.1016/j.intimp.2016.08.011 |

