


2. 浙江大学附属邵逸夫医院心血管内科,浙江 杭州 310014;
3. 浙江省立同德医院呼吸内科,浙江 杭州 310012;
4. 温州医科大学附属第一医院呼吸内科,浙江 温州 325000
 ,
LIN Jian-wei2
,
LIN Jian-wei2 ,
LI Guo-ping3,
REN Zhuo-chao1,
LI Ya-qing1,
YAN Jian-ping1
,
LI Guo-ping3,
REN Zhuo-chao1,
LI Ya-qing1,
YAN Jian-ping1
 ,
WANG Liang-xing4
,
WANG Liang-xing4

2. Dept of Cardiology, Sir Run Run Shaw Hospital, Clinical Medicine of Zhejiang University, Hangzhou 310016, China;
3. Dept of Respiratory Medicine, Tongde Hospital of ZheJiang Province, Hangzhou 310012, China;
4. Dept of Respiratory Medicine, the First Affiliated Hospital, Wenzhou Medical College, Wenzhou Zhejiang 325000, China
急性肺栓塞(pulmonary thromboembolism,PTE)为临床常见病、危重病[1]。急性PTE严重肺损伤和肺动脉高压是其引起死亡的直接原因。传统观念认为,急性PTE性肺动脉高压形成与血栓的机械阻塞作用关系密切[1]。然而,近年来研究发现,急性PTE血栓的机械阻塞程度与肺动脉压力的增高并不一致,即使机械性阻塞已基本解除,仍存在着肺动脉压力持续升高的现象[2]。又有研究证实,急性PTE时栓塞血管周围大量炎症细胞浸润,其释放的细胞因子可进一步加重肺动脉内皮的损伤,在PTE性肺动脉高压的形成中起到不可忽视的作用[3]。单核细胞趋化蛋白-1(monocyte chemoattractant protein-1,MCP-1) 是活化和聚集单核炎症细胞至血管内皮细胞的重要介导者。MCP-1属于趋化因子家族,趋化因子是具有趋化白细胞作用的一类蛋白质或多肽,可分为4类,即CXC趋化因子、CC型趋化因子、C趋化因子及CNC趋化因子。MCP-1是CC亚族其中一员,位于第17号染色体上,由多种细胞产生,包括单核细胞、内皮细胞、巨噬细胞、平滑肌细胞、脂肪细胞和系膜细胞等[4]。它能够趋化和活化诸如肥大细胞、树突状细胞、T淋巴细胞、自然杀伤细胞、单核细胞、中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞等炎性细胞[5],使各种炎性细胞向病变部位聚集,通过与各细胞上的CC趋化蛋白受体2(C-C chemokine receptor type 2,CCR2) 受体结合而发挥生物学作用。Eagleton等[6]发现,在PTE早期,肺动脉壁中MCP-1表达明显升高同时快速趋化炎症细胞浸润至肺动脉壁周围。可见,在启动血管的炎症反应及血管内皮细胞损伤中MCP-1是关键的炎症趋化因子,MCP-1与栓塞性肺动脉高压形成密切相关。
中药单体白藜芦醇(resveratrol, RES)是一种植物多酚,具有抗氧化、抗肿瘤及抗炎症效应[7]。Cullen等[8]报道,白藜芦醇可抑制血管内皮细胞MCP-1的合成和分泌。又有研究发现,白藜芦醇可抑制MCP-1在血管炎症动物模型中释放[9]。因此,本研究通过复制大鼠急性PTE模型,应用MCP-1中和抗体C1142及中药单体白藜芦醇对急性PTE后MCP-1表达的影响,评价MCP-1是否参与急性PTE性肺动脉高压的形成,以及白藜芦醇是否通过下调MCP-1的表达,从而降低急性PTE后肺动脉高压。
1 材料 1.1 动物SPF级标准健康♂Sprague-Dawley(SD)大鼠150只,体质量300~350 g,温州医学院实验动物中心提供。动物合格证为SCXK(浙)2005-0019。动物采用标准颗粒饲料喂养,自由进食、饮水。
1.2 试剂与仪器多克隆兔抗鼠MCP-1抗体(Abcam);白藜芦醇(Sigma);SYBR Green Real-time PCR Master(Toyobo);C1142(Centocor);RPMI 1640培养基、胎牛血清、TRIzol(Gibco)。PowerLab生理记录仪(AD Instruments);Bio-Rad PCR System S1000(Bio-Rad);聚乙烯导管1106(中国浙江宁波安来生命科学软件及器械公司)。
2 方法 2.1 实验分组150只SD大鼠按完全随机设计分为正常对照(C组)、溶剂对照组(S组)、急性PTE组(PTE组)、急性PTE+白藜芦醇组(PTE+Res组)和急性PTE+C1142(C1142) 组,各组又分为1、4、8 h共3个时点,每个时间点各10只大鼠。
2.2 急性PTE大鼠模型建立所有大鼠颈部剃除毛发,并对皮肤进行消毒,分离左颈动脉并接入19G头皮针留取0.5 mL血液使血栓形成。待血栓凝固后将其切成约11 mm×1 mm×3 mm大小的栓子。分离右颈静脉并插入装有血栓的聚乙烯导管-1106并与PowerLab连接。为最大程度地降低血栓输注过程中大鼠的致死率,设置血栓(180 mg·kg-1)输注时间大于5 min。并根据信号采集器显示的右心室压力控制在40 mmHg以保证最适宜的血栓输入量[10]。C组和S组分别输注等量的0.9%生理盐水和1% DMSO代替血栓,其余操作相同。分别在各组大鼠血栓输注后1、4、8 h,采用改良右心导管法进行肺动脉平均压力(mean pulmonary artery pressure,MPAP)测量。以上操作均在无菌条件下进行。
2.3 C1142及白藜芦醇药物干预PTE+C1142组在复制急性肺栓塞模型前1 h尾静脉注射C1142 2 mg·kg-1(溶于1%的DMSO);PTE+RES组复制急性PTE模型前1 h尾静脉注射白藜芦醇2.5 mg·kg-1(溶于1%的DMSO);C组于大鼠尾静脉注入等量无菌生理盐水;S组大鼠尾静脉注射等量1% DMSO溶液;以上操作均在无菌条件下完成。
2.4 标本收集各组大鼠均行下腔静脉取血后处死,切取部分肺组织,予4%多聚甲醛固定作免疫组化检测MCP-1蛋白表达,部分肺组织放人无菌去酶冻存管中,经过液氮速冻后再于-70℃冰箱保存,并行real-time PCR及Western blot检测肺组织MCP-1。
2.5 免疫组化检测MCP-1蛋白表达将肺组织经4%多聚甲醛固定后用石蜡包埋切片,将切片放入含兔抗大鼠MCP-1多克隆抗体室温下孵育2 h,再与辣根过氧化物酶标记的二抗共同孵育1 h,最后用含二氨基联苯的底物显色,苏木精复染。一抗用PBS代替作为空白对照组。黄色代表阳性,并按黄色深浅代表阳性强弱。
2.6 Real time-PCR检测MCP-1 mRNA表达使用TRIzol从100 mg快速冰冻组织中萃取总RNA。RNA浓度定量在波长260 nm处的吸光度,RNA纯度在波长260 nm和280 nm(A260/280) 被检测。取1 μg总RNA与2 μL 5×RT Buffer、0.5 μL RT Enzyme Mix、0.5 μL Primer Mix在Bio-Rad PCR system S1000上进行逆转录。将逆转录终产物溶于10 μL去RNA酶水中备用。MCP-1上游引物序列5′-GTCTCTGTCACGCTTCTG-3′,下游引物5′-TGCTGGTGATTCTCTTGTAG-3′。内参GAPDH上游引物序列5′-AGAACATCATCCCTGCATCC-3′,下游引物序列5′-TGGATACATTGGGGGTAGGA-3′。PCR参数设置如下:95℃ 2 min, 95℃ 15 s,62℃ 1 min 40个循环。所有PCR结果由ABI7500 System SDS软件分析,实验数据使用2-ΔΔCT方法分析。
2.7 Western blot检测MCP-1蛋白表达所有肺组织蛋白浓度均使用BCA法检测,采用15%的分离胶和5%的浓缩胶进行聚丙烯酰胺凝胶电泳(SDS-PAGE),分别用兔抗大鼠MCP-1多克隆抗体(1:500)4℃封闭过夜后,再与辣根过氧化物酶(HRP)标记的羊抗兔二抗(1:5 000) 孵育2 h;化学发光、显影、定影;将胶片进行扫描,用Quantity One凝胶图像分析软件分析各组蛋白表达。
2.8 统计学分析全部数据采用SPSS16.0统计软件分析。所有数据进行正态性检验,计数资料用x±s表示;多组样本均数比较进行方差齐性检验,组间比较采用单因素方差分析(one-way ANOVA)。方差齐性者两两比较采用LSD法,方差不齐者进行Dunnet′s T3检验。
3 结果 3.1 动物一般情况大鼠自体PTE模型制备完成共90只,其中自体栓塞成功且经右心导管法成功测得肺动脉压力(Fig 1)者为82只大鼠,成功率为91.1%(82/90), 中途死亡数8只,死亡率为8.9%(8/90)。大鼠表现有呼吸加快加深、口唇发绀、两肺出现弥漫性干湿啰音等PTE体征。大体组织见肺膨胀不全,多散在出血灶,肺组织光镜见肺动脉内有注入的血栓,同时见肺血管壁肌层组织水肿,提示急性PTE模型复制成功。

|
| Fig 1 The waveform chart of pulmonary artery pressure in rats |
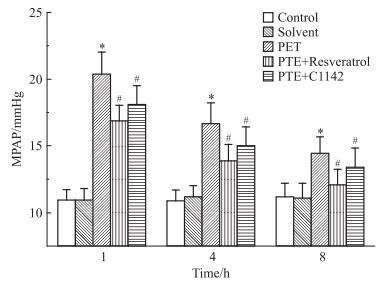
Fig 2结果显示,S组MPAP较C组有降低趋势,但两组间数据差异无统计学意义;急性PTE组MPAP明显高于S组,RES组MPAP明显低于急性PTE组,C1142组MPAP明显低于急性PTE组,它们之间的差异均有统计学意义(P<0.05)。
|
| Fig 2 Mean pulmonary artery pressure in five groups at 1, 4, and 8 h time points(x±s, n=10) At 4 and 8 h, MPAP levels were similarly elevated.*P < 0.05 vs solvent; #P < 0.05 vs PTE |
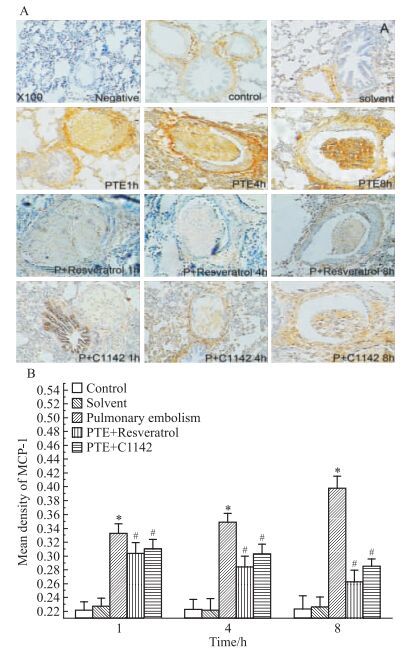
各相同时间点,各组大鼠肺组织免疫组织化学法MCP-1蛋白表达结果如Fig 3所示,C、S组大鼠肺组织内未见明显MCP-1蛋白表达;急性PTE组MCP-1蛋白表达较S组表达明显增高,两组间的差异有统计学意义(P<0.05);RES组及C1142组MCP-1蛋白表达较急性PTE组降低,两组间的差异有统计学意义(P<0.05)。
|
| Fig 3 Localization of MCP-1 protein in lung tissues by immunohistochemistry(×100) A: MCP-1 was intensively expressed in the pulmonary artery walls, bronchial walls and in the thrombus of the five groups. Tissue sections from rat lung were stained with anti-MCP-1 antibodies to determine localization. The negative group was the blank control group. B: The figure showed the optical density of MCP-1 in five groups(x±s, n=10).P:PTE.*P < 0.05 vs solvent; #P < 0.05 vs PTE |
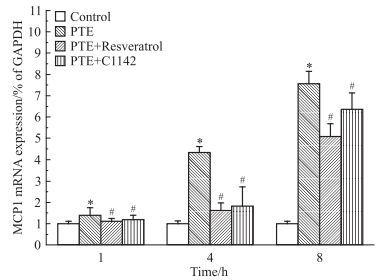
各相同时间点,各组大鼠肺组织MCP-1 mRNA表达结果如Fig 4所示,S组MCP-1 mRNA 2-ΔΔCT值设为1;急性PTE组MCP-1 mRNA表达的CT值较S组明显增高,差异有统计学意义(P<0.05);RES组及C1142组MCP-1 mRNA CT值均较急性PTE组降低,差异有统计学意义(P<0.05)。
|
| Fig 4 Effects of resveratrol or C1142 on expression of MCP-1 mRNA in rats by Real-time PCR(x±s, n=10) MCP-1 mRNA levels were expressed as CT-value and normalized to the expression of GAPDH mRNA. The value of MCP-1 mRNA in the solvent group was 1.*P < 0.05 vs solvent; #P < 0.05 vs PTE |
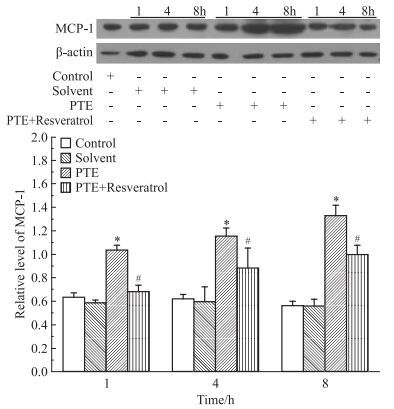
各相同时间点,各组大鼠肺组织Western blot法检测MCP-1蛋白表达结果见Fig 5、6。S组MCP-1蛋白表达与C组比较差异无统计学意义;急性PTE组MCP-1蛋白表达较S组明显增高,差异有统计学意义(P<0.05);RES组及C1142组MCP-1蛋白表达均较急性PTE组明显降低,差异有统计学意义(P<0.05)。
|
| Fig 5 Effect of resveratrol on protein expression of MCP-1 in rats by Western blot(x±s, n=10) Rats were treated with resveratrol, and levels of MCP-1 protein expression were measured by Western blot at 1, 4, and 8 h time points. β-actin was used to normalize protein loading.*P < 0.05 vs solvent; #P < 0.05 vs PTE |
|
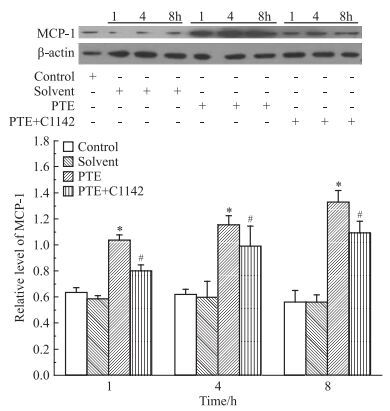
| Fig 6 Effect of C1142 on protein expression of MCP-1 in rats by Western blot(x±s, n=10) Rats were treated with C1142, and levels of MCP-1 protein expression were measured by Western blot at 1, 4, and 8 h time points. β-actin was used to normalize protein loading.*P < 0.05 vs solvent; #P < 0.05 vs PTE |
近年来研究证实,在启动血管的炎症反应中MCP-1可能是关键的炎症趋化因子,是活化和聚集炎症细胞至血管内皮的重要介导者[11]。又有报道指出,在大鼠PTE模型中观察到MCP-1在肺组织、肺动脉内皮细胞中均有大量表达,表明MCP-1可能与PTE后炎症细胞浸润及肺动脉高压形成过程中密切相关[12]。
本实验结果发现,急性PTE 1、4 h组血栓几乎阻塞了整个肺动脉管腔,由于血栓机械阻塞作用MPAP明显增高;急性PTE 8 h组血栓对血管的机械阻塞作用较4 h组减少,但MPAP值却未降低,差异无统计学意义。急性PTE后,由于体内纤溶系统迅速激活[13],血栓开始溶解,为何肺动脉压力仍持续增高?目前认为可能与PTE后,栓塞血管周围大量炎性细胞浸润,其释放的细胞因子加重肺动脉内皮的损伤有关[13],而MCP-1是活化和聚集单核炎症细胞至血管内皮细胞的重要介导者。Eagleton等[6]发现,在PTE后肺动脉壁中MCP-1表达量明显升高。本实验也观察到急性PTE组8 h组的MCP-1蛋白及mRNA表达明显增高。因此,本研究推测急性PTE后MCP-1的表达与急性PTE后肺动脉高压形成相关。为进一步探讨MCP-1表达与MPAP关系,本实验在1、4、8 h分别加用MCP-1特异性中和抗体C1142进行干预。实验结果显示,各相同时间点,C1142组MPAP值均较急性PTE组明显降低,差异有统计学意义。表明除血栓对肺动脉的机械阻塞作用外,急性PTE后MCP-1的表达增高参与肺动脉高压的形成。因此,抑制MCP-1表达是降低急性PTE后肺动脉压力的一种有效手段。
中药单体白藜芦醇属芪类化合物, 目前已经在21个科、31个属的72种植物中发现了白藜芦醇,其中,葡萄、虎杖和花生中白藜芦醇含量较高。化学名为3, 4′, 5-三羟基-1, 2-二苯乙烯(3, 4′, 5-trihydrolystilbene),分子式C14H12O3,相对分子质量为228.25,有顺、反两种结构。单体白藜芦醇为无色针状晶体溶于丙酮、乙醇、甲醇等有机溶剂,难溶于水。溶点为256℃~258℃。自从1997年Jang等[7]在《Science》发表中药单体白藜芦醇具有抗肿瘤作用后,该药备受关注。其药理作用包括抗癌、心血管保护作用、抗氧化及抗自由基作用[15-16]。其抗炎效应也已被证实。Park等[17]发现,白藜芦醇在动脉粥样硬化形成中可明显下调MCP-1的表达,预防血管壁泡沫细胞生成。Zhu等[18]亦证实了白藜芦醇可减少在TNF-α诱导下MCP-1的大量表达。本实验利用在体大鼠急性PTE模型,探究白藜芦醇对急性PTE后MCP-1表达及肺动脉高压的效应。实验结果发现,白藜芦醇可通过下调急性PTE后MCP-1 mRNA和蛋白水平,从而明显降低急性PET后肺动脉高压,减少栓塞后肺损伤。然而,目前关于白藜芦醇如何下调急性PTE后MCP-1表达,降低肺动脉压力的机制仍尚不明确。丝裂原活化蛋白激酶(mitogen-activated protein kinases, MAPKs)是生物细胞内一类丝氨酸/苏氨酸蛋白激酶。多项研究表明,MAPKs信号转导通路将细胞外刺激信号转导至细胞质及其核内,在引起生物学反应(如细胞分化、增殖、转化、凋亡等)过程中具有十分重要的作用。p38 MAPK通路是1993年发现的信号转导通路,属于MAPKs成员之一,一旦它被激活,细胞质中的非磷酸化p38 MAPK转化为磷酸化p38 MAPK,而后移位到细胞核内。既往研究证实p38 MAPK是MCP-1产生的关键上游分子,抑制p38 MAPK通道可以减少MCP-1的大量表达[19, 20]。Gresele等[21]发现白藜芦醇在急性缺血性心脏疾病中可通过p38 MAPK信号转导通路减少大量炎症趋化因子产生。Chakraborty等[22]亦报道白藜芦醇可通过抑制p38 MAPK信号转导通路激活减少炎症反应发生。SB203580是p38 MAPK的特异性的吡啶异咪哒唑类抑制剂的突出代表。本实验后续实验将加用p38 MAPK通路特效抑制剂SB203580预孵育,继续探究在急性PTE后白藜芦醇是否可通过抑制p38MAPK信号转导通路减少MCP-1的大量表达,抑制急性PTE后肺动脉高压的分子机制。
综上所述,本研究显示除血栓的机械性阻塞作用外,MCP-1的大量表达也参与急性PTE后肺动脉高压的形成;白藜芦醇通过下调急性PTE后MCP-1表达,从而降低肺动脉高压。白藜芦醇可能成为一种新型的预防急性PTE后肺动脉高压形成的药物。
( 致谢: 本实验主要在温州医科大学科研平台中心完成,在此对实验室各位老师及同学的帮助表示衷心的感谢!)
| [1] | Smulders Y M. Pathophysiology and treatment of haemodynamic instability in acute pulmonary embolism: the pivotal role of pulmonary vasoconstriction[J]. Cardiovasc Res, 2000, 48(1): 23-33. doi:10.1016/S0008-6363(00)00168-1 |
| [2] | Kimura H, Okada O, Tanabe N, et al. Plasma monocyte chemoattractant protein-1 and pulmonary vascular resistance in chronic thromboembolic pulmonary hypertension[J]. Am J Respir Crit Care Med, 2001, 164(2): 319-24. doi:10.1164/ajrccm.164.2.2006154 |
| [3] | Langer F, Schramm R, Bauer M, et al. Cytokine response to pulmonary thromboendarterectomy[J]. Chest, 2004, 126(1): 135-41. doi:10.1378/chest.126.1.135 |
| [4] | 姜懿纳, 陈乃宏. CCL2/MCP-1在其相关疾病的机制研究[J]. 中国药理学通报, 2016, 32(12): 1634-8. Jiang Y N, Chen N H. Mechanism of CCL2 / MCP-1 in its relevant diseases[J]. Chin Pharmacol Bull, 2016, 32(12): 1634-8. doi:10.3969/j.issn.1001-1978.2016.12.002 |
| [5] | Katsoulidis E, Li Y Z, Mears H, et al. The p38 mitogen-activated protein kinase pathway in interferon signal transduction[J]. J Interferon Cytokine Res, 2005, 25(12): 749-56. doi:10.1089/jir.2005.25.749 |
| [6] | Eagleton M J, Henke P K, Luke C E, et al. Inflammation and intimal hyperplasia associated with experimental pulmonary embolism[J]. J Vasc Surg, 2000, 36(3): 581-8. |
| [7] | Jang M, Cai L, Udeani G O, et al. Cancer chemopreventive activity of resveratrol a natural product derived from grapes[J]. Science, 1997, 275(5297): 218-20. doi:10.1126/science.275.5297.218 |
| [8] | Cullen J P, Morrow D, Jin Y, et al. Resveratrol, a polyphenolic phytostilbene, inhibits endothelial monocyte chemotactic protein-1 synthesis and secretion[J]. J Vasc Res, 2007, 44(1): 75-84. |
| [9] | Rius C, Abu-Taha M, Hermenegildo C, et al. Trans-but not cis-resveratrol impairs angiotensin-Ⅱ-mediated vascular inflammation through inhibition of NF-kappa B activation and peroxisome proliferator-activated receptor-gamma upregulation[J]. J Immunol, 2010, 185(6): 3718-27. doi:10.4049/jimmunol.1001043 |
| [8] | Runyon M S, Gellar M A, Sanapareddy N, et al. Development and comparison of a minimally-invasive model of autologous clot pulmonary embolism in Sprague-Dawley and Copenhagen rats[J]. Thromb, 2010, 8(3): 35-43. |
| [11] | Urs J, Heidemann S M. Heat stress decreases pulmonary MCP-1 production in endotoxemia[J]. Cytokine, 2014, 26(6): 243-6. |
| [12] | Watts J A, Zagorski J, Gellar M A, et al. Cardiac inflammation contributes to right ventricular dysfunction following experimental pulmonary embolism in rats[J]. Mol Cell Cardiol, 2006, 41(2): 296-307. doi:10.1016/j.yjmcc.2006.05.011 |
| [13] | 宋伟, 明章银. 血小板在静脉血栓形成及诊断中的作用研究进展[J]. 中国药理学通报, 2017, 33(7): 889-92. Song W, Ming Z Y. Resarch progress on role of platelets in development and diagnosis of venous thrombosis[J]. Chin Pharmacol Bull, 2017, 33(7): 889-92. |
| [14] | Rectenwald J E, Deatrick K B, Sukheepod P, et al. Experimental pulmonary embolism: Effects of the thrombus and attenuation of pulmonary artery injury by low-molecular-weight heparin[J]. J Vasc Surg, 2006, 43(4): 800-8. doi:10.1016/j.jvs.2005.12.010 |
| [15] | Subbaramaiah K, Chung W J, Michaluart P, et al. Resveratrol inhibits cyclooxygenase-2 transcription and activity in phorbol ester-treated human mammary epithelial cells[J]. J Biol Chem, 1998, 273(34): 21875-82. doi:10.1074/jbc.273.34.21875 |
| [16] | Asou H, Koshizuka K, Kyo T, et al. Resveratrol, a natural product derived from grapes, is a new inducer of differentiation in human myeloid leukemias[J]. Int J Hematol, 2012, 75(5): 528-33. |
| [17] | Park D W, Baek K, Kim J R, et al. Resveratrol inhibits foam cell formation via nadph oxidase 1-mediated reactive oxygen species and monocyte chemotactic protein-1[J]. Exp Mol Med, 2009, 41(3): 171-9. doi:10.3858/emm.2009.41.3.020 |
| [18] | Zhu J, Yong W, Wu X H, et al. Anti-inflammatory effect of resveratrol on TNF-alpha-induced MCP-1 expression in adipocytes[J]. Biochem Biophys Res Commun, 2008, 369(2): 471-7. doi:10.1016/j.bbrc.2008.02.034 |
| [19] | 李学娟, 陈泽彬, 魏红, 等. 大黄素对高糖培养的GMC增殖、FN表达及p38MAPK的影响[J]. 中国药理学通报, 2014, 30(2): 233-8. Li X J, Chen Z B, Wei H, et al. Effects of emodin on cell proliferation, FN expression and p38MAPK pathway in rat mesangial cells cultured under high glucose[J]. Chin Pharmacol Bull, 2014, 30(2): 233-8. |
| [20] | Green S R, Han K H, Chen Y, et al. The CC chemokine MCP-1 stimulates surface expression of CX3CR1 and enhances the adhesion of monocytes to fractalkine/CX3CL1 via p38 MAPK[J]. J Immunol, 2006, 176(12): 7412-20. doi:10.4049/jimmunol.176.12.7412 |
| [21] | Gresele P, Pignatelli P, Guglielmini G, et al. Resveratrol at concentrations attainable with moderate wine consumption, stimulates human platelet nitric oxide production[J]. Nutr, 2008, 138(9): 1602-8. |
| [22] | Chakraborty P K, Mustafi S B, Raha S. Pro-survival effects of repetitive low-grade oxidative stress are inhibited by simultaneous exposure to resveratrol[J]. Pharmacol Res, 2008, 58(5-6): 281-9. doi:10.1016/j.phrs.2008.08.007 |