


2. 锦州医科大学药理学教研室,辽宁 锦州 121000
2. Dept of Pharmacology, Jinzhou Medical University, Jinzhou Liaoning 121000, China
丘脑底核(subthalamic nucleus,STN)是基底神经节(basal ganglia,Bgl)重要的核团之一,主要调控机体的运动功能及行为。苍白球(globus pallidus,Gpe)和黑质网状部之间的重要中继站就是STN,在调节Bgl神经核团之间的生理功能及病理活动中起关键的整合作用[1-2]。神经内分泌生物活性肽优洛可定(urocortin,UCN)是由下丘脑分泌,具有多种神经及心血管功能[3]。目前的研究表明,UCN在生理及病理情况下可能对中枢神经系统(central nervous system, CNS)具有保护功能[4-5]。在本实验室既往的研究中发现,UCN对Bgl的另一个主要核团——纹状体(striatum, STR)的自发放电有抑制作用[6],另外,也发现UCN能通过抑制STR的多巴胺(dopamine,DA)神经元功能,同时抑制兴奋性神经递质的兴奋毒性,可能在帕金森疾病(Parkinson’s disease, PD)中发挥治疗作用[7]。但目前,UCN对STN的神经元放电的影响及对STN内神经递质(如兴奋性神经递质GLU及抑制性递质DA)的调节作用未见报道。本实验选用神经电生理中常用且经典的微电泳技术,结合细胞外记录的实验方法,微电泳UCN、促皮质素释放因子2型受体(corticotropin releasing factor 2 receptor,CRF-2R)抑制剂Astressin(AST),监测两者对STN神经元放电频率及波形影响,同时监测UCN对STN中抑制性DA能、兴奋性GLU能神经传递的改变,以探讨STN内兴奋及抑制性神经递质间的相互平衡及制约作用,及可能的神经通路机制。目前,很多研究已明确STN是导致PD的重要核团[8]。因此,本研究将为临床治疗神经系统常见疾病,如PD的诊断及治疗,提供有效而可靠的药物作用靶点。
1 材料与方法 1.1 实验动物与试剂Sprague-Dawley(SD)大鼠40只,由锦州医科大学实验动物中心提供,体质量180~220 g,动物合格证号:SCXK(辽) 2007-0009。UCN(10-6 mol·L-1);Astressin(AST,CRF-2R的受体阻断剂,10-6 mol·L-1);DA 0.5 mol·L-1;Cropromazine(CPM,为DA受体的阻断剂,1.0 mol·L-1);GLU(1.0 mol·L-1);MK-801(NMDA受体的常用阻断剂,1.0 mol·L-1);PKA及H-89,上述药品及试剂全部购自美国Sigma公司。
1.2 麻醉开颅并对STN定位取40只上述SD大鼠,乌拉坦腹腔注射(1 g·kg-1)全麻,麻醉成功后,将大鼠置于脑立体定位仪,定位STN,常规开颅术开颅。根据Paxions & Watson大鼠脑图谱,确定STN的坐标:中线旁开2.5~3.0 mm,前囟后3.8~4.0 mm,脑表下7.0~8.0 mm。
1.3 微电泳受试药物采用神经电生理学实验方法中的微电泳技术(51-217型微管拉制仪,美国STOELTING公司)及神经元细胞外记录相结合的实验方法。拉制的7管玻璃微电极呈伞装,中心管直径为4~8 μm间,中心电阻在5~12 MΩ作用。含有1%滂胺天蓝的NaCl溶液(3.0 mol·L-1)灌注于中心管内,作为本实验用引导电极;另外6个外周管的电阻均应控制在20~100 MΩ之间,分别灌注下列受试药物,包括UCN、AST、DA、CPM、GLU以及MK-801。
1.4 生物肽UCN对STN神经元放电影响微电极推进器将玻璃微电极接近定位的STN坐标位置,然后缓慢插入STN,DAM80微电极放大器采集STN神经元单位放电,经过滤波后,示波器上显示STN神经元放电波形,Spike2采集系统(英国CED公司)处理神经元输入的生物电信号。在本实验中,监测STN神经元自发放电情况,包括观察STN放电波形、STN神经元传出分布的方式及频率、是否有爆发式放电、放电的基本特征及形式。通过外周管分别微电泳不同的受试药物,包括微电泳不同浓度神经内分泌生物活性肽UCN及CRF-2R阻断剂AST,微电泳为电流40 nA,滞流的阻力电流为10 nA,微电泳时程20 s,记录UCN及CRF-2R阻断剂对STN神经元放电影响。微电泳UCN过程中给予AST,监测UCN及CRF-2R之间的关系。
1.5 生物肽UCN对STN内的DA能、GLU能神经传递的影响6个外周管实验前1 h灌注GLU及NMDA阻断剂MK-801,把GLU微电泳入STN神经元,观察STN内的神经元自发放电的变化,于微电泳GLU的41~60 s,微电泳20 s UCN,于微电泳GLU的81~100 s之间微电泳AST,20 s。监测UCN对STN内GLU能神经传递的影响。同上述方法,把DA及其受体阻断剂CPM微电泳入STN神经元,监测STN神经元放电的变化,于微电泳DA的41~60 s、81~100 s之间,分别微电泳UCN和CRF-2R阻断剂AST各20 s,监测UCN对STN内DA能神经传递的影响。最后,在微电泳CRF-2R阻断剂AST-2B、PKA及其阻断剂H-89,观察UCN对STN中神经元影响的可能信号机制。
1.6 数据统计实验数据经处理器输出后,生成系列密度直方图,自动统计观STN神经元数量,同时计数给药前后STN神经元放电频率、特征及波形等的变化。实验数据以x±s表示。数据分析采用SPSS13.0统计软件进行统计学处理。
2 结果 2.1 STN神经元自发放电情况共定位并成功观察到STN神经元58个,观察受试STN神经元的放电波形及特征。STN神经元放电频率比较缓慢并且规则,大多为单个神经元放电,为单峰,未见双向动作电位(action potential, AP),未见爆发式多棘放电。STN神经元放电频率一般在0~8 Hz之间。
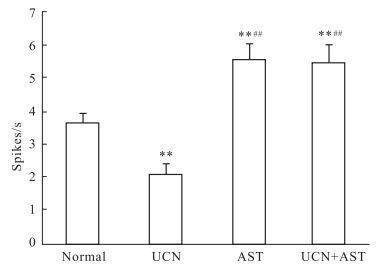
2.2 神经肽UCN及AST对STN神经元放电影响本部分实验中共观察STN神经元33个。将UCN(10-6 mol·L-1, 20 nA,20 s)微电泳入受试的STN神经元,81.81%(27/33) STN神经元自发放电频率被降低,对18.19%(6/33) STN神经元无明显改变。上述33个被观察的STN神经元的平均放电频率由微电泳前的(3.65±0.27) Hz减少至(2.05±0.33) Hz,给予UCN前、后STN神经元放电频率降低,差异具有显著性(P<0.01)。此外,选择对UCN产生抑制作用的STN神经元24个,给予AST(10-6 mol·L-1, 20 nA,20 s),实验中发现79.17%(19/24) STN的放电频率被CRF-2R阻断剂AST明显升高,由(3.45±0.36) Hz升高至(5.55±0.47) Hz(P<0.01)。选取对UCN产生抑制效应的上述STN神经元中的20个,微电泳UCN(20 nA,40 s)过程中给予AST(20 nA,20 s),实验中发现UCN的抑制效应被AST拮抗,差异具有显著性(P<0.01),可翻转85%(17/20) STN神经元的抑制效应,频率由(2.11±0.34) Hz增加至(5.45±0.53) Hz。见Fig 1。
|
| Fig 1 Effect of UCN on STN neuron's spontaneous discharge AST was used during the period of 21th-40th s in UCN. **P < 0.01 vs normal group; ##P < 0.01 vs UCN group. |
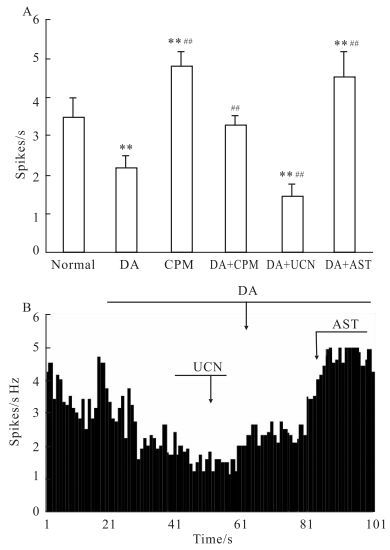
在本部分实验中,观察了对DA产生抑制效应的STN神经元共计21个。发现DA(20 nA,20 s)可使正常的STN神经元产生抑制效应,拮抗STN神经元的正常自发放电波形及频率。STN放电频率由(3.45±0.55) Hz降低至(2.17±0.32) Hz,该实验数据差异具有显著性(P<0.01)。然后,选取上述对DA产生抑制效应的21个STN神经元,于微电泳DA的21~40 s之间,外周管微电泳UCN(20 nA,20 s),发现71.42%(15/21) STN中的DA神经元的放电频率进一步下降,放电频率由(2.17±0.32) Hz明显减少至(1.45±0.29) Hz,(P<0.05)。最后,在微电泳DA的61~80 s之间,由外周管同时微电泳AST(20 nA,20 s),使原本抑制的76.19%(16/21) STN中DA神经元放电频率明显增加,放电频率由(1.65±0.27) Hz增加至(4.52±0.68) Hz,该实验数据差异具有显著性(P<0.05)。见Fig 2。
|
| Fig 2 Effects of UCN on DA-ergic neuron in STN A: UCN affected DA-ergic neuron in STN. UCN and AST were used to observe the effects of UCN on DA; B: The effects and wave of UCN on STN's DA-ergic neurons. **P < 0.01 vs normal group; ##P < 0.01 vs DA group. |
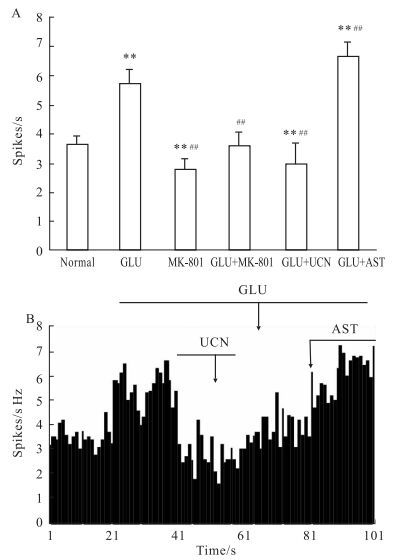
在本部分实验中,观察对GLU产生兴奋效应的STN神经元共计18个。由外周管微电泳GLU(20n A,20 s),77.78%(14/ 18) STN神经元产生兴奋效应,其自发放电频率明显加快,差异具有显著性(P<0.01)。然后,选择上述对GLU产生兴奋效应的14个STN神经元,在21~40 s之间由外周管微电泳UCN(20 nA,20 s),STN中的78.57%(11/14) 的GLU能放电频率明显减少(P<0.01),放电频率由(5.67±0.48) Hz减少至(2.93±0.77) Hz。最后,选用对GLU产生兴奋效应的GLU能神经元14个,在微电泳GLU的61~80 s,于外周管微电泳CRF-2R阻断剂AST(20 nA,20 s),AST可明显增加STN神经元放电频率(P<0.05),放电频率由(5.65±0.38) Hz增加至(6.65±0.47) Hz,见Fig 3。
|
| Fig 3 Effects of UCN on glu-ergic neuron in STN A: UCN affected GLU-ergic neuron in STN. UCN could inhibit the excited effects of GLU and AST could excited GLU in STN; B: The effects and wave of UCN on STN's GLU-ergic neurons. **P < 0.01 vs normal group; #P < 0.05, ##P < 0.01 vs GLU group. |
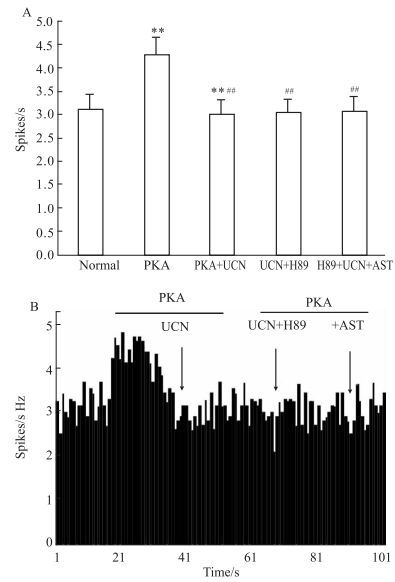
通路的影响在本研究中,另选择对PKA产生作用的STN神经元16个,在提前给予PKA通路激动剂后,再给予UCN,UCN可阻断PKA产生的兴奋效应,在21~40 s之间由外周管微电泳UCN(20 nA,20 s),STN中的75.0%(12/16) 的GLU能放电频率明显减少(P<0.01),放电频率由(4.29±0.37) Hz减少至(3.02±0.33) Hz。在微电泳PKA期间,于外周管微电泳H89(20 s),PKA的兴奋效应消失,而给予UCN,不能继续抑制STN神经的放电,放电频率由微电泳前的(3.06±0.34) Hz变化至(3.03±0.29) Hz。给予CRF-2R阻断剂AST(20 nA,20 s),AST也不再增加STN神经元放电频率,放电频率变化为(3.07±0.33) Hz(P>0.05)。见Fig 4。
|
| Fig 4 Effects of UCN on PKA in STN A: UCN affected CRF-2R and PKA in STN. During the period of PKA, administrated UCN, PKA and H89; B: The effects and wave of UCN on STN's PKA and CRF-2R. **P < 0.01 vs normal group; ##P < 0.01 vs PKA group. |
本实验结果表明,神经内分泌生物肽UCN可明显降低基底神经节中的STN神经元放电频率及波形,给药过程中未见爆发式放电,提示UCN抑制STN神经元的放电。然而,CRF-2R阻断剂AST明显加快STN神经元的放电频率,给予AST过程中偶见爆发式放电。另外,微电泳UCN期间同时微电泳AST,AST翻转UCN的抑制效应,实验结果进一步提示STN中存在UCN能神经元,并且UCN与CRF-2R结合后触发随后的生物学效应,产生对STN的抑制作用。
本实验中的结果进一步证实,DA能在STN的神经传递中起抑制效应,而由外周管同时微电泳UCN,UCN协同了DA的抑制效应。相反,AST产生兴奋效应,拮抗DA的抑制效应。本实验结果提示,DA能与UCN在STN的神经元中存在交汇现象。DA能与UCN都对STN放电产生抑制效应,进一步提示UCN可能在PD等病理情况下,对STN神经元起保护作用,并且这种保护作用是通过与CRF-2R结合而实现的。
本实验数据证实,GLU能神经投射纤维对STN神经元有明显的兴奋作用,神经生物肽UCN可以拮抗GLU的过度兴奋效应,且同时微电泳AST对GLU兴奋效应具有一定协同作用,提示UCN及GLU能在STN中存在汇聚作用,UCN与STN神经元中CRF-2R结合后,拮抗STN中的GLU能神经元的过度兴奋毒性。本实验室既往研究发现,在PD病理情况下,DA能神经元在Bgl中的黑质(substantia nigra, SN)——STR通路中受损,这就使DA的抑制作用减弱,从而使具有兴奋效应的神经递质,如乙酰胆碱能(acetyl choline,ACH)及GLU能等相对占优势,导致PD的肌张力增强的临床表现[9-10]。本实验的结果表明,UCN可以降低GLU能的神经兴奋性,降低PD等病理状态下GLU过度表达所产生的兴奋毒性,提示UCN可在PD等疾病中发挥神经保护效应及治疗作用。
UCN2与CRF-2R结合后是如何对STN神经元产生抑制效应的呢?UCN2可能在PD中发挥保护作用机制如何呢?在本实验研究的最后一部分对机制进行了初步研究。实验中发现,UCN能抑制PKA所引起的STN神经元的抑制效应,但UCN的抑制作用在给予PKA阻断剂后,该效应被取消,并且给予CRF-2R阻断剂后,也不再发挥作用,该实验结果提示,UCN很可能与CRF-2R结合后,进而通过激活PKA而引起随后的生物学效应,阻断了神经递质的兴奋毒性作用有关。
UCN是CRF肽类家族的一个新型的神经内分泌生物肽,具有抗焦虑、抗糖尿病心肌病变、降血压、扩血管等多种生理及药理作用[11-12]。另外,本实验室既往已经证实,在脑损伤过程中UCN具有神经保护作用,UCN可抑制STR神经元的过度放电,特别是在大鼠吗啡成瘾中减轻大鼠的成瘾性,能明显改善阿片类药物的成瘾及戒断综合症[7, 13-14],发挥抑制STR神经元过度放电的神经保护作用。但是,UCN是如何发挥其CNS的保护作用的呢?目前,其具体机制尚不明确[14]。在本实验中,证实UCN与CRF-2R结合后,发挥抑制STN自发性放电的效应,可能是UCN发挥神经元的保护作用的初始机制,并进一步证实UCN与CRF-2R结合后触发了PKA信号通路,这其中可能还涉及其他分子生物学机制,目前仍不明确,应在今后的研究中进一步阐述和证实。本实验结果表明,UCN通过与CRF-2R结合,进而通过激活PKA,抑制STN神经元放电活动,协同DA的抑制效应,降低STN神经元中GLU的过度兴奋性,UCN可能在生理及PD病理情况下发挥CNS保护作用。
| [1] | De la Casa-Fages B, Alonso-Frech F, Grandas F. Effect of subthalamic nucleus deep brain stimulation on balance in Parkinson's disease: A static posturographic analysis[J]. Gait Posture, 2016, 52(1): 374-80. |
| [2] | Smith Y, Villalba R. Striatal and extrastriatal dopamine in the basal ganglia: an overview of its anatomical organization in normal and Parkinsonian brains[J]. Mov Disord, 2008, 23(3): S534-47. |
| [3] | Cossu G, Pau M. Subthalamic nucleus stimulation and gait in Parkinson's disease: a not always fruitful relationship[J]. Gait Posture, 2016, 52(2): 205-10. |
| [4] | Sankar T, Li S X, Obuchi T, et al. Structural brain changes following subthalamic nucleus deep brain stimulation in Parkinson's disease[J]. Mov Disord, 2016, 31(9): 1423-5. doi:10.1002/mds.26707 |
| [5] | Wang G, Pan J, Chen S D. Kinases and kinase signaling pathways: potential therapeutic targets in Parkinson's disease[J]. Prog Neurobiol, 2012, 98(2): 207-21. doi:10.1016/j.pneurobio.2012.06.003 |
| [6] | 孙莹, 张迪, 郑久明, 等. 微电泳urocortinⅡ对大鼠纹状体神经元自发放电及DA、ACH能神经传递影响[J]. 中国药理学通报, 2013, 29(9): 1325-6. Sun Y, Zhang D, Zheng J M, et al. The effects of neuroactive peptide urocortinⅡ on striatum neuron's spontaneous discharge and DA and ACH-ergic neurotransmission[J]. Chin Pharmacol Bull, 2013, 29(9): 1325-6. |
| [7] | 张迪, 刘春娜, 刘新宇, 郑久明. 神经肽Urocortin对大鼠纹状体神经元自发放电及GLU能神经传递的影响[J]. 中国药理学通报, 2012, 28(10): 1443-6. Zhang D, Liu C N, Liu X Y, Zheng J M. Effects of neuroactive peptide urocortinⅡ on spontaneous discharge and GLU-ergic of striatum neurons[J]. Chin Pharmacol Bull, 2012, 28(10): 1443-6. |
| [8] | Takeuchi K, Kumano A, Abe N, Kotani T. Involvement of corticotropin-releasing factor and corticotropin-releasing factor 2 receptors in pathogenesis of ischemia/reperfusion-induced enteritis in rats[J]. J Physiol Pharmacol, 2016, 67(5): 697-707. |
| [9] | Andrade J S, Viana M B, Abrão R O, et al. CRF family peptides are differently altered by acute restraint stress and chronic unpredictable stress[J]. Behav Brain Res, 2014, 271(5): 302-8. |
| [10] | Stengel A, Tache Y. CRF and urocortin peptides as modulators of energy balance and feeding behavior during stress[J]. Front Neurosci, 2014, 8(4): 52-3. |
| [11] | Accolla E A, Herrojo Ruiz M. Brain networks modulated by subthalamic nucleus deep brain stimulation[J]. Brain, 2016, 139(9): 2503-15. doi:10.1093/brain/aww182 |
| [12] | Liu C, Liu X, Song F, et al. The effects of neuropeptide urocortin 2 on the spontaneous discharge and glutamatergic neurotransmission of striatum neurons[J]. Neuropeptides, 2015, 50(5): 17-21. |
| [13] | Zheng Y, Zhang Y M, Ni X. Urocortin 2 but not urocortin 3 promotes the synaptic formation in hipppocampal neurons via induction of NGF production by astrocytes[J]. Endocrinology, 2016, 157(3): 1200-10. doi:10.1210/en.2015-1812 |
| [14] | Lawrence K M, Jackson T R, Jamieson D, et al. Urocortin-from Parkinson's disease to the skeleton[J]. Int J Biochem Cell Biol, 2015, 60(8): 130-8. |

