


2. 浙江大学理学院化学系,浙江 杭州 310028;
3. 中国科学院物理化学研究所,北京 100190
2. Dept of Chemistry, Faculty of Science, Zhejiang University, Hangzhou 310028, China;
3. Technical Institute of Physics and Chemistry, Chinese Academy of Sciences, Beijing 100190, China
鬼臼毒素(podophyllotoxin, PPT)是从鬼臼属、八角莲属、山荷叶属和刺柏植物中提取的木质素类化合物。研究表明,鬼臼毒素具有明显的抗肿瘤[1-2]和抗病毒活性[3]。鬼臼毒素的软膏剂及酊剂(尤脱欣)已在临床上用于治疗人乳头状瘤病毒引起的尖锐湿疣[4]。已有报道称鬼臼树脂类在治疗女性妊娠期尖锐湿疣时具有致畸作用[5],但鬼臼毒素作为尖锐湿疣外用药,频繁甚至过量用药后对男性用药部位正常细胞的可能影响方面报道较少。课题组前期研究大鼠体内预实验发现,含鬼臼毒素的球果提取物可降低雄性大鼠的生育力,并发现其对附睾有一定的损伤。本文对鬼臼毒素体外对大鼠附睾上皮细胞的增殖抑制活性及其可能的作用机制进行了研究。
1 材料与方法 1.1 材料 1.1.1 实验动物Sprague Dawley(SD)大鼠,♂, 体质量200~220 g,由上海西普尔-必凯实验动物有限公司提供,合格证号:SCXK(沪)2013-0016。
1.1.2 药物与试剂鬼臼毒素(C22H22O8):高效液相色谱(high performance liquid chromatography, HPLC)≥98%,美国Enzo Life Sciences公司;DMEM/F12培养液(批号:1580817)、胎牛血清(批号:1502284)、汉克平衡盐缓冲液(Hank′s balanced salt solution, HBSS)(批号:1491037)、胰蛋白酶,美国Gibco公司;细胞计数试剂盒(cell counting kit-8, CCK-8)(批号:GB719),日本株式会社同仁化学研究所;Ⅰ型胶原酶(批号:1001424536)、二甲基亚砜(dimethylsulfoxide, DMSO),美国Sigma公司;Annexin V-FITC/PI凋亡检测试剂盒(批号:3337788)、PI/RNase染液(批号:2216713),美国BD公司;原位末端标记法(terminal-deoxynucleoitidyl transferase mediated nick end labeling,TUNEL)细胞凋亡检测试剂盒-Fluorescein(批号:10131400), 德国Roche公司;肿瘤坏死因子-α(tumor necrosis factor alpha, TNF-α)ELISA试剂盒(批号:320850),R&D Systems;蛋白酶抑制剂(批号:ME156877),美国Thermo公司;蛋白裂解液、BCA蛋白浓度测定试剂盒,上海碧云天生物科技有限公司;β-actin、细胞色素C、caspase-3、caspase-8、caspase-9抗体,英国Abcam公司。
1.1.3 仪器CO2培养箱(美国Thermo公司);细胞离心机(无锡瑞江离心机厂);AE31型倒置相差显微镜(厦门麦克奥迪实业集团有限公司);恒温水浴锅(上海医用恒温设备厂);ESCO超净工作台(新加坡艺思高生物科技有限公司);Synergy 2酶联免疫检测仪(美国伯腾仪器有限公司);透射电子显微镜(日本飞利浦公司);FACSCalibur型流式细胞仪(美国贝克曼公司);CFX-96型荧光定量PCR仪、电泳仪、电转仪、Western blot凝胶成像仪(美国伯乐公司)。
1.2 方法 1.2.1 原代细胞培养按照文献方法稍作修改,进行大鼠附睾上皮细胞的分离和培养[6]。将大鼠乙醚麻醉处死,解剖,取出双侧附睾置于含有HBSS的培养皿中,小心剥除脂肪等其他组织。分离好的附睾组织剪碎,用不含Ca2+、Mg2+的HBSS冲洗并过滤3遍,除去精子。附睾组织碎块移入0.25%胰酶(含EDTA)溶液中,32℃水浴振荡(80 r·min-1)消化20 min。组织样悬液离心(800 r·min-1, 5 min),弃上清,沉淀用Ⅰ型胶原酶(1 g·L-1)混悬,32℃水浴振荡(80 r·min-1)消化30~40 min,细胞团处于完全解离状态,静置5 min,70 μm孔径筛网过滤后,滤液离心(800 r·min-1,6 min)。弃上清,沉淀物大部分为附睾上皮细胞,分别用HBSS及培养液重悬。将细胞培养于含10%胎牛血清的DMEM/F12培养液中,培养24 h后,换液以去除未贴壁细胞,此后按1 :2反复传代纯化附睾上皮细胞。原代培养和传代过程中均于倒置显微镜下观察细胞的形态,实验使用第3~5代细胞。
1.2.2 CCK-8检测细胞增殖取对数生长期细胞,用胰酶消化,按每孔5×103个细胞接种于96孔培养板中,每孔接种100 μL,在细胞培养箱中培养24 h后,在培养液中依次加入不同浓度的鬼臼毒素,使培养液的总体积是100 μL。分别培养24、48、72 h后,加入10 μL的CCK-8,于37℃、5% CO2培养箱中培养2~3 h,在450 nm处测其OD值。按下式计算增殖抑制率:
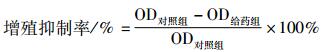
|
取对数生长期细胞加入鬼臼毒素,使其终浓度分别为0.024、0.24、2.4 μmol·L-1,对照组加等体积DMSO,置于37℃、5% CO2培养箱中培养48 h,消化、离心、收集细胞,用戊二醛与锇酸固定液固定细胞,乙醇脱水,LR White树脂渗透包埋,超薄切片,醋酸铀和柠檬酸铅双染色,透射电子显微镜观察细胞内部结构变化。
1.2.4 Annexin V-FITC/PI双染法检测细胞凋亡取106个对数生长期细胞接种于6孔板,不同浓度鬼臼毒素作用48 h后收集细胞,PBS洗细胞2次,按照试剂盒方法将细胞重悬于100 μL含Annexin V-FITC和PI的缓冲液中,室温避光孵育15 min,流式细胞仪检测细胞凋亡比率。
1.2.5 TUNEL细胞凋亡检测将细胞接种于6孔板中(含多聚赖氨酸处理过的盖玻片),置37℃、5% CO2的培养箱中培养过夜,更换新培养液并加入不同浓度的鬼臼毒素,药物作用48 h后取出细胞爬片。PBS清洗2遍,4%多聚甲醛固定30 min后,PBS清洗2遍,0.25% Triton X-100处理10 min后,PBS浸洗2遍,待玻片干后,加50 μL TUNEL反应混合液(5 μL TdT+45 μL荧光素标记的dUTP混匀)于标本上,加盖玻片在暗湿盒中反应1 h(37℃),PBS漂洗3次,加1滴PBS,在荧光显微镜下观察凋亡细胞(激发光波长为450~500 nm,检测波长为515~565 nm)。
1.2.6 RT-PCR法检测鬼臼毒素对TNF-α mRNA表达的影响不同浓度鬼臼毒素(2.4、0.24、0.024、0 μmol·L-1)处理细胞48 h后,TRIzol Reagent提取细胞总RNA,用逆转录试剂盒将RNA逆转录为cDNA。TNF-α引物设计序列为forward: 5′-CACCACGCTCTTCTGTCTACTG-3′, reverse:5′-TCCGCTTGGTGGTTTGC-3′,同时以GAPDH为内参照,GAPDH引物序列为forward:5′-AGTGCCAGCCTCGTCTCATAG-3′, reverse:5′-CGTTGAACTTGCCGTGGGTAG-3′。以合成的cDNA第1链为模板进行实时荧光定量PCR(按SYBR Green试剂盒说明进行)。PCR体系为20 μL,其中SYBR Premix Ex Taq Ⅱ(2×) 10.0 μL、cDNA 1 μL、上、下游引物各0.4 μL、去离子水8.2 μL。反应条件:预变性95℃ 15 min,变性95℃ 15 s,退火60℃ 25 s,40个循环。每个样品设3个复孔,Ct取其均值,以GAPDH做为内参。△Ct=CtTNF-α-CtGAPDH,△△Ct=△Ct处理组-△Ct对照组。不同样本的目的基因表达的相对差异量=2-△△Ct。
1.2.7 ELISA法检测鬼臼毒素对TNF-α分泌水平的影响取对数生长期细胞接种于6孔板中,细胞贴壁后加入终浓度分别为0(对照组)、0.0024、0.024、0.24、2.4 μmol·L-1的鬼臼毒素,每个药物组各设3个平行复孔。作用48 h后取上清液,按照ELISA试剂盒操作说明加上清液样品,酶标仪波长490 nm处读OD值,通过标准曲线,计算条件培养液中TNF-α含量。
1.2.8 Western blot技术检测鬼臼毒素对caspase-8、细胞色素C、caspase-9、procaspase-3和活性caspase-3蛋白表达的影响将5组(0、0.0024、0.024、0.24、2.4 μmol·L-1)鬼臼毒素分别作用细胞48 h后,冰上提取细胞蛋白,BCA蛋白定量试剂盒测定蛋白浓度。40 μg蛋白上样量进行SDS-PAGE电泳,转膜;5%脱脂奶粉室温封闭1 h,加一抗,4℃孵育过夜;PBS洗膜(15 min×3次)后,二抗(1:4 000) 室温孵育2 h;PBS充分洗涤,加ECL显影液,将膜置于凝胶成像仪中曝光,各目的条带与β-actin条带灰度值比值作为该目的蛋白的相对表达量,实验重复3次。
1.2.9 统计学分析实验数据采用SPSS 20.0统计软件进行统计分析,以x±s表示,各组数据采用One-way ANOVA统计学分析,两组间数据比较采用t检验。
2 结果 2.1 鬼臼毒素对附睾上皮细胞增殖的抑制作用CCK-8法检测结果显示,不同剂量组鬼臼毒素(0、0.00024、0.0024、0.024、0.24、2.4、24 μmol·L-1)分别作用于大鼠附睾上皮细胞24、48、72 h后,均能抑制细胞的增殖,且呈现明显的剂量依赖性,各组抑制率见Fig 1。由Fig 1可看出,鬼臼毒素作用24 h抑制增殖作用不及48、72 h;48 h的半数抑制率IC50为(0.37±0.01)μmol·L-1、72 h的半数抑制率IC50为(0.077±0.0009)μmol·L-1。

|
| Fig 1 Podophyllotoxin inhibits growth of cultured rat epididymal epithelial cells(x±s, n=3) *P < 0.05 vs control |
如Fig 2所示,正常细胞的细胞核较大,细胞器丰富,尤其是线粒体和粗面内质网较多,线粒体圆形或椭圆形;基质丰富,核内染色体分布均匀(Fig 2A)。当鬼臼毒素剂量为0.024 μmol·L-1时,细胞核固缩,大量线粒体肿胀并空泡化,细胞质变性(Fig 2B)。当鬼臼毒素剂量为0.24 μmol·L-1时,细胞核染色质固缩,细胞质空泡化严重(Fig 2C)。当鬼臼毒素剂量为2.4 μmol·L-1时,微绒毛脱落,胞质变性,出现细胞核碎片,细胞内部结构呈现典型的中晚期凋亡形态改变(Fig 2D)。

|
| Fig 2 The ultra structural change of epedidymal epithelial cells A:Control group; B:Treated with 0.024 μmol·L-1 podophyllotoxin; C:Treated with 0.24 μmol·L-1 podophyllotoxin; D:Treated with 2.4 μmol·L-1 podophyllotoxin. ☆, microtubule; ★, chromatin condensation and fragmentation; △, mitochondria; ▲, mitochondrial vacuolation; ■, nucleus fragments |
Annexin V-FITC/PI双标法流式细胞仪检测结果中呈现了不同标志的细胞群:正常细胞即双阴性细胞(Annexin V-/PI-)、早期凋亡细胞(Annexin V+/PI-)、晚期凋亡细胞(Annexin V+/PI+)和坏死细胞(Annexin V-/PI+)。不同浓度的鬼臼毒素作用附睾上皮细胞48 h后,各给药组与对照组(0 μmol·L-1鬼臼毒素)相比,细胞凋亡率均明显增加,且呈剂量依赖性,说明鬼臼毒素能明显诱导附睾上皮细胞凋亡(Tab 1、Fig 3)。
| C/μmol·L-1 | Apoptosis rate/% |
| 0 | 6.37±0.91 |
| 0.024 | 11.23±2.01* |
| 0.24 | 20.37±2.32* |
| 2.4 | 46.77±2.32* |
| *P<0.05 vs control | |

|
| Fig 3 Apoptotic rate of epididymal epithelial cells treated with podophyllotoxin for 48 h detected by Annexin V-FITC/PI double-staining The apoptotic rate of podophyllotoxin-treated cells increased in a dose-dependent manner after 48 h treatment |
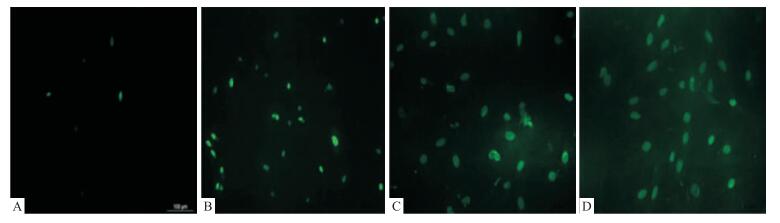
如Fig 4所示,用原位末端标记法观察细胞时,发现在对照组中活细胞核不显示绿色荧光,而在加药组中发现了凋亡细胞,它的核染色质着绿色荧光,呈固缩状,并且在鬼臼毒素2.4 μmol·L-1时出现明显的凋亡小体。
|
| Fig 4 Podophyllotoxin-induced apoptosis of epididymal epithelial cells assessed by TUNEL method A:0 μmol·L-1 PPT; B:0.024 μmol·L-1 PPT; C:0.24 μmol·L-1 PPT; D:2.4 μmol·L-1 PPT |
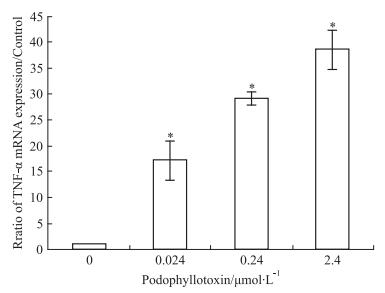
mRNA的表达RT-PCR数据分析显示,鬼臼毒素各剂量组均能升高TNF-α mRNA的表达,且呈剂量依赖性(Fig 5);当鬼臼毒素浓度为2.4 μmol·L-1时,TNF-α mRNA的表达量是对照组的38.7倍,反映了鬼臼毒素能明显提高细胞中TNF-α mRNA的表达。
|
| Fig 5 Effect of podophyllotoxin on expression of TNF-α mRNA in epididymal epithelial cells by real time RT-PCR(x±s, n=3) *P < 0.05 vs control |
ELISA结果显示(Tab 2),与对照组相比,鬼臼毒素能够明显增加细胞上清中TNF-α的水平(P<0.05), 其效应具有明显的剂量依赖性。
| C/μmol·L-1 | TNF-α(ng·L-1) |
| 0 | 2.53±0.61 |
| 0.0024 | 7.90±1.06* |
| 0.024 | 14.20±1.40* |
| 0.24 | 24.45±3.24* |
| 2.4 | 63.28±5.46* |
| *P<0.05 vs control | |
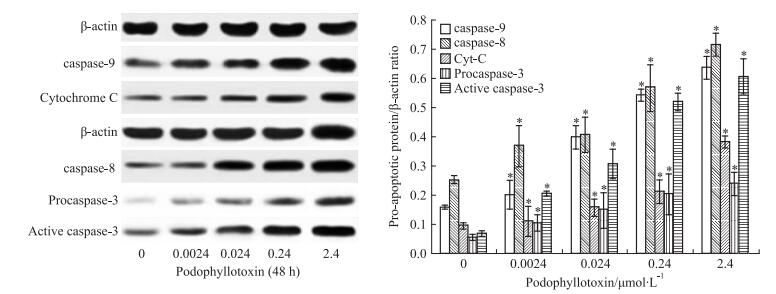
Western blot结果显示(Fig 6),不同浓度鬼臼毒素作用于附睾上皮细胞48 h后,与对照组相比,caspase-8、细胞色素C、caspase-9、procaspase-3和活性caspase-3蛋白条带灰度逐渐加深。图像分析结果显示,随着药物浓度的增加,caspase-8、细胞色素C、caspase-9、procaspase-3和活性caspase-3蛋白表达均有不同程度的增加, 同时活性caspase-3表达量高于procaspase-3 2倍,提示鬼臼毒素能上调附睾上皮细胞细胞色素C和caspase家族蛋白的表达。
|
| Fig 6 Podophyllotoxin-induced activation of caspases and cytochrome C in epididymal epithelial cells(x±s, n=3) *P < 0.05 vs control |
鬼臼毒素作为良好的抗病毒及抗肿瘤药物近年来备受关注,预实验发现,对雄性大鼠口服含鬼臼毒素的提取物7周后,大鼠生育力明显下降,组织学观察发现附睾上皮出现损伤,附睾内精子数量明显下降。为了进一步研究鬼臼毒素对附睾上皮的影响机制,本实验通过对体外原代培养附睾上皮细胞给药,发现鬼臼毒素明显抑制附睾上皮细胞的生长。通过细胞形态观察、透射电镜观察、流式细胞仪检测细胞凋亡率等,我们观察到鬼臼毒素具有明显诱导附睾上皮细胞发生凋亡的作用。
细胞凋亡是一个受到多基因调控的细胞自发的死亡,是一种程序性的生物学过程,又称为细胞程序性死亡。细胞凋亡主要的2种途径是线粒体途径和死亡受体途径[7]。线粒体途径的主要起始因子是细胞色素C和caspase-9, 细胞色素C自线粒体的释放标志着线粒体凋亡通路的激活,而caspase-9被募集到细胞色素C/dATP/Apaf-1组成的凋亡体,参与线粒体通路的细胞凋亡[8]。死亡受体途径的关键起始因子是caspase-8,活化的caspase-8被募集到Fas和肿瘤坏死因子受体(tumor necrosis factor receptor, TNFR)死亡受体复合物,参与死亡受体通路[9]。最终活化caspase-8、caspase-9等,激活caspase家族的关键效应因子caspase-3,活化的caspase-3通过对其底物蛋白的切割而使许多与细胞结构、细胞周期及DNA修复相关蛋白或激酶失活,从而使细胞发生不可逆转的凋亡[10]。
TNF-α具有诱导细胞凋亡的作用,其通过与细胞膜表面的特异性受体TNFR结合,活化初始caspase-8[11-12],活化的caspase-8一方面剪切Bid,剪切后的Bid促使Bax同源二聚体与线粒体膜结合,介导线粒体释放细胞色素C、凋亡诱导因子等,在细胞色素C、凋亡蛋白酶活化因子Apaf-1和caspase-9的参与下,形成有活性的二聚体,进一步激活caspase-3;另一方面,活化的caspase-8还可以直接激活下游的caspase-3[7]。活化的caspase-3能裂解DNA修复相关分子、凋亡抑制蛋白、细胞外基质蛋白及骨架蛋白等,促使细胞凋亡,从而连接起内源性和外源性凋亡途径。
在本研究中,RT-PCR及ELISA结果显示,鬼臼毒素可使TNF-α的mRNA水平及翻译水平升高,同时Western blot实验结果显示,鬼臼毒素作用附睾上皮细胞48 h后,可使caspase-8、细胞色素C、caspase-9、procaspase-3、活性caspase-3等蛋白的表达呈剂量依赖性升高,且活性caspase-3表达量高于procaspase-3,用药组活性caspase-3和procaspase-3二者总表达量远高于空白对照组,表明鬼臼毒素对外源性和内源性细胞凋亡均有明显的诱导作用。
综上所述,鬼臼毒素对大鼠附睾上皮细胞的增殖具有一定的抑制作用,其机制可能与鬼臼毒素促进附睾上皮细胞凋亡有关,该凋亡作用可能通过上调TNF-α及caspase家族蛋白的表达,进而诱导附睾上皮细胞发生内源性和外源性凋亡。
( 致谢: 本实验全部由上海市计划生育科学研究所药物发展室生殖药理组实验室朱焰老师课题组独立完成,曹霖教授给予了本实验指导性的意见;实验室桂幼伦、郭湘洁、李钊等老师均在实验过程中给予了重要帮助,谨此致以诚挚的谢意!)
| [1] | Doussot J, Mathieu V, Colas C, et al. Investigation of the lignan content in extracts from Linum, Callitris and Juniperus Species in relation to their in vitro antiproliferative activities[J]. Planta Med, 2017, 83(6): 574-81. |
| [2] | 高晨光, 张猜, 赵安妮, 等. 鬼臼毒素衍生物LN-13诱导多药耐药细胞K562/A02凋亡及其机制[J]. 中国药理学通报, 2017, 33(1): 100-4. Gao C G, Zhang C, Zhao A N, et al. Podophyllotoxin derivative LN-13 induced multidrug resistant cell K562/A02 apoptosis and its molecular mechanism[J]. Chin Pharmacol Bull, 2017, 33(1): 100-4. |
| [3] | 王琦, 韩凯, 陈平姣, 等. 鬼臼毒素及其衍生物在多种病毒性疾病中的应用[J]. 皮肤性病诊疗学杂志, 2014, 21(4): 348-50. Wang Q, Han K, Chen P J, et al. The application of podophyllotoxin and its derivatives in various viral diseases[J]. J Diagn Ther Dermato-Venereol, 2014, 21(4): 348-50. |
| [4] | 马海忠, 廖明琪, 邵婷玑, 等. 鬼臼毒素制剂在尖锐湿疣疾病中的应用[J]. 中国药房, 2013, 24(19): 1819-21. Ma H Z, Liao M Q, Shao T J, et al. The application of podophyllotoxin agent in genital wart[J]. China Pharm, 2013, 24(19): 1819-21. doi:10.6039/j.issn.1001-0408.2013.19.32 |
| [5] | 磨良群. 尖锐湿疣的研究进展[J]. 数理医药学杂志, 2005, 18(3): 268-72. Mo L Q. The research progress of condyloma acuminatum[J]. J Mathematical Med, 2005, 18(3): 268-72. |
| [6] | Kierszenbaum A L, Lea O, Petrusz P, et al. Isolation, culture, and immunocytochemical characterization of epididymal epithelial cells from pubertal and adult rats[J]. Proc Natl Acad Sci USA, 1981, 78(3): 1675-9. doi:10.1073/pnas.78.3.1675 |
| [7] | 贺艳杰, 李玉华, 卢会芳, 等. 线粒体通路和死亡受体通路在中华眼镜蛇毒组分诱导KG1a细胞凋亡中的作用[J]. 中国药理学通报, 2013, 29(3): 356-60. He Y J, Li Y H, Lu H F, et al. The action of mitochondrial apoptosis pathway and death receptor pathway in the process of Naja Naja Actra Venom component inducing the KG1a apoptosis[J]. Chin Pharmacol Bull, 2013, 29(3): 356-60. |
| [8] | Budihardjo I, Oliver H, Lutter M, et al. Biochemical pathways of caspase activation during apoptosis[J]. Annu Rev Cell Dev Biol, 1999, 15: 269-90. doi:10.1146/annurev.cellbio.15.1.269 |
| [9] | Audo R, Combe B, Hahne M, et al. The two directions of TNF-related apoptosis-inducing ligand in rheumatoid arthritis[J]. Cytokine, 2013, 63(2): 81-90. doi:10.1016/j.cyto.2013.04.011 |
| [10] | Budd S L, Tenneti L, Lishnak T, et al. Mitochondrial and extramitochondrial apoptotic signaling pathways in cerebrocortical neurons[J]. Proc Natl Acad Sci USA, 2000, 97(11): 6161-6. doi:10.1073/pnas.100121097 |
| [11] | 黄健, 吴立军, 田代真一, 等. oridonin部分通过TNFα信号转导途径诱导小鼠成纤维L929细胞凋亡[J]. 中国药理学通报, 2006, 22(4): 471-5. Huang J, Wu L J, TASHIRO Shin-ichi, et al. Oridon in induced L929 cell death partially through TNF α signal pathway[J]. Chin Pharmacol Bull, 2006, 22(4): 471-5. |
| [12] | Micheau O, Tschopp J. Induction of TNF receptor Ⅰ-mediated apoptosis via two sequential signaling complexes[J]. Cell, 2003, 114(2): 181-90. doi:10.1016/S0092-8674(03)00521-X |

