


红景天为景天科植物大花红景天[Rhodiola crenulata(Hook.f. et Thoms.) H.Ohba]的干燥根和根茎。具有益气活血、通脉平喘的功效,用于气虚血瘀、胸痹心痛、中风偏瘫、倦怠气喘[1]。红景天苷(salidroside,Sal)是红景天的主要有效成分,课题组前期研究[2-4]发现,红景天苷能降低局灶性脑缺血/再灌注大鼠(middle cerebral artery occlusion,MCAO)的脑梗死体积和神经功能损伤。本研究旨在观察红景天苷对MCAO模型大鼠神经功能恢复、缺血侧脑组织神经微丝蛋白200(neurofilament protein 200,NF200) 及Akt/糖原合成酶激酶-3β(glycogen synthase kinase-3β,GSK-3β)/脑衰蛋白反应调节蛋白2(collapsin response mediator protein-2,CRMP-2) 蛋白表达的影响,进一步探索红景天苷对MCAO模型大鼠神经保护的可能机制,为红景天苷开发治疗急性脑缺血疾病提供实验依据。
1 材料 1.1 实验动物健康成年♂ SD大鼠,SPF级,体质量(240~280) g,购于上海斯莱克实验动物有限公司,合格证号:2007000509960,许可证号:SCXK(沪)2007-0005,由福建中医药大学实验动物中心饲养。
1.2 药物与试剂红景天苷(批号:20151111,福建中医药大学药学院生物医药研发中心,纯度>98%);BCA蛋白定量检测试剂盒(碧云天生物技术有限公司,货号P0010);5×蛋白上样缓冲液(碧云天生物技术有限公司,货号P0015);预染蛋白Marker(美国赛默飞世尔科技有限公司,货号26616);兔抗p-Akt(Ser 473)、兔抗Akt、兔抗p-GSK-3β(Ser 9)、兔抗GSK-3β、兔抗p-CRMP-2(Thr 514)、兔抗CRMP-2、兔抗GAPDH(美国CST公司,货号分别为:4060、4685、9336、9315、9397、9393、2118);兔抗NF200(美国Sigma公司,货号N4142);山羊抗兔二抗(美国赛默飞世尔科技有限公司,货号31460);FITC标记山羊抗兔(北京中杉金桥生物技术有限公司,货号ZF-0311)。
1.3 仪器ChemiDoc XRS+凝胶成像分析系统(美国Bio-rad公司);PowerPac Basic基础电泳仪电源、Mini PROTEAN Tetra小型垂直电泳槽、Mini Trans-Blot小型转印槽(美国Bio-rad公司);Infinite M200 Pro多功能酶标仪(瑞士TECAN公司);HM325石蜡切片机(美国Thermo Fisher公司);LSM710激光共聚焦显微镜(德国Zeiss公司);Primo R高速台式冷冻离心机(美国赛默飞世尔科技有限公司);SK-1快速混匀器(常州国华电器有限公司)。
2 方法 2.1 造模、分组及给药实验前大鼠禁食不禁水12 h,10%水合氯醛(3 mL·kg-1)腹腔麻醉,参照本课题组前期的实验方法[2-4]进行造模,沿颈部正中切开皮肤,暴露右颈总动脉、颈外动脉和颈内动脉,结扎颈总动脉、颈外动脉。用动脉夹夹闭颈内动脉,眼科剪将颈总动脉剪个小口,插入线栓至颈内动脉,插入深度距动脉分叉约2 mm,结扎颈内动脉。栓塞2 h后,将线栓拔出。假手术组(Sham)进行相同的操作,除了不栓塞中脑动脉。采用Longa评分,神经功能缺损评分在1~3分的为模型成功,可纳入实验。将成模的大鼠随机分为模型对照组(MCAO)和红景天苷给药组(MCAO+Sal),每组12只。MCAO+Sal组腹腔注射红景天苷(50 mg·kg-1),连续6 d,末次给药2 h后,取脑用于实验。Sham组及MCAO组同法给予等量生理盐水。
2.2 神经功能评分按照Zea-Longa神经行为缺损评分标准对大鼠进行评价。0分:无神经功能缺损;1分:提尾时右前肢内收,不能完全伸展;2分:自发行走时向右侧转圈;3分:行走时身体向右侧倾倒;4分:不能自发行走,有意识丧失。评分过程至少由2人参与完成。
2.3 Western blot法检测大鼠缺血侧脑组织p-Akt、Akt、p-GSK-3β、GSK-3β、p-CRMP-2、CRMP-2的蛋白表达将各组大鼠缺血侧脑组织取下,液氮速冻,-80 ℃保存。提取总蛋白,经SDS-PAGE凝胶分离后,转移至PVDF膜,5%脱脂奶粉封闭2 h,p-Akt(Ser 473)、Akt、p-GSK-3β(Ser 9)、GSK-3β、p-CRMP-2(Thr 514)、CRMP-2一抗(均为1 :1 000)4℃过夜,山羊抗兔二抗(1 :5 000) 室温孵育1.5 h,加ECL试剂经凝胶成像分析系统检测,分析目标条带的灰度值,计算各给药组与空白对照组灰度值的比值,并统计各组之间的差异。
2.4 免疫荧光染色法检测缺血侧脑组织NF200蛋白表达10%水合氯醛(3.5 mL·kg-1)深度麻醉大鼠,开胸暴露心脏,经左心室插管至升主动脉并固定,右心耳剪一小洞放血,先快速灌注生理盐水250 mL冲去全身血液,后4%多聚甲醛溶液(pH 7.4) 灌流固定,直至大鼠全身僵硬、强直,立即断头取脑,置于4℃ 4%多聚甲醛溶液继续固定24 h[5],再进行后续的常规石蜡包埋切片,厚度5 μm,贴于防脱载玻片上,柠檬酸缓冲液(pH 6.0) 微波修复15 min,5% BSA(含10%山羊血清)封闭2 h,兔抗NF200(1 :80) 4℃孵育过夜,阴性对照用PBS代替一抗,FITC标记山羊抗兔IgG(1 :100) 室温1.5 h,DAPI复染核5 min,抗荧光淬灭封片液封片,激光共聚焦显微镜观察拍照。
2.5 统计学分析用SPSS 20.0对数据进行分析,结果以x±s表示,神经功能评分分析用非参数检验(Mann-Whitney test),其余各组间数据比较用单因素方差(ANOVA)分析。
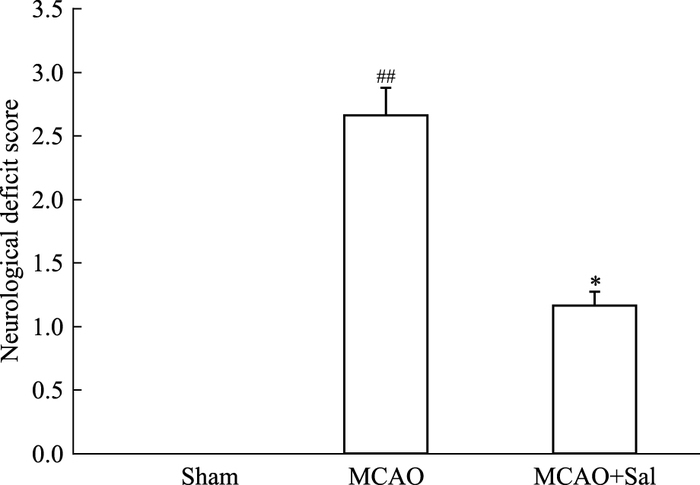
3 结果 3.1 红景天苷对MCAO大鼠神经功能评分的影响如Fig 1所示,与sham组比较,MCAO组大鼠神经功能评分较高,差异有统计学意义(P<0.01);与MCAO组比较,红景天苷给药6 d后,神经功能评分明显降低(P<0.05)。
|
| Fig 1 Effects of salidroside on neurological score in MCAO rats(x±s, n =6) ##P < 0.01 vs sham; *P < 0.05 vs MCAO |
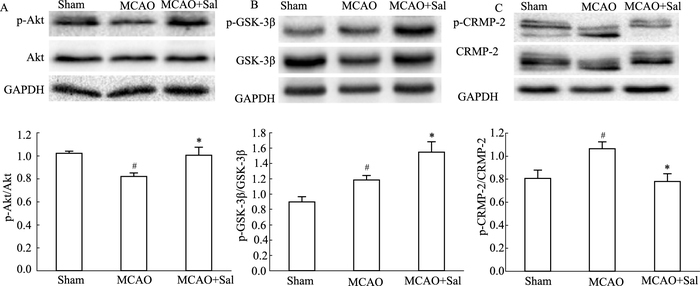
如Fig 2所示,与sham组比较,MCAO组p-Akt蛋白表达水平明显降低,p-GSK-3β、p-CRMP-2蛋白表达水平明显升高,差异具有统计学意义(P<0.05);与MCAO组比较,MCAO+Sal组p-Akt、p-GSK-3β蛋白表达水平明显升高,p-CRMP-2蛋白表达水平明显降低,差异具有统计学意义(P<0.05)。
|
| Fig 2 Effects of salidroside on p-Akt/Akt(A), p-GSK-3β/GSK-3β(B) and p-CRMP-2/CRMP-2(C) protein in MCAO rats (x±s, n =3) #P < 0.05 vs sham; *P < 0.05 vs MCAO |
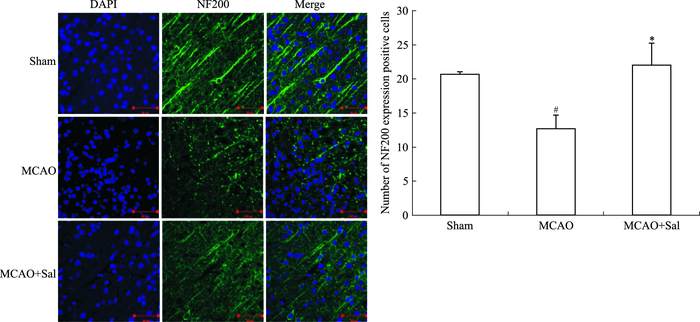
激光共聚焦显微镜下观察,NF200蛋白主要表达在胞膜和轴突膜上,各组大鼠缺血侧脑组织皮质均可见NF200阳性细胞,sham组皮质可见大量NF200阳性细胞,轴突较长,排列规则。与sham组相比,MCAO组缺血侧大脑皮质NF200阳性表达细胞数明显减少(P<0.05),且纤维结构紊乱,突起中断;与MCAO组相比,MCAO+Sal组缺血侧大脑皮质NF200阳性表达细胞数明显增加,差异有统计学意义(P<0.05),见Fig 3。
|
| Fig 3 Effect of salidroside on NF200 protein in MCAO rats by immunofluorescence staining(n=3, ×400, scale bar=50 μm) #P < 0.05 vs sham; *P < 0.05 vs MCAO |
缺血性脑卒中是指由血栓或栓塞所造成的缺血,发病率约占脑血管病的80%。尽管多年来人们不断努力寻求缺血性脑卒中的防治方法,但其发病率高、病死率高、致残率高、复发率高的特点仍未能根本改变。引起急性缺血性脑卒中最常见的原因是颈内或颅内血管的突然阻塞,导致脑组织急性缺糖缺氧。基于脑缺血神经损伤机制与时程变化的研究,目前损伤早期抗兴奋性毒性、抗神经炎性和抗凋亡,损伤后期促组织修复、再生是脑卒中治疗的主要策略[6-7]。
研究表明[8],在神经元的轴突形成过程中存在着一个信号网络,通过PI3K/Akt/GSK-3β/CRMP-2信号传导途径调节神经元轴突的特性。其中,Akt蛋白是一种在脑缺氧/缺血后发挥保护作用的重要促生存激酶。Akt通过磷酸化Ser473残基而激活,Akt激活后可使下游蛋白磷酸化,如GSK-3β、Bcl-XL/Bcl-2相关死亡促进因子(Bcl-XL/Bcl-2 associated death promoter,Bad)、半胱天冬氨酸蛋白酶-9(caspase-9) 等而抑制相关作用[9]。GSK-3β是一种在生物体内广泛存在的丝氨酸/苏氨酸蛋白激酶,参与糖代谢、细胞形态的形成及细胞增殖等多种细胞生物功能的调控,是Akt的下游因子,在信号通路中起着关键的作用。GSK-3β的Ser9残基磷酸化后其活性被抑制,调节CRMP-2的活性,继而促进了神经元轴突的生长[10]。CRMP-2在发育中的神经系统高表达,并在轴突生长导向中发挥重要作用[11]。CRMP-2磷酸化状态影响神经元的极性,CRMP-2 Thr-514位点磷酸化水平升高,最终抑制了神经元轴突的发生、发展和成熟[12]。
缺血在损伤修复时会刺激未受累的神经元出芽和形成新的突触联系[13],此过程中同时将伴随一些相关蛋白的合成和表达如生长相关蛋白-43(growth associated protein-43,GAP43)、NF200等。其中NF200是神经元特有的结构蛋白,在生理情况下对轴突运输和维持细胞的形态中起着很大作用,NF200表达水平能很好地反映神经轴突损伤和修复情况。因此,本研究采用NF200的免疫荧光染色作为轴突再生的评价指标。
综上所述,红景天苷对局灶性脑缺血/再灌注大鼠具有神经保护作用,其机制可能与促进Akt、GSK-3β的磷酸化,抑制CRMP-2的磷酸化,促进轴突再生,改善大鼠梗死后神经功能的恢复有关。
( 致谢: 本课题由康复技术协同创新中心和国家中医药管理局中医康复研究中心资助,并在福建省科技厅福建省中药学重点实验室完成。非常感谢福建中医药大学实验动物中心对动物实验的大力支持! )
| [1] | 国家药典委员会. 中华人民共和国药典(一部)[S]. 北京: 中国医药科技出版社, 2015: 144. Chinese Pharmacopoeia Commission. The pharmacopoeia of the People′s Republic of China(a)[S]. Beijing: China medical science and technology press, 2015:144. |
| [2] | 赖文芳, 张小琴, 洪海棉, 等. 红景天苷对大鼠局灶性脑缺血/再灌注损伤的神经保护作用[J]. 中国药理学通报, 2015, 31(6): 775-80. Lai W F, Zhang X Q, Hong H M, et al. Neuroprotective effects of salidroside against focal cerebral ischemia/reperfusion injury in rats[J]. Chin Pharmacol Bull, 2015, 31(6): 775-80. |
| [3] | 谢秀利, 洪海棉, 赖文芳, 等. 红景天苷对大脑中动脉闭塞模型大鼠的神经保护作用[J]. 中国药理学通报, 2015, 31(10): 1452-7. Xie X L, Hong H M, Lai W F, et al. Protective effects of salidroside in MCAO rats[J]. Chin Pharmacol Bull, 2015, 31(10): 1452-7. doi:10.3969/j.issn.1001-1978.2015.10.025 |
| [4] | 许力伟, 应雄, 李茗菊, 等. 红景天苷对局灶性脑缺血/再灌注大鼠脑组织Ephb3、Ephb6 mRNA表达的影响[J]. 福建中医药, 2016, 47(5): 9-10. Xu L W, Ying X, Li M J, et al. The effect of salidroside on expression of Ephb3 and Ephb6 mRNA in MCAO rats[J]. Fujian J Tradit Chin Med, 2016, 47(5): 9-10. |
| [5] | 李新娟, 魏林郁, 李超堃, 等. 硫化氢对大鼠局灶性脑缺血/再灌注损伤的保护作用及其机制[J]. 中国药理学通报, 2014, 30(9): 1271-5. Li X J, Wei L Y, Li C K, et al. Protective effect of hydrogen sulfide on focal cerebral ischemia /reperfusion injury in rats and its mechanism[J]. Chin Pharmacol Bull, 2014, 30(9): 1271-5. |
| [6] | Mozaffarian D, Benjamin E J, Go A S, et al. Heart disease and stroke statistics—2015 update: a report from the American Heart Association[J]. Circulation, 2015, 131(4): e29-322. doi:10.1161/CIR.0000000000000152 |
| [7] | Corbyn Z. Statistics: a growing global burden[J]. Nature, 2014, 510(7506): S2-3. doi:10.1038/510S2a |
| [8] | Yoshimura T, Arimura N, Kaibuchi K. Signaling networks in neuronal polarization[J]. J Neurosci, 2006, 26(42): 10626-30. doi:10.1523/JNEUROSCI.3824-06.2006 |
| [9] | Seheid M P, Woodgett J R. PKB/AKT:functional insights from genetic models[J]. Nat Rev Mol Cell Biol, 2001, 2(10): 760-8. doi:10.1038/35096067 |
| [10] | Grimes C A, Jope R S. The multifaceted roles of glycogen synthase kinase 3beta in cellular signaling[J]. Prog Neurobiol, 2001, 65(4): 391-426. doi:10.1016/S0301-0082(01)00011-9 |
| [11] | Chen A, Liao W P, Lu Q, et al. Upregulation of dihydropyrimidinase-related protein 2, spectrin a Ⅱ chain, heat shock cognate protein 70 pseudogene 1 and tropomodulin 2 after focal cerebral ischemia in rats-A proteomics approach[J]. Neurochem Int, 2007, 50(7-8): 1078-86. doi:10.1016/j.neuint.2006.11.008 |
| [12] | Nishimura T, Fukata Y, Kato K, et al. CRMP-2 regulates polarized Numb-mediated endoeytosis for axon growth[J]. Nat Cell Biol, 2003, 5(9): 819-26. doi:10.1038/ncb1039 |
| [13] | Stroemer R P, Kent T A, Hulsebosch C E. Neocortical neural sprouting, synaptogenesis, and behavioral recovery after neocorital infarction in rats[J]. Stroke, 1995, 26(11): 2135-44. doi:10.1161/01.STR.26.11.2135 |

