


2. 漯河市肿瘤发生与防治研究创新型科技团队,河南 漯河 462002;
3. 宁夏医科大学总医院核医学科,宁夏 银川 750004;
4. 宁夏回族自治区第三人民医院呼吸内科,宁夏 银川 750021
2. Tumor Occurrence and Prevention Research Innovation Team of Luohe, Luohe Henan 462002, China;
3. Dept of Nuclear Medicine, General Hospital of Ningxia Medical University, Yinchuan 750004, China;
4. Dept of Respiratory Medicine, the Third People′s Hospital of Ningxia, Yinchuan 750021, China
神经病理性疼痛(neuropathic pain, NP)是临床上常见的一种慢性病理性疼痛,以痛觉过敏、痛觉超敏、自发痛及感觉异常为特点[1-2]。神经病理性疼痛发病复杂,临床治疗效果欠佳,严重影响患者的工作和生活质量。神经病理性疼痛发病机制目前尚未阐明,但各种原因导致的炎症反应(如神经系统感染、免疫炎症反应及小胶质细胞激活等)诱发的外周神经病理生理改变是其中的重要原因之一。在众多的炎症信号通路中,Toll样受体(Toll-like receptors 4, TLR4)/ p38蛋白激酶(p38 mitogen activated protein kinases,p38 MAPK)信号通路是经典的炎症反应相关途径,其被激活后能促进炎性细胞聚集和活化,调控相关转录因子的合成和活化,促进炎症因子(如TNF-α、IL-1β等)大量表达,导致机体的炎症损伤[3-4]。槐果碱(sophocarpine,SC)是从中药苦豆子中提取的一种具有药理活性的生物碱。我们前期研究发现,槐果碱对坐骨神经慢性缩窄性损伤致神经病理性疼痛小鼠有较好的镇痛作用,其机制与其上调γ-氨基丁酸(γ-aminobutyric acid, GABA)、谷氨酸脱羧酶65(glutamic acid decarboxylase 65, GAD65) 表达和下调γ-氨基丁酸转运体1(γ-aminobutyric acid transporters-1,GAT1) 表达有关,但槐果碱缓解神经病理性疼痛是否与调控TLR4/p38 MAPK炎症信号通路有关,尚未见报道[5]。本研究采用保留性神经损伤(spared nerve injury, SNI)方法建立小鼠神经病理性疼痛动物模型,建模成功后用不同剂量的槐果碱进行性干预,观察其改善小鼠神经病理性疼痛的作用及对TLR4、p38 MAPK、IL-1β和TNF-α表达水平的影响,探讨其镇痛作用机制。
1 材料 1.1 动物60只SPF级ICR小白鼠,♂,体质量(20±2) g,湖南斯莱克景达实验动物有限公司提供,许可证号:SCXK (湘) 2016-0002。将小鼠分笼饲养于温度为(20±2)℃、湿度50%~70%的动物房,自由饮食水,12 h/12 h光照周期。
1.2 药品与试剂槐果碱(纯度≥98%),由南京泽朗生物科技有限公司提供,临用时用含有5%的乙醇生理盐水溶液配制;普瑞巴林(pregabalin,Pre),购自德国辉瑞制药有限公司,批号:20160215;戊巴比妥钠,Sigma-Aldrich公司,批号20121011;RNA prep pure Tissue Kit总RNA提取试剂盒、Fast King一步法RT-PCR试剂盒、PCR引物合成,由天根生化科技(北京)有限公司提供;RIPA蛋白裂解液、预染蛋白质Marker、BCA蛋白浓度测定试剂盒、兔抗小鼠TLR4、p38 MAPK、IL-1β及TNF-α抗体、羊抗兔HRP标记IgG二抗、PVDF膜、超敏ECL化学发光显色液、SDS-PAGE凝胶配制试剂盒等,均购自武汉博士德生物工程有限公司。
1.3 仪器Von Frey纤维丝机械痛阈测定套件,上海玉研科学仪器有限公司;XR1102智能热刺痛仪,上海欣软信息科技有限公司;BW-YLS-21A冷热板痛觉测定仪,上海软科隆科技发展有限公司;FA1604电子分析天平,上海光学仪器厂;GL-23M高速冷冻离心机,湖南湘仪离心机仪器有限公司;凝胶成像分析系统、电泳仪、电泳槽、PCR仪等,均为美国伯乐公司。
2 方法 2.1 SNI法建立小鼠神经病理性疼痛模型取♂ ICR小鼠,分别称重,用1%戊巴比妥钠10 mL·kg-1腹腔注射进行麻醉。待麻醉成功后,将小鼠俯卧位固定于手术台上,将右侧后上肢的毛剃除,并用碘伏消毒,沿坐骨神经分叉处切开右后肢外侧面皮肤,按肌束走行分离股二头肌和臀肌,充分暴露游离坐骨神经和其远心端3个分支,分别为内侧胫神经、中间腓总神经及外侧的腓肠神经,然后用4-0号线分别结扎胫神经与腓总神经并于远心端切断,术中避免牵拉腓肠神经,保持其完好,结扎完成后逐层缝合肌层和皮肤。假手术组手术操作过程与模型组相似,但只暴露游离神经,不进行结扎切断。
2.2 动物分组及给药将60只ICR小鼠随机分为6组,每组10只动物,分别为:假手术组(sham)、神经病理性疼痛模型组(model)、阳性对照组(SNI+Pre 10 mg·kg-1)、槐果碱高、中、低剂量组(SNI+ sophocarpine 40、20、10 mg·kg-1)。假手术组和模型组均腹腔注射生理盐水10 mL·kg-1,治疗组分别腹腔注射给予相应剂量药物10 mL·kg-1。各组小鼠从手术后d 8开始给药,连续7 d。
2.3 小鼠机械缩足反射阈值(paw withdrawal mechanical threshold, PWMT)测定采用上下法测定小鼠术前1 d、术后d 7(给药前1 d)及给药后1、3、5、7 d机械缩足反射阈值。操作方法:将小鼠置于金属网垫上(网格大小:5 mm×5 mm),并用透明有机玻璃罩将其限制在一定范围内,适应15 min后用不同折力(g)的Von frey纤维丝刺激小鼠足底,观察有无缩足反应,记录其阳性反应的折力值即为小鼠机械缩足反射阈值。
2.4 小鼠热刺激缩足反应潜伏期(paw withdrawal thermal latency, PWTL)的测定参照Hargreave法,使用XR1102智能热刺痛仪测定小鼠术前1 d、术后d 7(给药前1 d)及给药后1、3、5、7 d热缩足反应潜伏期。操作方法:用透明有机玻璃罩将小鼠限制于3 mm厚的玻璃板上,调整玻璃板高度,小鼠适应15 min后,用热刺痛仪辐射焦点对准小鼠足底进行照射,从开始照射至小鼠出现缩足现象即为小鼠热缩足反应潜伏期(s)。为避免热刺激烫伤,照射时长上限设定为20 s,每只小鼠测定3次,间隔10 min,取其平均值。
2.5 小鼠冷缩足反射次数(cold withdrawal times, CWT)的测定使用BW-YLS-21A冷热板痛觉测定仪测定小鼠术前1 d、术后d 7(给药前1 d)及给药后1、3、5、7 d冷缩足反射次数。操作方法:设置冷热板痛觉测定仪工作温度为(4±1)℃,将小鼠置于其上,并用玻璃罩限制活动范围,适应5 min,然后记录其5 min内患侧后肢的抬足、添足或抖足次数即为冷缩足反射次数。
2.6 RT-PCR法测定小鼠脊髓组织TLR4、p38 MAPK、IL-1β及TNF-α mRNA表达小鼠末次给药后24 h颈椎脱臼处死,迅速取出L4-L5节段脊髓组织,充分匀浆后,按照RNA提取试剂盒及Fast King一步法RT-PCR试剂盒说明书进行RT-PCR实验。所用引物序列如下,TLR4上游引物:5′-CCGCTCTGGCATCATCTTCA-3′,下游引物:5′-AGGTCCAAGTTGCCGTTTCT-3′,产物227 bp;p38 MAPK上游引物:5′-GTCCTGAGCACCTGGTTTCT-3′,下游引物:5′-GAGATGACAGTTCCCATCGGC-3′,产物294 bp;IL-1β上游引物:5′-CCAAACCTTTGACCTGGGCT-3′,下游引物:5′-GGAAGGTCCACGGGAAAGAC-3′,产物149 bp;TNF-α上游引物:5′-AACTGCCGAGAGACCCAAAG-3′,下游引物:5′-AGCCCTGCTTCCAGGATTTC-3′,产物185 bp;β-actin上游引物:5′-GATATTGCTGCCCTGGTCGT-3′,下游引物:5′-CTTGGGCGACCCACAATAGA-3′,产物107 bp。
2.7 Western blot法测定小鼠脊髓组织TLR4、p38 MAPK、IL-1β及TNF-α蛋白表达小鼠末次给药后24 h颈椎脱臼处死,迅速取出L4-L5节段脊髓组织,置于试管中,于冰上用电动匀浆器充分匀浆,然后加RIPA蛋白裂解液充分裂解,按照说明书进行总蛋白提取。调整各样本总蛋白浓度一致,加loading buffer混匀后,用沸水煮5 min,进行SDS-PAGE凝胶电泳,按照操作规程孵育一抗、二抗,然后在凝胶成像仪下成像拍照,以β-actin为内参分析待测蛋白相对表达值。
2.8 统计学处理所有实验数据以x±s表示,应用SPSS 19.0统计软件包进行分析,组间样本均数比较采用One-way ANOVA分析。
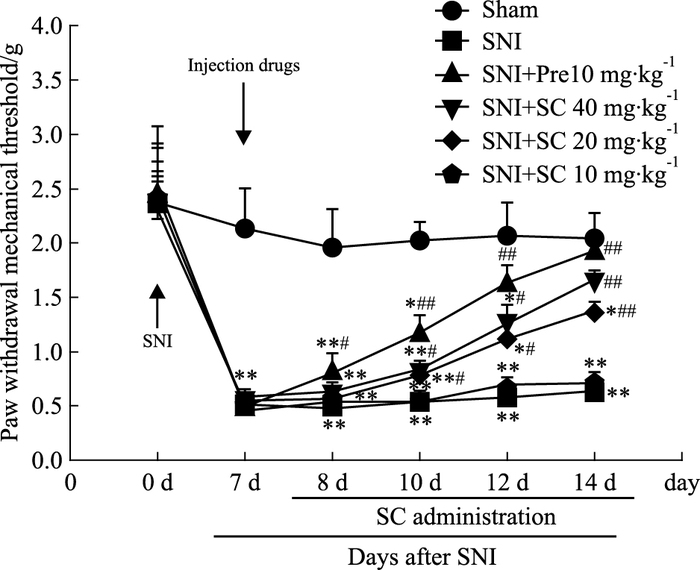
3 结果 3.1 槐果碱对SNI小鼠PWMT的影响Fig 1结果显示,与假手术组比较,神经病理性疼痛模型组及各给药组小鼠机械缩足反射阈值于SNI术后d 7明显降低(P<0.01);与模型组比较,给予槐果碱40、20 mg·kg-1后d 3、5、7,小鼠机械缩足反射阈值明显升高(P<0.05,P<0.01)。
|
| Fig 1 Effects of sophocarpine on paw withdrawal mechanical threshold in mice with neuropathic pain induced by SNI(x±s, n=10) *P < 0.05, **P < 0.01 vs sham group; #P < 0.05, ##P < 0.01 vs SNI group |
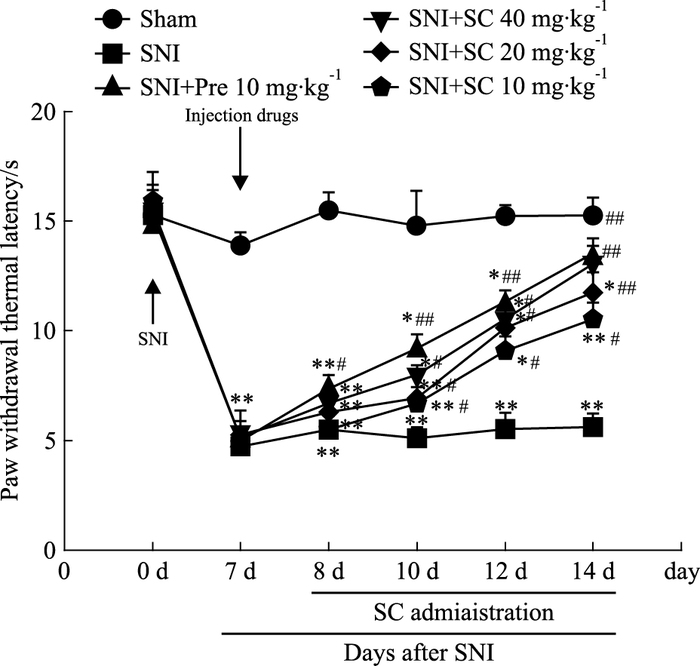
由Fig 2可见,与假手术组比较,神经病理性疼痛模型组及各给药组小鼠热刺激缩足反应潜伏期于SNI术后d 7明显缩短(P<0.01);与模型组比较,给予槐果碱40、20、10 mg·kg-1后d 3、5、7,小鼠热刺激缩足反应潜伏期明显延长(P<0.05,P<0.01)。
|
| Fig 2 Effects of sophocarpine on paw withdrawal thermal latency in mice with neuropathic pain induced by SNI(x±s, n=10) *P < 0.05, **P < 0.01 vs sham group; #P < 0.05, ##P < 0.01 vs SNI group |
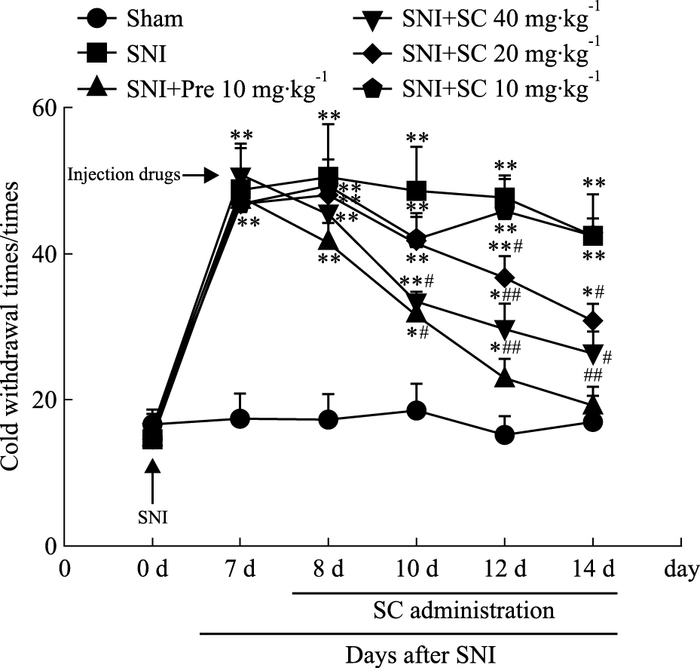
Fig 3结果显示,与假手术组比较,神经病理性疼痛模型组及各给药组小鼠冷缩足反射次数于SNI术后d 7明显增多(P<0.01);与模型组比较,给予槐果碱40 mg·kg-1后d 3及给予槐果碱40、20 mg·kg-1后d 5、7,小鼠冷缩足反射次数明显减少(P<0.05,P<0.01)。
|
| Fig 3 Effects of sophocarpine on cold withdrawal times in mice with neuropathic pain induced by SNI(x±s, n=10) *P < 0.05, **P < 0.01 vs sham group; #P < 0.05, ##P < 0.01 vs SNI group |
与假手术组比较,神经病理性疼痛模型组小鼠脊髓组织p38 MAPK、TLR4、TNF-α及IL-1β mRNA表达水平明显上调(P<0.01);与模型组比较,槐果碱40 mg·kg-1组小鼠脊髓组织p38 MAPK、TLR4、TNF-α及IL-1β mRNA表达水平明显下调(P<0.05,P<0.01)。见Fig 4。

|
| Fig 4 Effects of sophocarpine on spinal cord tissue expression levels of p38 MAPK, TLR4, TNF-α and IL-1β mRNA in mice with neuropathic pain induced by SNI(x±s, n=5) 1:Sham group; 2:SNI group; 3:SNI+SC 40 mg·kg-1 group.*P < 0.05, **P < 0.01 vs sham group; #P < 0.05, ##P < 0.01 vs SNI group |
MAPK、IL-1β及TNF-α蛋白表达的影响Fig 5结果显示,与假手术组比较,神经病理性疼痛模型组小鼠脊髓组织p38 MAPK、TLR4、TNF-α及IL-1β蛋白表达水平明显上调(P<0.01);与模型组比较,槐果碱40 mg·kg-1组小鼠脊髓组织p38 MAPK、TLR4、TNF-α及IL-1β蛋白表达水平明显下调(P<0.05,P<0.01)。

|
| Fig 5 Effects of sophocarpine on spinal cord tissue expression levels of p38 MAPK, TLR4, TNF-α and IL-1β protein in mice with neuropathic pain induced by SNI(x±s, n=5) 1:Sham group; 2:SNI group; 3:SNI+SC 40 mg·kg-1 group.*P < 0.05, **P < 0.01 vs sham group; #P < 0.05, ##P < 0.01 vs SNI group |
神经病理性疼痛是由各种原因引起的神经系统受损或病理改变,导致中枢或外周神经超敏,从而诱发异常疼痛的临床病症。研究认为[6-7],炎症是导致神经病理性疼痛痛觉过敏、痛觉超敏、自发痛等异常表现的重要机制之一。因此,减少神经系统的炎症反应是缓解神经病理性疼痛的主要治疗手段。
TLR4是机体免疫和炎症识别系统中一种重要的跨膜蛋白受体,可识别内、外源性炎症刺激因子并与之结合,促进细胞因子或炎症因子(如TNF-α、IL-1β等)释放,诱发炎症反应[8]。研究报道[9],在神经病理性疼痛时,由于神经组织受损,释放炎性刺激因子,TLR4被活化导致炎症性疼痛,加之释放的内源性炎症因子,使得疼痛放大,表现为痛过敏、痛超敏或自发痛等。p38 MAPK是丝裂原活化蛋白激酶家族中介导炎症反应的重要成员之一,活化后能够促进炎性细胞的聚积和活化,调控NF-κB等炎症因子的合成与释放,在炎症的发展与转归中发挥关键作用[10]。研究证实,TLR4与p38 MAPK是相互关联的上下游信号通路,TLR4表达上调后,可激活p38 MAPK信号通路,促进炎症介质因子网络失衡,从而诱发和加重神经受损后的炎症反应,导致病理性疼痛产生。同样,抑制TLR4活性,则可下调p38 MAPK的表达,使TNF-α、IL-1β等炎症因子生成释放减少,减轻炎症反应[11-12]。
综上所述,TLR4/p38 MAPK作为重要的炎症信号通路,参与了神经病理性疼痛的发生发展,针对调控TLR4/ p38 MAPK信号通路及相关炎症因子(如TNF-α、IL-1β等)等将是临床上缓解神经病理性疼痛的一个新策略。本研究观察到槐果碱40、20 mg·kg-1能明显增加SNI诱导的神经病理性疼痛小鼠机械缩足反射阈值,延长热刺激缩足反应潜伏期,减少冷缩足反射次数,提示槐果碱对神经病理性疼痛有较好的缓解作用,这与我们以往的研究结果一致[5];同时,我们检测到槐果碱40 mg·kg-1可明显下调SNI诱导的神经病理性疼痛小鼠脊髓组织TLR4、p38 MAPK、IL-1β、TNF-α mRNA与蛋白表达水平,提示其缓解疼痛机制与下调TLR4、p38 MAPK、IL-1β及TNF-α有关。
( 致谢: 本文实验是在漯河医学高等专科学校科研中心完成,感谢中心全体成员对本研究的支持和帮助 )
| [1] | Zhou J, Chen H, Yang C, et al. Reversal of TRESK downregulation alleviates neuropathic pain by inhibiting activation of gliocytes in the spinal cord[J]. Neurochem Res, 2017, 42(5): 1288-98. doi:10.1007/s11064-016-2170-z |
| [2] | 王依慰, 刘清珍, 陈春龙, 等. 白藜芦醇通过降低NF-κB p65乙酰化缓解大鼠神经病理性疼痛[J]. 中国药理学通报, 2016, 32(1): 89-93. Wang Y W, Liu Q Z, Chen C L, et al. Resveratrol facilitates neuropathic pain in rats model by decreasing acetylation of NF-κB p65[J]. Chin Pharmacol Bull, 2016, 32(1): 89-93. |
| [3] | 张利鹏, 赵焱, 刘国娟, 等. 乌司他丁通过干预p38MAPK/ERK信号通路减轻脓毒症性肺损伤[J]. 中国药理学通报, 2016, 32(9): 1311-6. Zhang L P, Zhao Y, Liu G J, et al. Ulinastatin attenuates lipopolysaccharide-induced acute lung injury by intervening p38MAPK /ERK signaling pathway[J]. Chin Pharmacol Bull, 2016, 32(9): 1311-6. |
| [4] | Jurga A M, Rojewska E, Piotrowska A, et al. Blockade of toll-like receptors(TLR2, TLR4) attenuates pain and potentiates buprenorphine analgesia in a rat neuropathic pain model[J]. Neural Plast, 2016, 2016: 5238730. |
| [5] | 金少举, 任丽平, 马奔晖, 等. 槐果碱对神经病理性疼痛小鼠GABA信号通路的影响[J]. 中药药理与临床, 2016, 32(3): 24-8. Jin S J, Ren L P, Ma B H, et al. The effects of sophocarpine on the GABA signaling pathway in mice with neuropathic pain[J]. Pharmacol Clin Chin Mater Med, 2016, 32(3): 24-8. |
| [6] | Carballo-Villalobos A I, Gonzalez-Trujano M E, Alvarado-Vazquez N, et al. Pro-inflammatory cytokines involvement in the hesperidin antihyperalgesic effects at peripheral and central levels in a neuropathic pain model[J]. Inflammopharmacology, 2017, 25(2): 265-9. doi:10.1007/s10787-017-0326-3 |
| [7] | Xu Y Q, Jin S J, Liu N, et al. Aloperine attenuated neuropathic pain induced by chronic constriction injury via anti-oxidation activity and suppression of the nuclear factor kappa B pathway[J]. Biochem Biophys Res Commun, 2014, 451(4): 568-73. doi:10.1016/j.bbrc.2014.08.025 |
| [8] | 黄铭涵, 黄健, 陈琴, 等. 健脾清化中药复方对大鼠慢性萎缩性胃炎TLR4-MyD88依赖途径蛋白表达及TNF-α的影响[J]. 中国药理学通报, 2016, 32(9): 1321-5. Huang M H, Huang J, Chen Q, et al. Effects of Jianpi Qinghua Chinese herbal compound on TLR4-MyD88-dependent pathway protein expression and TNF-α in animal model of chronic atrophic gastritis(CAG) in rats[J]. Chin Pharmacol Bull, 2016, 32(9): 1321-5. |
| [9] | Kuang X, Huang Y, Gu H F, et al. Effects of intrathecal epigallocatechin gallate, an inhibitor of Toll-like receptor 4, on chronic neuropathic pain in rats[J]. Eur J Pharmacol, 2012, 676(1-3): 51-6. doi:10.1016/j.ejphar.2011.11.037 |
| [10] | 朱桂军, 孟志强, 刘丽霞, 等. DATS通过p38 MAPK通路抑制LPS诱导的小鼠MH-S细胞TNF-α及IL-1β表达[J]. 中国药理学通报, 2012, 28(9): 1303-7. Zhu G J, Meng Z Q, Liu L X, et al. Inhibition of LPS-induced TNF-α and IL-1β expression by DATS through p38 MAPK pathway in MH-S cell[J]. Chin Pharmacol Bull, 2012, 28(9): 1303-7. |
| [11] | 李亚清, 严建平, 许武林, 等. 核因子-κB和p38丝裂原活化蛋白激酶调节脂多糖诱导的气道上皮细胞白细胞介素8的表达[J]. 中国药理学通报, 2011, 27(2): 182-6. Li Y Q, Yan J P, Xu W L, et al. Induction of interleukin-8 by lipopolysaccharide in human airway epithelial cells via NF-κB and p38 mitogen-activated protein kinase[J]. Chin Pharmacol Bull, 2011, 27(2): 182-6. |
| [12] | Nyati K K, Masuda K, Zaman M M, et al. TLR4-induced NF-kappa B and MAPK signaling regulate the IL-6 mRNA stabilizing protein Arid5a[J]. Nucleic Acids Res, 2017, 45(5): 2687-703. doi:10.1093/nar/gkx064 |

