


2. 沈阳医学院 辽宁省环境污染与微生态重点实验室,辽宁 沈阳 110034
2. Key Lab of Environmental Pollution and Microecology of Liaoning Province, Shenyang Medical College, Shenyang 110034, China
乳腺癌是常见女性恶性肿瘤,其中70%的患者为雌激素受体α(estrogen receptor α,ERα)阳性。ERα阳性的乳腺癌MCF-7细胞,其生长与增殖主要受ER信号系统驱动,此信号系统亦可被瘦素(Leptin)信号系统所激活[1]。女性体内瘦素水平增加,其患高恶性、低分化且预后不良的乳腺癌几率大大增加[2]。p21WAF1/CIP1是细胞周期依赖性蛋白激酶抑制剂,可使细胞周期停滞、促进细胞凋亡并抑制癌细胞的转移和侵袭。本研究的前期工作证实,瘦素处理后的小鼠乳腺癌4T1细胞p21WAF1/CIP1 mRNA及蛋白表达水平远远低于瘦素未处理组细胞[3]。组蛋白去乙酰化酶1 (histone deacetylases 1,HDAC1) 使组蛋白去乙酰化,可与一些调控肿瘤发生发展的基因启动子区结合,抑制这些基因的转录。辛二酰苯胺异羟肟酸(suberoylanilide hydroxamic acid,SAHA)是目前已知最经典的HDAC抑制剂(histone deacetylase inhibitor, HDACi)之一, 可抑制组蛋白去乙酰化酶活性,通过上调p21WAF1/CIP1引起细胞周期阻滞于G1期而抑制细胞增殖[4]。本实验旨在寻找HDAC1及ERα共同募集于p21WAF1/CIP1启动子区,调控其转录活性的具体作用位点,明确SAHA及瘦素在调节p21WAF1/CIP1启动子功能过程中的分子机制。
1 材料与方法 1.1 材料人乳腺癌细胞株MCF-7(美国ATCC细胞库), SAHA(Sigma), Leptin(Sigma), 完全型RPMI 1640培养液(Thermo), 改良型RPMI 1640培养液(Thermo), 磷酸盐缓冲液1×(Thermo), 0.25%胰酶-EDTA(Gibco), 89890 ZebaTM脱盐离心柱(Thermo), PierceTM Agarose ChIP试剂盒(Thermo), HDAC1及ERα抗体(Abcam), Power SYBR® Green PCR Master Mix(Life technologies), p21WAF1/CIP1 f1~f10引物(上海生工生物工程有限公司)。超净工作台(Thermo)、CO2恒温细胞培养箱(Thermo), Biofuge 28RS低温高速离心机(Heraeus), 倒置显微镜(Olympus), SK-D1807-E摇床(Scilogex), 恒温混匀器(Eppendorf), 7500 Real-time PCR仪(Life technologies)。
1.2 方法 1.2.1 细胞培养将MCF-7细胞接种在完全型RPMI 1640培养液(10%胎牛血清,青霉素、链霉素100 kU·L-1)中,37℃、5% CO2孵箱饱和湿度条件下贴壁传代培养,每2~3 d换液并传代1次。0.25%胰酶-EDTA消化。经2~3次传代, 取对数生长期的细胞等量分成3组,分别接种于完全型RPMI 1640培养液中,24 h后,再将细胞置于改良型RPMI 1640培养液中进行同步化处理24 h。此后,将3组细胞分别定义为SAHA组(完全型RPMI 1640培养液10 mL+20 μmol·L-1 SAHA 0.88 μL)、Leptin组(完全型RPMI 1640培养液10 mL+0.625 nmol·L-1 Leptin 10 μL)、Basal对照组(等量完全型RPMI 1640培养液)。
1.2.2 先后使用HDAC1及Eα抗体经两次ChIP (即ChIP-on-ChIP)方法处理样品MCF-7细胞的甲醛交联及细胞团的分离;细胞溶解及MNase消化,每组样品各得到50 μL的MNase消化产物,留取5 μL -20℃保存作为内对照,45 μL进行下一步的免疫沉淀处理,免疫沉淀过程中需向每个ChIP样品加入HDAC1抗体10 μg;HDAC1抗体-组蛋白-DNA免疫沉淀洗脱:向免疫沉淀物中加入150 μL 1×IP洗脱液,室温振荡孵育30 min,再加入150 μL 1×IP洗脱液,室温振荡孵育10 min。3 000×g 2 min离心收集洗脱下来的免疫沉淀物,将洗脱复合物置于到经1×IP稀释液预处理的Zeba脱盐洗脱柱上(参见操作手册),1 000×g离心2 min收集样品。向各组样品中加入1×IP稀释液至500 μL,加入Eα抗体7.5 μg,进行再次免疫沉淀(参见操作手册),最终3组MCF-7细胞均获得使用HDAC1及Eα抗体进行2次ChIP得到的DNA及各自的内对照。
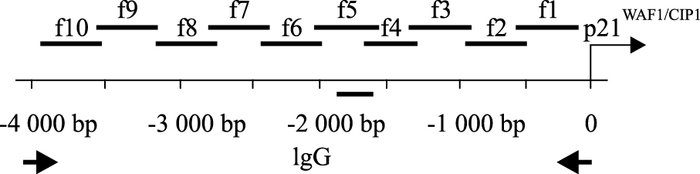
1.2.3 Real-time PCR检测各组p21WAF1/CIP1 f1~f10片段的DNA相对表达PCR反应体系为25 μL:DNA 1.5 μL,上、下游引物各0.75 μL,PCR Master Mix 12.5 μL, ddH2O 9.5 μL。反应条件为:50℃ 2 min, 95℃ 10 min预变性, 95℃ 15 s, 60℃ 1 min, 共40个循环。每个样品3个复孔,采用2-△△CT法计算各组DNA的相对表达量。p21WAF1/CIP1启动子区的10个片段的引物序列为:f1:Forward 5′-TCCTCCTGGAGAGTGCCAAC-3′,Reverse 5′-TTGGTGCGCTGGACACATTT-3′;f2:Forward 5′-TTCCCGGAAGCATGTGACAA-3′,Reverse 5′-GCACCTGGAGCACCTAG ACACC-3′;f3:Forward 5′-CCCGTTTCCCCAGCAGTGTA-3′,Reverse 5′-GCCAGGAAGGGGAGGATTTG-3′;f4:Forward 5′-AGGCCAAGGGGGTCTGCTAC-3′,Reverse 5′-CGGGGAGGACAGGCTTCTTT-3′;f5:Forward 5′-TGAAAGCAGAGGGGCTTCAA-3′,Reverse 5′-ACCATCCAAAGGGCTGGTTG-3′;f6:Forward 5′-TGTCCTTGGGCTGCCTGTTT-3′,Reverse 5′-AGCCCTGTCG CAAGGATCTG-3′;f7:Forward 5′-TTCTGCAGCCACCACTGAGC-3′,Reverse 5′-GTGGAGCAGCATGGGGTAGG-3′;f8:Forward5′-CCCACCTCAGCCACCTGAA T-3′,Reverse 5′-GGGCAGATCACAGGGTCAGG-3′;f9:Forward 5′-AGTGGGCACATTTAGACATAGCAGG T-3′,Reverse 5′-CCTCCCGGTCATGCCTTT C-3′;f10:Forward 5′-GTCAGGTGCCACTGGGGTCT-3′,Reverse 5′-CGGTCCCCTGTTTCAATGCT-3′。p21WAF1/CIP1启动子区+2~ -4000 bp 10个选定区域f1~f10(Fig 1)。
|
| Fig 1 Schematic diagram of HDAC1 and ERα response element for regulating transcriptional function of p21WAF1/CIP1 promoter |
所有数据均用x±s表示,采用SPSS17.0统计软件分析,采用方差分析进行统计学处理。
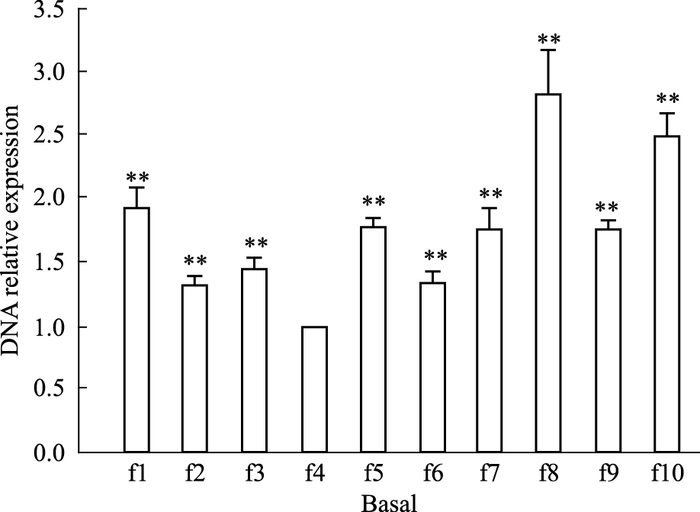
2 结果 2.1 Basal组MCF-7细胞p21WAF1/CIP1启动子区f1~f10片段HDAC1及ERα高功能结合位点筛选Basal组MCF-7细胞经HDAC1及ERα抗体2次ChIP处理后,45 μL样品与5 μL内对照的DNA分别与f1~f10引物作用进行Real-time PCR扩增,所得CT值之差为该样品在p21WAF1/CIP1启动子区各自片段的ΔCT值,再以f4片段为对照,其他片段的△CT值与其相减,得到Basal组样品在p21WAF1/CIP1启动子区f1~f10片段各自△△CT值,采用2-△△CT法计算各片段DNA的相对表达量。Basal组f1~f3、f5~f10片段DNA的相对表达量为(1.93±0.13)、(1.31±0.07)、(1.44±0.09)、(1.77±0.08)、(1.32±0.09)、(1.75±0.15)、(2.81±0.36)、(1.76±0.07)、(2.48±0.18),较f4片段相对表达量(1±0) 明显升高(P<0.01),f8片段达最高值(Fig 2)。
|
| Fig 2 Screening of high function bind site of HDAC1 and ERα among f1~f10 fragments of p21WAF1/CIP1 promoter region in basal group MCF-7 cells **P < 0.01 vs f4 fragment |
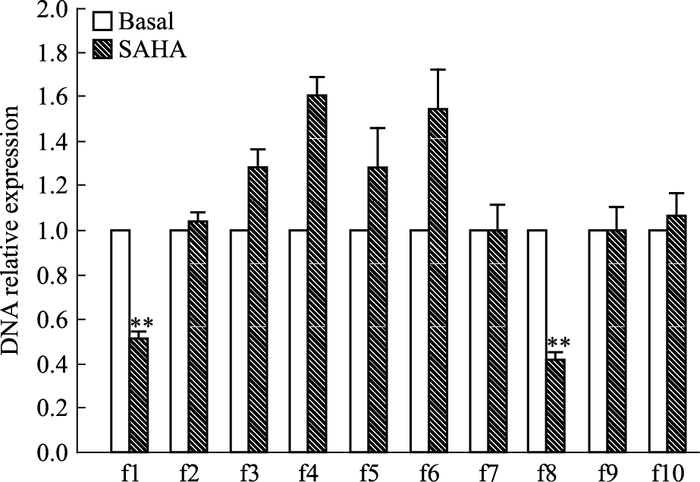
将SAHA处理后的MCF-7细胞的DNA组分,经HDAC1及ERα抗体2次ChIP处理后,进行Real-time PCR检测。结果表明,SAHA组MCF-7细胞的p21WAF1/CIP1启动子f1及f8片段结合HDAC1及ERα抗体的DNA相对表达量为(0.51±0.04)、(0.41±0.04),较Basal组对应片段相对表达量(1±0) 均明显降低(P<0.01),见Fig 3。
|
| Fig 3 Screening of high function bind site of HDAC1 and ERα among f1~f10 fragments of p21WAF1/CIP1 promoter region in SAHA group MCF-7 cells **P < 0.01 vs basal group |
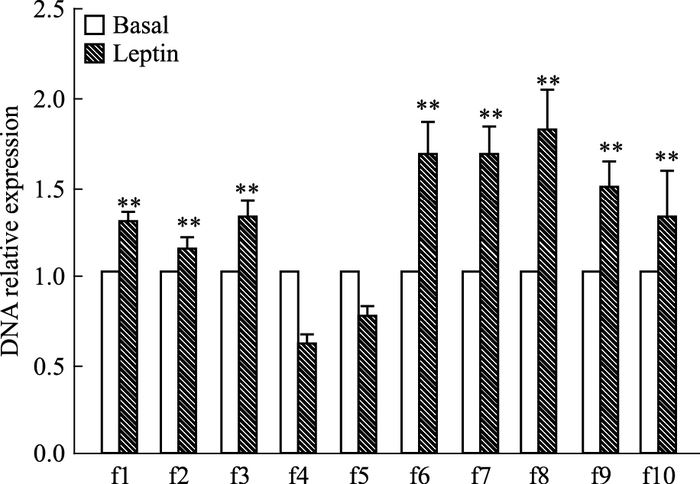
将Leptin处理后的MCF-7细胞的DNA组分,经HDAC1及ERα抗体2次ChIP处理后,进行Real-time PCR检测。结果表明,Leptin组细胞p21WAF1/CIP1启动子区f1~f3、f6~f10片段结合HDAC1及ERα抗体的DNA相对表达量为(1.28±0.06)、(1.12±0.07)、(1.32±0.08)、(1.66±0.17)、(1.66±0.15)、(1.80±0.22)、(1.48±0.14)、(1.32±0.25),较Basal组对应片段相对表达量(1±0) 均明显升高(P<0.01),f8片段达最高值(Fig 4)。
|
| Fig 4 Screening of high function bind site of HDAC1 and ERα among f1~f10 fragments of p21WAF1/CIP1 promoter region in Leptin group MCF-7 cells **P < 0.01 vs basal group |
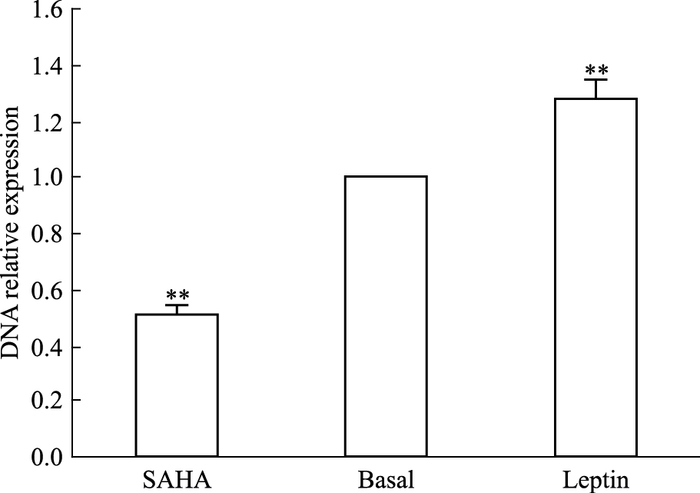
SAHA、Leptin组MCF-7细胞p21WAF1/CIP1启动子区f1片段结合HDAC1及ERα抗体的DNA相对表达量为(0.51±0.04)、(1.28±0.06),与Basal组对应片段相对表达量(1±0) 相比,差异均有统计学意义(P<0.01),见Fig 5。
|
| Fig 5 Comparison of high function bind of HDAC1 and ERα in f1 fragment of p21WAF1/CIP1 promoter region in MCF-7 cells among SAHA, Basal and Leptin group **P < 0.01 vs basal group |
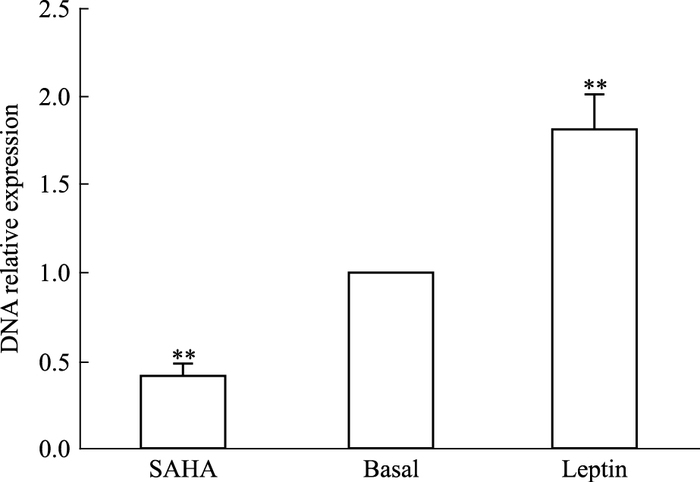
SAHA、Leptin组MCF-7细胞p21WAF1/CIP1启动子区f8片段结合HDAC1及ERα抗体的DNA相对表达量为(0.41±0.06)、(1.80±0.22),与Basal组对应片段相对表达量(1±0) 相比,差异均有统计学意义(P<0.01),见Fig 6。
|
| Fig 6 Comparison of high function bind of HDAC1 and ERα in f8 fragment of p21WAF1/CIP1 promoter region in MCF-7 cells among SAHA, Basal and Leptin group **P < 0.01 vs basal group |
乳腺癌MCF-7细胞为ER阳性的乳腺癌经典细胞系,其ERα位于细胞核内,是雌激素激活的转录因子,通过调节特异性靶基因的转录而发挥基因型调节效应。雌激素应答成分(estrogen response element, EREs)位于雌激素应答靶基因的启动子区,ERα可直接结合到EREs或通过与AP1、SP1、MTA1、HDAC1等其他转录因子结合,调控靶基因的转录,促进乳腺癌细胞的增生[5]。乳腺癌MCF-7细胞引起癌前病变及癌肿中ERα的表达均增高[6]。ERα是乳腺癌细胞增殖过程中的重要调控因素, ERα基因的表达及其转录活性的调控都离不开HDACs的参与[7], 尤其是HDAC1和HDAC7[8]。
本实验利用ChIP-on-ChIP方法研究发现,Basal组MCF-7细胞p21WAF1/CIP1基因TSS近端启动子调节区f1~f3和远端调节区f5~f10片段结合HDAC1及ERα抗体的DNA相对表达量较f4片段明显升高。这表明在细胞增殖过程中,HDAC1及ERα可被招募至p21WAF1/CIP1启动子区,其中f1及f8片段均与之有较高能力的结合。
在乳腺癌细胞增殖过程中,细胞增殖信号在p21WAF1/CIP1的启动子区可招募HDAC1转录因子,通过组蛋白去乙酰化表观遗传修饰影响p21WAF1/CIP1表达。前期研究证实,SAHA可降低HDAC1在p21WAF1/CIP1启动子区的结合[9]。此外,HDACi也显示出对ERα基因表达的下调作用[10]。SAHA可以从转录水平抑制ERα合成,同时可以通过增强Hsp90乙酰化修饰,促进ERα经泛素-蛋白酶体通路降解[11]。本研究发现,SAHA作用下的MCF-7细胞,p21WAF1/CIP1启动子区f1及f8片段结合HDAC1及ERα抗体的DNA相对表达量明显低于对照组,这表明f1及f8片段可能是SAHA发挥作用的功能敏感区。
Leptin可通过调控细胞周期、凋亡、影响细胞外环境等多重机制,促进雌激素受体阳性的MCF-7乳腺癌细胞增殖与转移[12]。Leptin可提高HDAC1的活性,使核心组蛋白去乙酰化,从而抑制p21WAF1/CIP1的表达,最终促进细胞周期从G1期到S期的进程[13]。另有报道,Leptin可通过促进芳香酶的表达,导致雌激素生成增多[14],也可上调乳腺癌MCF-7细胞中ERα的表达水平[15]。本实验中,Leptin作用下的MCF-7细胞,p21WAF1/CIP1启动子区f1~f3及f6~f10片段结合HDAC1及ERα抗体的DNA相对表达量较对照组增多,但根据SAHA组细胞p21WAF1/CIP1启动子区各片段结合HDAC1及ERα抗体情况的筛选结果,可以推断在乳腺癌发生、发展过程中,f1及f8片段可能是Leptin与SAHA均发挥作用的功能敏感区。
综上所述,本研究通过ChIP on ChIP实验技术筛选出Basal组乳腺癌MCF-7细胞p21WAF1/CIP1启动子区的HDAC1及ERα高功能结合位点,进而利用SAHA及Leptin的药理学特征,使用SAHA及Leptin对MCF-7细胞进行分组处理,ChIP on ChIP 2次抗体结合后DNA检测,进一步明确p21WAF1/CIP1启动子区0~400 bp、-2 800~-3 200 bp两区域可能是与HDAC1和ERα高度结合的功能活跃区。此研究发现丰富了SAHA和Leptin在调节p21WAF1/CIP1启动子功能过程中的分子机制,更为抗乳腺癌的药物研发及靶向治疗奠定了理论和实验基础。
| [1] | Xue R Q, Gu J C, Du S T, et al. Lentivirus-mediated RNA interference targeting the ObR gene in human breast cancer MCF-7 cells in a nude mouse xenograft model[J]. Chin Med J(Engl), 2012, 125(9): 1563-70. |
| [2] | Hancke K, Grubeck D, Hauser N, et al. Adipocyte fatty acid-binding protein as a novel prognostic factor in obese breast cancer patients[J]. Breast Cancer Res Treat, 2010, 119(2): 367-77. doi:10.1007/s10549-009-0577-9 |
| [3] | Zhou W, Guo S, Gonzalez-Perez R R. Leptin pro-angiogenic signature in breast cancer is linked to IL-1 signalling[J]. Br J Cancer, 2011, 104(1): 128-37. doi:10.1038/sj.bjc.6606013 |
| [4] | 韩翰, 王敏. SAHA和TRAIL联合使用对乳腺癌雌激素受体阳性细胞MCF-7生长的影响[J]. 中国药理学通报, 2016, 32(2): 223-8. Han H, Wang M. Effects of combination treatment with SAHA and TRAIL on ER positive breast cancer cell MCF-7[J]. Chin Pharmacol Bull, 2016, 32(2): 223-8. |
| [5] | Liao X H, Lu D L, Wang N, et al. Estrogen receptor α mediates proliferation of breast cancer MCF-7 cells via a p21/PCNA/E2F1-dependent pathway[J]. FEBS J, 2014, 281(3): 927-42. doi:10.1111/febs.2014.281.issue-3 |
| [6] | 张佳娜, 汪庆余, 曾磊, 等. 乳腺癌细胞中p73α与ERα的相互关系[J]. 实验与检验医学, 2013, 31(1): 4-6. Zhang J N, Wang Q Y, Zeng L, et al. Co-relation between ERα and p73α in breast cancer cells[J]. Exp Lab Med, 2013, 31(1): 4-6. |
| [7] | Margueron R, Duong V, Castet A, et al. Histone deacetylase inhibition and estrogen signalling in human breast cancer cells[J]. Biochem Pharmacol, 2004, 68(4): 1239-46. |
| [8] | Kurtev V, Margueron R, Kroboth K, et al. Transcriptional regulation by the repressor of estrogen receptor activity via recruitment of histonedeacetylases[J]. J Biol Chem, 2004, 279(23): 24834-43. doi:10.1074/jbc.M312300200 |
| [9] | 邹丹, 周伟强. 乳腺癌MCF-7细胞p21WAF1/CIP1启动子区HDAC1高功能结合位点的研究[J]. 中国药理学通报, 2017, 33(3): 317-21. Zou D, Zhou W Q. A study on high function binding site of HDAC1 in p21WAF1/CIP1 promoter region in breast cancer MCF-7 cells[J]. Chin Pharmacol Bull, 2017, 33(3): 317-21. |
| [10] | Margueron R, Duong V, Bonnet S, et al. Histone deacetylase inhibition and estrogen receptor alpha levels modulate the transcriptional activity of partial antiestrogens[J]. J Mol Endocrinol, 2004, 32(2): 583-94. doi:10.1677/jme.0.0320583 |
| [11] | Yi X, Wei W, Wang S Y, et al. Histone deacetylase inhibitor SAHA induces ERalpha degradation in breast cancer MCF-7 cells by CHIP-mediated ubiquitin pathway and inhibits survival signaling[J]. Biochem Pharmacol, 2008, 75(9): 1697-705. doi:10.1016/j.bcp.2007.10.035 |
| [12] | Feng X, Han H, Zou D, et al. Suberoylanilide hydroxamic acid-induced specific epigenetic regulation controls Leptin-induced proliferation of breast cancer cell lines[J]. Oncotarget, 2017, 8(2): 3364-79. |
| [13] | Gonzalez-Perez R R, Xu Y, Guo S, et al. Leptin upregulates VEGF in breast cancer via canonic and non-canonical signalling pathways and NF-kappaB/HIF-1alpha activation[J]. Cell Signal, 2010, 22(9): 1350-62. doi:10.1016/j.cellsig.2010.05.003 |
| [14] | Liu E, Samad F, Mueller B M. Local adipocytes enable estrogen-dependent breast cancer growth: role of leptin and aromatase[J]. Adipocyte, 2013, 2(3): 165-9. doi:10.4161/adip.23645 |
| [15] | Yu W, Gu J C, Liu J Z, et al. Regulation of estrogen receptors alpha and beta in human breast carcinoma by exogenous leptin in nude mouse xenograft model[J]. Chin Med J(Engl), 2010, 123(3): 337-43. |

