


2. 永州职业技术学院 基础医学部,湖南 永州 425100;
3. 南华大学附属湘潭医院病理科,湖南 湘潭 411101;
4. 南华大学附属第二医院病理科,湖南 衡阳 421001
2. Dept of Basic Medicine, Yongzhou Vocational Technical College, Yongzhou Hunan 425100, China;
3. Dept of Pathology, the Affiliated Xiangtan Hospital, University of South China, Xiangtan Hunan 411101, China;
4. Dept of Pathology, the Second Affiliated Hospital, University of South China, Hengyang Hunan 421001, China
胃癌是最常见的恶性肿瘤之一,发生率与死亡率分别为全球第4位与第3位[1]。据最新统计,胃癌在我国每年约新发67.9万,死亡49.8万人,发生率与死亡率位于第2。由于患者就诊时大多已发生侵袭转移,常规外科手术和化学药物治疗效果较差,5年生存率低于10%[2-3]。因此,开发高效低毒药物与寻找靶点对防治胃癌具有重要意义。
二烯丙基二硫(diallyl disulfide,DADS)是大蒜中烯丙基硫化物的一种脂溶性的有效成分,对多种肿瘤均有明显的抑制作用[4]。近年来,miRNAs在肿瘤中的作用引起人们高度关注。miRNAs是一类含量丰富且高度保守的非编码内源性小RNA分子,通过与靶基因mRNA的3′非编码区完全或不完全结合,抑制靶基因的表达,从而调控细胞增殖、分化与凋亡等重要过程[5]。我们先前研究表明,miR-22在胃癌中表达下调与临床分期和淋巴结转移有关[6]。并且,DADS作用人胃癌MGC803细胞的差异miRNAs中,发现miR-22上调[7]。本文进一步探讨DADS上调miR-22是否通过Wnt-1通路抑制MGC803细胞迁移与侵袭。
1 材料与方法 1.1 试剂质粒抽提试剂盒购自上海华瞬公司;逆转录试剂盒、荧光素酶活性检测试剂盒购自Promega公司;miR-22 mimics与Wnt-1基因3′UTR的结合位点序列分别由Exiqon公司与Invitrogen公司合成;qRT-PCR miRNA试剂盒购自上海吉玛公司;蛋白浓度测定试剂盒、ECL化学发光检测试剂盒购自Pierce公司;Wnt-1(sc-6280)、β-catenin (sc-7963)、TCF-4(sc-166699)、β-actin(sc-47778) 抗体购自Santa Cruz公司;RPMI 1640培养液购自Hyclone公司,胎牛血清购自四季青生物公司;转染用Opti-MEM培养液购自Invtrogen公司。
1.2 细胞培养与分组人胃癌MGC803细胞由本实验室保存,置于含10%小牛血清的RPMI 1640培养基中,37℃、5% CO2、饱和湿度的培养箱内传代培养。采用胰酶消化预先培养的MGC803细胞并接种于6孔板中,按每孔2 mL铺好,培养至细胞汇合度达30%~50%用于转染。用灭菌的无酶水稀释上述各种转染质粒干粉,按说明配制成20 μmol·L-1的溶液备用。用不含血清的Opti-MEM培养液分别稀释100 pmol转染质粒与5 μL的Lipofectamine 2000,混匀,室温孵育5 min。将MGC803细胞分为转染scramble对照组、scramble+DADS组、转染miR-22 mimics组与miR-22 mimics+DADS组,转染培养48 h,收获细胞。
1.3 MTT实验用胰酶消化上述各组细胞,吹打成单细胞悬液并收集离心。取200 μL的5×103个细胞接种于96孔板中,设复孔6个。未接种细胞的孔中加入RPMI 1640培养液作调零孔。于37℃、5% CO2细胞培养箱中培养24~48 h,细胞汇合度达90%。接种细胞的孔中加入灭菌MTT液20 μL,继续孵育4 h。取出培养板,吸弃上清液,加入150 μL DMSO溶液,低速振荡10 min,使结晶物溶解。选择570 nm波长,酶标仪测定各孔吸光度值,记录结果,实验重复3次。
1.4 划痕实验将上述细胞接种于6孔板中,RPMI 1640培养基37℃、5% CO2培养,直至形成单层细胞,每组3个平行样本。吸弃上层培养液,PBS缓冲液洗涤2次,用无菌10 μL Eppendorf Tip在细胞板上划痕,无血清培养液洗3次,加入新鲜无血清培养基。倒置显微镜下观察、测量划痕区相对距离。实验重复3次。
1.5 侵袭实验将基质胶稀释液铺置在transwell小室中制成膜。加无血清RPMI 1640培养液100 μL至transwell小室的上腔,水化基质胶20 min。取100 μL上述各组细胞稀释液接种至小室上腔,下腔中加入含10%胎牛血清的RPMI 1640培养液500 μL。37℃、5% CO2的培养箱中培养48 h,取出transwell小室,用棉签擦弃小室上层细胞,PBS液洗3遍。4%多聚甲醛固定10 min,0.1%结晶紫染色20 min,PBS液清洗,晾干。光镜下观察并随机选取4个高倍视野进行细胞计数,取平均值。实验重复3次。
1.6 miR-22的靶基因验证 1.6.1 通过在线预测软件(Targetscan and Miranda)寻找miR-22调控的靶基因 1.6.2 荧光素酶报告基因检测根据Wnt-1基因3′-UTR序列与miR-22结合位点,设计合成引物序列,Wnt-1-wt:F: 5′-CCGCTCGAGCCCTCCCCCAAAC-3′, R: 5′-GAATGCGGCCGCCTGGGAGTGGTAAAAGG GGAGGAT-3′;Wnt-1-mut:F: 5′-CCGCTCCTCCAAGCC ATTC-3′, R: 5′-ATGCCGACTTGGCCGAAT-3′。相应的上、下引物一起退火完成后,将其连接到含有荧光素酶报告基因的载体质粒上。将MGC-803细胞培养于12孔培养板,细胞分为转染miR-22 mimics与Wnt-1-wt组、转染scramble与Wnt-1-wt组、转染miR-22 mimics与Wnt-1-mut组和转染scramble与Wnt-1-mut组,48 h后收获细胞。按照Promega公司双荧光素酶活性检测试剂盒操作说明书,在单光子检测仪检测细胞荧光素酶的活性,计算相对荧光素酶活性=荧光素酶活性值/海肾荧光素酶活性。实验独立重复3次。
1.7 qRT-PCR检测收集上述各组细胞,采用RNA抽提试剂盒抽提细胞总RNA,逆转录合成cDNA。设计合成PCR引物序列:Wnt-1:F: 5′-TGGCTGGGTTTCTGCTACG-3′,R: 5′-CCCGGATTTTGGCGTATC-3′;GAPDH:F: 5′-GCTGAGAACGGGAAGCT TGT-3′, R: 5′-GCCAGGGGTGCTAAGCAG-3′。PCR扩增反应体系为20 μL,包括PCR primers(5 mmol·L-1)0.4 μL、RT product 2.0 μL、Taq DNA polymerase(5 U·μL-1)0.2 μL、2×SYBR Mix 10 μL、灭菌蒸馏水7.4 μL。反应条件:95 ℃ 3 min、95 ℃ 12 s、62 ℃ 35 s、72 ℃ 30 s,共40个循环。以GAPDH为内参,采用2-ΔΔCT法计算Wnt-1 mRNA相对表达量。
1.8 Western blot检测收集上述各组细胞,提取细胞总蛋白,BCA法测定蛋白浓度,每组取等量样本进行SDS-PAGE凝胶电泳,电泳后转膜,封闭1 h,加一抗,4 ℃过夜,TBST洗膜,加二抗,孵育1 h,洗膜,ECL发光,X线曝光、显影、定影。
1.9 统计学处理采用SPSS 16.0软件进行统计学分析。所有结果均以x±s表示。两组间比较用t检验,多组间比较用单因素方差分析。
2 结果 2.1 DADS和miR-22对MGC803细胞增殖的影响将miR-22 mimics转染于MGC803细胞中,转染miRNA的无关序列scramble作为对照,并用30 mg·L-1 DADS分别处理。Tab 1 MTT结果显示,48、72、96 h后,DADS与miR-22高表达均可明显抑制MGC803细胞增殖(P < 0.05)。表明DADS与miR-22能明显抑制MGC803细胞增殖,且miR-22可增强DADS的作用。
| Time/h | Control | DADS | miR-22 | miR-22+DADS |
| 24 | 0.469±0.125 | 0.401±0.926 | 0.378±1.461 | 0.337±0.947 |
| 48 | 0.640±0.042 | 0.463±0.528* | 0.417±0.830* | 0.324±0.412* |
| 72 | 0.819±0.061 | 0.524±0.015* | 0.465±0.524* | 0.382±0.058* |
| 96 | 1.024±0.103 | 0.568±0.053* | 0.540±0.072* | 0.407±0.046* |
| *P < 0.05 vs control group | ||||
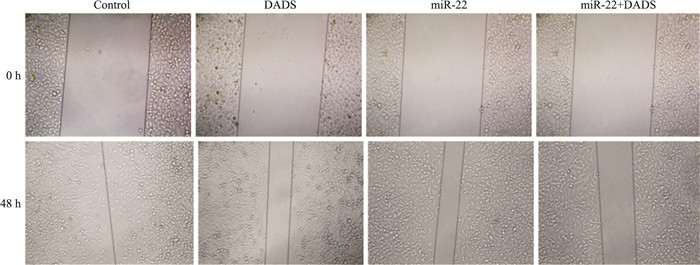
Fig 1显示,48 h后,DADS处理组、miR-22组与miR-22+DADS组伤口愈合率分别为(60.17±2.22)%、(61.57±1.54)%与(49.85±1.98)%,较对照组(91.94±2.01)%明显减缓(P < 0.01)。表明DADS与miR-22能明显抑制MGC803细胞的迁移能力,miR-22可增强DADS的抑制作用。
|
| Fig 1 Effect of DADS and miR-22 on migration of MGC803 cells(×20) |
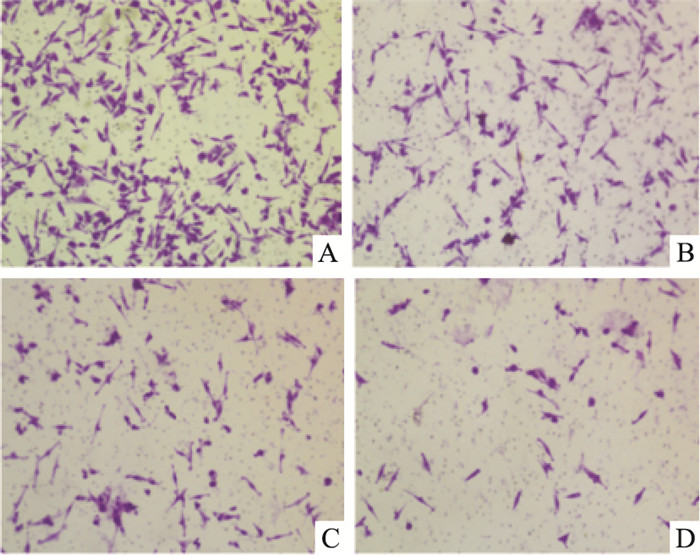
Fig 2显示,48 h后,DADS处理组、miR-22组与miR-2+DADS组穿过基质胶的细胞数分别为(137±11)、(120±9) 与(70±10),较对照组(253±16) 明显减少(P < 0.01)。表明DADS与miR-22高表达能明显抑制MGC-803细胞的侵袭能力,且miR-22可增强DADS的抑制作用。
|
| Fig 2 Effect of DADS and miR-22 on invasion in MGC803 cells(×10) A:Control; B:DADS; C:miR-22;D:miR-22+DADS |
为进一步明确miR-22调控胃癌生物学行为的作用机制,运用生物信息学方法,通过在线预测软件(Targetscan and Miranda)寻找miR-22相关蛋白编码的靶基因。经在线软件交叉预测后,发现miR-22有500多个靶基因,miR-22具有Wnt-1的3′UTR的结合位点,Wnt-1可能是miR-22的靶基因(Fig 3)。

|
| Fig 3 Putative binding sites of miR-22 and 3′UTRs of Wnt-1 |
因为证实miR-22作用预测的结合位点导致荧光素酶活性发生改变,设计Wnt-1 3′UTR缺失的miR-22结合位点的突变序列和野生序列插入报告质粒中。胃癌MGC803细胞分别转染miR-22 mimics、Wt-miR-22/Wnt-1和Mut-miR-22/Wnt-1重组质粒。荧光素酶报告基因检测发现(Tab 2),Mut-miR-22/Wnt-1荧光素酶活性为(1.033±0.128),较对照组(1.075±0.062) 差异无统计学意义(P>0.05)。但Wt-miR-22/Wnt-1荧光素酶活性为(0.522±0.318),较对照组(1.081±0.984) 明显下降(P < 0.05)。表明Wnt-1是miR-22直接的靶基因。
| Group | Relative luciferase activity | |
| Wnt-1 wt | scramble | 1.081±0.984 |
| miR-22 | 0.522±0.318* | |
| Wnt-1 mut | scramble | 1.075±0.062 |
| miR-22 | 1.033±0.128 | |
| *P < 0.05 vs scramble group | ||
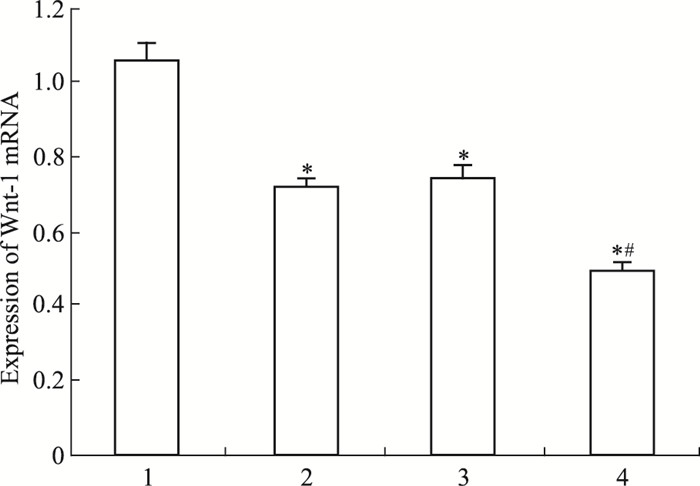
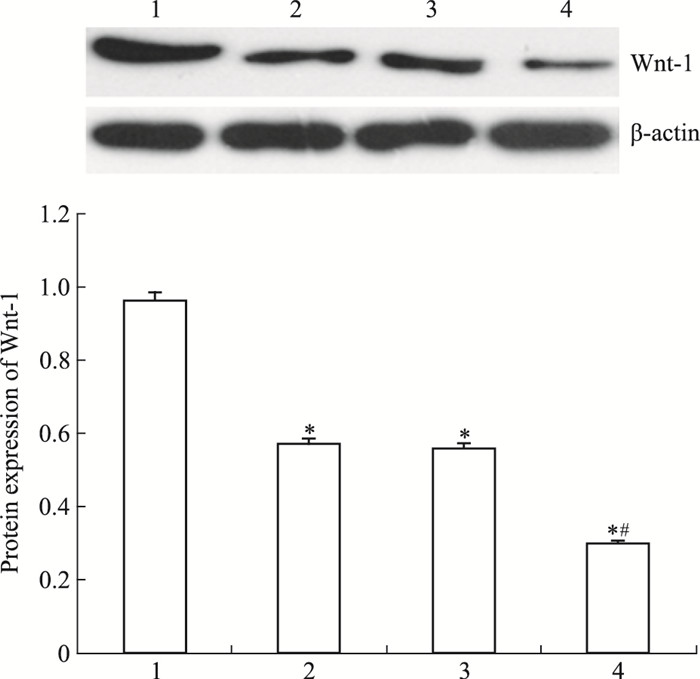
Fig 4 qRT-PCR结果显示,DADS组和miR-22组Wnt-1 mRNA的表达水平2-△△CT分别为(0.721±0.034) 与(0.745±0.038) 较对照组2-△△CT(1.066±0.714) 明显下降,并以miR-22+DADS组2-△△CT(0.495±0.029) 下降尤为明显(P < 0.05)。Fig 5 Western blot结果显示,DADS处理与miR-22高表达的MGC803细胞Wnt-1蛋白表达水平较对照组分别下调31.84%与28.77%,并且,miR-22+DADS下调尤为明显(48.9%)(P < 0.05)。
|
| Fig 4 Effect of DADS and miR-22 on Wnt-1 mRNA expression in MGC803 cells 1:Scramble; 2:Scramble+DADS; 3:miR-22;4:miR-22+DADS. *P < 0.05 vs scramble; #P < 0.05 vs miR-22. |
|
| Fig 5 Effect of DADS and miR-22 on Wnt-1 protein expression in MGC803 cells 1: Scramble; 2: Scramble+DADS; 3: miR-22; 4: miR-22+DADS. *P < 0.05 vs scramble; #P < 0.05 vs miR-22. |
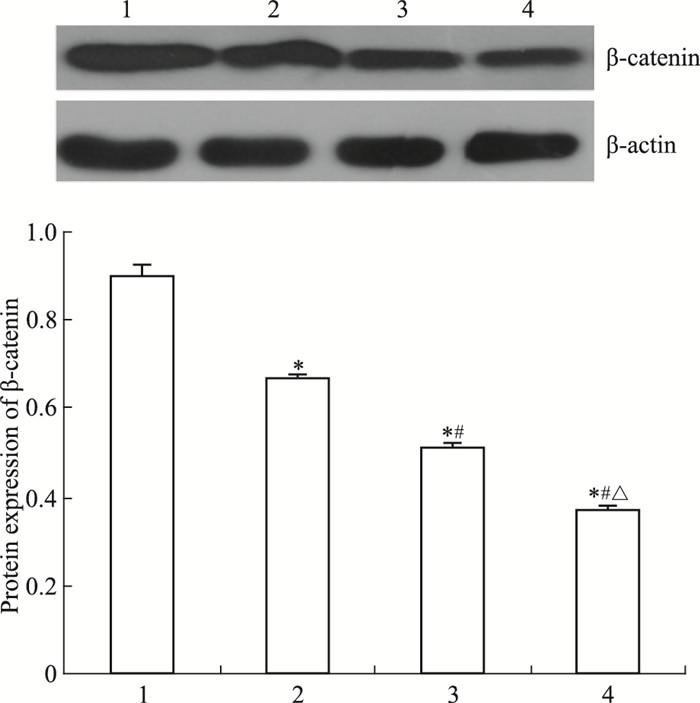
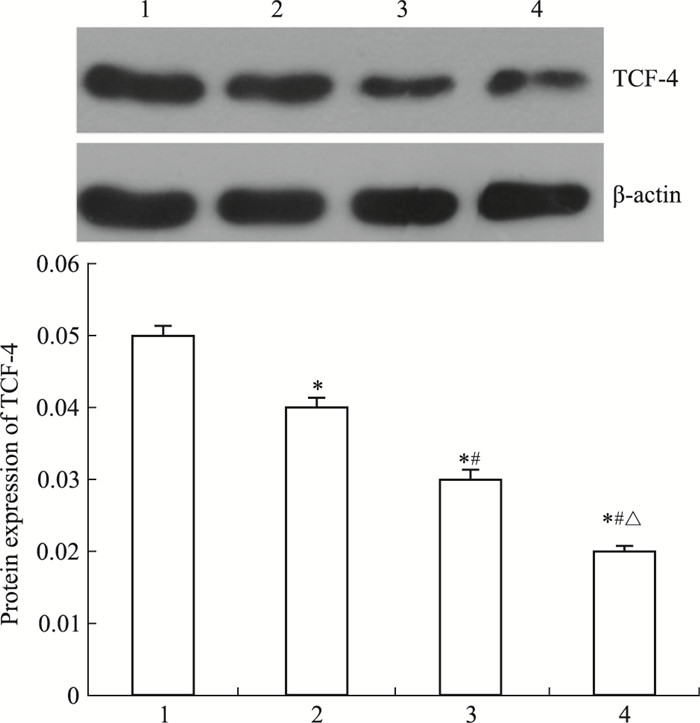
Western blot结果显示(Fig 6、7),DADS处理与miR-22高表达的MGC803细胞β-catenin与TCF-4蛋白表达水平较对照组分别下调,且miR-22+DADS下调尤为明显(P < 0.05)。表明DADS上调miR-22通过Wnt-1信号下调β-catenin与TCF-4。
|
| Fig 6 Effect of DADS and miR-22 on β-catenin protein expression in MGC803 cells 1: Scramble; 2: Scramble+DADS; 3: miR-22; 4: miR-22+DADS. *P < 0.05 vs scramble; #P < 0.05 vs miR-22;△P < 0.05 vs DADS. |
|
| Fig 7 Effect of DADS and miR-22 on TCF-4 protein expression in MGC803 cells 1: Scramble; 2: Scramble+DADS; 3: miR-22; 4: miR-22+DADS. *P < 0.05 vs scramble; #P < 0.05 vs miR-22;△P < 0.05 vs DADS. |
研究证实,miRNA在肿瘤中通过调控抑癌基因或癌基因的表达,表现为类似癌基因或抑癌基因样作用[8]。大量研究表明,miR-22在多种肿瘤中表达下调,可抑制肿瘤细胞迁移侵袭,表现为抑癌基因,其作用机制与靶向调控多种靶基因有关[9-19]。研究显示,miR-22通过靶向TIAM1抑制结肠癌HCT-116细胞增殖与迁移侵袭[9]。ATP citrate lyase(ACLY)在肺癌、前列腺癌、子宫颈癌、骨肉瘤等中表达上调,而miR-22表达下调,ACLY与miR-22表达呈负相关,且miR-22可直接靶向转录后调控ACLY抑制肿瘤生存与转移[10]。miR-22在胃癌中表达较正常组织明显下调,与淋巴结转移、远距离转移、临床分期和患者生存率下降有关。而miR-22高表达可通过靶向Sp1或MMP-14、Snail,抑制胃癌细胞迁移与侵袭[11-13]。Xu等[14]研究显示,miR-22通过靶向CDK6、MDM2、LEF1、MYB、FOS等基因在卵巢癌细胞迁移与侵袭中起着重要作用。miR-22在肾细胞癌表达下调与组织学类型、肿瘤分期和淋巴结转移有关,其通过直接靶向SIRT1,抑制肾细胞癌细胞增殖与迁移侵袭。miR-22高表达体外可抑制肾细胞癌细胞增殖、迁移侵袭与诱导凋亡,体内可抑制移植瘤生长。可活化p53及其下游靶点p21与PUMA,裂解CASP3与PARP,抑制EMT[15]。
众所周知,Wnt信号通路在肿瘤发生与侵袭转移中起着重要作用。当胞外Wnt蛋白增加时,Wnt与Frizzled结合,激活Dsh/Dvl蛋白,抑制GSK3β/APC/Axin复合物对β-catenin的降解,而促进β-catenin入核,与转录因子Tcf/Lef结合,引起靶基因的转录,导致肿瘤发生。研究发现,Wnt信号通路与miRNAs之间存在交叉对话,miRNA可调控Wnt信号通路,如miR-122、miR-148a、miR-22、miR-200b、miR-185-3p、miR-324-3p、miR-26a、miR-487b、miR-329、miR-410、miR-374b等可靶向抑制Wnt通路[16]。Liang等[17]研究显示,miR-22可负调控Wnt/β-catenin信号通路,抑制β-catenin表达。近年来,研发天然植物有效成分防治肿瘤已成为新策略。研究表明,miR-22在肿瘤发生发展中可抑制肿瘤干细胞(CSC)表型与功能。姜黄素、大豆异黄酮、茶多酚、白藜芦醇、维生素D等天然植物有效因子通过靶向CSC相关基因,上调miR-22,抑制肿瘤增殖、迁移、侵袭与转移[18]。我们研究显示,DADS可上调miR-22靶向Wnt-1通路,抑制人胃癌细胞增殖与诱导凋亡[7]。
我们前期工作证明,DADS可体内外抑制MGC803细胞的增殖,其机制与激活p38与抑制ERK通路,调节ATR/Chk1/Cdc25C/cyclin B1,上调组蛋白乙酰化与p21,G2/M阻滞等有关。并且,DADS可通过Rac1-Pak1/Rock1通路下调LIMK1、MMP-9,上调TIMP-3,抑制人胃癌细胞EMT与侵袭[19-22]。
本研究在前期研究的基础上,进一步确定DADS上调miR-22是否通过Wnt-1通路抑制MGC803细胞迁移与侵袭。结果表明,DADS与miR-22均可明显抑制MGC803细胞增殖。DADS处理组、miR-22组与miR-2+DADS组迁移能力较对照组明显降低,并且穿过基质胶的细胞数较对照组明显减少,表明DADS与miR-22能明显抑制MGC-803细胞的迁移侵袭能力,且miR-22可增强DADS的抑制作用。靶基因预测发现,miR-22具有Wnt-1的3′UTR的结合位点,Wnt-1可能是miR-22的靶基因。荧光素酶报告基因检测显示,Mut-miR-22/Wnt-1荧光素酶活性较对照组差异无显著性,而Wt-miR-22/Wnt-1荧光素酶活性较对照组明显下降,确定Wnt-1是miR-22直接的靶基因。qRT-PCR验证显示,DADS组和miR-22组Wnt-1 mRNA表达较对照组明显下降,并以miR-22+DADS组更为明显。Western blot显示,DADS组与miR-22组Wnt-1蛋白表达较对照组明显下调,并且miR-22+DADS下调尤为明显。另外,DADS组与miR-22组β-catenin与TCF-4蛋白表达较对照组明显下调,且miR-22+ DADS下调尤为明显。上述结果证明,DADS可上调miR-22,通过Wnt-1通路下调β-catenin与TCF-4,抑制人胃癌细胞增殖与迁移侵袭。
| [1] | Torre L A, Bray F, Siegel R L, et al. Global cancer statistics, 2012[J]. CA Cancer J Clin, 2015, 65(2): 87-108. doi:10.3322/caac.21262 |
| [2] | Chen W, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-32. doi:10.3322/caac.21338 |
| [3] | Orditura M, Galizia G, Sforza V, et al. Treatment of gastric cancer[J]. World J Gastroenterol, 2014, 20(7): 1635-49. doi:10.3748/wjg.v20.i7.1635 |
| [4] | 唐云云, 唐海林, 苏琦. MicroRNAs在胃癌中的生物学作用[J]. 中国肿瘤临床, 2014, 41(2): 131-3. Tang Y Y, Tang H L, Su Q. Biological role of microRNAs in gastric cancer[J]. Chin J Clin Oncol, 2014, 41(2): 131-3. |
| [5] | Yi L, Su Q. Molecular mechanisms for the anti-cancer effects of diallyl disulfide[J]. Food Chem Toxicol, 2013, 57: 362-70. doi:10.1016/j.fct.2013.04.001 |
| [6] | Tang Y Y, Liu X P, Su B, et al. microRNA-22 acts as a metastasis suppressor by targeting metadherin in gastric cancer[J]. Mol Med Rep, 2015, 11(1): 454-60. |
| [7] | Tang H, Kong Y, Guo J, et al. Diallyl disulfide suppresses proliferation and induces apoptosis in human gastric cancer through Wnt-1 signaling pathway by up-regulation of miR-200b and miR-22[J]. Cancer Lett, 2013, 340(1): 72-81. doi:10.1016/j.canlet.2013.06.027 |
| [8] | Cheng C J, Slack F J. The duality of oncomiR addiction in the maintenance and treatment of cancer[J]. Cancer J, 2012, 18(3): 232-7. doi:10.1097/PPO.0b013e318258b75b |
| [9] | Li B, Song Y, Liu T J, et al. miRNA-22 suppresses colon cancer cell migration and invasion by inhibiting the expression of T-cell lymphoma invasion and metastasis 1 and matrix metalloproteinases 2 and 9[J]. Oncol Rep, 2013, 29(5): 1932-8. |
| [10] | Xin M, Qiao Z, Li J, et al. miR-22 inhibits tumor growth and metastasis by targeting ATP citrate lyase: evidence in osteosarcoma, prostate cancer, cervical cancer and lung cancer[J]. Oncotarget, 2016, 7(28): 44252-65. |
| [11] | Wang W, Li F, Zhang Y, et al. Reduced expression of miR-22 in gastric cancer is related to clinicopathologic characteristics or patient prognosis[J]. Diagn Pathol, 2013, 8: 102. |
| [12] | Guo M M, Hu L H, Wang Y Q, et al. miR-22 is down-regulated in gastric cancer, and its overexpression inhibits cell migration and invasion via targeting transcription factor Sp1[J]. Med Oncol, 2013, 30(2): 542. doi:10.1007/s12032-013-0542-7 |
| [13] | Zuo Q F, Cao L Y, Yu T, et al. MicroRNA-22 inhibits tumor growth and metastasis in gastric cancer by directly targeting MMP14 and Snail[J]. Cell Death Dis, 2015, 6: e2000. doi:10.1038/cddis.2015.297 |
| [14] | Xu B, Zhao H, Xu C. Gene expression profiling analysis of the role of miR-22 in clear cell ovarian cancer[J]. Neoplasma, 2016, 63(6): 856-64. doi:10.4149/neo_2016_604 |
| [15] | Zhang S, Zhang D, Yi C, et al. MicroRNA-22 functions as a tumor suppressor by targeting SIRT1 in renal cell carcinoma[J]. Oncol Rep, 2016, 35(1): 559-67. |
| [16] | Peng Y, Zhang X, Feng X, et al. The crosstalk between microRNAs and the Wnt/β-catenin signaling pathway in cancer[J]. Oncotarget, 2017, 8(8): 14089-106. |
| [17] | Liang W C, Fu W M, Wang Y B, et al. H19 activates Wnt signaling and promotes osteoblast differentiation by functioning as a competing endogenous RNA[J]. Sci Rep, 2016, 6: 20121. doi:10.1038/srep20121 |
| [18] | Bao B, Li Y, Ahmad A, et al. Targeting CSC-related miRNAs for cancer therapy by natural agents[J]. Curr Drug Targets, 2012, 13(14): 1858-68. doi:10.2174/138945012804545515 |
| [19] | Su B, Xiang S L, Su J, et al. Diallyl disulfide increased histone acetylation and p21WAF1 expression in human gastric cancer cells in vivo and in vitro[J]. Biochem Pharmacol, 2012, 1(7): 1-10. |
| [20] | Su B, He H, Wang L, et al. Chk1, but not Chk2, is responsible for G2/M phase arrest induced by diallyl disulfide in human gastric cancer BGC823 cells[J]. Food Chem Toxicol, 2014, 68: 61-70. doi:10.1016/j.fct.2014.03.007 |
| [21] | 夏红, 向姝霖, 曾颖, 等. DADS对Chk1/2基因高表达人胃癌MGC803细胞G2/M期的影响[J]. 中国药理学通报, 2016, 32(2): 199-204. Xia H, Xiang S L, Zeng Y, et al. Overexpression of Chk1/2 gene to affect the G2/M arrest in MGC803 Cells induced by diallyl disulfide[J]. Chin Pharmacol Bul, 2016, 32(2): 199-204. |
| [22] | Su B, Su J, Zeng Y, et al. Diallyl disulfide suppresses epithelial-mesenchymal transition, invasion and proliferation by downregulation of LIMK1 in gastric cancer[J]. Oncotarget, 2016, 7(9): 10498-512. |

