


胶原三螺旋重复蛋白-1(collagen triple helix repeat containing-1, CTHRC1) 基因是在动脉损伤过程中筛选出的一种过表达基因。CTHRC1蛋白是具有血管损伤修复作用的分泌型蛋白,可减少胶原沉积、促进细胞迁移、参与组织重塑、影响血管和骨形成。近年来发现,CTHRC1在肿瘤和自身免疫性疾病中都有异常表达。CTHRC1通过促进细胞迁移、血管形成参与肿瘤病理进程,通过促进成纤维样滑膜细胞迁移和血管形成而参与类风湿性关节炎(rheumatoid arthritis, RA)血管翳形成。CTHRC1主要通过Wnt信号通路发挥其生理和病理作用。本文就CTHRC1结构、生物学功能以及参与肿瘤和RA病理过程等近年来研究进展进行综述。
1 胶原三螺旋重复蛋白-1结构特性胶原三螺旋重复蛋白-1(collagen triple helix repeat containing-1, CTHRC1) 是一种具有血管损伤修复作用的分泌型蛋白,因参与组织重塑、影响血管和骨形成而被人所熟知。非还原条件下,分泌型CTHRC1主要以二聚体(56 ku)和三聚体(84 ku)及多聚体(168 ku和252 ku)3种形式存在。膜型CTHRC1主要是二聚体和三聚体。还原条件下,由于翻译后修饰的不同,分泌型和膜型CTHRC1分子质量分别为30 ku和26 ku。CTHRC1存在4种不同的亚型,分子量约为26 ku(全长)、12.3 ku(变体2)、24.8 ku(变体3) 和16 ku(变体4)。与全长蛋白相比,变异体3包含一个交替的5′外显子和转录起始位点,但是缺乏用于细胞外分泌的信号序列[1]。CTHRC1在脊椎动物上高度保守,在结构上包含类似于C1q/肿瘤坏死因子α相关蛋白中的短胶原样基序[2]。
2 CTHRC1生物学功能CTHRC1是血管重构、成骨细胞形成以及创伤修复的调节器。CTHRC1在损伤动脉表达且通过促进细胞迁移参与血管损伤外膜重构,并且抑制成纤维样细胞和平滑肌细胞胶原合成[3]。CTHRC1受转化生长因子β(transforming growth factor, TGF-β)家族成员调控,仅限于受伤外膜和内膜表达,且在损伤动脉有短暂表达[4-5]。CTHRC1通过与TGF-β信号通路的相互作用参与胶原调节,损伤后的血管重塑在很大程度上由TGF-β调控,CTHRC1通过抑制TGF-β介导的Smad2/3信号通路活化,而减少胶原沉积[2, 4]。在血管疾病、修复和纤维化病程中具有重要作用[2]。在损伤动脉和皮肤伤口,CTHRC1能降低I型胶原mRNA和蛋白质表达,调节肌成纤维细胞迁移和胶原基质沉积[4, 6-7]。另外,CTHRC1蛋白在软骨和骨等多种胚胎和新生儿组织中表达。基因缺陷型和转基因小鼠实验证实CTHRC1在成骨细胞及骨形成中发挥关键调节作用[8]。
3 CTHRC1参与肿瘤的病理过程CTHRC1涉及多种病理过程,如组织损伤和肿瘤发生等。CTHRC1支持损伤组织的修复与重构,与肿瘤发生有着紧密联系[5]。近年来,越来越多的证据表明,CTHRC1广泛高表达在人类肿瘤基质细胞中[8],并且在肿瘤的发生中扮演重要角色。涉及的肿瘤包括黑色素瘤、肝细胞癌、乳腺导管癌、结肠癌、食道癌、非小细胞肺癌、胃癌、卵巢上皮性癌和胰腺癌等[9]。
3.1 CTHRC1促进肿瘤细胞的侵袭和转移CTHRC1通过增加肿瘤细胞的迁移参与肿瘤病程进展[5]。抑制CTHRC1的表达则导致肿瘤细胞迁移率明显降低。胰腺癌中,CTHRC1高度表达,调节肿瘤细胞迁移和粘附,参与胰腺癌的发生和转移。CTHRC1蛋白下调,则肿瘤细胞活性减弱[1]。CTHRC1的上调导致下游几个关键信号分子活化,包括非受体酪氨酸激酶(Src)、粘着斑激酶(focal adhesion kinase, FAK)、桩蛋白(paxillin)、丝裂原活化蛋白激酶(mitogen activated protein kinase, MAPK)、细胞外信号调节激酶(extracellular signal regulated kinase, ERK)、Rac(Ras相关的C3肉毒素底物)等[10]。CTHRC1与胰腺导管癌患者生存密切相关,提示CTHRC1可能是胰腺导管癌有意义的预后标志及潜在的治疗靶点[9]。
CTHRC1也参与非小细胞肺癌的侵袭转移。MiR-30b通过调节CTHRC1从而影响非小细胞肺癌细胞侵袭和迁移。非小细胞肺癌组织中MiR-30b下调以及CTHRC1 mRNA表达升高与肿瘤分化程度、临床分期和淋巴结转移相关[11]。CTHRC1mRNA在乳腺癌中表达也是增加的,其蛋白水平的过表达与乳腺癌患者淋巴结转移和临床病理分期也明显相关。免疫组化显示CTHRC1不仅在基质中表达而且表达在肿瘤细胞的细胞质和(或)细胞膜。分泌型CTHRC1通过改变肿瘤微环境中间质细胞外基质结构成分可以促进肿瘤进程和淋巴结转移。CTHRC1的过表达是浸润性导管癌预后不良的重要病理因素,因此CTHRC1可能也是乳腺癌预后的生物标志物和潜在治疗靶点[5]。在胃癌中CTHRC1是一个潜在的转移相关基因。胃癌肿瘤组织中CTHRC1表达明显增加,其过表达与肿瘤浸润程度有关。体外,CTHRC1促进肿瘤细胞侵袭,提示CTHRC1存在异位表达。胃癌细胞系用去甲基化药物(5-氮-2′-脱氧胞苷)处理后,CTHRC1表达上调。TGF-β1促进CTHRC1mRNA和蛋白水平表达。CTHRC1启动子甲基化和TGF-β1可能联合调控CTHRC1的表达[12]。CTHRC1在肝癌细胞中表达上调同时促进细胞增殖、迁移和侵袭。相较于正常或肝硬化组织,CTHRC1在肝癌中是高表达的,并且被认为是一个新的肝癌相关基因。免疫组化显示,相比高分化的肝细胞癌,在低分化肝细胞癌中和肝癌侵袭部位CTHRC1表达更明显。沉默CTHRC1可降低肝癌细胞迁移和侵袭能力[13]。
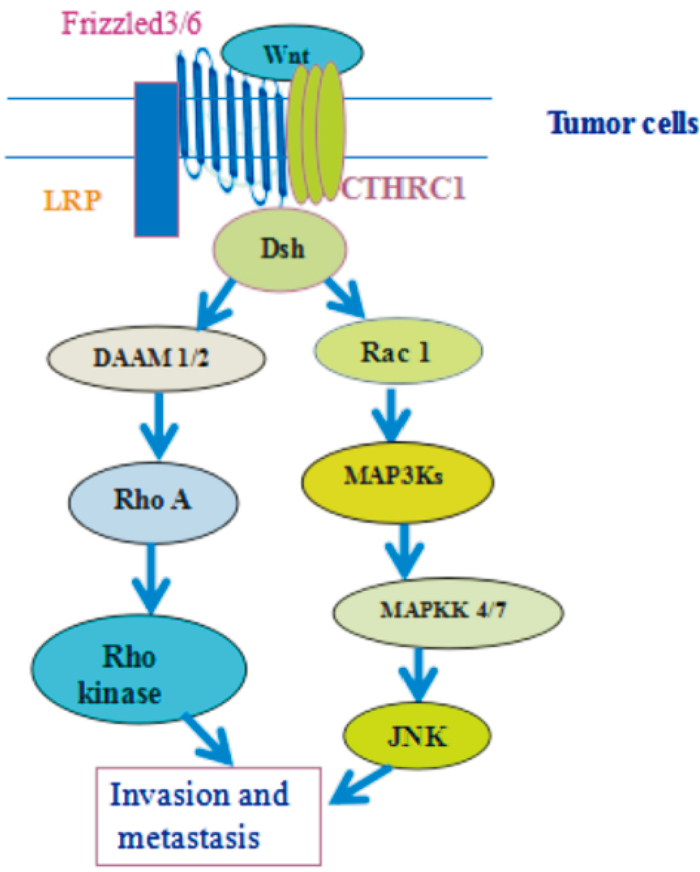
3.2 CTHRC1激活Wnt/PCP信号通路参与肿瘤细胞侵袭和转移CTHRC1通过激活Wnt/平面细胞极性(planar cell polarity, PCP)通路调节肿瘤细胞的侵袭和迁移[10]。Wnt蛋白是结合细胞表面上Fz受体的糖蛋白,具有重要的生物学功能,可参与细胞分化、胚胎发育、肢体发育和关节形成。CTHRC1激活Wnt / PCP Rho信号促进胃肠道间质瘤(gastrointestinal stromal tumor, GIST)细胞迁移和侵袭。在GIST中,重组CTHRC1蛋白激活Wnt/PCP Rho信号通路。Wnt/PCP信号通路的下游分子主要包括小GTP酶家族,如Rac1、RhoA和Cdc42。这些GTP酶在癌细胞迁移和侵袭中起重要作用。重组CTHRC1蛋白增强RhoA和Rac1的活性,但不增加Cdc42活性。CTHRC1对GIST肿瘤细胞运动具有促进作用,其促进作用可被Wnt/PCP信号通路下游关键分子ROCK和Rac1抑制剂所阻断。此外,重组CTHRC1可以提高Wnt5a磷酸化以及Wnt / PCP途径的另一下游分子c-Jun N末端激酶(N c-Jun terminal kinase, JNK)的磷酸化,表明CTHRC1可能通过Wnt/PCP-Rho-JNK通路促进GIST细胞侵袭(Fig 1)。Wnt5a中和抗体、Rac1或ROCK抑制剂可以逆转CTHRC1对GIST肿瘤细胞的促运动效应。因此,CTHRC1可作为GIST患者术后复发及预后的预测,CTHRC1 Wnt/PCP Rho轴可能是对GIST浸润和转移的干预治疗的新靶点[14]。
|
| Fig 1 CTHRC1 initiates Wnt-PCP signaling pathway in tumor cells In tumor cells, CTHRC1 acts as a helper receptor for Wnt receptors(Frizzled, Fz), and Wnt binds to CTHRC1 and Fz, which leads to the activation of Dishevelled(Dsh). Activated Dsh initiates two signaling pathways, namely DAAM1/2-RhoA-Rho kinase signal pathway and Rac 1 MAP3Ks-MAPKK4/7-JNK signaling pathway, and thus these signaling pathways promote the invasion and metastasis of tumor cells in further |
结肠上皮细胞和基质成纤维细胞是CTHRC1在结直肠癌(colorectal cancer, CRC)微环境的来源。CTHRC1也能促进CRC细胞迁移、侵袭和增殖。CTHRC1促进CRC细胞迁移和侵袭,可能是通过激活Wnt/PCP通路[18]。Wnt/PCP通路通过激活RHOA、JNK和nemo样激酶(nemo like kinase, NLK)信号级联调控细胞极性和运动[15]。
4 CTHRC1参与类风湿性关节炎慢性滑膜炎病理过程类风湿性关节炎(rheumatoid arthritis, RA)是一种T、B淋巴细胞参与的,以慢性滑膜炎、软骨和骨的破坏为病理特征的自身免疫性疾病[16-17],最终导致关节功能受损[18]。RA增生的滑膜组织伴有血管翳形成,成纤维样滑膜细胞(fibroblast-like synoviocytes, FLS)是侵袭性滑膜的关键组成部分,并在血管翳形成、关节破坏的发生和发展中起重要作用[19]。
4.1 CTHRC1参与FLS活化,促进骨和软骨侵蚀及血管翳的形成CTHRC1通过促进FLS迁移参与RA滑膜组织重塑。RA滑膜组织FLS增殖与细胞凋亡之间的失平衡导致增生性滑膜炎[20]。FLS中诱导性表达CTHRC1,CTHRC1mRNA表达与小鼠关节炎的严重程度相关。在滑膜血管翳部位可检测到CTHRC1表达[8]。在胶原抗体诱导的关节炎(collagen antibody-induced arthritis,CAIA)滑膜组织中发现CTHRC1mRNA高度表达[8]。CTHRC1增加了血管内皮细胞运动,促进细胞进入炎症滑膜组织,参与血管翳形成。CTHRC1还能够促进血管平滑肌细胞迁移,血管平滑细胞迁移、增殖和基质沉积是血管重构的关键因素[2]。CTHRC1通过两种方式调节RA患者FLS运动:直接作用和运动速度。直接作用显示在板状伪足的前缘CTHRC1通过招募潜在的CTHRC1传感器/受体诱导细胞多极化。CTHRC1的这种作用可能与WNT信号转导受体重新分布和细胞多极化相关。运动速度的影响不同于直接作用。速度效应涉及粘着斑形成/分解和应力纤维的调节,这与CTHRC1对FAK和RhoA的调节一致[8]。这些研究提示CTHRC1通过活化FLS促进骨和软骨侵蚀及血管翳形成。因此,CTHRC1可能是RA中FLS活化的一个新标志物[8]。
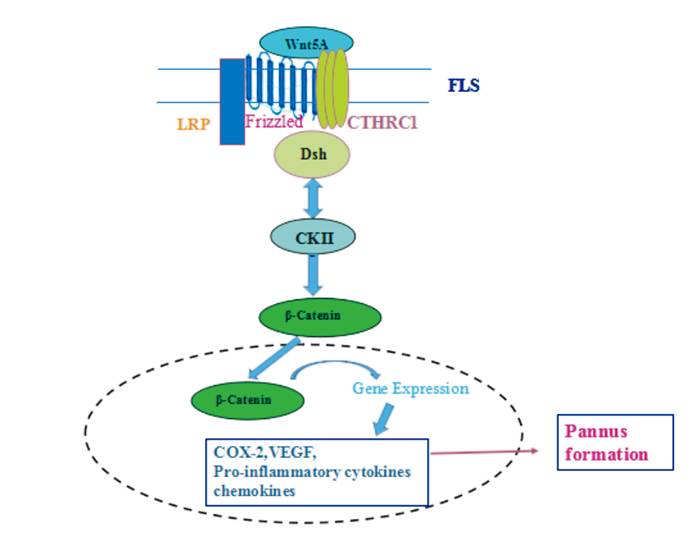
4.2 CTHRC1激活Wnt/β-catenin信号通路参与RA病程CTHRC1激活经典Wnt/ β-连环蛋白(β-catenin)信号通路参与RA滑膜炎病程中FLS活化、骨吸收和关节破坏。RA患者FLS中,β-catenin表达上调,明显高于骨关节炎。β-catenin是经典Wnt信号通路激活的关键调节因子,是介导细胞-细胞粘附连接中的β-catenin/E-钙黏蛋白复合物的主要组分。活化的β-catenin信号有助于FLS的稳定活化。RA中Wnt5A介导的信号促进促炎细胞因子、趋化因子和其它炎性因子产生,诱导环氧合酶-2(COX-2) 表达。此外,Wnt5A介导的信号通路还可以通过上调血管内皮细胞生长因子(vascular endothelial growth factor, VEGF)的表达来促进滑膜的血管生成[21](Fig 2)。Wnt信号通路抑制剂DKK1(dickkopf1) 是RA中成骨细胞-破骨细胞平衡的主要调节剂。RA成骨细胞中,DKK1通过与Wnt共受体-低密度脂蛋白受体相关蛋白5(low density lipoprotein receptor related protein 5, LRP5) 结合而抑制Wnt信号通路活化。提示不同类型的组织或细胞(如FLS和成骨细胞)中Wnt信号存在不同激活状态[21]。
|
| Fig 2 CTHRC1 initiates Wnt-β-catenin signaling pathway in synovial cells In synovial cells, CTHRC1 acts as a helper receptor for Wnt receptor (Frizzled, Fz), and Wnt binds to CTHRC1 and Fz, which leads to activation of Dishevelled (Dsh). Activated Dsh activates CKⅡ (calcium-sensitive enzyme calmodulin kinase Ⅱ, CamKⅡ). CKⅡ promotes the degradation of multi protein complex of β-catenin, and β-catenin is released. Then β-catenin enters into cell nucleu and induces the expression of some genes, including pro-inflammatory cytokines, chemokines, COX-2 and VEGF, which promotes the formation of pannus. |
总之,CTHRC1参与血管重塑、骨形成和发展以及细胞迁移和胶原沉积等生理病理过程。CTHRC1在肿瘤中的作用已经在国内外获得大量研究,在许多肿瘤中高度表达,通过促进肿瘤细胞迁移和侵袭参与肿瘤的发生、发展和血管形成。同时CTHRC1在RA中也参与FLS活化、骨破坏及血管翳形成。CTHRC1通过介导Wnt信号通路发挥其在肿瘤和炎症反应中重要作用。因此,阐明CTHRC1在肿瘤和炎症反应中的重要作用,对揭示肿瘤和自身免疫性疾病的病理机制、发现新的生物标志物以及药物作用新靶点具有重要意义。
| [1] | Eriksson J, Le Joncour V, Nummela P, et al. Gene expression analyses of primary melanomas reveal CTHRC1 as an important player in melanoma progression[J]. Oncotarget, 2016, 7(12): 15065-92. |
| [2] | LeClair R. The role of collagen triple helix repeat containing 1 in injured arteries, collagen expression, and transforming growth factor beta signaling[J]. Trends Cardiovasc Med, 2007, 17(6): 202-5. doi:10.1016/j.tcm.2007.05.004 |
| [3] | Lee J, Song J, Kwon E S, et al. CTHRC1 promotes angiogenesis by recruiting Tie2-expressing monocytes to pancreatic tumors[J]. Exp Mol Med, 2016, 48(9): e261. doi:10.1038/emm.2016.87 |
| [4] | LeClair R J, Durmus T, Wang Q, et al. Cthrc1 is a novel inhibitor of transforming growth factor-beta signaling and neointimal lesion formation[J]. Circ Res, 2007, 100(6): 826-33. doi:10.1161/01.RES.0000260806.99307.72 |
| [5] | Kim J H, Baek T H, Yim H S, et al. Collagen triple helix repeat containing-1(CTHRC1) expression in invasive ductal carcinoma of the breast: the impact on prognosis and correlation to clinicopathologic features[J]. Pathol Oncol Res, 2013, 19(4): 731-7. doi:10.1007/s12253-013-9636-y |
| [6] | Durmus T, LeClair R J, Park K S, et al. Expression analysis of the novel gene collagen triple helix repeat containing-1(Cthrc1)[J]. Gene Expr Patterns, 2006, 6(8): 935-40. doi:10.1016/j.modgep.2006.03.008 |
| [7] | Leclair R J, Wang Q, Benson M A, et al. Intracellular localization of Cthrc1 characterizes differentiated smooth muscle[J]. Arterioscler Thromb Vasc Biol, 2008, 28(7): 1332-8. doi:10.1161/ATVBAHA.108.166579 |
| [8] | Shekhani M T, Forde T S, Adilbayeva A, et al. Collagen triple helix repeat containing 1 is a new promigratory marker of arthritic pannus[J]. Arthritis Res Ther, 2016, 18: 171. doi:10.1186/s13075-016-1067-1 |
| [9] | Liu W, Fu X L, Yang J Y, et al. Elevated expression of CTHRC1 predicts unfavorable prognosis in patients with pancreatic ductal adenocarcinoma[J]. Am J Cancer Res, 2016, 6(8): 1820-7. |
| [10] | Park E H, Kim S, Jo J Y, et al. Collagen triple helix repeat containing-1 promotes pancreatic cancer progression by regulating migration and adhesion of tumor cells[J]. Carcinogenesis, 2013, 34(3): 694-702. doi:10.1093/carcin/bgs378 |
| [11] | Chen S, Li P, Yang R, et al. microRNA-30b inhibits cell invasion and migration through targeting collagen triple helix repeat containing 1 in non-small cell lung cancer[J]. Cancer Cell Int, 2015, 15: 85. doi:10.1186/s12935-015-0236-7 |
| [12] | Wang P, Wang Y C, Chen X Y, et al. CTHRC1 is upregulated by promoter demethylation and transforming growth factor-β1 and may be associated with metastasis in human gastric cancer[J]. Cancer Sci, 2012, 103(7): 1327-33. doi:10.1111/j.1349-7006.2012.02292.x |
| [13] | Tameda M, Sugimoto K, Shiraki K, et al. Collagen triple helix repeat containing 1 is overexpressed in hepatocellular carcinoma and promotes cell proliferation and motility[J]. Int J Oncol, 2014, 45(2): 541-8. |
| [14] | Ma M Z, Zhuang C, Yang X M, et al. CTHRC1 acts as a prognostic factor and promotes invasiveness of gastrointestinal stromal tumors by activating Wnt/PCP-Rho signaling[J]. Neoplasia, 2014, 16(3):265-78, 278.e1-13. |
| [15] | Yang X M, You H Y, Li Q, et al. CTHRC1 promotes human colorectal cancer cell proliferation and invasiveness by activating Wnt/PCP signaling[J]. Int J Clin Exp Pathol, 2015, 8(10): 12793-801. |
| [16] | Kobezda T, Ghassemi-Nejad S, Mikecz K, et al. Of mice and men: how animal models advance our understanding of T-cell function in RA[J]. Nat Rev Rheumatol, 2014, 10(3): 160-70. doi:10.1038/nrrheum.2013.205 |
| [17] | 张玲玲, 魏伟. BAFF/BAFF-R通过PI3K/Akt/mTOR信号转导通路调节B淋巴细胞功能在类风湿关节炎发病机制中的意义[J]. 中国药理学通报, 2010, 26(7): 847-50. Zhang L L, Wei W. The significance of BAFF/BAFF-R regulates the function of B lymphocyte in the pathogenesis of rheumatoid arthritis by PI3K/Akt/mTOR signal transduction pathway[J]. Chin Pharmacol Bull, 2010, 26(7): 847-50. |
| [18] | Tanaka Y. Next stage of RA treatment: is TNF inhibitor-free remission a possible treatment goal[J]. ?Ann Rheum Dis, 2013, 72(Suppl 2): ii124-7. doi:10.1136/annrheumdis-2012-202350 |
| [19] | De Bari C. Are mesenchymal stem cells in rheumatoid arthritis the good or bad guys[J]. ? Arthritis Res Ther, 2015, 17: 113. doi:10.1186/s13075-015-0634-1 |
| [20] | Bottini N. Duality of fibroblast-like synoviocytes in RA: passive responders and imprinted aggressors[J]. Nat Rev Rheumatol, 2013, 9(1): 24-33. |
| [21] | Miao C G, Yang Y Y, He X, et al. Wnt signaling pathway in rheumatoid arthritis, with special emphasis on the different roles in synovial inflammation and bone remodeling[J]. Cell Signal, 2013, 25(10): 2069-78. doi:10.1016/j.cellsig.2013.04.002 |

