


肝纤维化是多种肝损伤发展过程中的一种病理状态, 肝纤维化过程中肝星状细胞 (hepatic stellate cell,HSC) 持续激活是肝纤维化发展过程中的关键环节。HSC在多种因素刺激后被激活转换成为肌成纤维样细胞,细胞大量增殖,合成细胞外基质 (extracellular matrix, ECM) 并在肝脏过度沉积, 产生肝纤维化[1]。课题组前期研究表明,柴胡黄芩配伍水煎液 (CQ) 对大鼠肝纤维化模型有良好的保护作用[2],对四氯化碳 (CCl4) 损伤L02细胞有良好的保护作用[3]。在此基础上,本研究进一步观察柴胡黄芩水提液对HSC增殖的影响以及干预CCl4诱导活化HSC的作用。从体内TLR4-NF-κB信号通路的角度阐释柴胡黄芩水煎液抗肝纤维化的作用机制。
1 材料与方法 1.1 试剂与仪器大鼠肝星状细胞株HSC-T6,购自灏洋生物公司;改良型RPMI 1640培养基,购自博士德生物科技公司;胎牛血清,购自Hyclone公司;胰酶,购自Trypsin。TAK-242购自InvivoGen公司;BAY 11-7082购自江苏碧云天生物工程公司;透明质酸酶 (hyaluronidase,HA)、层黏连蛋白 (laminin,LN)、Ⅲ型前胶原 (procollagen Ⅲ,PCⅢ)、Ⅳ型胶原 (collagen type Ⅳ,Ⅳ-C) 检测试剂盒购自北京永辉生物科技有限公司;TLR4、NF-κB p65一抗、二抗购自武汉博士德生物工程公司。CO2培养箱:新加坡ESCO;倒置显微镜:奥特BDS200;酶标仪:美国BioTek ELx808;离心机:湘仪L530;双人型超净工作台:新加坡ESCO。
1.2 实验药品 1.2.1 柴胡黄芩配伍水提液中药材柴胡和黄芩购自陕西中医药大学校医院中药房,经鉴定为正品。参照文献及前期实验结果,称取柴胡50 g和黄芩25 g,用水浸泡30 min后,以8倍水煎煮2次,将2次水提液混匀浓缩至75 mL。
1.2.2 CCl4溶液的制备将100 μL CCl4与100 μL DMSO混匀,再用无血清培养基稀释,使其终浓度为6 mmol·L-1。
1.3 大鼠HSC培养及药物处理大鼠肝星状细胞株 (HSC-T6) 于改良型RPMI 1640培养基 (含10%的胎牛血清、100 kU·L-1青霉素、100 mg·L-1链霉素),37℃、5% CO2饱和湿度培养箱中培养并传代。取对数生长的HSC,在无血清培养基中培养24 h后,以1.5×109·L-1浓度接种到培养板中过夜。实验分组如下:空白对照组 (无药物处理),CCl4诱导组 (6 mmol·L-1 CCl4作用6 h),给药组 (6 mmol·L-1 CCl4作用6 h后,再用400、500、600 mg·L-1的CQ作用24 h),TLR4阻断剂TAK-242、NF-κB阻断剂BAY 11-7082组 (6 mmol·L-1 CCl4作用6 h后,再用TAK-242 10 mol·L-1、BAY 11-7082 2 mol·L-1作用24 h)。
1.4 CQ对CCl4诱导活化的HSC增殖的影响各组培养24 h后,加入5 g·L-1 MTT 10 μL,37℃孵育4 h,吸弃孔内培养液,每孔加入DMSO 150 μL, 低速震荡10 min,以溶解被还原的MTT结晶,酶标仪单波长检测各孔吸光度值,按下列公式计算大鼠HSC增殖抑制率。细胞抑制率/%=[1-(实验组A值/对照组A值)]×100%。
1.5 CQ对CCl4诱导活化的HSC分泌HA、LN、PCⅢ、Ⅳ-C的影响各组培养24 h后,收集细胞培养液,参照试剂盒使用说明书,应用ELISA法检测HA、LN、PCⅢ、Ⅳ-C含量。
1.6 CQ对CCl4诱导活化的HSC细胞TLR4和NF-κBp65的mRNA水平的影响各组培养24 h后,弃去上清液,胰酶消化收集,至少以1×106个为样本检测量。孵育24 h后抽提细胞总RNA,去除DNA污染后,通过RT-PCR的方法,检测TLR4和NF-κB p65 mRNA表达,PCR引物序列见Tab 1。
| Gene | Forward primer (5′ to 3′) | Reverse primer (5′ to 3′) |
| TLR 4 | ATAGACATGAAGGCCTCCCT | TACAGTGGCTACCACAAGCA |
| NF-κB | ACACTGGAAGCACGGATGAC | TGTCTGTGAGTTGCCGGTCT |
| rGAPDH | GGCAAGTTCAACGGCACAGT | ATGACATACTCAGCACCGGC |
各组培养24 h后,弃去上清液,胰酶消化收集,PBS洗涤2次,加入细胞裂解液和蛋白酶抑制剂充分裂解,4 ℃、12 000 r·min-1离心30 min。取上清,BCA试剂盒蛋白定量,细胞总蛋白加上样缓冲液煮沸变性,用10% SDS-PAGE分离蛋白,转膜后,用5%脱脂牛奶室温封闭2 h,一抗4 ℃孵育过夜,二抗室温杂交2 h,洗膜后,加入ECL发光液,进行检测,观察结果并扫描分析。TLR4和NF-κB p65蛋白表达水平用目的条带积分吸光度值 (integrated absorbance,IA) 与内参GAPDH蛋白条带的IA比值定量表示。
1.8 统计学处理数据资料以x±s表示,用SPSS 13.0计算机软件进行统计学分析, 组间比较采用单因素方差分析,两组间比较采用t检验。
2 结果 2.1 CQ对CCl4诱导活化的HSC增殖的影响与空白对照组比较,CCl4干预后,明显促进HSC增殖 (P<0.01),CQ对CCl4诱导的HSC增殖具有明显抑制作用,特别是剂量为600 mg·L-1时,作用最为明显;TAK-242和BAY 11-7082也对CCl4诱导的HSC增殖具有明显抑制作用。见Tab 2。
| Group | Dose | OD value |
| Normal | - | 0.32±0.14** |
| CCl4 | 6 mmol·L-1 | 0.54±0.08 |
| CQ | 600 mg·L-1 | 0.33±0.06** |
| 500 mg·L-1 | 0.36±0.07* | |
| 400 mg·L-1 | 0.40±0.08* | |
| TAK-242 | 10 mol·L-1 | 0.31±0.15* |
| BAY 11-7082 | 2 mol·L-1 | 0.33±0.10** |
| *P<0.05, **P<0.01 vs CCl4 group | ||
与空白对照组比较,CCl4干预后,HSC细胞分泌的HA、LN、PCⅢ、Ⅳ-C含量明显升高,CQ、TAK-242和BAY 11-7082对CCl4诱导的HSC细胞分泌的HA、LN、PCⅢ、Ⅳ-C具有明显抑制作用,特别是CQ剂量为600 mg·L-1时,作用最为明显。见Tab 3。
| Group | Dose | HA/μg·L-1 | Ⅳ-C/μg·L-1 | LN/μg·L-1 | PCⅢ/μg·L-1 |
| Normal | - | 234.26±29.64** | 10.69±2.01** | 42.67±6.28** | 80.21±7.61** |
| CCl4 | 6 mmol·L-1 | 498.36±98.08 | 25.34±2.64 | 71.25±10.21 | 142.65±9.92 |
| CQ | 600 mg·L-1 | 326.94±72.06* | 11.54±2.90** | 46.42±12.03** | 89.29±10.24** |
| 500 mg·L-1 | 376.22±69.49* | 15.02±2.87* | 56.15±9.52* | 115.39±10.04* | |
| 400 mg·L-1 | 473.67±72.84 | 23.64±2.91 | 59.21±11.65 | 138.57±11.68 | |
| TAK-242 | 10 mol·L-1 | 259.26±59.37** | 12.89±2.98* | 43.24±9.87** | 90.21±12.54** |
| BAY 11-7082 | 2 mol·L-1 | 309.18±81.65* | 11.03±1.24** | 40.21±10.24** | 84.15±9.34** |
| *P<0.05, **P<0.01 vs CCl4 group | |||||
与空白对照组比较,CCl4干预后,HSC中TLR4和NF-κB p65 mRNA表达增强,CQ和BAY 11-7082对CCl4诱导的HSC细胞TLR4和NF-κB p65 mRNA表达有下调作用,TAK-242对CCl4诱导的HSC细胞NF-κB p65 mRNA表达有下调作用,其中CQ 600 mg·L-1组、TAK-242和BAY 11-7082组差异有统计学意义 (P<0.05),见Tab 4。
| Group | Dose | NF-κB | TLR4 |
| Normal | - | 20.90±0.50* | 38.32±2.83* |
| CCl4 | 6 mmol·L-1 | 24.37±0.47 | 42.40±1.55 |
| CQ | 600 mg·L-1 | 21.34±1.92* | 40.02±0.03* |
| 500 mg·L-1 | 22.46±0.18 | 42.01±1.19 | |
| 400 mg·L-1 | 23.45±0.18 | 44.00±0.63 | |
| TAK-242 | 10 mol·L-1 | 21.45±1.20* | 42.19±0.82 |
| BAY 11-7082 | 2 mol·L-1 | 23.24±0.08* | 41.19±3.10* |
| **P<0.01, *P<0.05 vs CCl4 group | |||
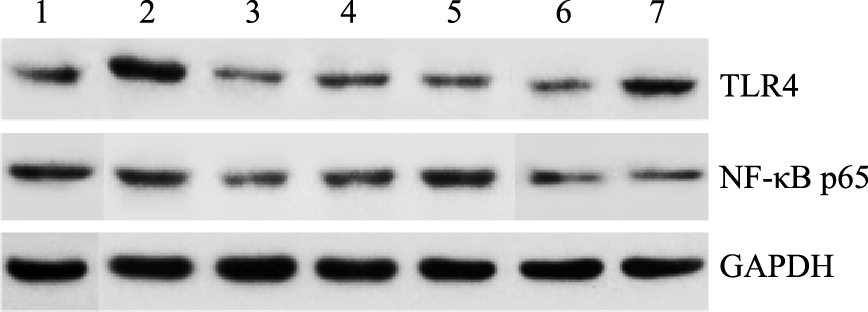
与空白对照组比较,CCl4干预后,HSC中TLR4和NF-κB p65蛋白表达增强,CQ、TAK-242对CCl4诱导的HSC中TLR4和NF-κB p65蛋白表达有下调作用,BAY 11-7082对CCl4诱导的HSC中NF-κB p65蛋白表达有下调作用,其中CQ 600 mg·L-1、TAK-242和BAY 11-7082组差异有统计学意义 (P<0.05),见Tab 5、Fig 1。
| Group | Dose | NF-κB | TLR4 |
| Normal | - | 0.35±0.00* | 0.20±0.01* |
| CCl4 | 6 mmol·L-1 | 0.80±0.02 | 0.60±0.02 |
| CQ | 600 mg·L-1 | 0.14±0.03** | 0.16±0.01** |
| 500 mg·L-1 | 0.24±0.02* | 0.18±0.00* | |
| 400 mg·L-1 | 0.61±0.01 | 0.16±0.04* | |
| TAK-242 | 10 mol·L-1 | 0.18±0.03* | 0.14±0.02** |
| BAY 11-7082 | 2 mol·L-1 | 0.15±0.02** | 0.52±0.01 |
| *P<0.05, **P<0.01 vs CCl4 group | |||
|
| Fig 1 Effect of CQ on protein expressions of TLR4, NF-κB in HSC 1: Normal group; 2: CCl4 group; 3: CQ 600 mg·L-1 group; 4: CQ 500 mg·L-1 group; 5: CQ 400 mg·L-1 group; 6: TAK-242; 7:BAY 11-7082 |
TLR4是细胞表面识别病原相关分子的一个重要识别受体,该受体激活后能通过信号转导激活其下游的NF-κB,导致炎性介质大量释放,引起肝脏损害[4-6]。经刺激活化的HSC是肝纤维化ECM的主要来源细胞。HSC在多种因素刺激后被激活转换成为肌成纤维样细胞, 细胞大量增殖,合成ECM, 并在肝内过量沉积, 发生肝纤维化,可见,TLR4-NF-κB信号通路异常与肝损伤关系密切[7-8]。文献研究[9-11]及课题组前期实验发现,柴胡黄芩配伍水煎剂有明显防治大鼠肝纤维化作用,其体内调控机制可能与TLR4-NF-κB信号通路调控的炎症反应有关[1]。本实验通过研究柴胡黄芩配伍水煎剂对HSC增殖影响,及对CCl4诱导活化后的HSC的分泌功能、TLR4和NF-κB p65基因及蛋白表达的影响,探讨其抗肝纤维化可能的作用机制。
实验结果显示,HSC经CCl4激活,大量增殖, 其培养液中HA、LN、PCⅢ、Ⅳ-C含量明显高于空白对照组。可见,CCl4对HSC增殖有一定激活作用,导致肝纤维化相关因子HA、LN、PCⅢ、Ⅳ-C分泌增加,表现出肝纤维化倾向。给予CQ干预后,HSC增殖受到一定抑制,并且HA、LN、PCⅢ、Ⅳ-C含量也降低,可见,CQ有一定抗肝纤维化作用。通过RT-PCR法和Western blot法检测CCl4活化后的HSC中TLR4和NF-κB p65 mRNA及蛋白的表达,与空白组比较,TLR4和NF-κB p65 mRNA表达和蛋白表达均明显增加,CQ干预后,TLR4和NF-κB p65 mRNA表达和蛋白表达均明显降低,其中CQ 600 mg·L-1时作用最为明显。同时,应用TLR4的拮抗剂TAK-242后,TLR4和NF-κB p65 mRNA表达和蛋白表达明显降低,而应用NF-κB p65拮抗剂BAY 11-7082后,NF-κB p65 mRNA表达和蛋白表达也明显降低,TLR4 mRNA表达和蛋白表达没有明显变化。可见,CQ能够减轻CCl4激活HSC的增殖,并降低肝纤维化因子HA、LN、PCⅢ、Ⅳ-C的含量,其作用机制之一是通过调控TLR4-NF-κB信号通路,具体的调控机制,还需进一步研究。
( 致谢: 本文实验在陕西中医药大学医学科研实验中心完成,在整个研究过程中得到了王宇老师、史迎莉的悉心指导和热忱帮助,在此次深表谢意! )
| [1] | Sahin H, Trautwein C, Wasmuth H E. TLR4 stresses the liver[J]. Gut, 2012, 61(9): 1241-2. doi:10.1136/gutjnl-2012-302188 |
| [2] | 王斌, 李敏, 侯建平. 基于TLR4-NFκB信号通路的柴胡-黄芩药对抗肝纤维研究[J]. 中药药理与临床, 2015, 31(3): 103-6. Wang B, Li M, Hou J P. Study of Bupleurum-Scutellariaon hepatic fibrosis in rats based on TLR4-NF-κB signal pathway[J]. Pharmacol Clin Chin Mater Med, 2015, 31(3): 103-6. |
| [3] | 李小菲, 李静, 王義雯, 等. 柴胡、柴胡和黄芩配伍对肝细胞损伤体外作用[J]. 吉林中医药, 2016, 36(2): 176-80. Li X F, Li J, Wang X W, et al. Water extraction from radix bupleuri and compatibility of radix bupleuri and scutellaria baicalensis georgi on carbon tetrachloride-injured hepatocyte in vitro[J]. Jilin J Tradit Chin Med, 2016, 36(2): 176-80. |
| [4] | Zhu Q, Zou L, Jagavelu K, et al. Intestinal decontamination inhibits TLR4 dependent fibronectin-mediated cross-talk between stellate cells and endothelial cells in liver fibrosis in mice[J]. Hepatology, 2012, 56(4): 893-9. doi:10.1016/j.jhep.2011.11.013 |
| [5] | Yu M, Shao D B, Liu J, Zhu J. Effects of ketamine on levels of cytokines, NF-κB and TLRs in rat intestine during CLP-induced sepsis[J]. Int Immunopharmacol, 2007, 7(8): 1076-82. doi:10.1016/j.intimp.2007.04.003 |
| [6] | 谷元婧, 孙妩弋, 张森, 等. β-arrestins与纤维化疾病的研究进展[J]. 中国药理学通报, 2015, 31(2): 171-5. Gu Y J, Sun W Y, Zhang S, et al. Advances in the study of β-arrestins and fibrosis[J]. Chin Pharmacol Bull, 2015, 31(2): 171-5. |
| [7] | Wu Y H, Yang L X, Wang F, et al. Hepatoprotective and antioxidative effects of total phenolics from Laggera pterodonta on chemical-induced injury in primary cultured neonatal rat hepatocytes[J]. Food Chem Toxicol, 2007, 45(8): 1349-55. doi:10.1016/j.fct.2007.01.011 |
| [8] | 李冬, 戴立里, 余斌斌, 等. 丹参素对大鼠肝星状细胞增殖、凋亡及NF-κB活性的影响[J]. 第三军医大学学报, 2009, 31(8): 724-7. Li D, Dai L L, Yu B B, et al. Tanshinol induces proliferation, apoptosis and NF-κB activation in cultured rat hepatic stellate cells after IL-1β inducement[J]. Acta Acad Med Mil Tert, 2009, 31(8): 724-7. |
| [9] | 纪辉, 迟宝荣, 张一宁. 肝纤维化与肝星状细胞[J]. 吉林大学学报 (医学版), 2008, 34(3): 538-41. Ji H, Chi B R, Zhang Y N. Liver fibrosis and hepatic stellate cells[J]. J Jilin Univ (Med Ed), 2008, 34(3): 538-41. |
| [10] | 郑丽娜, 韩涛, 王宝恩, 等. 柴胡对肝星状细胞胶原蛋白分泌的影响[J]. 天津医科大学学报, 2001, 7(4): 502-3. Zheng L N, Han T, Wang B E, et al. Effect of Bupleurum on collagen content in hepatic stellate cell media in vitro[J]. J Tianjin Med Univ, 2001, 7(4): 502-3. |
| [11] | 刘林华, 许景薇, 万玉英, 等. 猪牙皂正丁醇提取物体外对肝星状细胞活性的影响研究[J]. 抗感染药学, 2015, 12(6): 832-4. Liu L H, Xu J W, Wan Y Y, et al. Study on the effect of hepatic stellate cell activity of Fructus Gleditsiae n-butanol extract[J]. Anti-Infec Pharm, 2015, 12(6): 832-4. |

