


脊髓缺血/再灌注损伤是胸腹主动脉瘤手术最严重的并发症,是急需攻克的难题。血-脊髓屏障破坏是脊髓损伤的重要继发病理改变,而且进一步加重脊髓损伤[1]。MicroRNA在转录后水平调控基因表达,是目前研究基因治疗和寻找药物靶点的重要工具。最近研究证实,miR-122a介导紧密连接蛋白occludin的mRNA降解增加肠道通透性[2-3]。有关miR-122a在脊髓损伤中的作用及可能的机制目前尚不清楚。本研究拟探讨miR-122a对脊髓缺血/再灌注损伤后血-脊髓屏障的影响及其相关机制。
1 材料与方法 1.1 动物选择与分组SD大鼠36只,由中国医科大学实验动物中心提供,体质量200~250 g。采用随机数字表法,随机分为3组 (n=12):假手术组 (S组)、对照组 (C组)、miR-122a反义寡核苷酸 (miR-122a antagomir) 组 (M组)。S组开胸游离主动脉弓,但不阻断;C组和M组开胸阻断主动脉弓14 min造成脊髓缺血/再灌注损伤。M组和C组在脊髓缺血/再灌注损伤后30 min鞘内注射20 μL miR-122a antagomir (20 μmol·L-1,广州锐博公司),每日注射1次,共3次。C组脊髓缺血/再灌注损伤后鞘内注射等量miR-122a antagomir空白对照。实验室光照时间6 :00~18 :00,温度控制在18℃~22℃,造模后分笼饲养,保证充足的水和食物。
1.2 脊髓缺血/再灌注损伤模型的建立大鼠腹腔注射戊巴比妥钠 (40 mg·kg-1) 麻醉,经气管切开处行气管内插管机械通气。直肠内置入温度传感器,持续监测体温,应用电热毯维持核心温度 (37.5±0.5) ℃。脊髓缺血/再灌注损伤模型参照文献[4]制备。左颈总动脉置管测量近端动脉血压,尾动脉置管测量远端血压。摆右侧卧位,于左前肢和肩胛下角间行横切口,逐层分离暴露肋骨,于第2、3肋之间暴露胸腔,分离并显露主动脉弓。皮下注射肝素 (200 IU·kg-1),于左颈总动脉和左锁骨下动脉之间夹闭主动脉,阻断14 min后开放动脉夹,造成脊髓缺血/再灌注损伤。关胸,逐层缝合。术后将动物放置28℃的保温箱内,等待动物苏醒后回笼饲养。
1.3 Real-timePCR脊髓缺血/再灌注损伤后72 h,取新鲜缺血节段脊髓组织,根据TRIzol操作说明,提取细胞总RNA。提取的总RNA定量后,对于蛋白编码基因使用Oligo (dT) 作为逆转录引物,对于miRNA使用miRNA特异的逆转录引物,使用反转录试剂盒合成cDNA第一链。使用适量的cDNA作为PCR模板,MX3000P Real-time PCR扩增仪进行PCR反应,SYBR染料实时检测扩增产物的量,以GAPDH为内参分析蛋白编码基因表达情况,以U6为内参分析miRNA的表达情况。所使用引物序列如下:U6上游引物5′-CTCGCTTCGGCAGCACA-3′,U6下游引物5′-AACGCTTCACGAATTTGCGT-3′;GAPDH上游引物5′-TCAACGACCACTTTGTCAAGCTCA-3′,GAPDH下游引物5′-GCTGGTGGTCCAGGGGTCTTACT-3′。
1.4 Western blot脊髓缺血/再灌注损伤后72 h,取新鲜缺血节段脊髓组织,迅速液氮冷冻保存。标本取齐后,剪碎,加组织裂解液,冰上匀浆,4℃离心15 min,取其上清液,BCA法蛋白定量,经电泳、转膜、醋酸纤维素膜包被后,加入兔抗大鼠occludin一抗 (1 :500,Invitrogen公司),4℃孵育过夜,加入HRP标记的羊抗兔IgG二抗,室温孵育2 h,TBST冲洗,化学发光,凝胶成像系统拍摄。采用Image-Pro Plus 6.0图像分析软件对其进行半定量分析。
1.5 血-脊髓屏障通透性测定脊髓缺血/再灌注损伤后72 h,经鼠尾静脉缓慢注射2%伊文思蓝10 mL·kg-1,1 h后麻醉,经左心室灌注生理盐水500 mL·kg-1,取出脊髓缺血节段 (L4-6),迅速放入40 g·L-1多聚甲醛中,24 h后依次置于150、200、300 g·L-1的蔗糖中沉糖,沉糖完毕后包埋,冰冻切片,置于荧光显微镜绿色激光下观察。依照荧光光斑的大小、疏密、强弱来评价脊髓组织中伊文思蓝外渗量。
1.6 大鼠神经运动功能评价采用Basso Beattie Bresnahan (BBB) 评分标准对大鼠下肢运动神经功能进行评价。
1.7 统计学处理采用SPSS 13.0统计学软件进行分析,数据以x±s表示,统计学处理采用单因素方差分析。
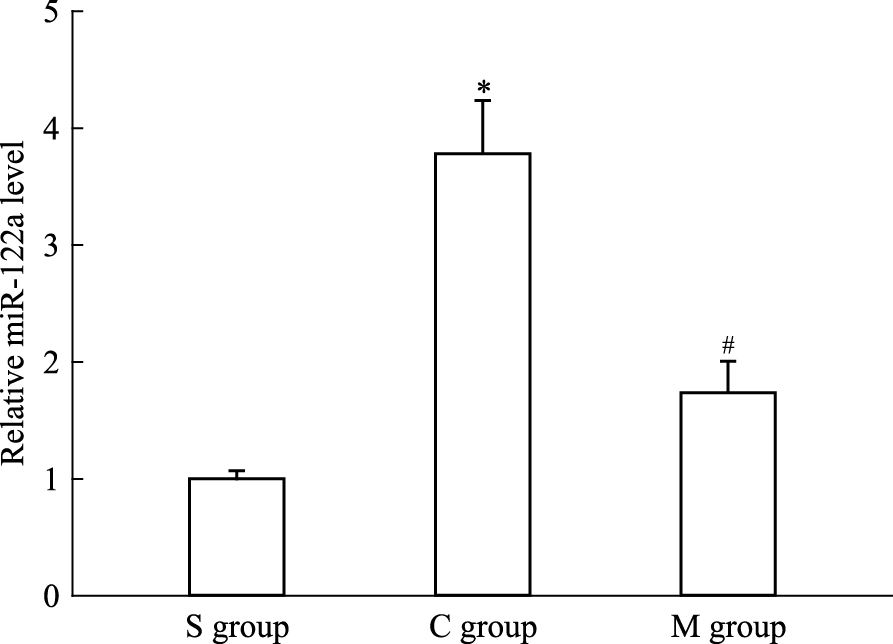
2 结果 2.1 Real-timePCR检测脊髓组织中miR-122a表达与S组 (1.00±0.07) 相比,C组miR-122a表达 (3.78±0.46) 增高 (P<0.05);与C组相比,M组miR-122a表达 (1.74±0.27) 降低 (P<0.05),Fig 1。
|
| Fig 1 miR-122a expression at 72 h after spinal ischemia-reperfusion injury (x±s, n=6) S:Sham; C: control; M:miR-122a antagomir.*P < 0.05 vs S group; #P < 0.05 vs C group |
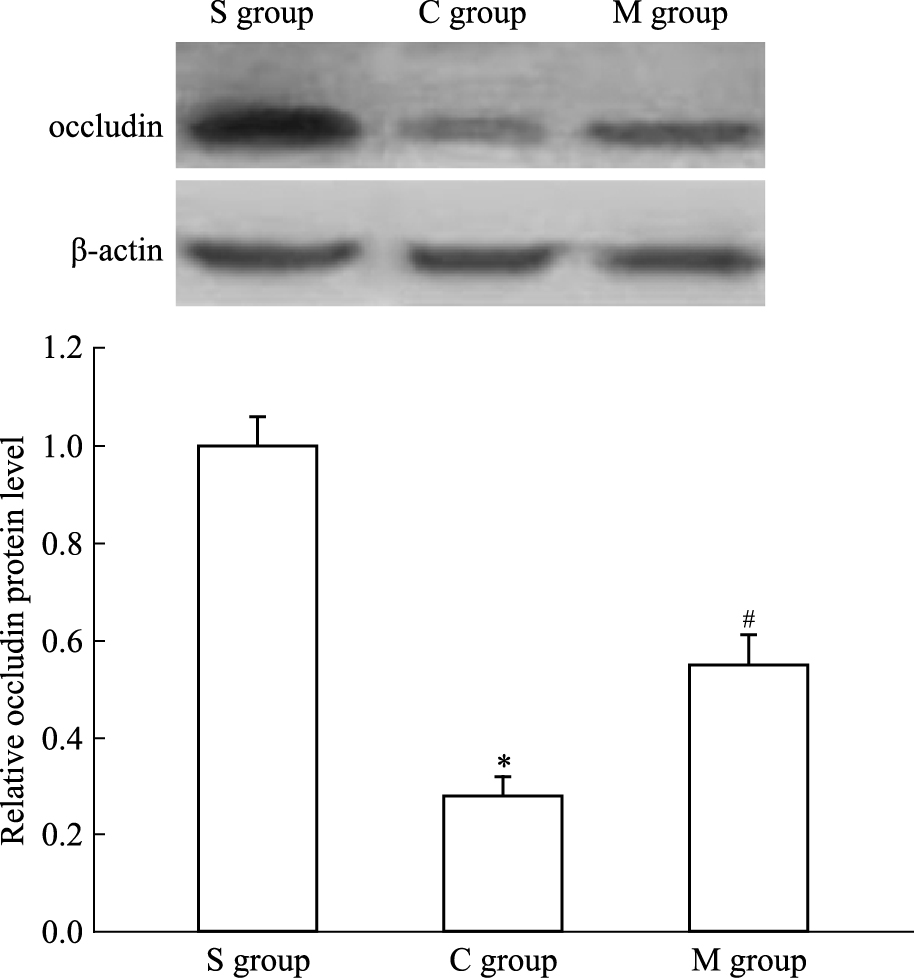
与S组 (1.00±0.06) 相比,C组occludin表达 (0.28±0.04) 降低 (P<0.05);与C组相比,M组occludin表达 (0.55±0.06) 增加 (P<0.05),Fig 2。
|
| Fig 2 Occludin expression at 72 h after spinal ischemia-reperfusion injury (x±s, n=6) S:Sham; C: control; M:miR-122a antagomir.*P < 0.05 vs S group; #P < 0.05 vs C group |
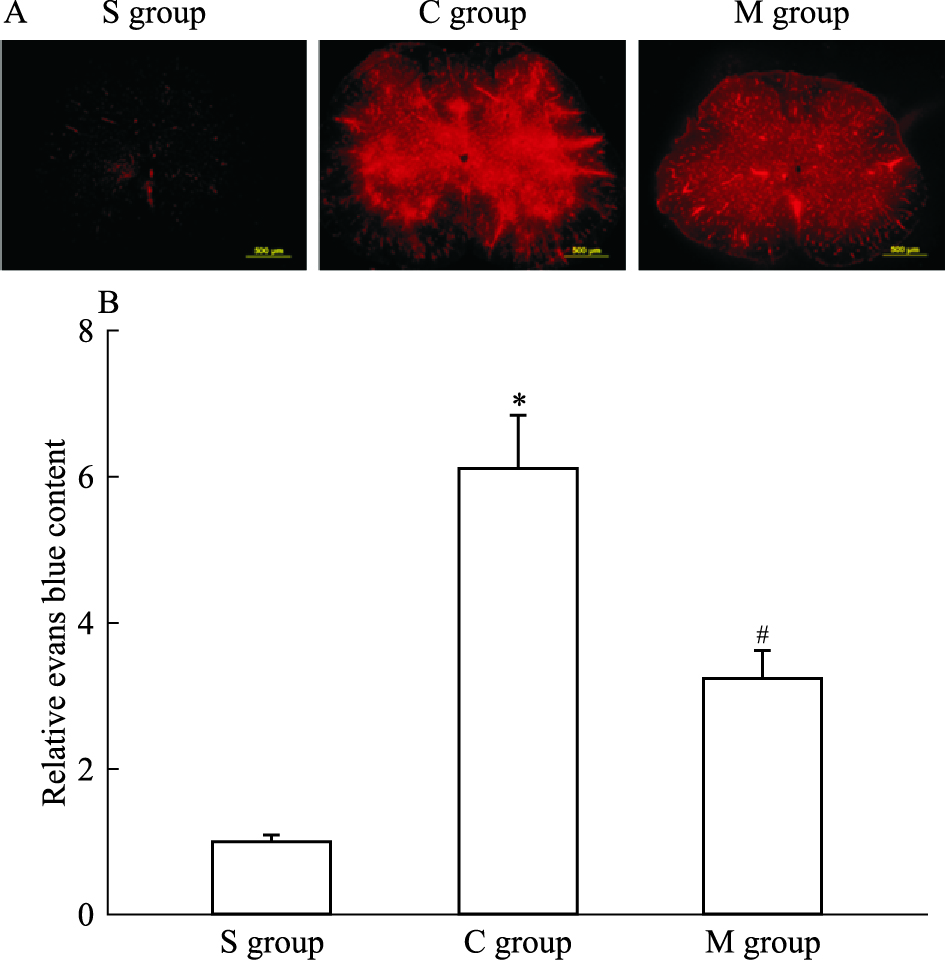
脊髓缺血/再灌注损伤后,血-脊髓屏障破坏,通透性增加,与S组 (1.00±0.08) 相比,C组伊文思蓝外渗量 (6.12±0.73) 增加 (P<0.05);与C组相比,M组伊文思蓝外渗量 (3.24±0.38) 减少 (P<0.05),Fig 3。
|
| Fig 3 Permeability of blood-spinal cord barrier at 72 h after spinal ischemia-reperfusion injury (x±s, n=6) A:Evans blue extravasation fluorescence; B:Quantitative analysis of evans blue extravasation.S:Sham; C: control; M:miR-122a antagomir.*P < 0.05 vs S group; #P < 0.05 vs C group |
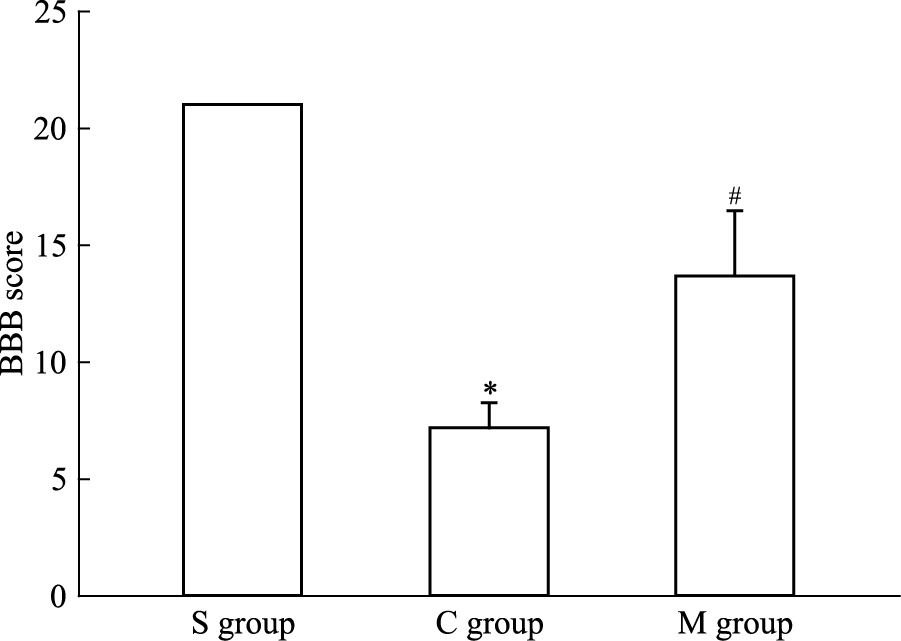
与S组 (21.0±0.0) 比较,C组BBB评分 (7.2±1.1) 降低 (P<0.05);与C组比较,M组BBB评分 (13.7±2.8) 增高 (P<0.05),Fig 4。
|
| Fig 4 BBB score at 72 h after spinal ischemia-reperfusion injury (x±s, n=6) S:Sham; C: control; M:miR-122a antagomir.*P < 0.05 vs S group; #P < 0.05 vs C group |
脊髓缺血/再灌注损伤是胸腹主动脉瘤手术最严重的并发症之一,可引起脊髓功能障碍,甚至截瘫。血-脊髓屏障与血-脑屏障相似,是一个复杂的细胞系统,调节脊髓液体微环境在较小的范围内波动,对维持中枢神经系统的内环境稳定起着非常重要的作用[5]。脊髓缺血/再灌注损伤后,血-脊髓屏障完整性破坏,通透性增加,造成脊髓组织水肿、炎症以及神经元凋亡,进一步加重脊髓损伤[6-9]。紧密连接是血-脊髓屏障的结构和功能基础,occludin是第一个被分离出的组成紧密连接的完整膜蛋白,主要参与微血管内皮细胞间紧密连接的形成。研究发现,脊髓缺血/再灌注损伤后occludin表达减少,导致血-脊髓屏障通透性增加[10],但其机制尚不完全明确。
MicroRNA属于调控RNA家族一员。当非编码小RNA与靶mRNA完全或不完全配对时,可引起mRNA降解,或发生在mRNA水平上诱导特异性序列基因表达部分或完全抑制的过程[11]。miR-122a作为肝脏特异性高表达的microRNA,对其研究多集中在肝癌的发生发展中[12-13]。最近研究表明,miR-122a也负向调控紧密连接蛋白occludin的表达[2, 3, 14],参与内皮细胞通透性调节,影响病理生理功能。
本研究发现,脊髓缺血/再灌注损伤后miR-122a表达上调,同时伴随occludin表达减少,血-脊髓屏障破坏。反义寡核苷酸在miRNA功能研究中是沉默miRNA的最常用,且行之有效的方法[15]。本研究鞘内注射miR-122a antagomir抑制了miR-122a表达,而且增加occludin表达,减轻血-脊髓屏障破坏,改善大鼠神经运动功能。
综上所述,miR-122a在脊髓缺血/再灌注损伤中通过调控血-脊髓屏障紧密连接蛋白occludin,进而发挥重要的作用。将其作为靶点,将为预防和治疗脊髓损伤提供新思路。
( 致谢: 本实验在中国医科大学附属第一医院实验中心、麻醉科实验室完成,在此特对以上实验室和实验过程中给予指导和帮助的老师表示感谢! )
| [1] | Sharma H S. Pathophysiology of blood-spinal cord barrier in traumatic injury and repair[J]. Curr Pharm Des, 2005, 11(11): 1353-89. doi:10.2174/1381612053507837 |
| [2] | Ye D, Guo S, Al-Sadi R, et al. MicroRNA regulation of intestinal epithelial tight junction permeability[J]. Gastroenterology, 2011, 141(4): 1323-33. doi:10.1053/j.gastro.2011.07.005 |
| [3] | Zhao H, Zhao C, Dong Y, et al. Inhibition of miR122a by Lactobacillus rhamnosus GG culture supernatant increases intestinal occluding expression and protects mice from alcoholic liver disease[J]. Toxicol Lett, 2015, 234(3): 194-200. doi:10.1016/j.toxlet.2015.03.002 |
| [4] | Award H, Ankeny D P, Guan Z, et al. A mouse model of ischemic spinal cord injury with delayed paralysis caused by aortic cross-clamping[J]. Anesthesiology, 2010, 113(4): 880-91. doi:10.1097/ALN.0b013e3181ec61ee |
| [5] | Maikos J T, Shreiber D I. Immediate damage to the blood-spinal cord barrier due to mechanical trauma[J]. J Neurotrauma, 2007, 24(3): 492-507. doi:10.1089/neu.2006.0149 |
| [6] | Fang B, Li X M, Sun X J, et al. Ischemic preconditioning protects against spinal cord ischemia-reperfusion injury in rabbits by attenuating blood spinal cord barrier disruption[J]. Int J Mol Sci, 2013, 14(5): 10343-54. doi:10.3390/ijms140510343 |
| [7] | Li X Q, Wang J, Fang B, et al. Intrathecal antagonism of microglial TLR4 reduces inflammatory damage to blood-spinal cord barrier following ischemia/reperfusion injury in rats[J]. Mol Brain, 2014, 7(28). doi:10.1186/1756-6606-7-28 |
| [8] | Fang B, Li X Q, Bi B, et al. Dexmedetomidine attenuates blood-spinal cord barrier disruption induced by spinal cord ischemia reperfusion injury in rats[J]. Cell Physiol Biochem, 2015, 36(1): 373-83. doi:10.1159/000430107 |
| [9] | 方波, 孙学军, 王赫, 等. 鞘内移植骨髓基质细胞对兔脊髓缺血/再灌注损伤早期水通道蛋白-4表达的影响[J]. 中国药理学通报, 2013, 29(4): 478-81. Fang B, Sun X J, Wang H, et al. Effects of intrathecal transplantation of bone marrow stromal cells on aquaporin-4 expression in spinal cord following spinal ischemia-reperfusion injury in rabbits[J]. Chin Pharmacol Bull, 2013, 29(4): 478-81. |
| [10] | Fang B, Wang H, Sun X J, et al. Intrathecal transplantation of bone marrow stromal cells attenuates blood spinal cord barrier disruption induced by spinal cord ischemia reperfusion injury in rabbits[J]. J Vasc Surg, 2013, 8(4): 1043-52. |
| [11] | Vriens M R, Weng J, Suh I, et al. MicroRNA expression profiling is a potential diagnostic tool for thyroid cancer[J]. Cancer, 2012, 118(13): 3426-32. doi:10.1002/cncr.26587 |
| [12] | Bai S, Nasser M W, Wang B, et al. MicroRNA-122 inhibits tumorigenic properties of hepatocellular carcinoma cells and sensitizes these cells to sorafenib[J]. J Biol Chem, 2009, 284(46): 32015-27. doi:10.1074/jbc.M109.016774 |
| [13] | Lin C J, Gong H Y, Tseng H C, et al. miR-122 targets an anti-apoptotic gene, Bcl-w, in human hepatocellular carcinoma cell lines[J]. Biochem Biophys Res Commun, 2008, 375(3): 315-20. doi:10.1016/j.bbrc.2008.07.154 |
| [14] | 马腾, 刘丽波, 王萍, 等. 血脑屏障氧糖剥夺体外模型大鼠脑微血管内皮细胞miRNA表达变化[J]. 解剖科学进展, 2011, 17(2): 128-30. Ma T, Liu L B, Wang P, et al. Changes of miRNA expression profiles in cultured brain microvascular endothelium of rat with blood brain barrier for oxygen glucose deprivation[J]. Prog Anatom Sci, 2011, 17(2): 128-30. |
| [15] | 夏新, 张小敏, 宋鹏飞, 等. 反义寡核苷酸介导的miRNA沉默研究[J]. 安徽农业科学, 2011, 39(24): 14545-7. Xia X, Zhang X M, Song P F, et al. Study of miRNA silencing mediated by antisense oligonucleotide[J]. J Anhui Agric Sci, 2011, 39(24): 14545-7. doi:10.3969/j.issn.0517-6611.2011.24.010 |

