


吡非尼酮 (pirfenidone,BT),化学名5-甲基-1-苯基-2 (1H)-吡啶酮, 是一种新型广谱抗纤维化药物。BT是一种有效的细胞因子抑制剂,能够通过参与调节某些因子,抑制成纤维细胞的生物学活性,导致细胞增殖受抑,基质胶原合成减少[1]。其主要作用机制为清除活性氧,抑制脂质过氧化;抑制转化生长因子-β(TGF-β) 基因的过度表达,减少TGF-β的生成;减少血小板衍化生长因子 (PDGF) 的生成;抑制肿瘤坏死因子-α(TNF-α) 的生成,减轻炎症反应等[2-3]。临床实验表明,BT可以改善特发性肺纤维化患者的肺功能下降,一定程度地延缓疾病进展[4-5]。BT在人体内经肝内细胞色素P450酶代谢后,约87.76%的药物以5-羧基吡非尼酮 (5-carboxy-pirfenidone,SBT) 的形式从尿液排出[6-7],该代谢物与吡非尼酮抗纤维化作用的相关性也在一定程度上得到了证明[8]。因此,同时描述BT和其主要代谢产物SBT的体内药代动力学行为,可以更全面评价该药的药代动力学特征。
目前,已有研究报道了人血浆中BT浓度的测定方法和临床药动学参数,主要方法有高效液相色谱法 (HPLC)[9-10]和液相色谱-串联质谱法 (LC-MS/MS)[11]。HPLC法繁琐且灵敏度较低,不利于临床应用时样品的批量分析。而LC-MS/MS法更为快速、灵敏度高、专属性强,更加适合人血浆中药物浓度的测定[12-13]。但在已报道的LC-MS/MS法中[11],研究者未建立SBT测定方法,这不利于对该药在人体内的吸收、分布、消除、代谢规律进行全面评价。基于此,本研究拟建立一种同时测定人体血浆中BT和SBT药物浓度的LC-MS/MS方法,并进行全面的方法学验证,以用于后续人体药代动力学的系统研究。
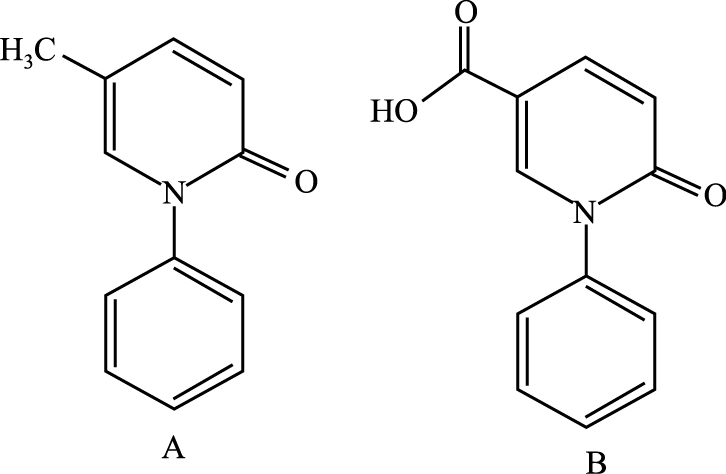
1 材料 1.1 药品与试剂吡非尼酮 (BT) 对照品 (浙江金华康恩贝生物制药有限公司,批号130603,含量100.2%,结构如Fig 1A所示);5-羧基吡非尼酮 (SBT) 对照品 (南京华威医药科技开发有限公司,含量99.79%,结构如Fig 1B所示);吡非尼酮-d5(dBT) 对照品 (BT的同位素内标,加拿大TRC公司,批号17-WG-177-2,化学纯度为99.7%,同位素纯度为98%,每瓶1 mg);5-羧基吡非尼酮-d5(dSBT) 对照品 (SBT的同位素内标,加拿大TRC公司,批号17-WG-177-1,化学纯度为99.9%,同位素纯度为99%,每瓶1 mg);甲酸 (ROE Scientific Inc.,USA,HPLC级,批号2B3026);甲醇和乙腈 (Merck Company,HPLC级);超纯水由Millipore Milli-Q Advantage A10超纯水机制备;其余试剂为分析纯。吡非尼酮片 (浙江金华康恩贝生物制药有限公司提供,批号1308002)。人空白血浆源自江苏省血液中心。
|
| Fig 1 Chemical structures of BT (A) and SBT (B) |
(Agilent) LC-(AB) API4000 MS/MS液质联用仪 (含Pump Agilent 1260G1312A,Auto Sampler Agilent 1260G1367E,Column Oven Agilent 1260G1316A和Mass spectrometer API4000),LC-MS/MS系统由Analyst 1.6 Software控制;CPA225D电子天平 (德国赛多利斯公司);高速低温离心机 (Thermo Sorvall Legend Micro 17R, PT021);VTX-3000L旋涡混合仪 (日本LMS公司)。
2 方法与结果 2.1 色谱与质谱条件色谱条件:Agilent ZORBAX SB C18色谱柱 (3.0 mm×100 mm,3.5 μm),Agilent ZORAX SB-C8预柱 (2.1 mm×12.5 mm,5 μm),流动相为水 (0.5%甲酸)/乙腈 (50/50),流速350 μL·min-1,柱温35 ℃,分析4 min,进样体积5 μL。
质谱条件:ESI离子源,正离子模式检测,扫描模式为多反应检测 (MRM)。BT的检测目标离子对为m/z185.958/77.1,DP为80 V,CE为40 eV,CXP为6 V;SBT的检测目标离子对为m/z 215.944/77.0,DP为85 V,CE为51 eV,CXP为6V;dBT的检测目标离子对为m/z 190.965/81.1,DP为76 V,CE为47 eV,CXP为6V;dSBT的检测目标离子对为m/z 220.948/99.1,DP为71 V,CE为41 eV,CXP为8 V。其他主要质谱参数如下:Dwell Time 150 ms,EP为10 V,碰撞气 (CAD)6 psi,气帘气 (CUR)35 psi,辅助气1(GS1)45 psi,辅助气2(GS2)45 psi,电喷雾电压 (IS)5 500 V,离子源温度 (TEM)550 ℃。
2.2 标准溶液的配制 2.2.1 BT和SBT对照品储备液的配制精密称取BT对照品12.57 mg和SBT对照品10.21 mg分别于10 mL容量瓶中,以甲醇溶解、定容,混匀即得浓度为1.257 g·L-1的BT标准曲线储备液和浓度为1.021 g·L-1的SBT标准曲线储备液,于4 ℃冰箱中保存备用。将BT和SBT储备液等体积混合均匀后,用甲醇将其逐级稀释得到含BT浓度分别为0.103 0、0.205 9、0.514 9、1.287、3.218、8.045、20.11、50.28、125.7 mg·L-1以及含SBT浓度分别为0.083 64、0.167 3、0.418 2、1.046、2.614、6.534、16.34、40.84、102.1 mg·L-1的系列标准曲线工作液。
精密称取BT对照品12.67 mg和SBT对照品10.39 mg分别于10 mL容量瓶中,以甲醇溶解、定容,混匀即得浓度为1.267 g·L-1的BT质控储备液和浓度为1.039 g·L-1的SBT质控储备液,于4 ℃冰箱中保存备用。以甲醇为溶剂,对BT和SBT质控储备液分别进行系列稀释,而后进行等体积混匀,得到BT浓度分别为0.519 0、12.97、202.7 mg·L-1和SBT浓度分别为0.425 6、10.64、166.2 mg·L-1的质控工作液。
2.2.2 内标储备液的配制分别取规格为每瓶1 mg的dBT和dSBT各1瓶,分别精密加入1 mL甲醇,涡旋混匀,即得浓度为1 g·L-1的dBT和dSBT储备液。将dBT和dSBT储备液分别用甲醇稀释100倍后,等体积混合均匀,即得浓度为5 mg·L-1的内标工作液。
2.3 血浆样品处理 2.3.1 受试者含药血浆样品处理自-70 ℃低温冰箱中取出受试者的含药血浆样品,室温解冻后,涡旋振荡30 s充分混匀,12 000 g×10 min,4 ℃, 超速离心。精密吸取离心后血浆中层100 μL于1.5 mL EP管中,分别依次加入浓度为5 mg·L-1的内标工作液20 μL,甲醇880 μL,涡旋3 min进行蛋白沉淀,12 000 g×10 min,4 ℃离心,吸取上清液300 μL,加入700 μL流动相 (即含0.25%甲酸的50%乙腈水溶液),涡旋混匀后进行LC-MS/MS分析。空白血浆除未加内标外,其余样品处理方法相同。
2.3.2 血浆标准曲线样品的配制与处理自-70 ℃低温冰箱中取出空白血浆样品,室温解冻后,涡旋振荡30 s充分混匀,12 000 g×10 min,4 ℃,超速离心。精密吸取离心后血浆中层100 μL于1.5mLEP管中,分别依次加入不同浓度的系列标曲工作液20 μL,得到含BT浓度分别为0.020 59、0.041 19、0.103、0.257 4、0.643 6、1.609、4.022、10.06、25.14 mg·L-1,含SBT浓度分别为0.016 73、0.033 46、0.083 64、0.209 1、0.522 8、1.307、3.267、8.168、20.42 mg·L-1的系列血浆标准曲线工作液,后续处理过程同“2.3.1”项下要求。同法制备并分析双空白样品和零点样品,其中双空白样品仅加入100 μL空白血浆和900 μL甲醇,而零点样品加入100 μL血浆、20 μL内标工作液和880 μL甲醇。
2.3.3 血浆质控样品的配制与处理取不同浓度的系列质控工作液各20 μL于1.5 mL EP管中,向其中分别加入100μL空白血浆,涡旋混匀,即得含BT浓度分别为0.051 90、1.297和20.27 mg·L-1,SBT浓度分别为0.042 56、1.064和16.62 mg·L-1的血浆质控样品,后续处理过程同“2.3.1”项下要求。
2.4 分析方法的验证 2.4.1 方法的特异性在选定的LC-MS/MS条件下,方法的特异性色谱图见Fig 2。SBT和dSBT色谱峰的保留时间为1.9 min左右,BT和dBT色谱峰的保留时间为3.0 min左右。空白血浆及空白溶剂均无杂质峰干扰分析物和内标的准确测定;内标及分析物间不存在影响测定准确度的相互干扰。所以本方法可以用于BT和SBT血浆药物浓度的准确测定。

|
| Fig 2 Typical LC-MS/MS chromatograms A:Blank human plasma; B:BT and SBT spiked plasma sample (0.020 59 and 0.016 73 mg·L-1) for LLOQ; C:Methanol solution of standard mixture for BT (1.297 mg·L-1), SBT (1.064 mg·L-1) and IS; D:BT and SBT spiked plasma sample (1.297 and 1.064 mg·L-1) for quality control; E:Plasma sample obtained from a volunteer 3 h after oral administration of pirfenidone tablets containing 200 mg of BT |
按照“2.3.2”项配制处理并测定血浆标准曲线样品,记录色谱图、分析物峰面积As和内标峰面积Ai。以分析物血药浓度C为X轴,以As与Ai的峰面积比值f(f=As/Ai) 为Y轴进行权重回归 (权重系数为1/C2),得BT的标准曲线回归方程为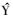

按“2.3.2”项配制处理标准曲线最低点浓度血浆样本 (LLOQ),同时按“2.3.3”项配制处理低、中、高3种浓度的血浆质控样本,每个浓度每批平行制备5个样本,连续制备并测定3批,每批随行一条标准曲线。记录色谱图、分析物峰面积As和内标峰面积Ai。计算As和Ai的比值f(f=As/Ai),将f值代入随行标准曲线求得实测浓度及其Ac%。批内和批间精密度分别用批内 (n=5) 和3批间 (n=15) 的浓度实测值的RSD值表示。考察结果如Tab 1、2所示,结果表明该方法的批内和批间精密度和准确度良好。
| Spiked concentration /mg·L-1 | 0.020 59 | 0.051 90 | 1.297 | 20.27 | |||||
| Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | ||
| Intra-batch (n=5) | Mean | 0.017 94 | 87.13 | 0.053 12 | 102.4 | 1.287 | 99.23 | 19.61 | 96.75 |
| SD | 0.004 71 | 2.29 | 0.002 61 | 5.01 | 0.026 | 2.07 | 1.09 | 5.41 | |
| RSD% | 2.62 | 2.63 | 4.91 | 4.89 | 2.05 | 2.08 | 5.57 | 5.59 | |
| Inter-batch (n=15) | Mean | 0.019 94 | 96.84 | 0.052 51 | 101.2 | 1.302 | 100.4 | 19.37 | 95.56 |
| SD | 0.001 78 | 8.66 | 0.001 95 | 3.76 | 0.039 | 3.03 | 0.86 | 4.26 | |
| RSD% | 8.94 | 8.94 | 3.72 | 3.72 | 3.01 | 3.02 | 4.46 | 4.46 | |
| Spiked concentration /mg·L-1 | 0.016 73 | 0.042 56 | 1.064 | 16.62 | |||||
| Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | ||
| Intra-batch (n=5) | Mean | 0.015 12 | 90.39 | 0.042 16 | 99.08 | 1.037 | 97.42 | 16.40 | 98.69 |
| SD | 0.000 97 | 5.81 | 0.001 26 | 2.98 | 0.035 | 3.25 | 0.82 | 4.93 | |
| RSD% | 6.42 | 6.42 | 3.00 | 3.01 | 3.35 | 3.34 | 5.00 | 5.00 | |
| Inter-batch (n=15) | Mean | 0.015 49 | 92.57 | 0.041 81 | 98.25 | 1.064 | 100.0 | 16.36 | 98.41 |
| SD | 0.000 83 | 4.98 | 0.001 58 | 3.72 | 0.043 | 4.03 | 0.88 | 5.32 | |
| RSD% | 5.37 | 5.37 | 3.78 | 3.78 | 4.02 | 4.02 | 5.39 | 5.41 | |
精密吸取“2.2”项下新鲜配制的BT、SBT、dBT和dSBT储备液 (Ⅰ) 和已于4 ℃冰箱中放置156 d的储备液 (Ⅱ) 适量,分别用甲醇将其稀释至适当浓度后进样分析,每种储备液平行3份。以储备液 (Ⅰ) 稀释液的平均测定值标定储备液 (Ⅱ) 稀释液的浓度,并求其Ac%和RSD%(n=3)。测定结果显示,与储备液 (Ⅰ) 相比,储备液 (Ⅱ) 中SBT、BT、dSBT和dBT的Ac%分别为101.2、100.2、100.7和101.0,RSD%分别为0.71、0.38、0.88和1.76。结果表明,分析物和内标于4 ℃冰箱中放置156 d后仍稳定。
2.4.4.2 血浆样本稳定性按“2.3.3”项配制QA低、中、高3种浓度的血浆质控样本,平行3份。分别考察血浆样本室温放置4 h、-70 ℃冰箱中保存并反复冻融3次、-70 ℃冰箱保存10、29、52 d及样品处理后自动进样器 (8 ℃) 中放置24 h的稳定性。考察结果见Tab 3、4,结果表明在上述各种条件下样品的稳定性良好。
| Spiked concentration /mg·L-1 | 0.051 90 | 1.297 | 20.27 | ||||
| Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | ||
| Short-term (4 h, room temperature) | Mean | 0.052 15 | 100.5 | 1.237 | 95.33 | 19.81 | 97.68 |
| SD | 0.004 48 | 8.65 | 0.053 | 4.03 | 1.35 | 6.64 | |
| RSD% | 5.02 | 5.02 | 4.07 | 4.06 | 2.87 | 2.89 | |
| Freeze and thaw stability (cycle 1) | Mean | 0.051 65 | 99.52 | 1.282 | 98.79 | 19.56 | 96.50 |
| SD | 0.002 59 | 4.99 | 0.052 | 4.01 | 0.56 | 2.79 | |
| RSD% | 5.02 | 5.02 | 4.07 | 4.06 | 2.87 | 2.89 | |
| Freeze and thaw stability (cycle 2) | Mean | 0.055 26 | 106.5 | 19.44 | 95.90 | 1.254 | 96.72 |
| SD | 0.002 04 | 3.93 | 1.08 | 5.32 | 0.060 | 4.66 | |
| RSD% | 3.70 | 3.69 | 5.56 | 5.55 | 4.79 | 4.82 | |
| Freeze and thaw stability (cycle 3) | Mean | 0.053 02 | 102.1 | 1.244 | 95.89 | 18.90 | 93.24 |
| SD | 0.002 01 | 3.84 | 0.020 | 1.52 | 0.30 | 1.49 | |
| RSD% | 3.78 | 3.76 | 1.58 | 1.59 | 1. 60 | 1.60 | |
| Long-term (10 days, -70 ℃) | Mean | 0.052 55 | 101.3 | 1.273 | 98.10 | 19.43 | 95.85 |
| SD | 0.001 63 | 3.18 | 0.011 | 0.86 | 0.90 | 4.41 | |
| RSD% | 3.11 | 3.14 | 0.87 | 0.87 | 4.61 | 4.60 | |
| Long-term (29 days, -70 ℃) | Mean | 0.056 12 | 108.1 | 1.318 | 101.6 | 18.91 | 93.25 |
| SD | 0.002 32 | 4.45 | 0.018 | 1.35 | 0.44 | 2.19 | |
| RSD% | 4.13 | 4.11 | 1.37 | 1.33 | 2.34 | 2.34 | |
| Long-term (52 days, -70 ℃) | Mean | 0.054 88 | 105.7 | 1.341 | 103.3 | 18.77 | 92.56 |
| SD | 0.001 01 | 1.9 | 0.028 | 2.2 | 0.95 | 4.65 | |
| RSD% | 1.85 | 1.83 | 2.10 | 2.08 | 5.04 | 5.02 | |
| Post-preparative stability/24 h, 8℃ | Mean | 0.053 18 | 102.5 | 1.261 | 97.21 | 19.09 | 94.20 |
| SD | 0.000 67 | 1.31 | 0.061 | 4.70 | 0.83 | 4.08 | |
| RSD% | 1.26 | 1.28 | 4.81 | 4.83 | 4.34 | 4.33 | |
| Spiked concentration /mg·L-1 | 0.051 90 | 1.297 | 20.27 | ||||
| Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | Measured/mg·L-1 | Accuracy/% | ||
| Short-term (4 h, room temperature) | Mean | 0.040 92 | 96.14 | 0.961 3 | 90.35 | 16.42 | 98.78 |
| SD | 0.000 66 | 1.55 | 0.046 7 | 4.39 | 1.16 | 7.02 | |
| RSD% | 1.61 | 1.63 | 4.86 | 4.85 | 7.07 | 7.10 | |
| Freeze and thaw stability (cycle 1) | Mean | 0.041 87 | 98.41 | 1.040 | 97.70 | 16.56 | 99.61 |
| SD | 0.001 55 | 3.65 | 0.046 | 4.33 | 0.68 | 4.03 | |
| RSD% | 3.71 | 3.71 | 4.46 | 4.43 | 4.08 | 4.04 | |
| Freeze and thaw stability (cycle 2) | Mean | 0.044 27 | 104.0 | 16.82 | 101.2 | 1.056 | 99.23 |
| SD | 0.000 64 | 1.51 | 0.90 | 5.41 | 0.04 | 4.14 | |
| RSD% | 1.45 | 1.46 | 5.35 | 5.34 | 4.14 | 4.17 | |
| Freeze and thaw stability (cycle 3) | Mean | 0.041 41 | 97.31 | 1.021 | 95.90 | 16.80 | 101.1 |
| SD | 0.000 77 | 1.81 | 0.034 | 3.17 | 0.05 | 0.26 | |
| RSD% | 1.86 | 1.86 | 3.31 | 3.31 | 0.28 | 0.26 | |
| Long-term (10 days, -70 ℃) | Mean | 0.042 74 | 100.4 | 1.042 | 97.96 | 16.84 | 101.3 |
| SD | 0.002 05 | 4.81 | 0.009 | 0.81 | 0.52 | 3.14 | |
| RSD% | 4.79 | 4.79 | 0.84 | 0.83 | 3.10 | 3.10 | |
| Long-term (29 days, -70 ℃) | Mean | 0.041 15 | 96.67 | 1.053 | 98.96 | 15.73 | 94.65 |
| SD | 0.001 41 | 3.30 | 0.016 | 1.47 | 0.40 | 2.42 | |
| RSD% | 3.44 | 3.41 | 1.53 | 1.49 | 2.57 | 2.55 | |
| Long-term (52 days, -70 ℃) | Mean | 0.044 22 | 103.9 | 1.082 | 101.6 | 16.05 | 96.52 |
| SD | 0.001 36 | 3.2 | 0.018 | 1.7 | 0.71 | 4.27 | |
| RSD% | 3.08 | 3.07 | 1.66 | 1.66 | 4.42 | 4.43 | |
| Post-preparative stability (24 h, 8℃) | Mean | 0.042 72 | 100.4 | 1.073 | 100.8 | 17.14 | 103.1 |
| SD | 0.001 79 | 4.19 | 0.046 | 4.30 | 1.02 | 6.11 | |
| RSD% | 4.19 | 4.18 | 4.28 | 4.27 | 5.93 | 5.93 | |
按“2.3.3”项配制处理并测定低、中、高3种浓度的血浆质控样本,每个浓度平行3个样本。记录色谱图、分析物峰面积 (As)B和内标峰面积 (Ai)B,计算其峰面积比值fB[fB=(As)B/(Ai)B]。按“2.3.1”项处理获得空白血浆洗脱液若干用于配制未经提取含药血浆样品。分别精密吸取低、中、高质控工作液各20 μL于1.5 mL EP管中,向其中分别依次加入内标工作液20 μL、空白血浆洗脱液960 μL,涡旋混匀,吸取上清液300 μL,加入流动相700 μL,涡旋混匀后进行LC-MS/MS分析。每个浓度平行3个样本。记录色谱图、分析物峰面积 (As)A和内标峰面积 (Ai)A,计算其峰面积比值fA[fA=(As)A/(Ai)A],并求算同一浓度样品的比值平均值 (fA)mean(n=3)。分析物的相对提取回收率REC=fB/(fA)mean。结果显示:SBT低、中、高3个浓度血浆质控样本的平均提取回收率分别为94.32%、90.72%和88.73%,RSD分别为3.01%、1.45%和3.25%;BT低、中、高3个浓度血浆质控样本的平均提取回收率分别为106.4%、105.3%和101.9%,RSD分别为3.07%、1.32%和3.91%。结果表明,该方法BT和SBT的提取回收率精密且可重现。
2.4.6 基质效应按“2.3.1”项处理6种不同来源的空白血浆,获得其相应的空白血浆洗脱液。分别精密吸取低、中、高质控工作液各20 μL于1.5 mL EP管中,向其中分别依次加入内标工作液20 μL、甲醇960 μL,涡旋混匀,涡旋混匀,吸取上清液300 μL,加入流动相700 μL,涡旋混匀后进行LC-MS/MS分析。每个浓度平行3个样本。记录色谱图、分析物峰面积 (As)C和内标峰面积 (Ai)C。计算分析物基质因子fA=As/(As)C,内标基质因子fi=Ai/(Ai)C,进一步计算经内标归一化的基质因子fAi=(fA)mean/(fi)mean。结果显示:SBT低、中、高3个浓度血浆质控样本的平均归一化基质因子分别为102.5%、95.16%和102.7%,RSD分别为11.23%、3.96%和1.34%;BT低、中、高3个浓度血浆质控样本的平均归一化基质因子分别为96.33%、95.30%和101.3%,RSD分别为2.30%、3.65%和1.79%。结果表明,该方法中SBT和BT的基质效应精密且可重现。
2.4.7 分析系统残留在进样标准曲线ULOQ样品后设置进样空白甲醇样品,记录色谱图,考察分析物的系统残留。考察结果显示,其色谱图中BT、SBT、dBT和dSBT保留时间附近均无明显干扰峰存在。这表明,在选定的LC-MS/MS条件下,系统的残留效应在可接受范围内,不影响测定准确度。
2.5 应用36名健康受试者,男女各半,签署知情同意书,并经南京中医药大学附属医院伦理委员会审批同意,均分为低、中、高3个剂量组进行药代动力学实验。3组分别口服剂量为200、400、600 mg的BT片,采集口服前、口服开始后10、20、30、45 min和1.0、1.5、2、3、4、6、8、12 h由肘静脉取血4 mL置肝素化采血管中,混匀,离心 (3 000 r·min-1,4 ℃,10 min),分离上层血浆,将血浆分成两等份,转移至EP管中,于-70 ℃冰箱中保存待测。测定结果显示,低、中、高3个剂量组的BT血药浓度范围分别为0.025 06~3.887 mg·L-1,0.04278~5.19mg·L-1,0.045 26~6.792 mg·L-1;SBT血药浓度范围分别为0.031 19~4.854 mg·L-1,0.040 19~14 mg·L-1,0.065 07~9.965 mg·L-1。上述结果表明,所建立的BT和SBT血药浓度LC-MS/MS分析测定方法适用于BT和SBT人体药代动力学的系统研究。
3 讨论本研究建立并验证了同时测定人血浆中BT和SBT的LC-MS/MS方法,与先前报道的测定BT的LC-UV和LC-MS/MS方法相比,均具有一些改进之处。与LC-UV相比,该方法分析时间大幅度缩短,仅在4 min内便实现了对BT、SBT及其内标的完全分离;而与先前LC-MS/MS法相比,本方法同时对人血浆中BT和SBT浓度实现准确测定,从而可更全面地监测BT在机体内的代谢和消除情况。此外该方法采用dBT和dSBT作为定量用内标,使得方法的稳定性和准确度更加良好;同时相比分析物而言,我们采用了不同的离子对监测同位素内标,消除了内标和分析物间的相互干扰,使得方法具有良好的特异性;而储备液稳定性考察结果则表明分析物和同位素内标均很稳定。
3个不同剂量组的人体药代动力学研究中血药浓度测定结果显示,所有样品中BT和SBT的血药浓度均可在方法的线性范围内得到准确测定,充分证明了该方法在BT人体药动学和生物等效性等相关研究中的适用性。
| [1] | Schaefer C J, Ruhrmund D W, Pan L, et al. Antifibrotic activities of pirfenidone in animal models[J]. Eur Respir Rev, 2011, 20(120): 85-97. doi:10.1183/09059180.00001111 |
| [2] | 陈钰清, 闫永吉, 仇美华, 等. 吡非尼酮抗纤维化作用的研究进展[J]. 临床药物治疗杂志, 2016, 14(5): 1-7. Chen Y Q, Yan Y J, Qiu M H, et al. Research progress on antifibrotic effect of pirfenidone[J]. Clin Med J, 2016, 14(5): 1-7. |
| [3] | Margaritopoulos G A, Vasarmidi E, Antoniou K M. Pirfenidone in the treatment of idiopathic pulmonary fibrosis: an evidence-based review of its place in therapy[J]. Core Evid, 2016, 11: 11-22. doi:10.2147/CE |
| [4] | King T E Jr, Bradford W Z, Castro-Bernardini S, et al. A phase 3 trial of pirfenidone in patients with idiopathic pulmonary fibrosis[J]. N Engl J Med, 2014, 370(22): 2083-92. doi:10.1056/NEJMoa1402582 |
| [5] | 刘传梅, 蔡后荣. 特发性肺纤维化药物治疗进展[J]. 临床药物治疗杂志, 2015, 13(3): 1-4. Liu C M, Cai H R. Progress in treatment for idiopathic pulmonary fibrosis[J]. Clin Med J, 2015, 13(3): 1-4. |
| [6] | Azuma A. Pirfenidone: antifibrotic agent for idiopathic pulmonary fibrosis[J]. Expert Rev Respir Med, 2010, 4(3): 301-10. doi:10.1586/ers.10.32 |
| [7] | Huang N Y, Ding L, Wang J, et al. Pharmacokinetics, safety and tolerability of pirfenidone and its major metabolite after single and multiple oral doses in healthy Chinese subjects under fed conditions[J]. Drug Res (Stuttg), 2013, 63(8): 388-95. doi:10.1055/s-00023610 |
| [8] | Togami K, Kanehira Y, Tada H. Possible involvement of pirfenidone metabolites in the antifibrotic action of a therapy for idiopathic pulmonary fibrosis[J]. Biol Pharm Bull, 2013, 36(10): 1525-7. doi:10.1248/bpb.b13-00452 |
| [9] | 陈敏纯, 王茂湖, 曹青, 等. 高效液相色谱法测定人血浆中吡非尼酮的含量[J]. 中国新药与临床杂志, 2013, 32(6): 473-6. Chen M C, Wang M H, Cao Q, et al. Determination of pirfenidone in human plasma by HPLC[J]. Chin J New Drugs Clin Rem, 2013, 32(6): 473-6. |
| [10] | 师少军, 吴健鸿, 陈汇, 等. 高效液相色谱法测定人血浆吡非尼酮浓度[J]. 中国药学杂志, 2011, 46(2): 138-41. Shi S J, Wu J H, Chen H, et al. Determination of pirfenidone in human plasma by HPLC[J]. Chin Pharm J, 2011, 46(2): 138-41. |
| [11] | 何秀玲, 许馨文, 张明, 等. 吡非尼酮在中国健康受试者单剂量及多剂量的药动学研究[J]. 中国药学杂志, 2015, 50(13): 1134-7. He X L, Xu X W, Zhang M, et al. Pharmacokinetics of pirfenidone after a single dose and multiple-dose administration in Chinese healthy volunteers[J]. Chin Pharm J, 2015, 50(13): 1134-7. |
| [12] | 刘泽娟, 赵萍, 陈娟, 等. LC-MS/MS法测定人血浆中甲磺酸雷沙吉兰的浓度及其体内药动学研究[J]. 中国药理学通报, 2016, 32(7): 1017-22. Liu Z J, Zhao P, Chen J, et al. Determination of rasagiline mesylate in human plasma by LC-MS/MS and its pharmacokinetics study[J]. Chin Pharmacol Bull, 2016, 32(7): 1017-22. |
| [13] | 李长印, 储继红, 张军, 等. LC-MS/MS法测定人血浆中羟基红花黄色素A的浓度[J]. 中国药理学通报, 2014, 30(10): 1402-7. Li C Y, Chu J H, Zhang J, et al. Determination of hydroxysafflor yellow A in human plasma by LC-MS/MS analysis[J]. Chin Pharmacol Bull, 2014, 30(10): 1402-7. doi:10.3969/j.issn.1001-1978.2014.10.016 |

