


黄连碱 (coptisine,COP) 为毛茛科植物黄连中重要有效成分[1-2],是一类具有季铵基团的异喹啉类生物碱,研究表明具有抗菌、抗炎[3-4]等多种活性[5-7]。前期体外抗炎结果表明黄连碱可剂量依耐性的抑制内毒素刺激的炎症反应,为进一步明确其在整体动物水平的抗炎作用的量效关系及作用时间窗,我们采用药动学 (PK)-药效学 (PD) 结合模型的研究方法,以定量描述黄连碱在内毒素 (LPS) 致炎大鼠体内的血药浓度-药效作用的关系。
在细菌内毒素感染过程中,机体中炎症因子IL-1β、TNF-ɑ等合成大量增加,使室周器和下丘脑区域的PGE2合成增加从而使体温升高[8-11],并引起全身性炎症反应。因此在药物抗炎作用研究中,体温可作为最为直接、最宏观的药效评价指标。PK-PD结合模型能有效阐述“浓度-时间-效应”三者之间的关系,能更好地认识体内药物的作用机制,对于优选临床给药方案、疗效预测等领域具有重要的参考价值[12]。
1 材料与仪器 1.1 药品与试剂黄连碱对照品 (批号MUST-15011004, 纯度≥0.9999,成都曼思特生物科技有限公司);黄连碱注射液 (由本实验室自制,热源和渗透压符合要求);盐酸小檗碱对照品 (批号110713-200208,中国药品生物制品检定所);内毒素 (批号032M4082V,Sigma);除甲醇、乙腈和甲酸为色谱级外,其余试剂均为分析纯。
1.2 仪器SHIMADZU UPLC LC-30超高效液相色谱仪;AllegraX-30R Centrifuge高速冷冻离心机 (BECKMAN COULTER);MTN-2800W氮吹仪 (AUTO-SIENCE);TSO电子体温计 (豪展医疗科技有限公司)。
1.3 动物SPF级SD大鼠,♂,体质量 (220~240) g,由四川省医学科学院实验动物研究所提供,动物许可证号SCXK (川) 2013-15。动物饲养环境温度 (24±2)℃,40%~80%湿度,12 h昼夜交替循环,自由进食和给水。所有动物在实验前适应饲养环境3 d,大鼠实验前3 d每天测肛温2次,使其适应操作,实验前12 h禁食不禁水。
2 方法 2.1 色谱条件色谱柱Agilent Eclipse Plus C8(3.0 mm×150 mm, 1.8 μm);流动相:乙腈 (A)-0.1%甲酸水溶液 (B);流速:0.7 mL·min-1;紫外检测波长:345 nm;梯度洗脱:0~10 min,90%B~60%B;10~20 min,60%B;20~25 min,90%B;进样量80 μL;柱温40℃。
2.2 血浆预处理取50 μL血浆样品,加入261.0 μg·L-1小檗碱甲醇溶液10 μL,涡旋2 min,加入NaOH (1 mmol·L-1)10 μL溶液,涡旋1 min,加入200 μL乙腈,涡旋2 min,超声60 s。13 000 r·min-1离心10 min后,上清N2吹干,加入乙腈-0.1%甲酸水溶液 (40:60,V/V)100 μL复溶,13 000 r·min-1离心10 min.取上清为供试品溶液。
2.3 分组与给药动物实验前3 d连续测试大鼠肛温,以平均体温为基础体温值,剔除体温超过38℃或连续两次体温相差大于0.5℃的大鼠,筛选出合格大鼠根据其基础体温和体质量随机分为模型组、黄连碱高剂量组、黄连碱低剂量组,每组3只动物。于实验前1 h内测肛温4次,剔除应激的高体温数值,选取基础平均值为大鼠的基础体温。各组大鼠均尾静脉注射含100 μg·kg-1 LPS无菌生理盐水溶液,30 min后,高、低剂量组大鼠分别以3.87 mg·kg-1和1.93 mg·kg-1尾静脉注射黄连碱注射液,模型组大鼠给予等体积的注射剂溶媒。
2.4 药效学及药动学指标采集分别于注射LPS后0.5、1、1.5、2、3、4、5、6、8、12 h测定肛温,并在注射LPS后0.667、1、2、4、6、8、12、24 h尾静脉取血0.3 mL,置于肝素化离心管中,放于37 ℃水浴30 min,于4 ℃、3 500 r·min-1离心15 min后分离血浆,取上清分装50 μL保存于-80 ℃冰箱中,直至分析。
2.5 数据分析黄连碱浓度和解热抗炎效应与时间变化关系使用Monolix version 4.3.3软件应用群体方法分析,PK-PD模型中个体参数均假定服从对数正态分布,误差模型均采用线性比例模型。按照软件使用说明,低于定量限的浓度点在拟合时标注为LLQ,于拟合时采用半定量已知加以处理。
2.5.1 PK模型黄连碱体内动力学性质通过房室模型描述,即采用一、二、三房室进行拟合,以-2对数似然值 (-2LL)、最小化信息量 (AIC)、贝叶斯信息准则 (BIC) 为主要拟合优度参数的标准,选择拟合优度最高的PK模型。
2.5.2 PD模型采用以下微分方程表示[8]造模后大鼠体温的变化:
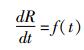
|
(1) |
dR/dt代表造模后体温的变化率;表示造模后体温变化的模拟函数,比较多种的函数形式,并结合观察LPS致炎后模型组大鼠体温变化值时量曲线,最终采用高斯函数作为模拟函数。高斯函数是正态分布的密度函数,其函数方程表示为:
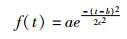
|
(2) |
其中a、b、c均为常数:a代表曲线峰的高度;b代表峰中心位置,c代表峰的半最大值的全宽。对此PD模型而言,a的生物学意义可表征为最大体温升高率,b代表出现最大体温升高率的出现时间点,c为最大体温升高率出现时间点的标准差。
给药组大鼠体温变化由以下方程 (3) 表示,为黄连碱对温度变化的抑制效应 (COP) 带入上述的微分方程 (1) 所得。
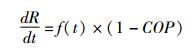
|
(3) |
基于药物效应动力学理论,COP可采用线性、对数线性、Emax以及Sigmod Emax不同的PD模型拟合,分析黄连碱血药浓度对内毒素大鼠体温变化的影响。
3 结果 3.1 血浆样本中黄连碱的检测方法采用前述的血浆样品分析方法,用加权 (1/ci2) 最小二乘法进行回归分析,得标准曲方程为
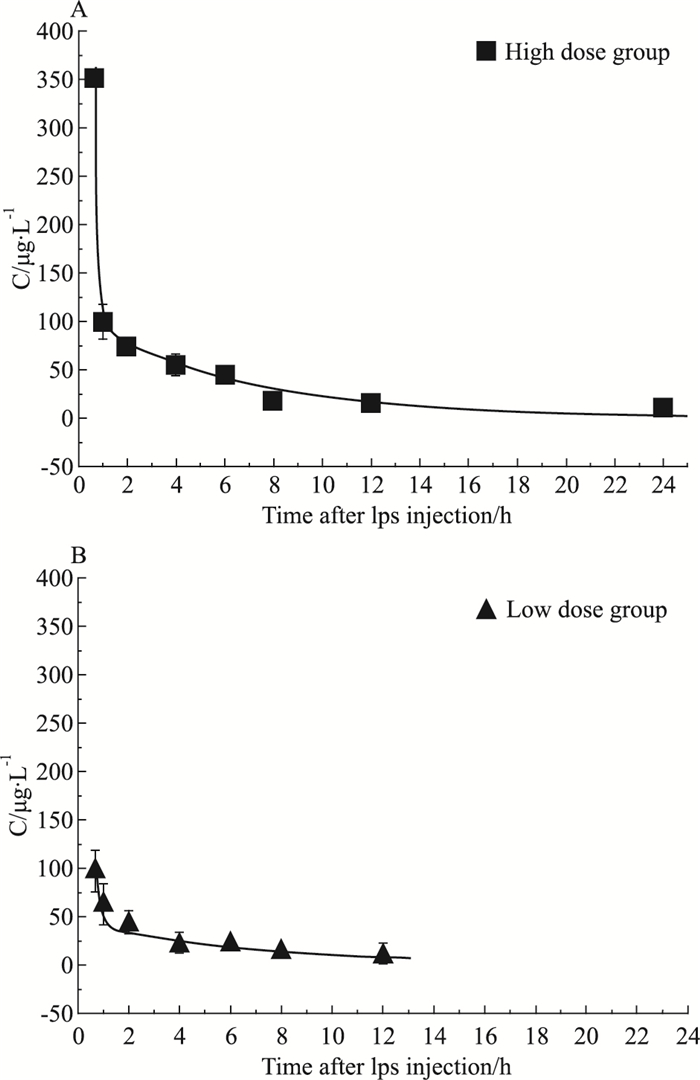
黄连碱PK以二房室模型较优,PK-PD总模型拟合的药时曲线如Fig 1所示。给予黄连碱注射液10 min后,黄连碱高、低剂量的平均血药浓度峰值分别为 (351.1±97.46) μg·L-1、(97.63±21.53) μg·L-1。
|
| Fig 1 Time course of mean plasma concentrations fitting results of coptisine A and B represent pharmacokinetics of coptisine for high dose group and low dose group, respectively (Symbols represent mean observed data, lines represent typical model predictions, and vertical lines represent standard deviations) |
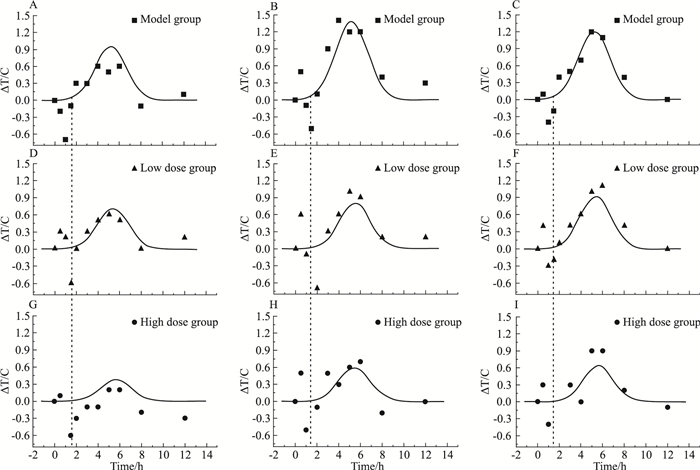
PK-PD总模型拟合的大鼠各个体体温变化值曲线如Fig 2所示。各组大鼠造模前平均体温为 (37.33±0.10)℃,差异无统计学意义 (P > 0.05)。模型组大鼠于注射内毒素 (5.5±0.5) h时,体温上升的最大值为 (38.27±0.30)℃,随后逐渐下降,于12 h时测定的体温值为 (37.43±0.06)℃;黄连碱高、低剂量组分别在注射内毒素后的最高体温值为 (37.97±0.35)℃和 (38.2±0.26)℃,具有一定的剂量依赖性。
|
| Fig 2 Fitting results of rectal △T after lps injection A、B、C-shows fitting results of body temperature in model group; D、E、F and G、H、I-represent fitting results of body temperature for low dose group and high dose group, respectively. (symbols, mean observations; lines, typical model predictions) |
最终采用Emax函数表征了黄连碱对体温升高的抑制作用,在个体参数均为对数正态分布的设定下,进行了无协变量的群体PK-PD模型拟合,最终模型拟合的AIC值是564.73,BIC值为568.67,-2对数似然函数值 (-2LL) 为524.73,说明该模型拟合度较精确。所得模型参数拟合值如Tab 1所示,PK拟合结果如Fig 1所示,个体温度变化拟合结果如Fig 2所示。
| Parameter | Estimate | s.e.(lin) | r.s.e./% |
| V/L·kg-1 | 14.2 | 2.13 | 15 |
| K/h-1 | 0.395 | 0.067 | 17 |
| K12/h-1 | 2.56 | 0.98 | 38 |
| K21/h-1 | 2.51 | 0.38 | 15 |
| a/℃·h-1 | 1.22 | 0.21 | 17 |
| b/h | 5.21 | 0.21 | 4 |
| c/h | 2.1 | 0.28 | 13 |
| Emax/℃ | 1.88 | 3.3 | 178 |
| EC50/μg·L-1 | 89.7 | 240 | 267 |
| Precision of the estimates is expressed as relative standard error (r.s.e.), (r.s.e.) is standard error (s.e.) divided by the parameter estimate | |||
本研究选取体温作为药效学衡量指标,观察大鼠给药后不同时间点的体温变化与血药浓度关系。在进行PD建模时,参照有关以体温为PD指标的PK-PD建模文献,比较了线性、线性分段函数、二次函数等方法刻画和表征温度变化值,但PD模型拟合均较差。分析个体体温变化的时量曲线,发现其在最初体温下降段过后均多呈现高斯型变化,因此最终采用了高斯函数表征了这种体温变化。最终拟合结果也表明,对实验大鼠的各个体,在LPS造模后1.5 h的温度变化拟合较佳,对前期 (Fig 2竖线前时间点) 拟合较差。但考虑到黄连碱为0.5 h给药,其解热作用主要体现为1.5 h后对升温作用的抑制,因此最终的PK-PD模型仍保证了对药物浓度与作用的较为精确的刻画。同时,高斯函数各参数的生理意义在建模也可合理解释,拟合结果也表明采用这一函数计算的各体温变化最大值与最大时也与观测结果一致。
黄连碱解热作用EC50群体值为89.7 μg·L-1,Emax大小为1.88 ℃, 表明黄连碱具有较强的解热效能和较优的效价强度。本室前期研究表明大黄酸和黄芩苷解热作用的Emax分别为1.283 ℃[13]和0.56 ℃[14],黄连碱解热效能分别是大黄酸和黄芩苷的1.5和3.4倍,表明黄连碱解热效能明显优于大黄酸和黄芩苷。这一结果也与相关的细胞实验结果较为吻合。但同时注意到,文献报道黄连碱口服绝对生物利用度为8.9%[7],远低于大黄酸和黄芩苷的绝对生物利用度 (23.8%[15]和23.67%[16])。因此,提高一些中药或复方中高活性物质的生物利用度,可能是改善整体疗效的一个重要研究方向。
研究表明黄连碱LD50约为7.74 mg·kg-1[17-18],因此本实验考察了不同剂量黄连碱给药的解热作用,结果表明1/2 LD50(3.87 mg·kg-1) 和1/4 LD50(1.93 mg·kg-1) 解热作用较为明显,1/8 LD50解热作用已较差,因此最终实验采用了1/2和1/4 LD50作用高低剂量。在此剂量下黄连碱静注后消除速率常数为0.395 h-1,表明该药物具有代谢快、机体内保留时间短等特点,与文献报道的黄连碱药代动力学特点一致[7]。
综上所述,本研究建立的PK-PD模型研究结果表明黄连碱的解热作用具有效能高和效价强的特点,提示改善其非血管给药时的生物利用度可能是提高相关中药疗效的重要研究方向。
( 致谢: 本实验在成都中医药大学药理学实验室设计并完成研究,衷心感谢本研究室各位同学、老师在实验中给予的指导与帮助。 )
| [1] | 马航, 胡慭然, 邹宗尧, 等. 黄连生物碱降糖作用研究及构效关系初探[J]. 中国药理学通报, 2015, 31 (11): 1575-9. Ma H, Hu Y R, Zou Z Y, et al. Preliminary evaluation of antihyper-glycemic effect Rhizoma coptidis alkaloids and their structure-activity relation-ships[J]. Chin Pharmacol Bull, 2015, 31 (11): 1575-9. doi:10.3969/j.issn.1001-1978.2015.11.019 |
| [2] | 邹宗尧, 王燕枝, 胡慭然, 等. 黄连生物碱促小鼠睡眠实验研究[J]. 中国药理学通报, 2014, 30 (12): 1752-6. Zou Z Y, Wang Y Z, Hu Y R, et al. Study of Rhizoma Coptidisalkaloids on promoting sleep in mice[J]. Chin Pharmacol Bull, 2014, 30 (12): 1752-6. doi:10.3969/j.issn.1001-1978.2014.12.027 |
| [3] | Wu J, Zhang H, Hu B, et al. Coptisine from Coptischinensis inhibits production of inflammatory mediators in lipopolysaccharide-stimulated RAW 264.7 murine macrophage cells[J]. Eur J Pharmacol, 2016, 780: 106-14. doi:10.1016/j.ejphar.2016.03.037 |
| [4] | Zou Z Y, Hu Y R, Ma H, et al. Coptisine attenuates obesity-related inflammation through LPS/TLR-4-mediated signaling pathway in Syrian golden hamsters[J]. Fitoterapia, 2015, 105: 139-46. doi:10.1016/j.fitote.2015.06.005 |
| [5] | 陈柏年, 于晓彦, 孙加琳, 等. 黄连碱对L-NAME诱导高血压大鼠胸主动脉功能的影响[J]. 中国药理学通报, 2011, 27 (5): 610-3. Chen B N, Yu X Y, Sun J L, et al. Effect of coptisine on the function of isolated thoracic aorta of L-NAME induced hypertensive rats[J]. Chin Pharmacol Bull, 2011, 27 (5): 610-3. |
| [6] | Jung H A, Min B S, Yokozawa T, et al. Anti-Alzheimer and antioxidant activities of CoptidisRhizoma alkaloids[J]. Biol Pharm Bull, 2009, 32 (8): 1433-8. doi:10.1248/bpb.32.1433 |
| [7] | Su J, Miao Q, Miao P, et al. Pharmacokinetics and brain distribution and metabo-lite identification of coptisine, a protoberberine alkaloid with therapeutic potential for CNS disorders, in Rats[J]. Biol Pharm Bull, 2015, 38 (10): 1518-28. doi:10.1248/bpb.b15-00293 |
| [8] | Josa M, Urizar J P, Rapado J, et al. Pharmacokinetic/pharmacodynamic modeling of antipyretic and anti-inflammatory effects of naproxen in the rat[J]. J Pharmacol Exp Ther, 2001, 297 (1): 198-205. |
| [9] | 王宏, 刘刚, 符炜, 等. Nrf2在丙泊酚抑制内毒素性急性肺损伤中的作用[J]. 中国药理学通报, 2013, 29 (9): 1286-90. Wang H, Liu G, Fu W, et al. Effect of Nrf2 on propofol inhibiting lipopolysaccharide-induced acute lung injury in mice[J]. Chin Pharmacol Bull, 2013, 29 (9): 1286-90. |
| [10] | 和晓韵, 底妍, 张利东, 等. 沉默PDE4B对内毒素刺激的小胶质细胞内cAMP的影响[J]. 中国药理学通报, 2013, 29 (11): 1541-5. He X Y, Di Y, Zhang L D, et al. Effect of siRNA-mediated silencing of phosphodiesterase 4B expression on concentration of cAMP in endotoxin-stimulated primary cultured micoglia[J]. Chin Pharmacol Bull, 2013, 29 (11): 1541-5. doi:10.3969/j.issn.1001-1978.2013.11.016 |
| [11] | 王旭垒, 王雪, 蒋维, 等. Ghrelin拮抗LPS诱导的肝细胞损伤的保护作用[J]. 中国药理学通报, 2013, 29 (4): 486-90. Wang X L, Wang X, Jiang W, et al. Protective effect of Ghrelin against LPS-induced liver cell injury[J]. Chin Pharmacol Bull, 2013, 29 (4): 486-90. |
| [12] | Voss L J, Ludbrook G, Grant C, et al. A comparison of pharmacokinetic/pharmaco-dynamic versus mass-balance measurement of brain concentrations of intravenous anesthetics in sheep[J]. Anesth Analg, 2007, 104 (6): 1440-6. doi:10.1213/01.ane.0000263274.62303.1a |
| [13] | 李红, 张艳, 于宜平, 等. 大黄解热作用与降低血浆一氧化氮作用的PK-PD研究[J]. 中国中药杂志, 2013, 38 (8): 1231-6. Li H, Zhang Y, Yu Y P, et al. Pharmacokinetic /pharmacodynamic modeling of antipyretic and reducingplasma concentration of NO effects of Rheum palmatum in rat[J]. China J Chin Mater Med, 2013, 38 (8): 1231-6. |
| [14] | 于宜平, 张艳, 李红, 等. 黄芩苷对角叉菜胶致热大鼠解热作用的PK-PD模型研究[J]. 中草药, 2014, 45 (4): 527-31. Yu Y P, Zhang Y, Li H, et al. Pharmacokinetic-pharmacodynamic study on antipyretic effects of baicalin on carrageenan-induced pyrexia of rats[J]. Chin Trad Herbal Drugs, 2014, 45 (4): 527-31. |
| [15] | 张锦雯, 孙建国, 王广基, 等. 大黄酸在大鼠和比格犬体内的吸收动力学研究[J]. 中国临床药理学与治疗学, 2010, 15 (5): 511-8. Zhang J W, Sun J G, Wang G J, et al. Pharmacokinetic comparision in absorption of Rhein in SD rats and Beagle dogs[J]. Chin J Clin Pharmacol Ther, 2010, 15 (5): 511-8. |
| [16] | 龚明涛, 虞丽芳, 陈庆华, 等. 黄芩苷在大鼠体内的口服生物利用度屏障研究[J]. 中国药学杂志, 2008, 43 (17): 1332-5. Gong M T, Yu L F, Chen Q H, et al. Study on oral bioavailability of Baicalin in rats[J]. Chin Pharm J, 2008, 43 (17): 1332-5. doi:10.3321/j.issn:1001-2494.2008.17.012 |
| [17] | Kheir M M, Wang Y, Hua L, et al. Acute toxicity of berberine and its correlation with the blood concentration in mice[J]. Food Chem Toxicol, 2010, 48 (4): 1105-10. doi:10.1016/j.fct.2010.01.033 |
| [18] | Yi J, Ye X, Wang D, et al. Safety evaluation of main alkaloids from RhizomaCoptidis[J]. J Ethnopharmacol, 2013, 145 (1): 303-10. doi:10.1016/j.jep.2012.10.062 |

