


2. 英属哥伦比亚大学脑研究中心,温哥华,BC V6T 2B5,加拿大
2. Centre for Brain Health, University of British Columbia, 2211 Wesbrook Mall, Vancouver, BC V6T2B5, Canada
神经性疼痛是一种神经系统原发损害或功能障碍引起的慢性疼痛疾病,常见于糖尿病性神经痛 (Diabetic neuropathic pain, DNP)、带状疱疹后遗神经痛 (post-herpetic neuralgina, PHN)、艾滋病相关的神经性疼痛、神经性腰背部疼痛、癌症相关的神经痛、复合性局部疼痛综合征和术后神经痛等疾病。由于许多神经性疼痛确切病因较为复杂,可选择的针对神经性疼痛的治疗药物也较为有限,且大多疗效不确切。
研究提示,芳香类药用植物中的某些单萜类、倍半萜、三萜类等芳香成分具有抗炎镇痛的功效[1]。其中,天然的呈香化合物香叶醇,又名“牻牛儿醇”,化学名称为反-3, 7-二甲基-2, 6-辛二烯-1-醇,是橙花醇的顺式异构体,结构上属于单萜烯醇类化合物,具有单萜类化合物的某些结构特点,可能具有潜在的镇痛效用。香叶醇天然存在于牻牛儿苗科天竺葵属香叶天竺葵 (Pelargonium gravedens Her),禾本科香茅属 (Cymbopogon) 亚香茅、柠檬草、枫茅、爪哇香茅等,樟科木姜子属 (Litsea Lam.) 山苍子的果实,蔷薇科蔷薇属 (Rosaceae) 玫瑰的花,茜草科栀子属 (Gardenia) 栀子 (GardeniajasminoidesEllis.) 等250多种植物中。天然提取物中,以香叶 (精) 油[oil of geranium (Pelargonium gravedens Her.)]中的香叶醇含量较高,广泛应用于药物、烟草、食品配料等领域[2-4]。已有研究发现香叶醇在抗肿瘤、平喘、抗菌,驱蚊等方面具有潜在的药学应用价值[4]。但目前还少见香叶醇对镇痛作用的研究报道。
我们在对香叶醇的研究中,发现了其对实验性神经病理性疼痛的良好镇痛效果,本文将展示香叶醇在实验性神经痛模型上的镇痛效果和并对可能的作用机制进行初步探讨,测试其对痛觉相关的钠离子通道和瞬时受体电位通道的影响, 以期通过我们的努力,深入挖掘香叶醇的药用价值,推动其作为药物先导化合物开发神经痛镇痛新药的可能性,同时也为神经病理性疼痛症的治疗提供参考。
1 材料 1.1 动物实验动物为成年SD大鼠,♂,(200±20) g,由上海斯莱克实验动物有限公司提供。动物实验许可证号SYXK (沪)2013-0040。饲养条件为封闭式通气笼分笼饲养,自由摄食和饮水,室温保持在20℃~25℃,湿度60%,每日光照与黑暗时间均为12 h。饲养和手术操作等按照国家动物福利与保护相关规定进行。
1.2 细胞株稳定表达重组hNav1.7通道蛋白的HEK293(pcDNA3.1-hNav1.7) 细胞株,稳定表达重组hTRPA1通道蛋白的HEK293(pcDNA3.1-hTRPA1) 细胞株,由中国科学院上海药物研究所提供。
1.3 试剂耗材香叶醇 (TCI)、盐酸利多卡因一水合物 (Sigma),植物油 (国产葵花子油)、氨苄青霉素 (鼎国生物),DMEM培养基 (Gibco)、胎牛血清 (Gibco)、Poly-D-lysine (分子质量70 000~150 000)(Sigma),胰蛋白酶 (含EDTA)(sigma),抗体anti-NeuN MAb (Milipore Anti-NeuN,Clone A60),荧光 (Cy3) 标记羊抗小鼠IgG-Cy3,其它化学试剂均为国产分析纯。细胞培养皿、移液管等 (Greiner),医用真丝编织线,规格:3-0(上海金环),带线缝合针 (规格4-0,灭菌型)(上海金环) 等。
1.4 仪器设备电子Von frey足底测试仪 (Ugo basile),Axon常规膜片钳系统Axopatch 200B (Molecular Devices),实验动物剔毛器,CO2通气恒温细胞培养箱 (Thermofisher),倒置式台式荧光显微镜 (OLYMPUS CKX41),-80℃超低温冰箱 (Thermo),眼科剪、眼科镊、显微镊等手术器械 (上海医疗器械批发部)。
2 方法 2.1 坐骨神经保留性损伤 (spared nerve injury, SNI) 模型的建立参考Richner等[5]以及Shields等[6]的方法,使用1%戊巴比妥钠腹腔注射 (按40 mg·kg-1体质量给药) 麻醉成年SD大鼠,剔除左后肢外侧面坐骨神经相应位置被毛,纵向切开剔毛区皮肤,钝性分离股二头肌,暴露坐骨神经及其3个分支:胫神经、腓总神经和腓肠神经;分别双重结扎胫神经、腓总神经,在双重结扎的中央切断,并分别去除末端2~4 mm的神经干;术中避免接触或牵拉腓肠神经,保持其完整;术后分层缝合伤口,抗生素抗炎。假手术对照组则只暴露坐骨神经及其分支而不切断不结扎,其余过程同手术组。术后连续喂养2周以上,待手术伤口痊愈后,测定左后肢足底的机械痛阈水平,左后肢足底的机械痛阈水平明显低于右后肢足底时,且手术组左后肢足底的机械痛阈水平明显低于假手术对照组相应位置的机械痛阈水平时,SNI模型达到预期效果。本研究中,术后第3周开始相关给药及检测。
2.2 大鼠机械痛阈的行为学测定机械痛阈测定:根据手术分组和试验目的,测试时间安排在8点~16点,参照Dixon的方法[7],使用电子触觉测量仪 (electronic Von Frey,eVF) 进行机械痛阈测定。将大鼠置于升高的金属网上,并盖以透明的有机玻璃罩,适应20min,用eVF仪器的压力感受针垂直刺激足底2、3跖趾间皮肤敏感处,逐渐加压直至实验动物出现缩足反应,仪器自动记录瞬时的峰值压力,而身体活动所引起的缩足反应不记入统计数据。每次刺激间隔10s,每只动物重复刺激5次。
剂量-效应关系试验分组:①假手术对照组;② SNI模型溶剂对照组;③~⑨ SNI模型不同香叶醇剂量注射组。每组6只大鼠,每只大鼠检测5次。SNI术后第3周开始给药,给药后30 min检测,采取分组给药、分组测定的方法。
时间-效应关系试验分组:①溶剂对照组 (植物油);②利多卡因20 mg·kg-1体质量组;③香叶醇200 mg·kg-1体质量组。测定时间点定为:10、30、60、120、180、240、300 min。每组6只大鼠,每只大鼠检测5次。采取分组给药、分组测定的方法。
2.3 急性分离背根神经节神经元及鉴定参照Yu等[8]的方法,将大鼠击昏、断头,迅速分离胸至腰段脊柱,并将脊柱沿椎管上缘背面中线两侧纵向剪开,去除脊椎骨,暴露脊髓,小心摘除脊髓,取出两侧椎体外侧隐窝中的球形透亮的背根神经节 (dorsal root ganglion,DRG),置0℃通氧饱和的DMEM培养液中,并仔细剪去两侧的神经索,然后剪碎DRG,加入等体积0.25%胰蛋白酶 (含EDTA),置37℃,消化20 min,随后加入终浓度10%的胎牛血清终止消化,用吸管吹吸打散组织块,制成细胞悬液,1 500 r·min-1离心3 min,弃去上清液,加入无血清培养液重悬细胞沉淀,使用70 μm尼龙滤器过滤细胞悬液,滤液分别移入多聚赖氨酸包被过的直径为35 mm的培养皿中,静置30 min,细胞贴壁后用氧饱和的细胞外液替换培养液,可直接用于全细胞膜片钳实验。
少部分细胞分散液加到6孔板预先准备好的包被过多聚赖氨酸的盖玻片上,37℃培养3 d,制作细胞爬片,爬片使用anti-NeuN MAb (10 mg·L-1) 的抗体溶液孵育,加入羊抗小鼠IgG-Cy3二抗特异性荧光显色,Hoechst 33258复染,荧光显微镜观察记录细胞免疫荧光鉴定结果。
2.4 大鼠背根神经节神经元电压门控钠离子通道电流记录载有神经元的盖玻片转移到倒置式显微镜载物台上的培养皿中,室温下用人工脑脊液润洗,选择中等直径 (25~40 μm) 的大鼠背根神经结 (DRG) 神经元。使用全细胞膜片钳技术,尖端电阻为2~5 MΩ左右的玻璃微电极连接至MultiClamp 200B (Molecular Devices) 膜片钳放大器,先将采集模式设在默认的细胞贴附模式 (ON-CELL),待电极尖端与细胞膜之间形成高阻抗封接 (> 1 GΩ) 后, 将采集模式改成全细胞模式 (WHOLE-CELL),加负压破膜,使电极内液与电极内液相通,记录所有的经过该神经元离子通道的电流。
细胞外液:140 mmol·L-1 NaCl,3 mmol·L-1 KCl,1 mmol·L-1 CaCl2,1 mmol·L-1 MgCl2,10 mmol·L-1 HEPES和20 mmol·L-1 Glucose,用NaOH调节pH至7.3。电极内液:140 mmol·L-1 CsF,10 mmol·L-1 NaCl,10 mmol·L-1 HEPES,1.1 mmol·L-1 EGTA和20 mmol·L-1 Glucose,用CsOH调节pH至7.3。全细胞记录模式下, 钾电流被Cs+阻断, 钙电流被胞内EGTA、F离子和相对高浓度的Mg2+阻断,通过这种药理学方式可以分出Na+电流。
2.5 电压门控钠离子通道hNav1.7电流记录在室温下,利用全细胞膜片钳技术记录异源表达于HEK293细胞中的hNav1.7通道电流。尖端电阻为2~5 MΩ左右的玻璃微电极连接至Multi Clamp 200B (Molecular Devices) 膜片钳放大器。钳制电压和数据记录由pClamp 10软件通过电脑控制和记录,采样频率为10 kHz,滤波频率为2 kHz。在全细胞记录模式下,将细胞钳制于-80 mV,后给予时程20 ms,0 mV的测试电压诱发hNav1.7电流,刺激频率为0.2 Hz,检测化合物灌流前后的电流变化百分比。每个浓度至少测试3个细胞 (n≥3)。实验使用的细胞外液和电极内液配方与DRG神经元Na+通道电流记录方法中使用的配方相同。
2.6 瞬时受体电位通道TRPA1电流记录在室温下,利用全细胞膜片钳技术记录异源表达于HEK293细胞中的TRPA1通道电流。尖端电阻为2~5 MΩ的玻璃微电极连接至HEKA EPC10膜片钳放大器。钳制电压和数据记录由PatchMaster软件通过电脑控制和记录,采样频率为10 kHz,滤波频率为2 kHz。每个浓度至少测试3个细胞 (n≥3)。
试样准备:测试当天,将香叶醇母液 (1 mol·L-1) 用细胞外液稀释得到1 mmol·L-1检测浓度。测试化合物的DMSO含量不超过0.1%,此浓度的DMSO对检测的离子通道电流没有影响。细胞外液配方:140 mmol·L-1 NaCl,5 mmol·L-1 KCl,1 mmol·L-1 MgCl2,0.5 mmol·L-1 EGTA,10 mmol·L-1 HEPES和10 mmol·L-1 Glucose,用NaOH调节pH至7.4。电极内液配方:140 mmol·L-1 CsCl,0.1 mmol·L-1 CaCl2,10 mmol·L-1 HEPES,5 mmol·L-1 EGTA和1 mmol·L-1 MgCl2,用CsOH调节pH至7.2。
2.7 数据分析数据采集分析处理采用patchmaster、pClamp10、GraphPad Prism 5和Excel软件,所有数据均以x ± s表示,采用非配对双尾t-test进行统计学分析,P≤0.05表示差异有显著性。化合物对电流的影响用以下公式计算:加药前后的抑制率/%=[1-加药后电流的大小 (I) /加药前电流的大小 (Io)]×100%
3 结果 3.1 香叶醇镇痛作用的剂量-效应关系如Fig 1所示,经腹腔注射给予溶剂 (植物油) 的SNI模型组 (vehicle) 大鼠手术侧足底缩爪反射阈值 (paw withdrawal threshold, PWT)(27.98±5.19) gf较假手术组 (sham) 大鼠同侧足底PWT (44.57±6.31) gf明显降低。腹腔注射12.5 mg·kg-1体质量~300 mg·kg-1体质量香叶醇的其它SNI模型组,给药30 min后进行手术侧足底机械痛阈PWT检测,结果显示随着香叶醇剂量的提高,大鼠PWT逐步升高,高于50 mg·kg-1体质量香叶醇后,SNI模型大鼠手术侧足底的PWT水平可恢复到并超过假手术组大鼠同侧足底PWT。200 mg·kg-1体质量剂量下香叶醇的效用达到顶点[PWT=(67.44±23.92) gf],PWT均值较溶剂对照组提高了2.4倍,并明显高于假手术组的水平。给予高于200 mg·kg-1体质量香叶醇不能进一步提高实验动物的PWT值。

|
| 图 1 Effect of doses of geraniol on neuropathic pain (x ± s,n=6) *P < 0.05 vs sham group |
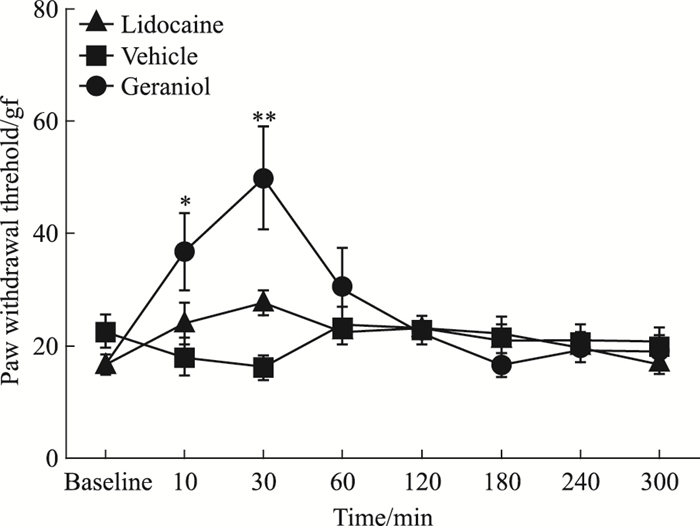
香叶醇在大鼠SNI模型上表现出快速起效的特点。如Fig 2所示,香叶醇腹腔注射后2 h内 (120 min) 大鼠手术侧足底机械刺激的PWT值均高于给药前测定的基础阈值 (baseline),给药后30 min内效果最强,30 min后阈值逐渐回落,刺激部位对机械性刺激的敏感性逐渐加强。在效应表现最强的10 min到60 min期间,PWT从基础值 (14.8±2.51) gf提高到 (49.87±20.49) gf,提高了3.37倍。溶剂对照组 (植物油) 的PWT在检测时间内变化不大,注射后足底PWT测定值基本保持稳定,注射操作后30 min内相对注射前阈值还有一定程度降低,可能与注射动作本身对实验动物的刺激性影响有关。阳性药物利多卡因按照20 mg·kg-1体质量腹腔注射给药,表现出一定的镇痛效应,最高效用出现的时间也在30 min左右,PWT从基础值 (16.86±1.35) gf,提高到 (37.7±4.96) gf,提高了2.23倍。
|
| 图 2 Time phase of analgesic effect of geraniol (x ± s,n=6) *P < 0.05, **P < 00.01 vs vehicle group |
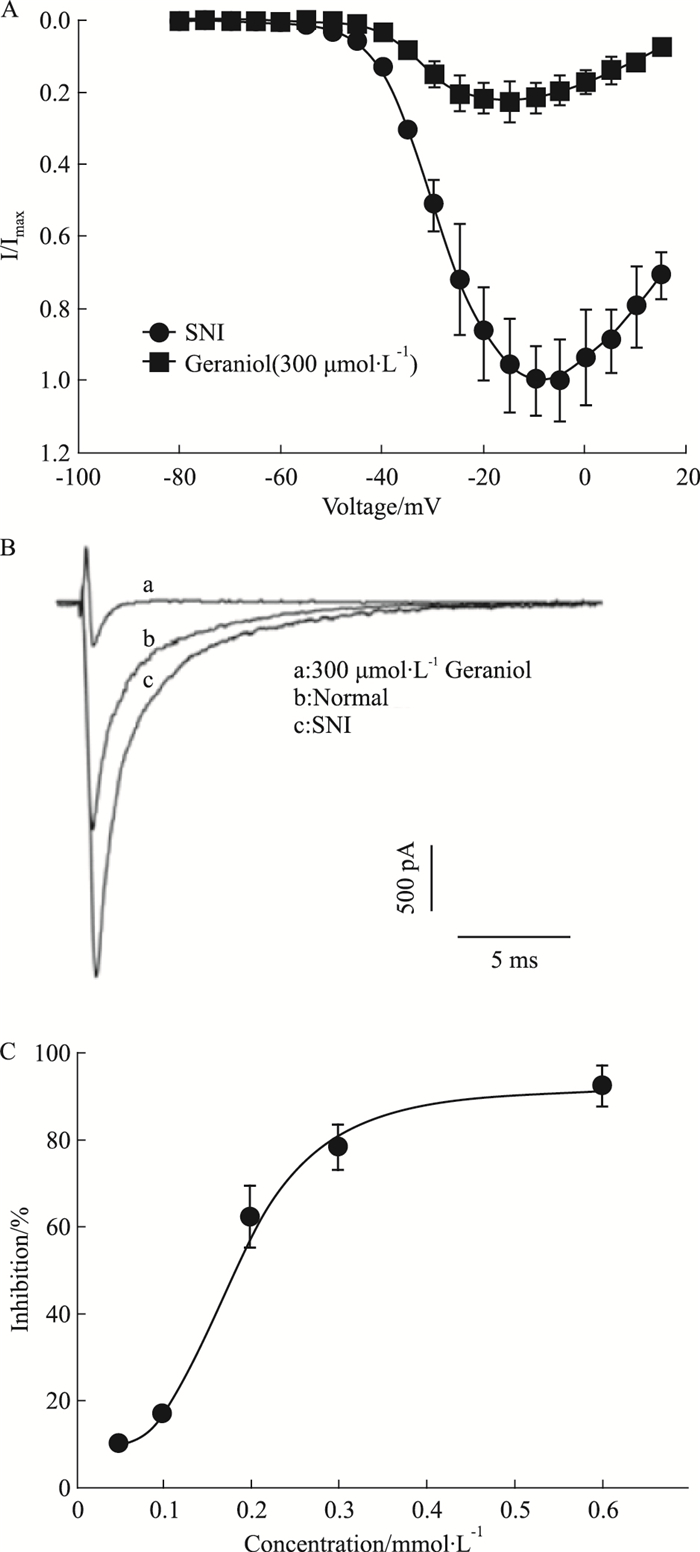
在进入全细胞记录状态后,DRG细胞钳制于-80 mV,后给予步幅+5 mV的阶跃刺激方波,时程50 ms,由-80 mV去极化至+15 mV,刺激频率为0.2 Hz。以急性分离制备的SNI模型大鼠中等直径的DRG神经元膜电位为横坐标,分别对给药前后经给药前最大峰电流值标准化的系列峰电流值 (I/Imax) 作图,叠加得到SNI模型大鼠DRG神经元给药前后的I-V曲线对比图 (Fig 3A)。结果显示,DRG神经元INa激活电压均在-40 mV左右,给药前SNI模型DRG神经元电压门控Na+通道最大峰电流值 (Imax) 对应刺激电压为-10 mV,加入300 μmol·L-1香叶醇后,DRG神经元I-V曲线发生上移,越靠近最大峰电流的激活电压,峰电流值的上移幅度越大,并且给药后最大峰电流值的对应刺激电压相对于给药前稍稍左移。
|
| Fig 3 Geraniol inhibited activated Na+ channels in DRG neuron A:Effect of step stimulation voltage on sodium channel current; B:Effect of geraniol on sodium channel current at 0 mV test potential; C:Effect of dose of geraniol on activated Na+ channels |
在全细胞记录模式下,DRG细胞钳制于-80 mV,后给予时程30 ms,0 mV的测试电压诱发Na+通道电流,刺激频率为0.2 Hz,检测香叶醇灌流前后的电流变化百分比。对比正常大鼠DRG神经元以及SNI模型大鼠DRG神经元在香叶醇灌流前后Na+电流变化,如Fig 3B所示,急性分离的SNI模型DRG神经元经0 mV测试电压诱发的Na+电流峰值明显高于正常大鼠DRG神经元,300 μmol·L-1香叶醇近乎完全阻断了DRG神经元的Na+通道电流。在测试的50 μmol·L-1~600 μmol·L-1浓度范围内,经曲线拟合计算得出,香叶醇对DRG神经元电压门控Na+通道的半数抑制浓度为0.1815 mmol·L-1(Fig 3C)。
3.4 香叶醇对hNav1.7通道的作用形成稳定的全细胞记录模式后,HEK293(hNav1.7) 细胞钳制于-80 mV,后给予0 mV的测试电压诱发Na+通道电流 (INa),时程50 ms,刺激频率为0.2 Hz,在细胞外液中分别加入终浓度1/27 mmol·L-1、1/9 mmol·L-1、1/3 mmol·L-1、1 mmol·L-1和3 mmol·L-1的香叶醇,待电流变化稳定后记录加药后的INa,计算香叶醇灌流前后的电流变化百分比。结果见Fig 4,不同浓度香叶醇对INa的抑制率分别为:(7±1)%、(17±2)%、(41±4)%、(94±1)%和 (100±0)%(n=3),其中, 各浓度组抑制率之间差异均有显著性, 表明香叶醇对INa的抑制呈浓度依赖性关系。经数据拟合计算,香叶醇对表达在HEK293细胞上的重组人源性钠离子通道hNav1.7的半数抑制浓度IC50约为424 μmol·L-1。

|
| Fig 4 Inhibition of geraniol on activated hNav1.7 channels in HEK293 |
测试起始,HEK293(hTRPA1) 细胞膜电位钳制于0 mV,每2 s给予一个-100 mV到+100 mV时程300 ms的斜坡电压。0 s~30 s:单纯细胞外液 (EC) 灌流,不加入其它成分;30 s-测试终点 (250 s):加入50 μmol·L-1 AITC持续灌流,使细胞外液中AITC浓度保持在50 μmol·L-1;90 s-测试终点 (250 s):加入终浓度1 mmol·L-1香叶醇,保持灌流直至检测终点。取各个时间点-100 mV和+100 mV电压相对应的电流值,对记录时间作图,得到Fig 5A。如图中所示,TRPA1电流由50 μmol·L-1 AITC诱发,诱发的TRPA1内向和外向电流随时间进程逐渐加大,经60 s后1 mmol·L-1香叶醇的加入致使AITC诱发的TRPA1通道电流发生突变,内外向电流均陡增,到108 s时诱发的TRPA1电流波动达到顶峰,随后逐渐走弱,越来越低,到测试终点250 s时接近于诱发前水平。

|
| Fig 5 Effect of geraniol on hTRPA1 channels in HEK293 A:I-t plot; B:I-V plot |
以达到最大振幅处的hTRPA1诱发电流,对-100 mV到+100 mV间的相应斜坡电压作图,得到I-V曲线图 (Fig 5B)。图中显示,加入1 mmol·L-1香叶醇的细胞I-V曲线斜率明显高于只加AITC的对照组细胞TRPA1通道的I-V曲线斜率;两条曲线交于0 mV电压处,0 mV电压条件下AITC和香叶醇均没有诱发TRPA1通道电流效应;偏离0 mV电压越远诱发TRPA1通道电流的作用越强,且在负电压下诱发的内向TRPA1通道电流远高于同等数值的正电压下诱发的外向TRPA1通道电流;香叶醇只改变I-V曲线斜率,并没有使曲线偏离0 mV原点,没有改变TRPA1通道本身的电流特性。我们未列出数据的实验测定表明,低于1 mmol·L-1的香叶醇没有扩大AITC诱发的TRPA1通道电流幅度作用,只有浓度达到1 mmol·L-1以上才有类似效应,且可以确定在低于1 mmol·L-1浓度条件下香叶醇也不能直接诱发TRPA1通道电流。
4 讨论本研究在复制大鼠保留性损伤模型 (SNI) 的基础上,运用电子von frey足底测试仪测试机械痛阈,确定了香叶醇在病理性神经痛模型上的镇痛作用;并使用急性分离的大鼠DRG神经元、重组表达hNav1.7通道蛋白的HEK293细胞株以及重组表达hTRPA1通道蛋白的HEK293细胞株,使用全细胞膜片钳技术针对可能与香叶醇镇痛作用相关的离子通道进行了初步探讨,研究结果提示香叶醇可能通过抑制DRG神经元上分布的Nav1.7通道蛋白起到对SNI模型机械痛觉超敏的改善作用。
目前比较常用的神经病理性疼痛模型主要有3种,分别是大鼠坐骨神经保留性损伤模型 (spared nerve injury,SNI)、坐骨神经慢性压迫性损伤 (chronic constriction injury,CCI) 和脊神经选择结扎模型 (the spinal nerve ligation model,SNL)[9]。SNI模型和SNL模型主要形成机械性痛敏[10],SNI具有复制容易,模型动物个体之间的痛敏差异小的优点。CCI模型可同时具备机械性痛敏和热痛敏效果,但存在模型动物个体差异大,对制作熟练度要求高的限制。在已证实香叶醇对SNI模型镇痛效果的基础上,未来可以使用对病理性神经痛更具有代表性的CCI模型进一步进行效果验证。
背根神经节是感觉神经痛觉信息由外周向中枢传递的主要节点,尤其Nav1.7、Nav1.8、Nav1.9几种痛觉相关Na+通道亚型在DRG部位集中分布。Nav1.7主要分布在大直径DRG神经元 (直径>40 μm) 和中等直径的DRG神经元 (直径在25~40 μm之间),Nav1.8和Nav1.9主要分布在小直径DRG神经元 (直径<25 μm)。本研究中使用数量占比较高的中等大小DRG神经元,代表了Nav1.7分布较多的那部分DRG神经元的反应特点,但在实验中并未通过实验手段区分其中主要起作用的Na+通道亚型,有待在进一步的研究中利用Nav1.7通道的河豚毒素敏感 (tetrodotoxin-sensitive,TTX-S) 特性,在排除Nav1.7通道作用的条件下,观察香叶醇对河豚毒素抗性 (tetrodotoxin-resistance,TTX-R) 的Nav1.8,Nav1.9的影响[11]。
本研究中,发现1 mmol·L-1香叶醇对AITC诱导TRPA1通道电流有协同作用,增强TRPA1激活带来的冷刺激感受,而低浓度的香叶醇没有检测到类似效应。TRPA1通道为冷刺激感受通道,TRPA1激动剂的一个应用是能激动周围感觉神经元上的TRPA1离子通道, 随后长时间脱敏离子通道, 并产生由此介导的镇痛作用。文献报道在DRG中97%的TRPA1和TRPV1共表达[12-13]。薄荷醇、樟脑、冰片等单萜类化合物大部分都对TRPs家族的离子通道蛋白有激活或抑制作用[14-16],是否香叶醇在对TRPA1通道协同诱导的同时,对同是TRPs家族的辣椒素受体通道TRPV1有抑制效应,进而对热痛或辣椒素等引起的烧灼感有抑制作用,有待进一步研究。
( 致谢: 本文实验在上海中药创新研究中心药理研究室和中国科学院上海药物研究所神经药理学研究国际科学家工作站实验室完成,感谢所有提供技术平台和技术协作的同事和老师们。 )
| [1] | 陈婷, 宿树兰, 华永庆, 段金廒. 芳香类药用植物抗炎镇痛活性成分及其作用机制研究进展[J]. 中草药, 2011, 42 (6): 1221-8. Chen T, Su S L, Hua Y Q, Duan J A. Advances in studies on constituents with anti-inflammatory and analgesia activity in aromatic medicinal plants and their mechanisms[J]. Chin Tradit Herbal Drugs, 2011, 42 (6): 1221-8. |
| [2] | 上海香料研究所, 北京北大正元科技有限公司. 食品添加剂香叶 (精) 油[S]. 见: 全国香料香精化妆品标准化技术委员会, 主编. 中华人民共和国国家标准GB 11959-2008: 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会, 2008. Shanghai spice Research Institute, Beijing Peking university zoteq Co., Ltd. Food additive-Oil of geranium (Pelargonium gravedens Her.)[S]. People's Republic of China national standard GB 11959-2008: General Administration of quality supervision, inspection and Quarantine of the People's Republic of China, The National Standardization Management Committee of China, 2008. |
| [3] | 孙立宏, 孙立明. 香叶醇的研究进展[J]. 西北药学杂志, 2009, 24 (5): 428-30. Sun L H, Sun L M. Research progress of geranium[J]. Northwest Pharm J, 2009, 24 (5): 428-30. |
| [4] | 任洪涛, 周斌, 秦太峰, 等. 栀子花挥发性成分的提取和对比分析[J]. 香料香精化妆品, 2012 (3): 17-21. Ren H T, Zhou B, Qin T F, et al. Extraction and analysis of the volatile components in Gardenia jasminoides[J]. Flavour Fragrance Cosmetics, 2012 (3): 17-21. |
| [5] | Richner M, Bjerrum O J, Nykjaer A, et al. The spared nerve injury (SNI) model of induced mechanical allodynia in mice[J]. J Vis Exp, 2011, 54 (e3902): 1-3. |
| [6] | Shields S D, Eckertw A 3rd, Basbaum A I. Spared nerve injury model of neuropathic pain in the mouse: a behavioral and anatomic analysis[J]. J Pain, 2003, 4 (8): 465-70. doi:10.1067/S1526-5900(03)00781-8 |
| [7] | 聂发传, 王金保, 苏东, 等. 补体抑制剂对大鼠神经病理性疼痛模型的作用研究[J]. 中国疼痛医学杂志, 2009, 15 (4): 240-2. Nie F C, Wang J B, Su D, et al. Effect of complements inhibitor on the neuropathic pain model in rats[J]. Chin J Pain Med, 2009, 15 (4): 240-2. |
| [8] | Yu S S, Yu K, Gu Y, et al. Taurine-induced modulation of voltagesensitive Na+ channels in rat dorsal root ganglion neurons[J]. Brain Res Bull, 2005, 26 (3): 259-67. |
| [9] | 金小高, 罗爱林, 张广雄. 三种大鼠神经病理性疼痛模型的制备和效果比较[J]. 临床麻醉学杂志, 2005, 21 (5): 338-40. Jin X G, Luo A L, Zhang G X. Comparison of the establishment and afficacy of three neuropathic pain models[J]. J Clin Anesthesiol, 2005, 21 (5): 338-40. |
| [10] | Smith A K, O'Hara C L, Stucky C L. Mechanical sensitization of cutaneous sensory fibers in the spared nerve injury mouse model[J]. Mol Pain, 2013 (9): 61-6. |
| [11] | 章艳, 陈少锐, 贾岩岩, 等. 苯佐卡因对大鼠背根神经节神经元河豚毒素不敏感型钠离子通道的影响[J]. 中国药理学通报, 2011, 27 (12): 1653-5. Zhang Y, Chen S R, Jia Y Y, et al. Effects of benzocaine on tetrodotoxin-resistant sodium channels in rat dorsal root ganglion neurons[J]. Chin Pharmacol Bull, 2011, 27 (12): 1653-5. |
| [12] | Story G M, Peier A M, Reeve A J, et al. ANKTM1, a TRP-like channel expressed in nociceptive neurons, Is activated by cold temperatures[J]. Cell, 2003, 112 (6): 819-29. doi:10.1016/S0092-8674(03)00158-2 |
| [13] | Hinman A, Chuang H H, Bautista D M, et al. TRP channel activation by reversible covalent modification[J]. Proc Natl Acad Sci USA, 2006, 103 (51): 19564-8. doi:10.1073/pnas.0609598103 |
| [14] | Karashima Y, Damann N, Prenen J, et al. Bimodal action of menthol on the transient receptor potential channel TRPA1[J]. J Neurosci, 2007, 27 (37): 9874-84. doi:10.1523/JNEUROSCI.2221-07.2007 |
| [15] | Namer B, Seifert F, Handwerker H O, et al. TRPA1 and TRPM8 activation in humans: effects of cinnamaldehyde and menthol[J]. Neuroreport, 2005, 16 (9): 955-9. doi:10.1097/00001756-200506210-00015 |
| [16] | Xu H, Blair N T, Clapham D E. Camphor activates and strongly desensitizes the transient receptor potential vanilloid subtype 1 channel in a vanilloid-independent mechanism[J]. J Neurosci, 2005, 25 (39): 8924-37. doi:10.1523/JNEUROSCI.2574-05.2005 |

