


2. 重庆医科大学基础医学院解剖学教研室, 重庆 400016;
3. 重庆医科大学神经科学研究中心, 重庆 400016
2. Dept of Anatomy, College of Basic Medicine, Chongqing Medical University, Chongqing 400016, China;
3. Neuroscience Research Center, Chongqing Medical University, Chongqing 400016, China
利尿药 (diuretics) 是临床常用于治疗心、肾功能衰竭所致的水肿以及高血压等非水肿性疾病的药物,主要通过增加肾脏对电解质及水的排出发挥作用[1-2]。目前的利尿药根据作用部位和效能分为三类:高效能和中效能利尿药分别通过特异性抑制髓袢升支的Na+/K+/2Cl-共同转运体和远曲小管的Na+/Cl-共同转运体,选择性抑制NaCl的重吸收、降低肾的尿浓缩功能达到利尿的效果,但存在引起电解质紊乱的风险。低效能利尿药作用于集合管和远曲小管,通过拮抗醛固酮起到排钠保钾的利尿作用,长期使用可引起高血钾的不良反应[3-4]。鉴于临床对利尿药的广泛需求,开发不影响电解质代谢的新型利尿药具有重要意义。近年来,随着人们对尿素通道蛋白 (urea transporters, UTs) 家族在尿浓缩机制中作用及机制认识的不断深入,为以尿素通道蛋白为靶点的新型利尿药物开发指引了新的方向[5-7]。本课题组前期通过体外模型筛选出PU1424,具有特异、高效抑制尿素通道蛋白转运尿素的作用,且无明显的细胞毒性[8]。因此,本研究通过动物实验验证其在体内的利尿效果,以及对机体代谢和肝脏、肾脏功能的影响,为利尿药物的研发提供实验基础。
1 材料 1.1 药品和主要试剂PU1424来自美国圣地亚哥ChemDiv公司;氢氯噻嗪 (H2910,Sigma);2-羟丙基-β-环糊精 (128446, Sigma);尿素检测试剂盒 (Roche,QuantichromTM urea assay kit-DIUR-500);全波长紫外分光光度仪 (BIOTEK, MQX200)。
1.2 主要仪器全自动化生化分析仪 (AU-2700,OLYMPUS);电子天平 (Santorius),超低温冰箱 (Thermo Scientific,700);低温离心机 (Eppendorf);冰点渗透压仪 (Gonotec);标准外科手术器械 (国产) 等。
2 方法 2.1 实验动物分组及给药实验动物采用♂ SD大鼠,(200±50) g,购自北京大学医学部动物实验中心,实验严格按照动物伦理学委员会要求执行。
8~12周龄♂ SD大鼠随机分为3组:2-羟丙基-β-环糊精 (2-HP-β-CD) 溶剂对照组、PU1424组和氢氯噻嗪 (hydrochlorothiazide,HCTZ) 组为阳性对照,每组6只,体质量 (200±50) g。大鼠分组后分别于代谢笼中适应性喂养1周,保持室温24℃~28℃,相对湿度50%~70%,自由饮食、饮水。
PU1424用浓度为40%(103 g·L-1) 的2-羟丙基-β-环糊精 (2-HP-β-CD) 水溶液制成混悬液。按照参考文献方法给药[7-8],d1 7:00 A.M.,腹部按摩排空大鼠膀胱,各组大鼠背部皮下分别注射100 mg·kg-1的PU1424,同体积的HCTZ和溶剂对照,然后在24:00 P.M.和d 2 6 :00 A.M.、12 :00 A.M.、18 :00 P.M.分别给各组大鼠注射50 mg·kg-1的PU1424、同体积的HCTZ和溶剂对照。注射后每6 h收集尿液至相应EP管,且计算出在此期间的大鼠饮水量。末次给药3 h后,戊巴比妥钠麻醉大鼠 (40 mg·kg-1),心脏穿刺取血,全血室温静置30 min,5 000 r·min-1离心15 min,取上清备用。
2.2 检测指标及方法 2.2.1 尿液称重及浓度检测将收集的尿液按1 g=1 mL的公式进行重量和体积折算。尿素试剂盒检测尿液、血清中尿素浓度。将冰箱中取出的试剂盒平衡至室温,临用前20 min内准备足量的A、B等量混合工作液, 按每孔100 μL用量计算。尿素标准品梯度:取6个0.2 mL EP管,尿素标准品 (50 mg·dL-1) 各管分别加入:①尿素标准液10 μL;②尿素标准液8 μL+ddH2O 2 μL;③尿素标准液6 μL+ddH2O 4 μL;④尿素标准液4 μL+ddH2O 6 μL;⑤尿素标准液2 μL+ddH2O 8 μL;⑥ ddH2O 10 μL。待测样本:各管分别取标准液5 μL,样本5 μL。尿素标准品梯度与待测样本依次加入洁净的96孔板,各孔加入100 μL工作液 (50 μL A液+50 μL B液)。室温孵育20 min,用全波长紫外分光光度仪于520 nm处测出OD值。根据尿素标准品梯度绘制标准曲线和前面的蛋白定量结果,换算出尿液、血清中的尿素浓度。
2.2.2 渗透压检测用冰点渗透压仪检测尿液和血清的渗透压值。
2.2.3 生物化学指标检测全自动生化分析仪检测血清指标:血脂指标包括甘油三酯 (TG)、胆固醇 (T-CHO)、高密度脂蛋白 (HDL-C)、低密度脂蛋白 (LDL-C);血糖浓度;谷丙转氨酶 (GPT/ALT)、谷草转氨酶 (GOT/AST)、碱性磷酸酶 (ALP)、总蛋白 (TP)、白蛋白 (Alb)、血清Na+、K+、Cl-、肌酐 (Cr)、尿酸 (UA) 水平;以及尿液Na+、K+、Cl-、Cr、UA水平。
2.3 统计学方法本实验采用SPSS22.0版本统计软件包处理。进行独立样本t检验,相关分析检验水平设定P < 0.05。
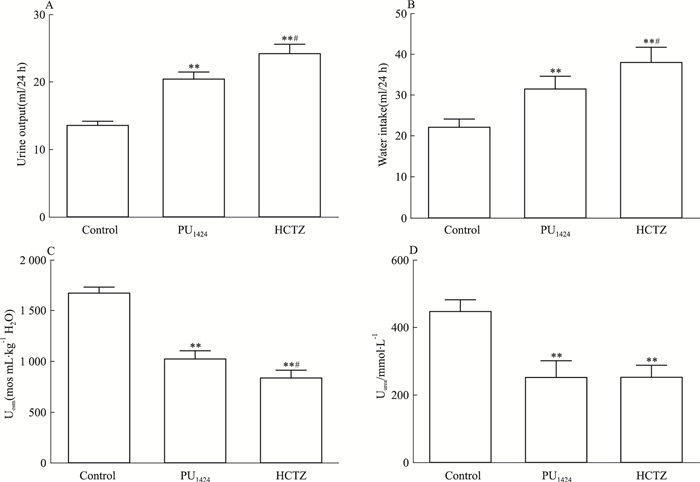
3 结果 3.1 PU1424和HCTZ降低大鼠的尿浓缩能力PU1424组和HCTZ组大鼠的尿量明显增加,分别达到溶剂对照组尿量的1.52倍和1.78倍 (P < 0.01, Fig 1A),并且HCTZ组大鼠的尿量比PU1424组增加了17.2%(P < 0.05, Fig 1A)。与此同时,PU1424组和HCTZ组大鼠的饮水量相应增加为溶剂对照组的1.42倍和1.56倍 (P < 0.01, Fig 1B),HCTZ组大鼠的饮水量比PU1424组增加了20.3%(P < 0.05, Fig 1B)。PU1424和HCTZ组大鼠的平均尿渗透压分别降低为对照组的61.5%和50.4%,且HCTZ组较PU1424组降低了17.9%(P < 0.01, P < 0.05, Fig 1C)。尿尿素浓度分别降低为对照组的57.1%和56.8%(P < 0.01, Fig 1C,1D)。与PU1424相比,HCTZ尿量和饮水量增加得更多。研究结果证明 (Fig 1),PU1424能够降低尿浓缩能力发挥利尿作用,但稍弱于HCTZ。
|
| Fig 1 Effect of PU1424 and HCTZ on the urinary concentrating ability in rats (x±s, n=6) A:Urea output; B:Water intake; C:Urinary osmolality (Uosm); D:Urine urea concentration (Uurea).#P < 0.05 vs PU1424 treated group.**P < 0.01 vs control |
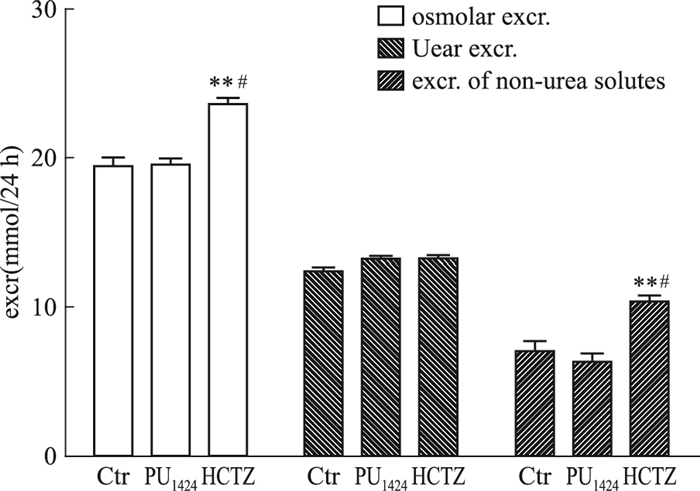
根据此前尿渗透压值、尿尿素浓度和排尿量计算出24 h总渗透性分子的排泄量、尿素排泄量和非尿素溶质的排泄量。结果显示 (Fig 2),与对照组比较,连续给予PU1424后尿素排泄量及非尿素排泄量均无明显变化,而HCTZ对照组总渗透性分子排泄量及非尿素排泄量均明显高于溶剂对照组和PU1424组 (P < 0.01, P < 0.05, Fig 2)。如连续给药后尿液及血清中与尿浓缩相关的主要离子水平 (Na+、K+、Cl-) 的检测结果显示 (Tab 1),PU1424组与HCTZ组大鼠尿液中Na+、K+、Cl-水平均明显降低 (P < 0.01);与溶剂对照组比较,PU1424组与HCTZ组血清中Na+、K+、Cl-水平均无差异 (P > 0.05)。研究结果提示,在较短时间段内PU1424的利尿作用降低了尿液中的电解质水平,但对血浆电解质平衡无明显影响。
|
| 图 2 Effect of PU1424 and HCTZ on renal handling of urea in rats (x±s, n=6) #P < 0.05 vs PU1424 treated group; **P < 0.01 vs control. |
| Control | PU1424 | HCTZ | |
| Urinary Na | 123.8±15.80 | 55.0±14.20** | 53.8±10.41** |
| Urinary K | 234.1±26.12 | 68.6±13.88** | 57.7±10.23** |
| Urinary CL | 197.7±8.43 | 64.7±14.31** | 54.9±8.82** |
| Serum Na | 153.38±15.38 | 151.2±12.73 | 143.2±10.72 |
| Serum K | 4.52±0.15 | 4.40±0.10 | 4.36±0.15 |
| Serum CL | 101.4±8.43 | 99.70±7.03 | 96.9±9.04 |
| **P < 0.01 vs control | |||
3组大鼠的血糖、血脂指标具体见表 (Tab 2)。与溶剂对照组比较,PU1424组的血糖水平稍有升高但无统计学意义 (P > 0.05),HCTZ组的血糖水平明显高于溶剂对照组 (P < 0.01) 和PU1424组 (P < 0.05)。大鼠血脂检测结果显示,PU1424组与溶剂对照组的LDL-C水平相当,PU1424组的T-CHO、TG、HDL-C水平较PU1424组稍有升高但无统计学意义;HCTZ组大鼠血清T-CHO和TG水平明显高于溶剂对照组 (P < 0.01) 和PU1424组 (P < 0.05)。结果显示,PU1424在短期作用时间内对体内糖代谢和脂代谢无明显影响,而HCTZ可升高血糖和总胆固醇。
| Control | PU1424 | HCTZ | |
| Blood glucose | 6.44±0.56 | 6.87±0.44 | 8.80±0.50**# |
| Serum T-CHO | 1.59±0.19 | 1.64±0.14 | 2.24±0.33**# |
| Serum TG | 0.44±0.09 | 0.47±0.14 | 0.63±0.16* |
| Serum HDL-C | 0.59±0.15 | 0.67±0.11 | 0.68±0.18 |
| Serum LDL-C | 0.28±0.08 | 0.28±0.07 | 0.33±0.08 |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05 vs PU1424 treated group | |||
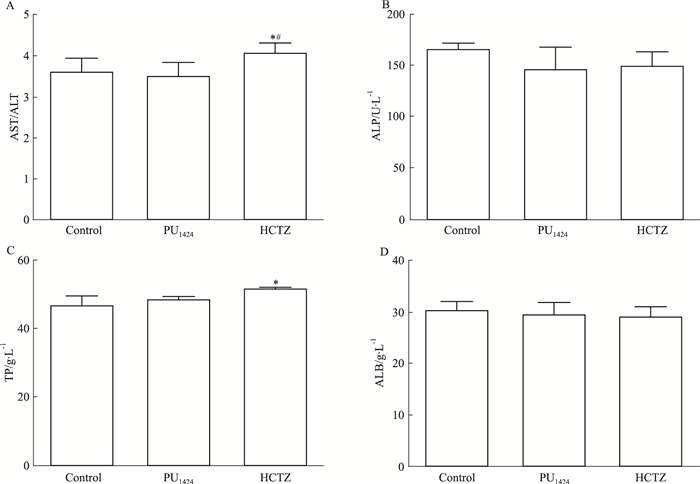
血清中谷丙转氨酶/谷草转氨酶 (谷丙/谷草)、碱性磷酸酶和总蛋白、白蛋白的水平是反应肝功能的常用指标。结果显示 (Fig 3A、B和C),连续给予PU1424处理后,大鼠血清谷丙/谷草、碱性磷酸酶和总蛋白水平均无明显变化 (P > 0.05)。连续给予HCTZ后,除血清谷丙/谷草比值有明显升高外 (P < 0.05和P < 0.05),碱性磷酸酶和总蛋白水平亦均无明显变化 (P > 0.05)。研究结果证明PU1424对大鼠的肝功能无明显的影响。
|
| Fig 3 Effect of PU1424 or HCTZ on AST/ALT ratio, ALP activity and albumin level in rats (x±s, n=6) A:AST/ALT ratio; B:ALP activity; C:Total protein level; D:Albumin level.*P < 0.05 vs control; #P < 0.05 vs PU1424 treated group. |
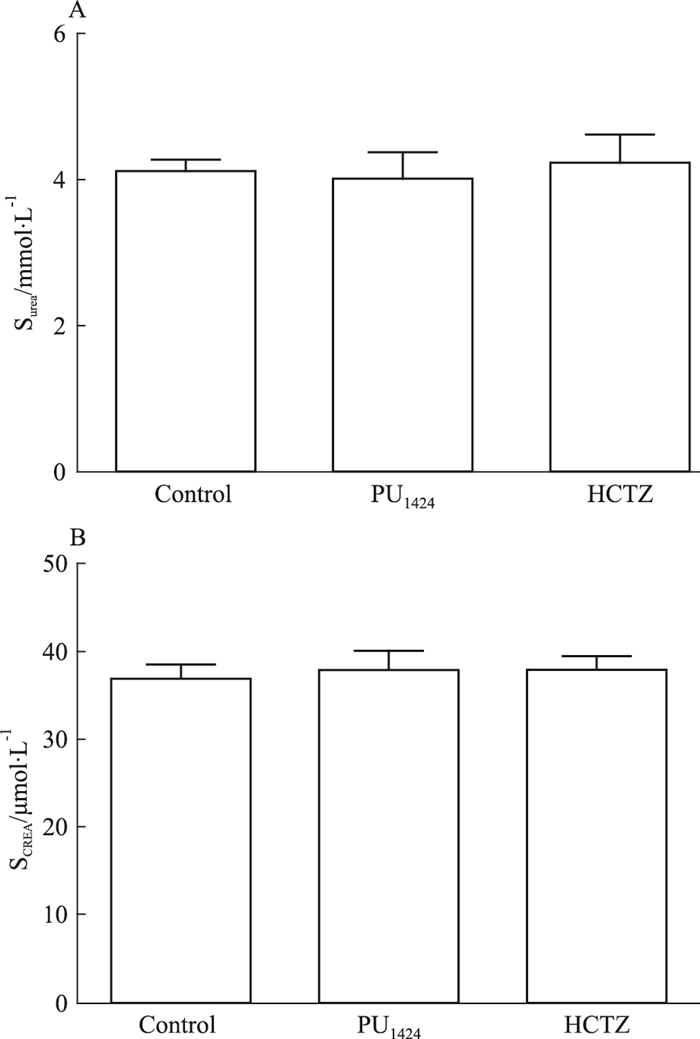
血清中尿素、肌酐水平显示,连续给予PU1424处理后,PU1424处理组和HCTZ组的大鼠血清尿素 (Fig 4A)、肌酐 (Fig 4B) 水平均无明显改变 (P > 0.05),提示两者对肾功能都无影响。
|
| Fig 4 Effect of PU1424 or HCTZ on kidney functions in rats (x±s, n=6) A:Serum urea level; B:Serum creatinine level |
利尿药一直作为一线降压药治疗高血压,噻嗪类利尿药作为最广泛应用的利尿药已有超50年的历史。然而,长期使用包括噻嗪在内的利尿药带来一系列的副作用,如电解质紊乱和机体代谢障碍[2-3]。目前,电解质紊乱等不良反应已经成为限制这些利尿药临床应用的最大问题,所以研发不引起电解质紊乱的新型利尿药是利尿药物研发领域的热点。因而在体外实验筛选出Phenylphthalazines化合物PU1424具有特异、高效抑制尿素通道蛋白转运尿素、且无明显细胞毒性的基础下[8],对新型利尿候选化合物PU1424进行体内利尿效果的验证,结果显示其可通过增加尿量、降低尿渗透压发挥利尿作用,不影响机体中主要电解质 (Na+、K+、Cl-)、血糖、血脂代谢的明显改变,且对血清中谷丙/谷草、碱性磷酸酶和总蛋白、白蛋白的水平等肝脏功能指标和尿素、肌酐水平等肾脏功能指标均无明显影响,具有新型利尿药研究和开发的价值。
正常人每天形成的原尿约180升,经过尿浓缩过程后导致排出的终尿量只有1.5升左右。在这一过程中,肾髓质通过逆流倍增、逆流交换的肾内尿素循环机制使得尿素浓度呈现由外髓向内髓组织逐渐增加的趋势,因此,尿素作为肾髓质的主要溶质与肾皮质的氯化钠共同形成不同部位的渗透压梯度,通过渗透性调节达到有效吸收水和某些溶质而浓缩尿液的作用[9-11]。在这一循环过程中,除内髓的直小血管升支内皮细胞以微孔方式通透尿素外,肾脏其余各部分均由尿素通道 (urea transporters,UTs) 介导尿素的通透性[10]。尿素通道蛋白作为特异性通透尿素的膜通道蛋白,包括UT-A和UT-B两个亚家族,表达于肾脏的不同部位,如UT-A1、UT-A3和UT-A4分布于肾脏集合管上皮细胞,UT-A2分布于肾脏髓袢降支细段,UT-B分布于肾脏直小血管降支内皮细胞[9-11],分别介导相应部位的尿素通透,共同参与肾内尿素循环过程,并在尿浓缩机制中发挥重要作用。
UT-B敲除小鼠的研究结果显示[12],敲除小鼠的肾脏体质重比、肾小球滤过率以及尿中主要溶质 (Na+、K+、Cl-) 的清除率均无明显变化;但出现尿量增加、尿渗透压降低、尿中尿素浓度降低等改变,提示其尿浓缩能力下降。UT-Al/UT-A3基因敲除小鼠尿量比野生型小鼠高3倍,尿浓缩能力降为野生型小鼠的35%[13]。因此,选择性抑制尿素通道蛋白功能,可达到不影响其它电解质的尿素选择性利尿作用;采用小分子化合物对尿素通道蛋白进行化学性敲除,对于避免绝大多数高血压药物长期使用引起电解质紊乱的不良反应具有重要意义。
以尿素通道蛋白为靶点的利尿药物研究已成为目前利尿药的重要研究方向,Verkman采用的红细胞筛选模型因其简单、准确的特性使得高通量小分子化合物的药物筛选成为了可能[14]。本研究的前期实验通过高通量红细胞模型筛选出对UT-B和UT-Al均有抑制作用的Phenylphthalazines化合物PU1424,其对人和小鼠红细胞膜通透尿素抑制作用的半数有效剂量分别为0.03 μmol·L-1和1.5 μmol·L-1,提示其对人尿素通道蛋白的抑制作用比小鼠更敏感,效果更强;并且还具有抑制作用可逆性、有效剂量浓度范围内无细胞毒性等优势,是较好的候选化合物[8]。因此,需要对PU1424的体内利尿作用以及对电解质水平、机体代谢的影响进行验证。
多次给药结果显示,PU1424可以明显增加大鼠的尿量至对照组的1.52倍,伴随着尿渗透压和尿尿素浓度分别降低为对照组的61.5%和57.1%,尿液中Na+、K+、Cl-的浓度降低明显,提示PU1424能够降低尿浓缩能力发挥利尿作用,且尿尿素的排出多于尿渗透压的降低,显示其可能是尿素渗透性利尿作用;尽管HCTZ的利尿作用强于PU1424,但其尿尿素的排出少于尿渗透压的降低 (Fig 2),且尿液中Na+、K+、Cl-的浓度降低更为明显,提示其促进Na+、K+、Cl-等其它溶质的排泄作用更强,可能会引起电解质失衡。实验中PU1424和HCTZ均未引起血清Na+、K+、Cl-水平明显改变,但因观察时间较短,还需要后期进行长期用药对大鼠血清电解质影响的观察。对大鼠体内代谢的结果显示,PU1424对大鼠的血糖、血脂水平明显影响,而HCTZ可升高血糖和总胆固醇,与文献报道一致[15]。与此同时,尽管PU1424和HCTZ均不影响大鼠肾功能;但连续给予HCTZ可升高血清谷丙/谷草比值,影响肝功能,而PU1424对大鼠血清谷丙/谷草、碱性磷酸酶和总蛋白水平均无影响。综上所述,PU1424在体外抑制尿素通道蛋白转运尿素的作用在体内实验得到了验证,结合前期研究得出主要通过尿素渗透性利尿发挥作用,且在本实验的观察时间段内不影响电解质水平、机体糖脂代谢和肝脏、肾脏功能,具有药物开发的价值。
( 致谢: 此研究主要在重庆医科大学基础医学院组织细胞工程与干细胞研究室及解剖学教研室实验室完成,北京大学医学部药理学系杨宝学教授课题组对实验过程进行了课题指导等工作,特此感谢! )
| [1] | Appel L J. The verdict from ALLHAT-thiazide diuretics are the preferred initial therapy for hypertension[J]. JAMA, 2002, 288 (23): 3039-42. doi:10.1001/jama.288.23.3039 |
| [2] | Faris R, Flather M, Purcell H, et al. Current evidence supporting the role of diuretics in heart failure: a meta analysis of randomised controlled trials[J]. Int J Cardiol, 2002, 82 (2): 149-58. doi:10.1016/S0167-5273(01)00600-3 |
| [3] | Barzilay J I, Davis B R, Pressel S L, et al. Long-term effects of incident diabetes mellitus on cardiovascular outcomes in people treated for hypertension the ALLHAT diabetes extension study[J]. Circ Cardiovasc Qual Outcomes, 2012, 5 (2): 148-9. doi:10.1161/CIRCOUTCOMES.112.965178 |
| [4] | Zillich A J, Garg J, Basu S, et al. Thiazide diuretics, potassium, and the development of diabetes: a quantitative review[J]. Hypertension, 2006, 48 (2): 219-24. doi:10.1161/01.HYP.0000231552.10054.aa |
| [5] | Yao C, Anderson M O, Zhang J, et al. Triazolothienopyrimidine inhibitors of urea transporter UT-B reduce urine concentration[J]. J Am Soc Nephrol, 2012, 23 (7): 1210-20. doi:10.1681/ASN.2011070751 |
| [6] | Li F, Lei T, Zhu J, et al. Novel small-molecule thienoquinolin urea transporter inhibitor acts a potential diuretic[J]. Kidney Int, 2013, 83 (6): 1076-86. doi:10.1038/ki.2013.62 |
| [7] | Ren H, Wang Y, Xing Y, et al. Thienoquinolins exert diuresis by strongly inhibiting UT-A urea transporters[J]. Am J Physiol Renal Physiol, 2014, 307 (12): F1363-72. doi:10.1152/ajprenal.00421.2014 |
| [8] | Ran J H, Li M, Yang B X, et al. Phenylphthalazines as small-molecule inhibitors of urea transporter UT-B and their binding model[J]. Acta Pharmacol Sin, 2016, 37 (7): 973-83. doi:10.1038/aps.2016.4 |
| [9] | Sands J M. Renal urea transporters, curr opin nephrol hypertens[J].2004, 13(5):525-32. |
| [10] | Yang B, Bankir L. Urea and concentrating ability: new insights from studies in mice[J]. Am J Physiol Renal Physiol, 2005, 288 (5): F881-96. doi:10.1152/ajprenal.00367.2004 |
| [11] | Klein J D, Blount M A, Sands J M. Urea Transport in the kidney[J]. Compr Physiol, 2011, 1 (2): 699-729. |
| [12] | Bankir L, Chen K, Yang B. Lack of UT-B in vase recta and red blood cells prevents urea-induced improvement of urinary concentrating ability[J]. Am J Physiol Renal Physiol, 2004, 286 (1): F144-51. |
| [13] | Fenton R A, Flynn A, Shodeinde A. Renal phenotype of UT-A urea transporter knockout mice[J]. J Am Soc Nephrol, 2005, 16 (6): 1583-92. doi:10.1681/ASN.2005010031 |
| [14] | Esteva-Font C, Anderson M O, Verkman A S. Urea transporter proteins as targets for small-molecule diuretics[J]. Nat Rev Nephrol, 2015, 11 (2): 113-23. |
| [15] | Marazzi G, Volterrani M, Caminiti G, et al. Effectiveness of nebivolol and hydrochlorothiazide association on blood pressure, glucose, and lipid metabolism in hypertensive patients[J]. Adv Ther, 2010, 27 (9): 655-64. doi:10.1007/s12325-010-0053-2 |

