


2. 暨南大学生命科学技术学院,细胞生物学系,广东 广州 510632
2. Dept of Cell Biology, College ofLife Science and Technology, Jinan University, Guangzhou 510632, China
病原微生物感染,首先启动的是简并识别的固有免疫系统,其中吞噬细胞起着关键作用。吞噬细胞表面或细胞内部的模式识别受体 (pattern recognition receptor, PRR),识别病原相关分子模式 (pathogen-associated molecular pattern, PAMP),如革兰阴性菌的脂多糖 (lipopolysaccharide, LPS),启动炎症反应,包括激活NF-κB信号通路,上调肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)、白细胞介素-1β前体 (pro-interleukin-1β, pro-IL-1β, 31 ku) 等炎症细胞因子的表达;并能进一步激活炎症小体和caspase-1[1],使pro-IL-1β剪切成为成熟的IL-1β(17 ku)。激活炎症小体是机体最重要的固有免疫防御机制之一,包括:激活半胱氨酸天冬氨酸酶-1/-11(caspase-1/-11),剪切pro-IL-1β、gasdermin D等,促进IL-1β等炎症因子成熟和释放[2]。然而,最近有研究表明,成熟IL-1β只有在细胞死亡时才会被释放到细胞外[3]。与成熟IL-1β释放相关的细胞死亡可以通过PAMP (如:核酸、脂蛋白和LPS) 首先激活巨噬细胞,然后以ATP或其他内源性损伤相关分子模式 (danger-associated molecular patterns, DAMPs)(如尿酸钠晶体) 刺激来诱导其发生;这种细胞死亡方式伴随着炎症小体和caspase-1的活化 (产生caspase-1 p10活性片段),称之为细胞焦亡。细胞焦亡的特征表现为细胞膜孔的快速形成 (碘化丙锭等细胞核染料可籍此进入细胞),从而导致细胞内炎症物质的释放和细胞破裂,而有研究表明caspase-1的活化可以增加细胞内钙离子水平和细胞膜的通透性,从而有利于成熟IL-1β、HMGB1以及其他内容物通过溶酶体胞吐作用释放到胞外[4]。
二甲双胍 (metformin) 是一种用于治疗2型糖尿病的一线药物,许多研究也表明二甲双胍不仅能通过改善代谢参数,如高血糖、胰岛素抵抗、动脉粥样硬化、血脂异常等来改善慢性炎症,同时具有直接的抗炎作用[5]。为了探索二甲双胍药物对急性炎症条件下发生的细胞焦亡和IL-1β释放的影响,本研究利用LPS作为PAMP活化腹腔巨噬细胞,以ATP作为DAMP激活炎症小体并诱导细胞焦亡的发生,探讨了二甲双胍对巨噬细胞的细胞焦亡、caspase-1活化和成熟IL-1β释放的影响。
1 材料与方法 1.1 实验材料C57BL/6小鼠,♀,6~8周龄,体质量 (20.0±2.0) g,购于南方医科大学实验动物中心。细菌脂多糖 (LPS)、三磷酸腺苷 (ATP)、碘化丙锭 (propidium iodide, PI)、Hoechst 33342、Tween-80、兔抗P2X7嘌呤能受体7抗体等购于Sigma-Aldrich公司。巯基乙酸盐 (thioglycolate, TG) 购自Becton Dickinson公司。DMEM、胎牛血清 (fetal bovine serum, FBS)、青霉素、链霉素、L-谷氨酰胺为Gibco/Invitrogen公司的产品。二甲双胍 (metformin) 购买于Beyotime公司。抗β-tubulin、IL-1β、caspase-1等抗体以及辣根过氧化物酶标记二抗购买于Cell Signaling Technology公司。AlexaFluor488-CD11b购自eBioscience公司。
1.2 实验仪器SDS-PAGE电泳系统 (美国Bio-Rad公司MINI Protean2);Zeiss荧光倒置显微镜 (德国Zeiss公司,Axio Observer D1);Alpha化学发光凝胶成像系统 (美国Alpha Innotech,FluorChem 8000)。
1.3 细胞培养C57BL/6小鼠腹腔注射500 μL 30 g·L-1 TG溶液,4 d后,断颈处死,用含50 mL·L-1 FBS和0.5 mmol·L-1 EDTA的PBS洗出小鼠腹腔液,300×g离心10 min,重悬于完全培养基中 (含青霉素100 000 U·L-1、链霉素100 mg·L-1、L-谷氨酰胺25 mmol·L-1、100 mL·L-1 FBS)。在37℃,5% CO2培养箱中培养2 h后,洗去非贴壁细胞,换成新鲜的完全培养基,剩下的贴壁细胞即为腹腔巨噬细胞,将其在培养箱中培养过夜。
1.4 细胞焦亡检测参考前文[6]方法,简述如下:将30 g·L-1 TG诱导产生的腹腔巨噬细胞接种在24孔板中。过夜后,加入二甲双胍处理1 h,其浓度从低到高依次为0.22、0.67、2 mmol·L-1,接着用0.5 mg·L-1的LPS诱导4 h,然后加入2 mmol·L-1 ATP刺激30 min,最后PI和Hoechst 33342双染色10 min,置于蔡司倒置荧光显微镜下观察并拍照。
1.5 免疫印迹法将30 g·L-1 TG诱导产生的腹腔巨噬细胞接种在6孔板中,分成9组;先用0.5 mg·L-1的LPS诱导4 h,然后二甲双胍 (0.22、0.67、2 mmol·L-1) 处理1 h,最后加入2 mmol·L-1 ATP刺激30 min;分别提取细胞和上清 (各样品等体积) 中的总蛋白,对细胞裂解液中的蛋白进行定量;分别进行SDS-PAGE电泳,将凝胶上的蛋白转移到PVDF膜上,用封闭液 (含50 g·L-1脱脂奶粉和1 mL·L-1 Tween-20的PBS溶液) 封闭1 h,一抗在4℃摇床孵育过夜,然后辣根过氧化物酶标记二抗37℃孵育1 h,碧云天公司的BeyoECL Plus化学发光试剂盒显色,X光片显影。最后用FluorChem 8000成像仪记录结果,用AlphaEaseFC软件进行条带灰度分析。
1.6 免疫荧光分析参考前文[7]方法,简述如下:将30 g·L-1 TG诱导产生的腹腔巨噬细胞接种在玻底培养皿中,LPS和二甲双胍的处理方法同上。最后吸弃其培养基,每孔加1 mL 40 g·L-1多聚甲醛,室温固定15 min,然后每孔加2 mL冷甲醇于-20℃条件下通透10 min,再用封闭液室温封闭1 h,加一抗 (100 μL每孔,其中P2X7R为1 :100,AlexaFluor488-CD11b为1 :50),4℃孵育过夜,洗涤后加无交叉反应的CF568-山羊抗兔IgG (美国Biotium公司),室温孵育1 h,Hoechst 33342染核10 min并避光,蔡司荧光显微镜观察,拍照。
1.7 统计学分析数据以x±s表示,用GraphPad Prism 4.0软件进行单因素方差分析,多组间比较采用Tukey检验。
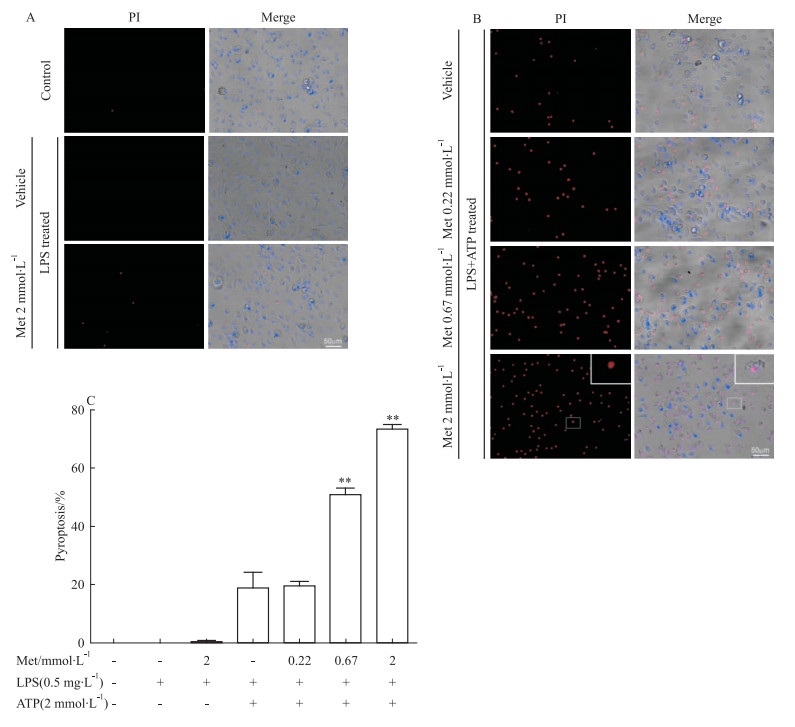
2 结果 2.1 二甲双胍促进ATP诱导的腹腔巨噬细胞的细胞焦亡在本实验中,采用文献常用的LPS+ATP处理诱导细胞焦亡,PI染色用于指示焦亡的细胞[8]。结果表明,LPS和二甲双胍本身不能诱导腹腔巨噬细胞发生焦亡 (Fig 1A)。ATP可刺激LPS激活的腹腔巨噬细胞发生焦亡,且二甲双胍处理,可明显促进LPS+ATP诱导的细胞焦亡并具有量效关系 (Fig 1B, 1C)。从细胞形态上,加入ATP之后,细胞膜明显变圆肿胀,甚至破裂成细胞碎片。PI染料可穿过细胞膜进入核内,发出红色荧光。上述结果表明,二甲双胍可剂量依赖性地促进ATP诱导的巨噬细胞焦亡。
|
| Fig 1 Metformin promotes cell pyroptosis of TG-elicited peritoneal macrophages induced by LPS+ATP (n=4) A & B: Fluorescence images of TG-elicited peritoneal macrophages stained with propidium iodide (PI)(red) and Hoechst 33342(blue) dyes. The insets showed one of the PI-positive (pyroptotic) cells.C:Statistical analysis of the ratios of pyroptotic cells (PI-positive) in each group; **P < 0.01 vs LPS+ATP group |
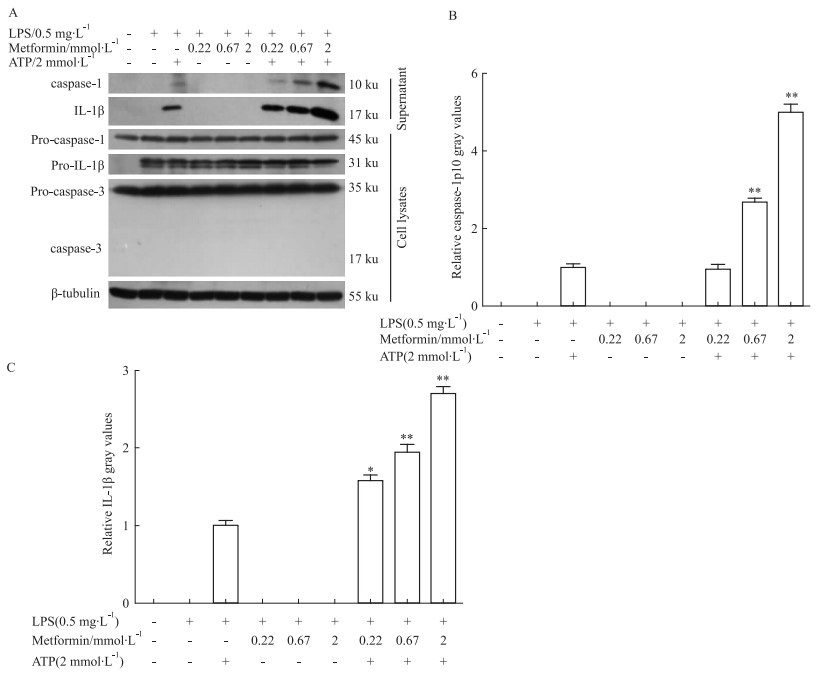
文献提示,细胞焦亡伴随着炎症小体和caspase-1的活化以及成熟的IL-1β(17 ku) 的释放[3]。由于ATP诱导细胞焦亡,因此本研究通过免疫印迹法从蛋白表达水平上分析二甲双胍对LPS+ATP处理的腹腔巨噬细胞表达IL-1β及其他炎症小体活化标志性蛋白caspase-1活化的影响。结果显示,单独LPS刺激可促进腹腔巨噬细胞pro-IL-1β(31 ku) 的表达,但不影响腹腔巨噬细胞内pro-caspase-1(45 ku) 的表达水平 (Fig 2A, cell lysates),而且细胞培养上清中未检测到活化的caspase-1p10(10 ku) 和成熟的IL-1β(17 ku) 释放 (Fig 2A, supernatant,所有样品来自等体积的细胞培养上清)。当细胞加入第二信号ATP刺激后,细胞培养上清中可明显检出被细胞释放的活化的caspase-1p10(10 ku) 和成熟的IL-1β(17 ku)(Fig 2A, 2B, 2C, supernatant)。二甲双胍处理可进一步促进上述ATP诱导的巨噬细胞释放活化的caspase-1p10(10 ku) 和成熟的IL-1β(17 ku) 蛋白,并具有明显的量效关系;但如果没有ATP的刺激,二甲双胍本身 (或与LPS联合) 不能促进活化的caspase-1和成熟的IL-1β的释放水平 (Fig 2A, 2B, 2C, supernatant)。因此,上清中活化的caspase-1p10和成熟的IL-1β的释放水平,可能与细胞焦亡率密切相关。这一点与上述细胞焦亡检测结果以及前人发表的文献相符[3]。值得一提的是,细胞裂解液中只检测到pro-caspase-3(35 ku) 的表达,而没有检测到活化的caspase-3(17、19 ku) 的表达水平 (Fig 2A, cell lysates),说明细胞凋亡 (一种依赖caspase-3的细胞死亡方式) 可能未参与上述活化的caspase-1p10和成熟的IL-1β的释放过程。
|
| Fig 2 Metformin promotes release of IL-1β and caspase-1 p10 from TG-elicited peritoneal macrophages induced by LPS+ATP stimulation (n=3) A:Western blot bands of proteins from the supernatants and cell lysates, respectively; Total proteins in the supernatant of each group came from an equal volume of supernatant of equal cell numbers. B & C: The relative gray levels of the Western blot bands of caspase-1 p10(B) and mature IL-1β(C) from respective cell culture supernatants, setting the gray-scale value of (LPS+ATP) bands as 1, respectively. *P < 0.05, **P < 0.01 vs LPS+ATP group |
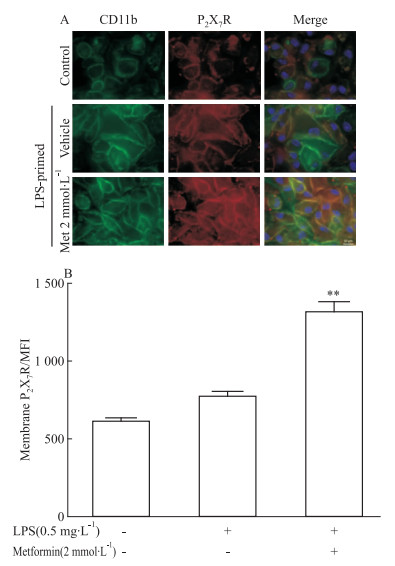
上述结果中发现二甲双胍可促进LPS+ATP诱导的腹腔巨噬细胞发生焦亡,并伴随成熟IL-1β和活化caspase-1p10的释放。有趣的是,机体受细菌感染后可释放ATP,胞外ATP经细胞膜上的受体介导,尤其是P2X7R,导致K+的释放和炎症小体的活化[9],提示二甲双胍促进炎症反应和细胞焦亡可能与上调ATP受体P2X7R的表达有关。结果如Fig 3(A, B)所示,经2 mmol·L-1二甲双胍处理的LPS激活的腹腔巨噬细胞的细胞膜上P2X7R的荧光强度明显大于对照组和单独LPS处理组的荧光强度。这表明,二甲双胍可能是通过上调P2X7R在细胞膜上的表达来促进细胞焦亡以及成熟IL-1β和活化caspase-1p10的释放。
|
| Fig 3 Metformin increases membranous immunofluorescenceintensity indicating redistribution of P2X7R (n=100) A:Immunofluorescence images of P2X7R (red) and CD11b (green, cell membrane marker of peritoneal macrophages); the nuclei were revealed by Hoechst 33342 staining (blue) and the merged images of P2X7R, CD11b and nuclei were also shown. B:Statistical analysis of the mean fluorescence intensities of P2X7R on cell membranes. **P < 0.01 vs control |
LPS是革兰阴性菌表达的PAMP,可被Toll样受体4(TLR4) 或细胞内的caspase-11识别[10]。LPS与TLR4结合后,可以激活炎症信号通路,上调pro-IL-1β和炎症小体组分NLRP3等蛋白的表达;当以ATP为第二信号刺激后,引起NLRP3炎症小体的组装,激活caspase-1的活化 (形成具有蛋白酶活性的caspase-1p10片段并释放到胞外),促进IL-1β的成熟,并在细胞膜上形成孔洞,使成熟的IL-1β等炎症因子得以释放[3]。因此,活化的caspase-1p10和成熟的IL-1β的释放,可作为巨噬细胞炎症小体激活的标志。多项研究表明,caspase-1/-11的表达及其介导的炎症因子释放和细胞焦亡,有利于抑制感染 (包括葡聚糖硫酸钠DSS诱导的小鼠急性肠炎),加快组织修复[11-12]。细胞焦亡有利于胞内致病菌的释放,并被其他吞噬细胞所吞噬、杀伤而清除,防止致病菌在胞内的繁殖和持续存在[13]。因此,增强感染部位的炎症小体的活化和感染细胞 (或被激活细胞) 的焦亡,可能有利于加强局部炎症反应,加速清除致热源 (病原微生物及其PAMP所激活的固有免疫细胞)、促进损伤组织的修复和疾病的痊愈。另一方面,细胞焦亡是活化巨噬细胞的重要退出机制之一;如果巨噬细胞持续激活而不发生焦亡,其免疫代谢通路已经发生改变,导致脂类沉积,成为泡沫细胞或脂肪巨噬细胞,这些细胞持续不断地分泌炎症因子和趋化因子,募集其他免疫细胞至病灶组织,将增加动脉粥样硬化和肥胖症等慢性炎症性疾病的风险[14]。本研究发现,二甲双胍可以促进LPS激活的腹腔巨噬细胞在ATP刺激下导致的细胞焦亡以及成熟IL-1β的释放。有趣的是,介导IL-1β成熟的蛋白酶caspase-1p10(活性形式) 的释放量亦随之增加。也就是说,二甲双胍可增强ATP诱导的腹腔巨噬细胞的炎症小体的活化及其信号通路。该结果提示,二甲双胍可用于增强感染部位的炎症反应,促进被感染细胞 (或被激活细胞) 发生焦亡,从而清除病灶中的活化细胞,防止其因细胞长期存活而持续释放炎症细胞因子,降低慢性炎症性疾病 (如动脉粥样硬化和肥胖) 的风险。
然而,全身性感染 (败血症) 可引起多器官功能衰竭,因感染而诱发的细胞焦亡可能是器官功能衰竭的原因之一[15-16]。由于多器官功能衰竭进程非常迅速,机制尚不明确,目前尚无特异性的治疗办法。在这种情况下,防止细胞焦亡可能是防止败血症病人多器官功能衰竭的关键。二甲双胍可以促进ATP诱导的巨噬细胞发生焦亡,提示在机体受到严重感染 (包括败血症) 的情况下,2型糖尿病患者不宜服用二甲双胍。
本研究发现,二甲双胍促进ATP诱导的腹腔巨噬细胞发生焦亡,可能与其上调ATP受体在细胞膜上的分布有关。由于细胞焦亡的发生非常迅速 (30 min以内),ATP受体如何通过快速重分布而增强ATP诱导细胞焦亡的作用,需要更多的实验数据才能明确。另外,二甲双胍有多种生物学效应,包括上调AMPK的活性,其促进细胞焦亡效应是否与此有关,也需要更多的实验证据支持。深入研究上述问题,可扩展二甲双胍的临床用途,如用于增强局部炎症小体的激活,促进细胞焦亡,从而快速清除感染病灶,去腐生肌,防止发展为迁延性的慢性炎症性疾病;也有利于更好地指导糖尿病患者合理服用二甲双胍。
( 致谢: 本论文实验在暨南大学生命科学技术学院免疫生物学系完成。魏红霞、李陈广负责动物饲养、细胞培养和药物处理等工作;徐丽慧、梁译丹参与了动物腹腔巨噬细胞的诱导和培养实验;徐丽慧、潘浩参与了免疫荧光实验;欧阳东云教授、何贤辉教授参与了实验设计、实验指导等工作。 )
| [1] | 王伟, 戴敏, 徐忠东. 丹皮酚对脂多糖/三磷酸腺苷诱导的小胶质细胞NLRP3炎症小体激活的影响[J]. 中国药理学通报, 2014, 30 (5): 652-6. Wang W, Dai M, Xu Z D. Effects of paeonol on lipopolysaccharide/adenosine 5'-triphosphate induced NLRP3 inflammasome activation in primary rat microglia[J]. Chin Pharmacol Bull, 2014, 30 (5): 652-6. |
| [2] | Kayagaki N, Stowe I B, Lee B L, et al. Caspase-11 cleaves gasdermin D for non-canonical inflammasome signalling[J]. Nature, 2015, 526 (7575): 666-71. doi:10.1038/nature15541 |
| [3] | Cullen S P, Kearney C J, Clancy D M, et al. Diverse activators of the NLRP3 inflammasome promote IL-1β secretion by triggering necrosis[J]. Cell Rep, 2015, 11 (10): 1535-48. doi:10.1016/j.celrep.2015.05.003 |
| [4] | Davis M J, Swanson J A. Technical advance: caspase-1 activation and IL-1β release correlate with the degree of lysosome damage, as illustrated by a novel imaging method to quantify phagolysosome damage[J]. J Leukoc Biol, 2010, 88 (4): 813-22. doi:10.1189/jlb.0310159 |
| [5] | 李业琼, 叶山东, 翟丽敏, 胡闻. 二甲双胍对2型糖尿病模型大鼠肾组织AGEs表达的影响[J]. 中国药理学通报, 2016, 32 (5): 703-7. Li Y Q, Ye S D, Zhai L M, Hu W. Effects of metformin on expression of renal tissue AGEs in type 2 diabetic rats[J]. Chin Pharmacol Bull, 2016, 32 (5): 703-7. |
| [6] | Lin Q R, Li C G, Zha Q B, et al. Gossypol induces pyroptosis in mouse macrophages via a non-canonical inflammasome pathway[J]. Toxicol Appl Pharmacol, 2016, 292: 56-64. doi:10.1016/j.taap.2015.12.027 |
| [7] | Huang M Y, Pan H, Liang Y D, et al. Chemotherapeutic agent CPT-11 eliminates peritoneal resident macrophages by inducing apoptosis[J]. Apoptosis, 2016, 21 (2): 130-42. doi:10.1007/s10495-015-1193-2 |
| [8] | Py B F, Jin M, Desai B N, et al. Caspase-11 controls interleukin-1β release through degradation of TRPC1[J]. Cell Rep, 2014, 6 (6): 1122-8. doi:10.1016/j.celrep.2014.02.015 |
| [9] | Idzko M, Ferrari D, Eltzschig H K. Nucleotide signalling during inflammation[J]. Nature, 2014, 509 (7500): 310-7. doi:10.1038/nature13085 |
| [10] | Shi J, Zhao Y, Wang K, et al. Cleavage of GSDMD by inflammatory caspases determines pyroptotic cell death[J]. Nature, 2015, 526 (7575): 660-5. doi:10.1038/nature15514 |
| [11] | Demon D, Kuchmiy A, Fossoul A, et al. Caspase-11 is expressed in the colonic mucosa and protects against dextran sodium sulfate-induced colitis[J]. Mucosal Immunol, 2014, 7 (6): 1480-91. doi:10.1038/mi.2014.36 |
| [12] | Oficjalska K, Raverdeau M, Aviello G, et al. Protective role for caspase-11 during acute experimental murine colitis[J]. J Immunol, 2015, 194 (3): 1252-60. doi:10.4049/jimmunol.1400501 |
| [13] | Jorgensen I, Miao E A. Pyroptotic cell death defends against intracellular pathogens[J]. Immunol Rev, 2015, 265 (1): 130-42. doi:10.1111/imr.12287 |
| [14] | Li X, Zhang Y, Xia M, et al. Activation of Nlrp3 inflammasomes enhances macrophage lipid-deposition and migration: implication of a novel role of inflammasome in atherogenesis[J]. PLoS One, 2014, 9 (1): e87552. doi:10.1371/journal.pone.0087552 |
| [15] | Bauer C, Duewell P, Mayer C, et al. Colitis induced in mice with dextran sulfate sodium (DSS) is mediated by the NLRP3 inflammasome[J]. Gut, 2010, 59 (9): 1192-9. doi:10.1136/gut.2009.197822 |
| [16] | Wree A, Eguchi A, McGeough M D, et al. NLRP3 inflammasome activation results in hepatocyte pyroptosis, liver inflammation, and fibrosis in mice[J]. Hepatology, 2014, 59 (3): 898-910. doi:10.1002/hep.v59.3 |

