


在神经系统中,嘌呤类物质三磷酸腺苷 (ATP) 不仅参与神经元-神经胶质细胞间信号网络相关生理功能的调控,还能调节突触信号传递,影响神经细胞的生长和发育。有研究表明,神经胶质细胞释放的ATP在神经胶质细胞与神经胶质细胞及神经元与神经胶质细胞间的交流中起着重要作用[1-2]。而神经元和神经胶质细胞分泌的ATP有时也会引起缺氧或脑损伤等各种病理变化。研究显示,细胞死亡时向细胞外释放的毫摩尔浓度的ATP,既可激活保护、再生作用,也可激活伤害机制[1]。本文对嘌呤受体在神经元和神经胶质细胞间信息传递作用及其在神经系统疾病中的作用进行综述。
1 嘌呤受体 1.1 嘌呤受体的提出及其分类ATP不仅是细胞内能量物质,而且可作用于细胞表面嘌呤受体产生信号传导作用。ATP作为一种兴奋性神经递质或调质广泛存在于外周及中枢神经系统[3]。1959年Holton在刺激外周神经引起逆行性血管扩张时发现感觉神经末梢有三磷酸腺苷 (ATP) 释放,首次提示ATP参与感觉神经的信息传递。Burnstock根据ATP的实验结果提出了“嘌呤能神经学说”,认为嘌呤核苷酸/ATP作为一种神经递质作用于嘌呤能神经[4];1978年Burnstock提出了“嘌呤受体 (Purinoceptor)”或“嘌呤能受体 (Purinergic receptor)”的概念,并将其分为腺苷作用的P1受体和ATP及其类似物作用的P2受体两大类。P1受体已克隆出A1、A2A、A2B、A3 4种亚型;P2受体分为P2X (配体门控的非选择性阳离子通道受体) 和P2Y (G-蛋白耦联受体)。目前己有7种P2X1-7亚型、8种哺乳动物的P2Y受体亚型 (P2Y1、2、4、6、11、12、13、14) 被克隆[5]。
1.2 嘌呤受体在神经元和神经胶质细胞中的表达P1受体的4种亚型A1、A2A、A2B、A3广泛表达于神经元、星形胶质细胞、少突胶质细胞和小胶质细胞。P2X受体亚型 (P2X1-7) 主要表达在神经元和星形胶质细胞,其中少数受体亚型也在少突胶质细胞、施万细胞和小胶质细胞表达[3],从而参与不同的生理过程,如快速突触传递,突触可塑性和神经元-神经胶质细胞信号的快速传导。相比之下,P2Y代谢型受体与长时程营养功能相关。8种P2Y受体亚型中P2Y1、2、4、6与Gq蛋白偶联激活磷脂酶C,而P2Y12、13、14与Gi蛋白偶联抑制腺苷酸环化酶而减少细胞cAMP的生成[6]。大多数P2Y受体亚型表达于中枢和周围神经系统中的神经元和神经胶质细胞,参与神经元-星形胶质细胞间的双向联系,并在细胞增殖、分化、迁移和凋亡方面发挥着重要作用。
中枢神经系统神经元表达多种嘌呤受体,P2X3受体表达于中脑突触末端、脊髓背角和背根神经节;P2X2和P2X4受体广泛表达于大脑皮层、海马、小脑、脊髓和不同脑核团;P2X7受体表达于突触前末梢和轴突生长锥,在生理和病理条件下影响神经元的活动并协调小胶质细胞与神经元/星形胶质细胞间的反应。P2Y1受体主要表达于神经元,而P2Y2受体在中枢神经系统各个区域均有低水平地表达,P2Y4、P2Y6、P2Y11、P2Y12、P2Y13和P2Y14受体也表达于不同类型的神经元[3, 7]。
中枢神经系统的胶质细胞表达不同的嘌呤受体。星形胶质细胞表达P2X1、P2X2、P2X3、P2X5、P2X7、P2Y1、P2Y2、P2Y4、P2Y6、P2Y12、P2Y14和腺苷A1、A2A、A2B、A3受体。小胶质细胞表达P2X4、P2X7、P2Y1、P2Y2、P2Y2/4、P2Y6和P2Y12受体。少突胶质细胞表达P2X7、P2Y1、P2Y2、P2Y4、P2Y6、P2Y11、P2Y13和A1受体。外周神经系统的胶质细胞也表达不同嘌呤受体,如无髓鞘的雪旺氏细胞表达A2A、A2B、P2X7、P2Y1、P2Y2受体[7]。
1.3 嘌呤和嘌呤受体在中枢神经系统神经元和神经胶质细胞间的作用在神经系统,ATP发挥包括神经元-胶质细胞信号网络在内的多种生理功能调节作用。例如,ATP可调节突触传递,并促进神经细胞生长、发育等营养作用。神经元突触前末梢和突触后膜均可释放ATP。星形胶质细胞和其他神经胶质细胞也可释放ATP。神经胶质细胞释放的ATP对神经胶质细胞之间及神经元与神经胶质细胞间的交流起着重要作用。当然,神经元和神经胶质细胞分泌的ATP有时也会导致各种病变,如缺氧或其他类型的脑损伤。
ATP功能多样性不仅通过嘌呤受体来调节,也可通过调节细胞外ATP、ADP、AMP和腺苷 (ADO) 浓度的核苷酸酶来调控。这种嘌呤浓度的可调性使嘌呤系统成为调节神经元和神经胶质细胞不同活动的重要机制。因此,嘌呤系统下调与神经系统病变密切相关。大量的嘌呤受体和受其调节的不同信号通路使该系统异常复杂,而各种因素之间的特定联系拓宽了嘌呤信号系统的功能 (见Fig 1)[7]。
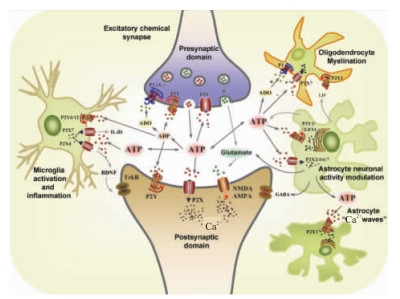
|
| 图 1 The coordinated action of glial and neuronalpurinergic receptors and purines in CNS |
突触前膜释放谷氨酸和ATP。谷氨酸作用于突触后膜AMPA受体和/或NMDA受体;胞外ATP被降解为ADP和ADO,ATP和ADP可作用于突触后膜P2X和P2Y受体。细胞外的ATP及其降解产物ADP和ADO分别作用于突触前膜的P2X、P2Y和P1(A3) 受体。突触前膜释放的ATP可通过作用于小胶质细胞P2X7受体促进IL-1β释放,也可通过作用于小胶质细胞P2X4受体引起脑源性神经营养因子 (BDNF) 的释放,再作用于疼痛通路神经元TrkB受体。活化的小胶质细胞表达的P2Y6受体介导受损部位的细胞吞噬作用。由星形胶质细胞释放的ATP、谷氨酸和γ-氨基丁酸 (GABA) 均可通过各自相应受体调节神经元的活动。ATP作用于星形胶质细胞导致其释放白血病抑制因子 (LIF),LIF通过作用于少突胶质细胞P2Y1受体促进其形成髓鞘。少突胶质细胞上的P2X7受体可介导细胞凋亡而腺苷通过作用于P1受体对细胞起到保护作用。星形胶质细胞间可通过ATP和P2Y1受体或钙波进行联系。
兴奋性化学突触的突触前膜释放共递质谷氨酸和ATP。谷氨酸作用于突触后膜AMPA受体和/或NMDA受体;ATP被胞外核苷酸酶降解成ADP和腺苷 (ADO),ATP和ADP可作用于突触后膜P2X和P2Y受体。反过来,释放到细胞外的ATP及其降解产物ADP和腺苷分别作用于突触前膜的P2X、P2Y和P1(A3) 受体调节突触前膜神经递质的释放。静息状态下的小胶质细胞表达参与神经病理性疼痛的P2X4和P2X7受体[8],突触前膜释放的ATP可通过P2X7受体促进IL-1β释放,也可通过P2X4受体引起脑源性神经营养因子 (brain derived neurotrophic factor, BDNF) 的释放。BDNF作用于疼痛通路神经元TrkB受体。P2X7和P2Y1受体介导损伤后静息小胶质细胞的迁移,而在活化的小胶质细胞表达的P2Y6受体介导受损部位的细胞吞噬作用。由星形胶质细胞释放的ATP、谷氨酸和γ-氨基丁酸 (GABA) 均可通过各自相应受体调节神经元的活动[9]。ATP作用于星形胶质细胞导致其释放白血病抑制因子 (leukemia inhibitory factor, LIF),LIF通过作用于少突胶质细胞P2Y1受体促进其形成髓鞘。少突胶质细胞上的P2X7受体可介导细胞凋亡,而腺苷通过作用于P1受体对细胞起到保护作用[1, 3, 9]。
2 嘌呤受体参与神经系统疾病神经元和神经胶质细胞上生理性表达的嘌呤受体功能性下调参与了中枢和外周神经系统的多种病理过程,包括神经损伤、精神病和神经系统退行性病变,以及神经系统功能异常等。
2.1 嘌呤受体与神经病理性疼痛慢性疼痛与神经元及其周围的神经胶质细胞之间的信息交流有关。事实上,神经元-神经胶质细胞通过嘌呤能信号进行交流也参与神经病理性疼痛。中枢神经系统中与疼痛相关的主要是小胶质细胞和星形胶质细胞,而周围神经系统主要是卫星胶质细胞 (satellite glial cells, SGC)[10]。P2X3受体主要表达于背根神经节 (dorsal root ganglion, DRG) 神经元,P2X7受体主要表达于卫星胶质细胞[11]。在DRG感觉神经元中表达的P2X3受体和在SGC中表达的P2X7受体是参与成人DRG中神经元-SGC通信的两个主要受体[12]。研究发现在DRG中,释放的ATP可通过P2X7受体激活卫星胶质细胞[13],引起肿瘤坏死因子-α(tumor necrosis factor, TNF-α) 的释放并增强邻近神经元P2X3受体介导的反应。P2X7受体的激活能够降低P2X3受体的表达,从而抑制成年大鼠的异常疼痛行为[11]。
此外,ATP和P2受体在神经病理性疼痛中的作用已有广泛研究。ATP可通过P2X2/P2X3受体产生持久的异常性疼痛。初级感觉神经元中P2X3/P2X2/3受体依赖性胞质磷脂酶A2(cytosolic phospholipase A2, cPLA2) 是神经病理性疼痛的关键因素[14]。小胶质细胞P2X4受体诱发触觉异常和痛觉过敏并产生疼痛。外周神经损伤后,脊髓小胶质细胞P2X4受体免疫反应性增强,椎管内应用P2X4受体拮抗剂可抑制触觉异常。P2X7受体的激活可促进炎症反应和神经病理性疼痛;而阻断P2X7受体可产生镇痛作用,因为阻断P2X7受体后巨噬细胞和小胶质细胞释放的促炎介质IL-1β减少,周围组织或中枢神经系统的痛觉传递神经元的伤害性感受器活性缺失而产生镇痛作用[14]。此外,IL-1β可暂时增加人星形胶质细胞P2X7受体的表达和活性,从而形成一个正反馈环路。
P2Y1受体通过阻断脊髓背角感觉神经元电压敏感性钙离子通道,减少DRG神经元释放谷氨酸来降低疼痛程度。P2Y13受体可对抗P2Y1受体的镇痛效应。神经病理性疼痛研究最多的P2Y受体就是P2Y12受体,在腰神经损伤模型脊髓同侧小胶质细胞中,P2Y12受体mRNA的表达增加。P2Y12受体的激活可诱导促炎细胞因子IL-1β和TNF-α的释放并引发神经病理性疼痛。P2Y12受体对损伤后小胶质细胞快速反应时的突起延伸是必需的,P2Y12受体特异性拮抗剂可抑制附着在有髓轴突上的小胶质细胞数量的增加,防止脱髓鞘以及触诱发痛的产生[14]。神经病理性疼痛时,小胶质细胞P2X4、P2X7和P2Y12受体的激活可以通过复杂的神经元-神经胶质细胞的相互作用维持痛觉敏感性,而这些受体特异性拮抗剂可减少神经病理性疼痛[14]。
2.2 嘌呤受体与阿尔茨海默病嘌呤受体参与了神经退行性疾病,在阿尔茨海默病 (Alzheimer disease, AD) 患者大脑海马齿状回的外层组织中A1受体表达降低,而额叶皮质中A1和A2A受体的表达增加。AD模型小鼠的β淀粉样蛋白 (amyloid beta protein, Aβ) 斑块周围P2X7受体表达上调,AD患者大脑尤其是有Aβ斑块的小胶质细胞P2X7受体表达也上调[15]。此外,体外培养的人胚胎小胶质细胞暴露在淀粉样蛋白Aβ1-42肽时P2X7受体水平及Ca2+反应均增加,而P2X7受体抑制剂可使其降低。细胞外ATP可通过P2X7受体改变β淀粉样肽诱导的巨噬细胞和小胶质细胞释放细胞因子,从而使该受体亚型成为AD相关神经炎症的重要调节因子。小胶质细胞P2X7受体上调和活性氧 (reactive oxygen species, ROS) 的产生与Aβ的增加是同步的,并与AD模型的突触毒性和脑损伤有关[16]。P2X7受体参与AD是通过AD小鼠模型中Aβ的堆积可被P2X7受体拮抗剂阻断而证实。因此,在AD大脑,P2X7受体可通过激活小胶质细胞介导嘌呤炎症反应。
其他P2嘌呤受体也与AD有关。Aβ诱导凋亡相关蛋白介导啮齿动物神经元P2X4受体的降解。P2X4受体水平降低可减少Aβ1-42诱导的神经细胞死亡,而增加神经元P2X4受体的表达可增强Aβ1-42的毒性作用。在大脑小胶质细胞中,P2X4可能具有类似的有助于CNS内的神经元兴奋性的功能。P2Y2受体密度降低与AD患者死后顶叶皮质中突触素免疫反应性降低相关。P2Y1受体出现在AD典型结构中,如神经原纤维缠结、神经炎性斑块和神经纤维丝。嘌呤受体也可作用于星形胶质细胞参与AD的病理改变。例如,Aβ25-35激活的星形胶质细胞释放ATP和谷氨酸可激活神经元半通道并导致神经损伤[17-18]。
虽然目前还没有防止和逆转AD的有效方法,但治疗可以减缓AD的发病进程并减少AD患者的数量[18]。嘌呤受体选择性激动剂和拮抗剂对许多在体和离体的AD动物模型有治疗作用。在来自AD患者的死后新皮层和海马组织中,报道了A1受体与Aβ在老年斑中的共定位[19]。这表明,在人神经母细胞瘤细胞中,A1受体激活的PKC、p21Ras和ERK1/2,导致可溶性Aβ片段的增加。这些发现将暗示A1受体存在于Aβ代谢,表明这些受体的激动剂可能用于治疗已确立或晚期AD的有用药物[20]。神经元P1受体 (A1与A2A) 主要是针对促进非淀粉样β淀粉样前体蛋白 (amyloid beta amyloid precursor protein, APP) 的处理和防止淀粉样蛋白诱导的神经毒性。P2X和P2Y受体针对神经元、小胶质细胞和星形胶质细胞调节多种治疗反应,包括减少炎症和神经毒性,提高非淀粉样APP处理,促进抗体的摄取和降解、促进神经再生[18]。ATP通过P2Y受体的激活和新的蛋白质合成,引起缺血性耐受并增强培养的原代皮层神经元中存活APP的加工,两种不同的核苷酸受体P2X7和P2Y2调节,对α-分泌酶活性具有相反的作用[21]。这表明P2Y2受体的激活剂与P2X7受体拮抗剂的组合可以通过减少淀粉样蛋白斑而具有有益效果。
2.3 嘌呤受体与癫痫细胞外核苷酸和嘌呤受体都参与了癫痫发作[22]。胞外核苷酸酶在不同癫痫动物模型的海马区有着不同程度的表达和激活,如核苷酸双磷酸酶2和3及胞外-5′核苷酸酶。细胞外ATP浓度也会增加并被迅速分解为腺苷。嘌呤受体表达增加同时发现不同细胞外核苷酸酶被激活。事实上,在癫痫病人的血清中,ATP、ADP、AMP的水解率都明显增强。部分研究提出增加大脑皮层和海马A1受体的密度可通过星形胶质细胞释放谷氨酸降低癫痫发作的频率。另一方面,星形胶质细胞也调节腺苷在大脑中介导的内源性抗惊厥作用。除了腺苷参与癫痫发作,ATP和ADP也可能参与。
研究表明慢性癫痫发作大鼠的海马对ATP的异常反应与P2X7受体的表达上升有关,提示P2X7受体也参与癫痫发作。小胶质细胞的P2X7受体上调可能参与了癫痫的炎症反应以及颞叶癫痫的病理生理过程。海人藻酸诱导癫痫发作后可导致小胶质细胞的P2X7受体水平升高,在癫痫持续状态后7 d的海马齿状回出现了P2X7受体免疫反应明显升高[23]。P2Y12受体是高度敏感的细胞外ATP传感器[24]。在大脑中,P2Y12受体几乎仅在小胶质细胞中表达。研究表明P2Y12受体是小胶质细胞趋化性动力学的关键调节物。例如,NMDA受体活性可导致ATP的局部产生[25]。在一些激活条件下,其诱导针对神经元活性的P2Y12受体依赖性小胶质细胞生长 (癫痫)。总之,细胞外核苷酸参与癫痫和癫痫发作的调控,促进了嘌呤受体在癫痫病人脑中星形胶质细胞和小胶质细胞的激活,影响神经系统功能[26]。
近年来,已经开发了许多不同类别的小分子量、药物样P2X7受体配体,并且在P2X受体家族中P2X7受体已经被定性为最“可能药物”的靶点。近期研究也提出有效的P2X7受体拮抗剂的发展。通过化合物文库的系统搜索已进一步发现新的P2X7受体拮抗剂和变构调节剂可用于基础研究或药物开发。天然化合物的分析也产生了几种有价值的P2X7受体配体。虽然P2X7受体拮抗剂 (例如CE-224, 535[27]和AZD 9056[28]) 发展的终产物在Ⅱ期试验中未被证明有效。但在类风湿性关节炎患者的临床研究中显示这种拮抗剂可作为一个整体的可接受的安全性和耐受性,打开了在新的领域例如CNS疾病中发展P2X7受体靶向化合物的可能性[29]。
3 结论嘌呤受体在中枢神经系统和周围神经系统中的所有细胞类型中都有表达,并参与复杂的细胞信号转导系统。多种类型的嘌呤、嘌呤受体和胞外核苷酸酶的结合精确调节神经元和神经胶质细胞活动,协调不同的生理和病理状态。嘌呤受体在神经胶质细胞中已经被广泛研究,主要是星形胶质细胞和小胶质细胞。虽然有较多研究表明嘌呤受体参与神经系统疾病中神经元与神经胶质细胞的相互作用,但到目前为止仍然没有可在临床上使用的针对嘌呤受体的特异性的药物。因此,嘌呤受体特异性的药物研发可能是其研究的一个新热点。
( 致谢: 感谢南昌大学江西医学院神经生理实验室老师和同学的帮助。 )
| [1] | Castellano B, Bosch-Queralt M, Almolda B, et al. Purine Signaling and Microglial Wrapping[J]. Adv Exp Med Biol, 2016, 949: 147-65. doi:10.1007/978-3-319-40764-7 |
| [2] | Lalo U, Verkhratsky A, Pankratov Y. Ionotropic ATP receptors in neuronal-glial communication[J]. Semin Cell Dev Biol, 2011, 22 (2): 220-8. doi:10.1016/j.semcdb.2011.02.012 |
| [3] | Burnstock G. An introduction to the roles of purinergic signalling in neurodegeneration, neuroprotection and neuroregeneration[J]. Neuropharmacology, 2016, 104: 4-17. doi:10.1016/j.neuropharm.2015.05.031 |
| [4] | Ralevic V, Burnstock G. Receptors for purines and pyrimidines[J]. Pharmacol Rev, 1998, 50 (3): 413-92. |
| [5] | Amadio S, Apolloni S, D′Ambrosi N, et al. Purinergic signalling at the plasma membrane: a multipurpose and multidirectional mode to deal with amyotrophic lateral sclerosis and multiple sclerosis[J]. J Neurochem, 2011, 116 (5): 796-805. doi:10.1111/jnc.2011.116.issue-5 |
| [6] | Jacobson K A, Muller C E. Medicinal chemistry of adenosine, P2Y and P2X receptors[J]. Neuropharmacology, 2016, 104: 31-49. doi:10.1016/j.neuropharm.2015.12.001 |
| [7] | Del Puerto A, Wandosell F, Garrido J J. Neuronal and glial purinergic receptors functions in neuron development and brain disease[J]. Front Cell Neurosci, 2013, 7: 197. |
| [8] | Ulmann L, Levavasseur F, Avignone E, et al. Involvement of P2X4 receptors in hippocampal microglial activation after status epilepticus[J]. Glia, 2013, 61 (8): 1306-19. doi:10.1002/glia.v61.8 |
| [9] | Kuboyama K, Harada H, Tozaki-Saitoh H, et al. Astrocytic P2Y (1) receptor is involved in the regulation of cytokine/chemokine transcription and cerebral damage in a rat model of cerebral ischemia[J]. J Cereb Blood Flow Metab, 2011, 31 (9): 1930-41. doi:10.1038/jcbfm.2011.49 |
| [10] | Chen Y, Li G, Huang L Y. P2X7 receptors in satellite glial cells mediate high functional expression of P2X3 receptors in immature dorsal root ganglion neurons[J]. Mol Pain, 2012, 8: 9. |
| [11] | Chen Y, Zhang X, Wang C, et al. Activation of P2X7 receptors in glial satellite cells reduces pain through downregulation of P2X3 receptors in nociceptive neurons[J]. Proc Natl Acad Sci USA, 2008, 105 (43): 16773-8. doi:10.1073/pnas.0801793105 |
| [12] | Gu Y, Chen Y, Zhang X, et al. Neuronal soma-satellite glial cell interactions in sensory ganglia and the participation of purinergic receptors[J]. Neuron Glia Biol, 2010, 6 (1): 53-62. doi:10.1017/S1740925X10000116 |
| [13] | 焦晓翠, 张会然, 张璇, 司曼. 卫星胶质细胞对外周神经元作用的研究进展[J]. 中国药理学通报, 2014, 30 (5): 612-4. Jiao X C, Zhang H R, Zhang X, Si M. Research progress in interactions between neuron and satellite glial cells[J]. Chin Pharmacol Bull, 2014, 30 (5): 612-4. |
| [14] | Burnstock G. Purinergic Mechanisms and Pain[J]. Adv Pharmacol, 2016, 75: 91-137. doi:10.1016/bs.apha.2015.09.001 |
| [15] | Delarasse C, Auger R, Gonnord P, et al. The purinergic receptor P2X7 triggers alpha-secretase-dependent processing of the amyloid precursor protein[J]. J Biol Chem, 2011, 286 (4): 2596-606. doi:10.1074/jbc.M110.200618 |
| [16] | Lee H G, Won S M, Gwag B J, et al. Microglial P2X (7) receptor expression is accompanied by neuronal damage in the cerebral cortex of the APPswe/PS1dE9 mouse model of Alzheimer′s disease[J]. Exp Mol Med, 2011, 43 (1): 7-14. doi:10.3858/emm.2011.43.1.001 |
| [17] | Orellana J A, Froger N, Ezan P, et al. ATP and glutamate released via astroglial connexin 43 hemichannels mediate neuronal death through activation of pannexin 1 hemichannels[J]. J Neurochem, 2011, 118 (5): 826-40. doi:10.1111/jnc.2011.118.issue-5 |
| [18] | Woods L T, Ajit D, Camden J M, et al. Purinergic receptors as potential therapeutic targets in Alzheimer′s disease[J]. Neuropharmacology, 2016, 104: 169-79. doi:10.1016/j.neuropharm.2015.10.031 |
| [19] | Angulo E, Casado V, Mallol J, et al. A1 adenosine receptors accumulate in neurodegenerative structures in Alzheimer disease and mediate both amyloid precursor protein processing and tau phosphorylation and translocation[J]. Brain Pathol, 2003, 13 (4): 440-51. |
| [20] | Gomes C V, Kaster M P, Tome A R, et al. Adenosine receptors and brain diseases: neuroprotection and neurodegeneration[J]. Biochim Biophys Acta, 2011, 1808 (5): 1380-99. doi:10.1016/j.bbamem.2010.12.001 |
| [21] | Leon-Otegui M, Gomez-Villafuertes R, Diaz-Hernandez J I, et al. Opposite effects of P2X7 and P2Y2 nucleotide receptors on alpha-secretase-dependent APP processing in Neuro-2a cells[J]. FEBS Lett, 2011, 585 (14): 2255-62. doi:10.1016/j.febslet.2011.05.048 |
| [22] | Rassendren F, Audinat E. Purinergic signaling in epilepsy[J]. J Neurosci Res, 2016, 94 (9): 781-93. doi:10.1002/jnr.23770 |
| [23] | Rappold P M, Lynd-Balta E, Joseph S A. P2X7 receptor immunoreactive profile confined to resting and activated microglia in the epileptic brain[J]. Brain Res, 2006, 1089 (1): 171-8. doi:10.1016/j.brainres.2006.03.040 |
| [24] | Nayak D, Roth T L, McGavern D B. Microglia development and function[J]. Annu Rev Immunol, 2014, 32: 367-402. doi:10.1146/annurev-immunol-032713-120240 |
| [25] | Dissing-Olesen L, LeDue J M, Rungta R L, et al. Activation of neuronal NMDA receptors triggers transient ATP-mediated microglial process outgrowth[J]. J Neurosci, 2014, 34 (32): 10511-27. doi:10.1523/JNEUROSCI.0405-14.2014 |
| [26] | Marchi N, Granata T, Janigro D. Inflammatory pathways of seizure disorders[J]. Trends Neurosci, 2014, 37 (2): 55-65. doi:10.1016/j.tins.2013.11.002 |
| [27] | Stock T C, Bloom B J, Wei N, et al. Efficacy and safety of CE-224, 535, an antagonist of P2X7 receptor, in treatment of patients with rheumatoid arthritis inadequately controlled by methotrexate[J]. J Rheumatol, 2012, 39 (4): 720-7. doi:10.3899/jrheum.110874 |
| [28] | Keystone E C, Wang M M, Layton M, et al. Clinical evaluation of the efficacy of the P2X7 purinergic receptor antagonist AZD9056 on the signs and symptoms of rheumatoid arthritis in patients with active disease despite treatment with methotrexate or sulphasalazine[J]. Ann Rheum Dis, 2012, 71 (10): 1630-5. doi:10.1136/annrheumdis-2011-143578 |
| [29] | Ali Z, Laurijssens B, Ostenfeld T, et al. Pharmacokinetic and pharmacodynamic profiling of a P2X7 receptor allosteric modulator GSK1482160 in healthy human subjects[J]. Br J Clin Pharmacol, 2013, 75 (1): 197-207. doi:10.1111/bcp.2013.75.issue-1 |

