


2. 沈阳医学院 辽宁省环境污染与微生态重点实验室,辽宁 沈阳 110034
2. Key Laboratory of Environmental Pollution and Microecology of Liaoning Province, Shenyang Medical College, Shenyang 110034, China
乳腺癌的发生发展与多种肿瘤细胞增殖、凋亡、侵袭、转移的蛋白有关。组蛋白去乙酰化酶1(histone deacetylases 1,HDAC1) 使组蛋白去乙酰化,增加组蛋白与DNA双链的亲和性,可与一些调控肿瘤发生发展的基因启动子区结合而抑制这些基因的转录。HDAC抑制剂 (histone deacetylase inhibitor, HDACi) 是一类可以抑制组蛋白去乙酰化酶活性、维持组蛋白乙酰化水平的化合物,可促使肿瘤细胞生长停滞并诱发细胞凋亡。辛二酰苯胺异羟肟酸 (suberoylanilide hydroxamic acid,SAHA) 是目前已知最经典的HDACi之一, 主要用于皮肤T细胞淋巴瘤的治疗。SAHA可以通过上调p21WAF1/CIP1引起细胞周期阻滞于G1期而抑制细胞增殖[1]。
p21WAF1/CIP1是细胞周期依赖性蛋白激酶抑制剂,可使细胞周期停滞、促进细胞凋亡并抑制癌细胞的转移和侵袭。乳腺癌p21WAF1/CIP1的表达与细胞分化程度无关,与淋巴结转移显著负相关,p21WAF1/CIP1的高表达有抑制肿瘤转移的作用[2]。
瘦素 (Leptin) 是肥胖基因的表达产物,主要由脂肪细胞合成和分泌,包含167个氨基酸,通过与瘦素受体OB-Rb结合发挥作用。Leptin血清水平与脂肪储存量成正比[3],研究表明:随着女性体内Leptin水平增加,其患高恶性、低分化且预后不良的乳腺癌几率大大增加[4]。本研究的前期工作证实Leptin处理后的小鼠乳腺癌4T1细胞p21WAF1/CIP1 mRNA及蛋白表达水平远远低于Leptin未处理组细胞[5]。
本实验旨在找出HDAC1募集于p21WAF1/CIP1启动子区调控其转录活性的具体作用位点,明确SAHA及Leptin在调节p21WAF1/CIP1启动子功能过程中的分子机制。
1 材料与方法 1.1 材料人乳腺癌细胞株MCF-7(美国ATCC细胞库), SAHA、Leptin (Sigma), 完全型RPMI 1640培养液、改良型RPMI 1640培养液、磷酸盐缓冲液1X (Thermo), 0.25%胰酶-EDTA (Gibco), PierceTM Agarose ChIP试剂盒 (Thermo), HDAC1抗体 (Abcam), Power SYBR® Green PCR Master Mix (Life technologies), p21WAF1/CIP1 f1~f10引物 (上海生工生物工程有限公司), 超净工作台、CO2恒温细胞培养箱 (Thermo), Biofuge 28RS低温高速离心机 (Heraeus), 倒置显微镜 (Olympus), SK-D1807-E摇床 (Scilogex), 恒温混匀器 (Eppendorf), 7500 Real-Time PCR仪 (Life Technologies)。
1.2 方法 1.2.1 细胞培养将MCF-7细胞接种在完全型RPMI 1640培养液 (10%胎牛血清,青霉素、链霉素100 kU·L-1) 中,37℃、5% CO2孵箱饱和湿度条件下贴壁传代培养,每2~3天换液并传代1次。0.25%胰酶-EDTA消化。经2~3次传代, 取对数生长期的细胞等量分成3组,分别接种于完全型RPMI 1640培养液中,24 h后,再将细胞置于改良型RPMI 1640培养液中进行同步化处理24 h,此后将3组细胞分别定义为SAHA组 (S组,即完全型RPMI 1640培养液10 mL+20 μmol·L-1 SAHA 0.88 μL)、Leptin组 (L组,即完全型RPMI 1640培养液10 mL+0.625 nmol·L-1 Leptin 10 μL),Basal对照组 (B组,即加等量完全型RPMI 1640培养液)。
1.2.2 应用染色质免疫共沉淀技术 (chromatin-immunoprecipitation, ChIP) 处理样品MCF-7细胞的甲醛交联及细胞团的分离;细胞溶解及MNase消化,每组样品各得到50 μL的MNase消化产物,留取5 μL-20℃保存作为内对照,45 μL进行下一步的免疫沉淀处理,免疫沉淀过程中需向每个ChIP样品加入HDAC1抗体10 μg,实验步骤均按操作手册完成。最终3组MCF-7细胞均获得ChIP得到的DNA及各自的内对照。
1.2.3 Real-time PCR检测各组p21WAF1/CIP1 f1~f10片段的DNA相对表达PCR反应体系为25 μL:DNA 1.5 μL,上下游引物各0.75 μL,PCR Master Mix 12.5 μL, ddH2O 9.5 μL。反应条件为:50℃ 2 min, 95℃ 10 min预变性, 95℃ 15 s, 60℃ 1 min, 共40个循环。每个样品3个复孔,采用2-ΔΔCT法计算各组DNA的相对表达量。
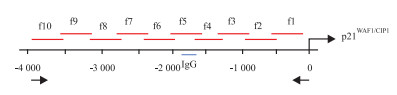
p21WAF1/CIP1启动子区的10个片段的引物序列为: f1:Forward 5′-TCC TCC TGG AGA GTG CCA AC-3′,Reverse 5′-TTG GTG CGC TGG ACA CAT TT-3′;f2:Forward 5′-TTC CCG GAA GCA TGT GAC AA-3′,Reverse 5′-GCA CCT GGA GCA CCT AGA CAC C-3′;f3:Forward 5′-CCC GTT TCC CCA GCA GTG TA-3′,Reverse 5′-GCC AGG AAG GGG AGG ATT TG-3′;f4:Forward 5′-AGG CCA AGG GGG TCT GCT AC-3′,Reverse 5′-CGG GGA GGA CAG GCT TCT TT-3′;f5:Forward 5′-TGA AAG CAG AGG GGC TTC AA-3′,Reverse 5′-ACC ATC CAA AGG GCT GGT TG-3′;f6:Forward 5′-TGT CCT TGG GCT GCC TGT TT-3′,Reverse 5′-AGC CCT GTC GCA AGG ATC TG-3′;f7:Forward 5′-TTC TGC AGC CAC CAC TGA GC-3′,Reverse 5′-GTG GAG CAG CAT GGG GTA GG-3′;f8:Forward 5′-CCC ACC TCA GCC ACC TGA AT-3′,Reverse 5′-GGG CAG ATC ACA GGG TCA GG-3′;f9:Forward 5′-AGT GGG CAC ATT TAG ACA TAG CAG GT-3′,Reverse 5′-CCT CCC GGT CAT GCC TTT C-3′;f10:Forward 5′-GTC AGG TGC CAC TGG GGT CT-3′,Reverse 5′-CGG TCC CCT GTT TCA ATG CT-3′。p21WAF1/CIP1启动子区+2~-4 000 bp 10个选定区域f1~f10(Fig 1)。
|
| Fig 1 Schematic diagram of HDAC1 response element forregulating transcriptional function of p21WAF1/CIP promoter |
所有数据均用x±s表示,采用GraphPad Prism 6.0软件分析,t检验进行统计学处理。
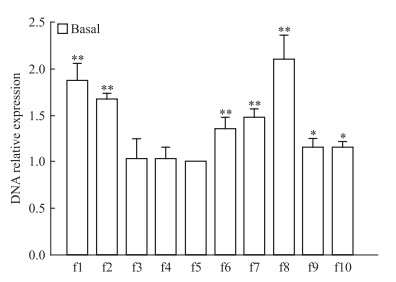
2 结果 2.1 B组MCF-7细胞p21WAF1/CIP1启动子区f1~f10片段HDAC1高功能结合位点筛选B组MCF-7细胞经HDAC1抗体Chip处理后,45 μL样品与5 μL内对照的DNA分别与f1~f10引物作用进行Real-time PCR扩增,所得CT值之差为该样品在p21启动子区各自片段的ΔCT值,再以f5片段为对照,其它片段的ΔCT值与其相减,得到B组样品在p21启动子区f1~f10片段各自ΔΔCT值,采用2-ΔΔCT法计算各片段DNA的相对表达量。B组f1、f2、f6、f7、f8片段DNA的相对表达量 (1.88±0.18、1.68±0.07、1.35±0.13、1.49±0.09、2.11±0.26) 较f5片段相对表达量 (1±0) 明显升高 (P < 0.01),f8片段达最高值 (Fig 2)。
|
| Fig 2 Screening of high function bindsite of HDAC1 among f1~f10 fragmentsof p21WAF1/CIP promotor region in basal group MCF-7 cells *P < 0.05, **P < 0.01 vs f5 fragment |
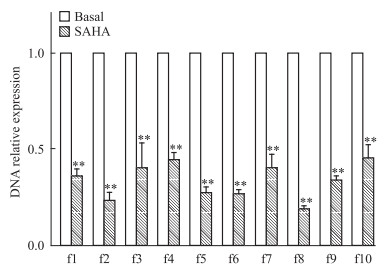
S组MCF-7细胞DNA组分经HDAC1抗体ChIP处理后,进行Real-time PCR检测。结果表明:S组MCF-7细胞的p21WAF1/CIP启动子f1~f10片段DNA的相对表达量 (0.36±0.03、0.23±0.04、0.39±0.13、0.44±0.03、0.27±0.03、0.27±0.02、0.40±0.07、0.19±0.02、0.34±0.02、0.45±0.07) 较B组对应片段相对表达量 (1±0) 均明显降低 (P < 0.01),f8片段达最低值 (Fig 3)。
|
| Fig 3 Screening of high function bindsite of HDAC1 among f1~f10 fragments ofp21WAF1/CIP promotor region in MCF-7 cells in SAHA group **P < 0.01 vs basal group |
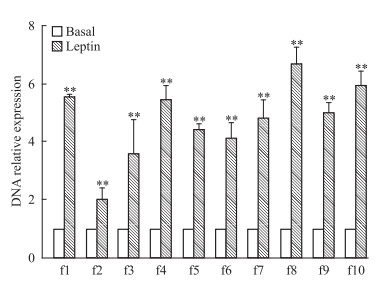
将Leptin处理后的MCF-7细胞的DNA组分经ChIP实验后进行Real-time PCR检测。结果表明:L组细胞p21WAF1/CIP启动子区f1~f10片段结合HDAC1抗体的DNA相对表达量 (5.54±0.17、2.01±0.39、3.59±1.15、5.43±0.48、4.49±0.16、4.14±0.49、4.79±0.66、6.68±0.57、5.02±0.31、5.94±0.45) 较B组对应片段相对表达量 (1±0) 均明显升高 (P < 0.01),f8片段达最高值 (Fig 4)。
|
| Fig 4 Screening of high function bind siteof HDAC1 among f1~f10 fragments of p21WAF1/CIPpromotor region in MCF-7 cells in Leptin group **P < 0.01 vs basal group |
乳腺癌是女性恶性肿瘤之首,其中0.7~0.8的患者为雌激素受体 (estrogen receptor,ER) 阳性[6],因此选择ER阳性的MCF-7乳腺癌细胞系探索乳腺癌的发病机制及治疗药物尤为重要。
表观遗传改变是基因DNA序列不发生变化,但基因表达却发生了可遗传的改变。组蛋白乙酰化及去乙酰化等共价修饰是表观遗传学的主要研究内容,现已逐渐成为乳腺癌研究和治疗的热点[7]。在乳腺癌细胞增殖过程中,细胞增殖信号在p21WAF1/CIP1的启动子区招募HDAC1转录因子,通过组蛋白去乙酰化表观遗传修饰影响p21WAF1/CIP表达。SAHA通过抑制此过程而上调p21WAF1/CIP1基因的转录。Leptin通过激活HDAC1的活性使核心组蛋白去乙酰化,从而抑制p21WAF1/CIP1的表达,最终促进细胞周期从G1期到S期的进程[8]。
ChIP可真实、完整地反映结合在DNA序列上的靶蛋白的调控信息, 是目前基于全基因组水平研究DNA-蛋白质相互作用的标准实验技术。本实验利用这一方法研究发现:B组MCF-7细胞p21WAF1/CIP基因转录起始点近端启动子调节区f1和远端调节区f8片段结合HDAC1抗体的DNA相对表达量较其它区域明显升高。这表明在细胞增殖过程中,HDAC1可被招募至p21WAF1/CIP启动子区,促使组蛋白去乙酰化,增强组蛋白与DNA的亲和力,抑制p21WAF1/CIP基因转录。
SAHA作用下的MCF-7细胞,与p21WAF1/CIP启动子区DNA结合的HDAC1抗体明显减少,这表明作用于p21WAF1/CIP启动子区的HDAC1明显减少, 且在f8片段 (-2 800 bp至-3 200 bp) 处受SAHA影响HDAC1与p21WAF1/CIP启动子区DNA的结合量最少。SAHA作为一种广谱的HDACi,可抑制HDAC1的活性,从而提高组蛋白乙酰化的程度。高乙酰化的组蛋白可提高相关基因 (如p21WAF1/CIP) 的转录水平,最终表现为肿瘤细胞的增殖抑制、分化和凋亡[9]。另有研究报道:SAHA可降低HDAC1的表达而抑制癌组织的生长[10-11]。
Leptin可通过调控细胞周期、凋亡、影响细胞外环境等多重机制促进雌激素受体阳性的MCF-7乳腺癌细胞增殖与转移[12-14]。本实验中:Leptin作用下的MCF-7细胞,与p21WAF1/CIP启动子区DNA结合的HDAC1抗体明显增多,表明作用于p21WAF1/CIP启动子区的HDAC1明显增多,且在f8片段处受Leptin影响HDAC1与p21WAF1/CIP启动子区DNA的结合量最多。这一实验现象表明:在乳腺癌发生、发展过程中,某些细胞增殖信号招募HDAC1于p21WAF1/CIP启动子特定区域,调控Leptin对p21WAF1/CIP基因转录的作用。
综上所述,本研究通过ChIP技术筛选出乳腺癌MCF-7细胞p21WAF1/CIP1启动子区的HDAC1高功能结合位点,进而通过对SAHA及Leptin处理过的乳腺癌MCF-7细胞进行ChIP检测,明确p21WAF1/CIP启动子区-2 800 bp至-3 200 bp区域可能是与HDAC1高度结合的功能活跃区。此研究发现丰富了SAHA和Leptin在调节p21WAF1/CIP1启动子功能过程中的分子机制,更为抗乳腺癌的药物研发及靶向治疗奠定了理论和实验基础。
( 致谢: 衷心感谢沈阳医学院辽宁省环境污染与微生态重点实验室为本实验顺利完成提供的实验设备,感谢实验室全体工作人员对本实验的大力协助。 )
| [1] | Lee Y J, Won A J, Lee J, et al. Molecular mechanism of SAHA on regulation of autophagic cell death in tamoxifen-resistant MCF-7 breast cancer cells[J]. Int J Med Sci, 2012, 9 (10): 881-93. doi:10.7150/ijms.5011 |
| [2] | Thor A D, Liu S, Moore D H, et al. p21(WAF1/CIP1) expression in breast cancers: associations with p53 and outcome[J]. Breast Cancer Res Treat, 2000, 61 (1): 33-43. doi:10.1023/A:1006455526894 |
| [3] | Grossmann M E, Ray A, Nkhata K J, et al. Obesity and breast cancer: status of leptin and adiponectin in pathological processes[J]. Cancer Metastasis Rev, 2010, 29 (4): 641-53. doi:10.1007/s10555-010-9252-1 |
| [4] | Hancke K, Grubeck D, Hauser N, et al. Adipocyte fatty acid-binding protein as a novel prognostic factor in obese breast cancer patients[J]. Breast Cancer Res Treat, 2010, 119 (2): 367-77. doi:10.1007/s10549-009-0577-9 |
| [5] | Zhou W, Guo S, Gonzalez-Perez R R. Leptin pro-angiogenic signature in breast cancer is linked to IL-1 signalling[J]. Br J Cancer, 2011, 104 (1): 128-37. doi:10.1038/sj.bjc.6606013 |
| [6] | Chargari C, Toillon R A, Macdermed D, et al. Concurrent hormone and radiation therapy in patients with breast cancer: what is the rationale[J]. Lancet Oncol, 2009, 10 (1): 53-60. doi:10.1016/S1470-2045(08)70333-4 |
| [7] | Connolly D, Yang Z, Castaldi M, et al. Septin 9 isoform expression, localization and epigenetic changes during human and mouse breast cancer progression[J]. Breast Cancer Res, 2011, 13 (4): R76. doi:10.1186/bcr2924 |
| [8] | Gonzalez-Perez R R, Xu Y, Guo S, et al. Leptin upregulates VEGF in breast cancer via canonic and non-canonical signalling pathways and NF-kappaB/HIF-1alpha activation[J]. Cell Signal, 2010, 22 (9): 1350-62. doi:10.1016/j.cellsig.2010.05.003 |
| [9] | Fiskus W, Hembruff S L, Rao R, et al. Co-treatment with vorinostat synergistically enhances activity of Aurora kinase inhibitor against human breast cancer cells[J]. Breast Cancer Res Treat, 2012, 135 (2): 433-44. doi:10.1007/s10549-012-2171-9 |
| [10] | Jin J S, Tsao T Y, Sun P C, et al. SAHA inhibits the growth of colon tumors by decreasing histone deacetylase and expression of cyclin D1 and survivin[J]. Pathol Oncol Res, 2012, 18 (3): 713-20. doi:10.1007/s12253-012-9499-7 |
| [11] | 韩翰, 王敏. SAHA和TRAIL联合使用对乳腺癌雌激素受体阳性细胞MCF-7生长的影响[J]. 中国药理学通报, 2016, 32 (2): 223-8. Han H, Wang M. Effects of combination treatment with SAHA and TRAIL on ER positive breast cancer cell MCF-7[J]. Chin Pharmacol Bull, 2016, 32 (2): 223-8. |
| [12] | Perera C N, Chin H G, Duru N, et al. Leptin-regulated gene expression in MCF-7 breast cancer cells:mechanistic insights into leptin-regulated mammary tumor growth and progression[J]. J Endocrinol, 2008, 199 (2): 221-33. doi:10.1677/JOE-08-0215 |
| [13] | Strong A L, Ohlstein J F, Biagas B A, et al. Leptin produced by obese adipose stromal/stem cells enhances proliferation and metastasis of estrogen receptor positive breast cancers[J]. Breast Cancer Res, 2015, 17 : 112. doi:10.1186/s13058-015-0622-z |
| [14] | 冯秀艳, 韩翰, 周伟强. SAHA在Leptin诱导的乳腺癌MCF-7细胞增殖过程中的调控作用[J]. 中国药理学通报, 2016, 32 (4): 503-8. Feng X Y, Han H, Zhou W Q. Regulation of SAHA on cell proliferation induced by leptin in breast cancer cell line MCF-7[J]. Chin Pharmacol Bull, 2016, 32 (4): 503-8. |

