


2. 安徽省医学科学研究院,安徽 合肥 230022
2. Anhui Academy of Medical Sciences, Hefei 230022, China
心肌缺血/再灌注损伤是目前临床面临的主要挑战及难题。氧化应激和炎症是心肌缺血/再灌注损伤的主要机制,研究发现Toll样受体4(Toll-like receptor 4, TLR4) 是参与心肌缺血/再灌注损伤的主要炎症反应[1]。TLR4在不同细胞中均可表达,被激活后导致促炎性细胞因子的产生及其表达上调[2]。据报道,TLR4与病原相关分子结合后,启动髓样分化因子88(myeloid differentiation factor 88, MyD88) 进行细胞内信号转导,激活核因子-κB (nuclear factor κB,NF-κB)。NF-κB和IκBα是一个相互调节的系统,IκBα的迅速积累可抑制NF-κB活性,TNF-α诱导含IκBα的细胞后,可见NF-κB高度表达,进而刺激一系列的炎症介质如TNF-α和IL-1β等的释放,破坏机体心脏免疫系统,最终引起炎症因子大量释放,刺激炎症反应发生,致使心肌细胞发生凋亡等[3-5]。
黄精多糖(Polygonatum sibiricum polysaccharides,PSP) 是百合科黄精属黄精的干燥根茎通过水提醇沉、超声波提取或微波辅助提取等提取方法而得,主要由4种化学结构不同的单糖组成,其中以β-(1, 2) 键相连的果糖为主链,以α构型的葡萄糖为侧链连接于主链上。PSP的相对分子质量为8 921 u,其中果糖:葡萄糖=8.7 :1[6]。PSP具有抗炎、抗肿瘤、抗凋亡和降低脂肪等多种生物活性[7-8]。研究报道,PSP对缺血/再灌注模型大鼠的心肌损伤具有改善作用,能够减轻炎症反应,其修复缺血心肌损伤的机制可能与调节NF-κB信号通路有关[9]。TLR4是NF-κB上游调控基因,期间有依赖性分子MyD88衔接,但有关PSP对TLR4/MyD88/NF-κB信号通路的调节作用未见报道。因此,本研究采用TLR4抑制剂TAK-242[10],以缺氧/复氧(hypoxia-reoxygenation,H/R) 诱导H9c2心肌细胞损伤为模型,旨在探讨:① PSP对H/R损伤心肌细胞的影响;② PSP能否降低H/R诱导H9c2细胞的TLR4/MyD88/NF-κB的炎性表达;③ PSP与H/R介导的TLR4/MyD88/NF-κB的关系如何;④ PSP能否通过调控TLR4/MyD88/NF-κB对抗H/R引起的心肌损伤。
1 材料与方法 1.1 材料 1.1.1 细胞株H9c2大鼠胚胎心肌细胞株购于中国科学院上海生命科学研究所细胞资源中心。
1.1.2 药物与试剂黄精多糖(由安徽省医学研究院提取并检测,含多糖为97%,应用前采用培养液稀释成浓度为1.5 g·L-1使用);TLR4抑制剂TAK-242(购于InvivoGen公司);DMEM、胎牛血清、TRIzol、DMSO和Tween-20均购于美国Life Technologies公司;四甲基偶氮唑蓝(MTT, Sigma公司);TNF-α、IL-1β酶联免疫吸附试剂盒购自武汉博士德生物有限公司;NF-κB、IκBα和β-actin抗体购于Abcam公司;RIPA裂解液、BCA蛋白浓度测定试剂盒、SDS-PAGE凝胶配制试剂盒、超敏ECL化学发光试剂盒(上海碧云天公司);PVDF膜(美国密理博公司);引物由Invitrogen公司鉴定并合成;逆转录试剂盒(Revert AidTM First Strand cDNA Synthesis Kit)(Thermo公司)。
1.1.3 仪器3111型-恒温CO2培养箱(美国Thermo公司);ATOM全自动酶联免疫工作站(意大利MAROCHE);3K15-高速冷冻离心机(德国Sigma公司);SW-CJ系列洁净工作台(AIRTECH,苏州安泰空气技术有限公司);缺氧小室(加拿大Stem Cell公司);CXY-6C型电泳仪(北京六一仪器厂);荧光定量PCR仪(Thermo PIKOREAL96)。
1.2 方法 1.2.1 H9c2心肌细胞培养将H9c2心肌细胞株放于37℃、95%空气-5% CO2培养箱中,用含15%胎牛血清的DMEM完全培养基培养。待细胞融合度为85%左右时,用质量浓度为0.25 g·L-1的胰酶消化,计数,以1.0×106个细胞接种于25 cm2的培养瓶进行传代,每2 d换液1次,每3~4 d传代1次。取对数生长期的心肌细胞用于后续实验。
1.2.2 H9c2心肌细胞缺氧/复氧损伤模型建立待细胞融合至95%后,弃掉细胞培养基,加入预先经37℃、95% N2-5% CO2的混合气体饱和30 min的无血清DMEM模拟缺氧液,放入缺氧小室中,通入95% N2-5% CO2的混合气体5 min驱除氧气,置于37℃培养箱中培养21 h进行缺氧,然后将缺氧液换为含正常培养基,于37℃、95%空气-5% CO2培养箱中培养6 h模拟复氧[11-12]。
1.2.3 实验分组及处理将培养的H9c2心肌细胞随机分为5组:正常对照组(C组)、H/R组、TAK-242组、PSP组和PSP+TAK-242组。C组细胞用正常培养液(质量浓度为15 g·L-1胎牛血清的DMEM完全培养基) 在37℃、95%空气-5% CO2培养箱中培养27 h;H/R组细胞处理同“1.2.2”步骤;TAK-242组、PSP组和PSP+TAK-242组的细胞在缺氧培养21 h前,缺氧处理方法同步骤“1.2.2”,先分别加入含TAK-242、PSP和PSP+TAK-242的培养基培养12 h,在37℃、95%空气-5% CO2培养箱中复氧培养6 h。
1.2.4 MTT法检测细胞存活率将经15%胎牛血清DMEM培养的细胞悬液制成5.0×107·L-1细胞悬液,以每孔0.1 mL接种于96孔板,边缘孔用不含细胞的正常培养液填充,将细胞培养板置于37℃、95%空气-5% CO2培养箱培养。待细胞融合至95%后,按照“1.2.3”步骤进行分组及处理,结束后每孔加入0.02 mL MTT溶液(0.5 mg·L-1),于37℃、95%空气-5% CO2培养箱孵育4 h,吸去细胞上清液,每孔加入0.15 mL二甲基亚砜,于低速摇床振荡10 min,置于酶标仪上490 nm测定各组吸光度值。空白对照组只加培养液不加细胞,并将其设为调零孔。细胞存活率/%=(OD实验组-OD空白对照组)/(OD正常对照组-OD空白对照组)×100%,并计算平均值。每组6个复孔,实验独立重复3次。
1.2.5 ELISA法检测细胞培养液TNF-α和IL-1β含量将经15%胎牛血清的DMEM培养的细胞悬液制成1.0× 108·L-1细胞悬液,以每孔1 mL接种于无菌6孔板,将6孔板置于37℃、95%空气-5% CO2培养箱培养,待细胞融合至95%后,按照“1.2.3”步骤进行分组及处理细胞。结束后,收集孔板内的细胞培养液,3 000×g,离心10 min。取上清20 μL。严格按照ELISA试剂盒说明书操作。实验独立重复3次。
1.2.6 Western blot法检测NF-κB、IκBα蛋白表达将含细胞的培养液制成1.0×108·L-1细胞悬液,以每孔1 mL接种于无菌6孔板,将6孔板置于37℃、95%空气-5% CO2培养箱培养,待细胞融合至95%后,按照“1.2.3”步骤进行分组及处理细胞。结束后,每孔加入1 mL含PMSF质量浓度为10 g·L-1的蛋白裂解液,于冰上裂解30 min后,将其置于4℃、20 000 r·min-1离心15 min,收集上清液,采用BCA蛋白定量法测定蛋白浓度并调整。应用SDS-PAGE凝胶试剂盒配制分离胶,每个泳道蛋白上样量为20 μg,跑胶时电压为80 V,待条带进入分离胶,电压增至120 V。于120 V、2 000 mA恒流转膜120 min后,用质量浓度为5 g·L-1脱脂奶粉将PVDF膜封闭2 h,之后置于摇床上,TBST漂洗3次,每10 min 1次,将含蛋白的PVDF膜孵一抗,4℃过夜。次日用TBST液于摇床上漂洗,每10 min 1次,3次后,将膜放入二抗中37℃孵育2 h,TBST漂洗3次后,采用ECL发光试剂盒,在Tanon全自动凝胶成像系统中自动曝光,采集图像,并进行蛋白条带灰度扫描。目的蛋白相对表达量=目的蛋白条带光密度值/β-actin条带光密度值,再以C组为标准,进行统计学分析。
1.2.7 荧光定量PCR检测心肌细胞TLR4、MyD88 mRNA表达水平将含细胞的培养液制成1.0×108·L-1细胞悬液,以每孔1 mL接种于无菌6孔板,将6孔板置于37℃、95%空气-5% CO2培养箱培养,待细胞融合至95%后,按照“1.2.3”步骤进行分组及处理细胞。结束后,弃掉细胞培养液,PBS小心清洗2次,TRIzol试剂完全裂解细胞,将细胞裂解液用氯仿抽提,异丙醇沉淀,回收总RNA于-80℃贮存备用。质量浓度为1 g·L-1琼脂糖凝胶电泳和紫外分光光度计(A260/A280) 鉴定RNA浓度及纯度。取1 μL进行反转录,在荧光定量PCR仪上进行PCR扩增和检测,反转录反应条件为:42℃、60 min,99℃、2 min,4℃保存。TLR4、MyD88、β-actin的引物序列见Tab 1。PCR反应条件是:94℃ 45 s,55℃ 50 s,72℃ 75 s。循环扩增40次结束后,获得TLR4 mRNA、MyD88 mRNA的循环阈值(cycle threshold,Ct),应用△△Ct (△△Ct=△Ct目的基因-△Ct内参基因) 方法分析,计算出2-△△Ct目的基因的相对表达量后,进行统计分析。
| Gene | Primer sequence | Length/bp | |
| TLR4 | Forward | 5′-TGATCATGGCATTGTTCCTT -3′ | 94 |
| Reverse | 5′-TGATCCATGCATTGGTAGGT -3′ | ||
| MyD88 | Forward | 5′-TGGTGGTTGTTTCTGACGAT -3′ | 101 |
| Reverse | 5′-GATCAGTCGCTTCTGTTGGA -3′ | ||
| β-actin | Forward | 5′-CCCATCTATGAGGGTTACGC -3′ | 150 |
| Reverse | 5′-TTTAATGTCACGCACGATTTC -3′ | ||
计量资料用x±s表示,采用SPSS17.0统计软件处理。组间数据比较用单因素方差分析,两两比较用t检验。
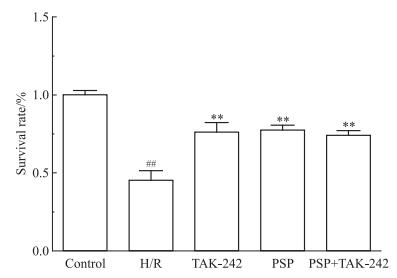
2 结果 2.1 PSP对H9c2心肌细胞H/R损伤后存活率的影响如Fig 1所示,H9c2心肌细胞经过缺氧21 h复氧6 h处理后,细胞存活率(45.08±0.08)%明显降低,与C组(98.12±0.03)%比较差异有明显统计学意义(P < 0.01);PSP组(78.12±0.03)%、TAK-242组(76.26±0.08)%和PSP+TAK-242组(74.22±0.04)%的心肌细胞存活率明显升高,与H/R组比较差异有统计学意义(P < 0.01)。
|
| Fig 1 Effect of PSP on survival rates of H9c2 cells exposed to simulated H/R ##P < 0.01 vs control; **P < 0.01 vs H/R |
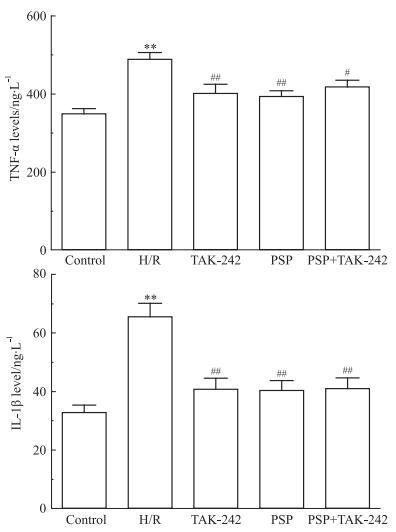
如Fig 2所示,与正常对照组相比,H/R组细胞培养液中炎性因子TNF-α和IL-1β的含量均明显增多(P < 0.01);而PSP处理组的心肌细胞培养液中炎性因子TNF-α和IL-1β含量均明显少于H/R组(P < 0.01),其中PSP+TAK-242组中炎性因子TNF-α和IL-1β的含量明显下调(P < 0.01)。
|
| Fig 2 Effect of PSP on TNF-α and IL-1β expression of myocardial cells by H/R #P < 0.05, ##P < 0.01 vs H/R; **P < 0.01 vs control |
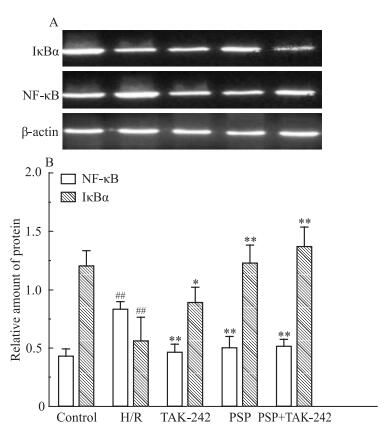
NF-κB是介导炎症反应的关键调控蛋白。Fig 3 Western blot结果显示,PSP能明显抑制H/R刺激的H9c2心肌细胞NF-κB (0.88±0.13) 至(0.52±0.19)(P < 0.01),抑制H/R诱导的IκBα蛋白的降解(0.59±0.04) 至(1.30±0.22)(P < 0.01);其中TAK-242组中NF-κB和IκBα蛋白表达水平与PSP组比较无统计学意义(P>0.05)。
|
| Fig 3 Effects of PSP on NF-κB and IκBα protein expression of H9c2 cells by H/R A:Western blot analysis of NF-κB, IκBα and β-actin protein; B:The relative protein expression of NF-κB and IκBα bands was normalized to β-actin.##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs H/R |
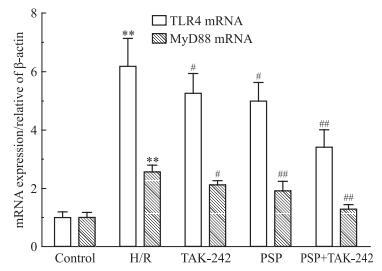
结果如Fig 4所示,正常对照组中H9c2心肌细胞的TLR4和MyD88的mRNA表达水平很低(0.95±0.33) 和(1.06±0.18),H/R损伤后表达均明显上调(5.83±2.04) 和(2.56±0.24)(P < 0.01),PSP组和TAK-242组均能抑制上述基因的表达。
|
| Fig 4 Effects of PSP on mRNA levels of TLR4 and MyD88 in H/R-stimulated H9c2 cells **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs H/R |
TLR4是Toll家族的一类分子,它的结构及其在促炎、促免疫细胞成熟分化及调节免疫应答等方面研究较清楚。机体受到外界刺激时,首先启动先天性免疫反应,激活TLR4表达,促使获得性免疫应答开启,通过其依赖性接头蛋白MyD88信号转导途径,诱导NF-κB活化。一些内源性配体通过激活TLR4受体及激活NF-κB,致使炎性因子如TNF-α、IL-1β和IL-6等释放[13]。MyD88是TLR4信号途径中起重要作用的分子。MyD88有依赖性和非依赖性2种途径,其依赖性途径主要是通过介导NF-κB信号通路的活化及与相关细胞因子所产生。NF-κB是炎性反应基因的重要转录激活因子,它的激活能调控许多炎性因子的表达,是炎症反应发生、发展的关键环节[14]。
心肌缺血/再灌注患者的心肌组织严重受损,受损的心肌组织暴露于缺氧的环境中,促使大量TLR4等巨噬细胞的募集,明显增加了心肌细胞对缺血/缺氧环境的敏感性,因此激活了TLR4/MyD88/NF-κB信号通路[15]。研究发现,TLR4抑制剂TAK-242对H/R细胞处理后,心肌细胞的炎性渗出因子、核因子和TLR4、MyD88的mRNA表达较H/R组明显下降,提示TLR4抑制剂TAK-242可有效阻断TLR4的启动,中断炎性因子的释放及其对机体的损伤。PSP处理后TLR4、MyD88、NF-κB水平明显下调,心肌细胞液中炎性因子TNF-α和IL-1β含量明显降低,而同时加入PSP和TLR4抑制剂后,NF-κB蛋白表达明显下调,有效抑制H/R刺激IκBα的降解,推测PSP保护心肌细胞的作用机制可能与抑制TLR4/MyD88/NF-κB通路有关。
综上所述,本实验以体外培养H/R诱导H9c2心肌细胞为研究对象,发现PSP对H/R损伤H9c2心肌细胞具有保护作用,其保护作用机制通过阻断TLR4-MyD88-NF-κB信号通路,下调H/R介导心肌细胞炎性因子表达,从而减轻细胞炎症反应。
( 致谢: 本文所有实验均在安徽中医药大学中西药研究与开发重点实验室、安徽中医药大学科学实验中心完成。 )
| [1] | Gao Y, Fang X B, Tong Y, et al. TLR4-mediated MyD88-dependent signaling pathway is activated by cerebral ischemia-reperfusion in cortex in mice[J]. Biomed Pharmacother, 2009, 63 : 442-50. doi:10.1016/j.biopha.2008.06.028 |
| [2] | Liu L, Gu H, Liu H, et al. Protective effect of resveratrol against IL-1β-induced inflammatory response on human osteoarthritic chondrocytes partly via the TLR4/MyD88/NF-κB signaling pathway:an"in vitro study"[J]. Int J Mol Sci, 2014, 15 (4): 6925-40. doi:10.3390/ijms15046925 |
| [3] | 邓超, 任改艳, 孙阿宁, 等. 豆蔻明对TLR4/MyD88/NF-κB/iNOS信号通路的调节作用[J]. 中国药理学通报, 2016, 32 (6): 779-83. Deng C, Ren G Y, Sun A N, et al. The regulatory effect of cardamonin on TLR4/MyD88/NF-κB/iNOS pathway[J]. Chin Pharmacol Bull, 2016, 32 (6): 779-83. |
| [4] | Chen Z J, Parent L, Maniatis T, et al. Site-specific phosphorylation of IκBα by a novel ubiquitination-dependent protein kinase activity[J]. Cell, 1996, 84 (6): 853-62. doi:10.1016/S0092-8674(00)81064-8 |
| [5] | Wu B Y, Woffendin C, Duckett C S, et al. Regulation of human retroviral latency by the NF-κB/IκB family:inhibition of human immunodeficiency virus replication by IκB through a Rev-dependent mechanism[J]. Proc Natl Acad Sci USA, 1995, 92 (5): 1480-4. doi:10.1073/pnas.92.5.1480 |
| [6] | 李丽, 田丽娜, 任振兴, 等. 黄精多糖的结构分析及功能活性研究进展[J]. 中国实验方剂学杂志, 2015, 21 (15): 231-5. Li L, Tian L N, Ren Z X, et al. Structural analysis and functional activity research progress of Polygonatum sibiricum polysaccharides[J]. Chin J Exp Tradit Med Form, 2015, 21 (15): 231-5. |
| [7] | 段华, 王保奇, 张跃文. 黄精多糖对肝癌H22移植瘤小鼠的抑瘤作用及机制研究[J]. 中药新药与临床药理, 2014, 25 (1): 5-8. Duan H, Wang B Q, Zhang Y W. Anti-tumor effects and mechanism of rhizoma polygonati polysaccharide on H22 tumor bearing mice[J]. Tradit Chin Drug Res Clin Pharmacol, 2014, 25 (1): 5-8. |
| [8] | 胡国柱, 聂荣庆, 肖移生, 等. 黄精多糖对新生大鼠大脑皮层神经细胞缺氧性凋亡的影响[J]. 中药药理与临床, 2005, 21 (4): 37-40. Hu G Z, Nie R Q, Xiao Y S, et al. Influence of polygonatum polysaccharide on apoptosis of primary cultured neonate rat cerebral cortical neurons caused by hypoxia[J]. Pharmacol Clin Chin Mater Med, 2005, 21 (4): 37-40. |
| [9] | 李丽, 龙子江, 黄静, 等. 黄精多糖对急性心肌梗死模型大鼠NF-κB介导的炎症反应及心肌组织形态的影响[J]. 中草药, 2015, 46 (18): 2750-5. Li L, Long Z J, Huang J, et al. Effect of Polygonatum sibiricum polysaccharides on inflammatory reaction mediated by NF-κB and myocardium tissue morphology in acute myocardial infarction rats[J]. Chin Tradit Herb Drugs, 2015, 46 (18): 2750-5. |
| [10] | Hua F, Tang H L, Wang J, et al. TAK-242, an antagonist for Toll-like receptor 4, protects against acute cerebral ischemia/reperfusion injury in mice[J]. J Cereb Blood Flow Metab, 2015, 35 (4): 536-42. doi:10.1038/jcbfm.2014.240 |
| [11] | Park M, Youn B, Zheng X L, et al. Globular adiponectin, acting via AdipoR1/APPL1, protects H9c2 cells from hypoxia/reoxygen-action-induced apoptosis[J]. PLoS One, 2011, 6 (4). |
| [12] | 韩正怡, 何淑芳, 程洁, 等. 吗啡预处理对H9c2心肌细胞缺氧/复氧时microRNA表达的影响[J]. 中国药理学通报, 2015, 31 (11): 1552-7. Han Z Y, He S F, Cheng J, et al. Effects of morphine preconditioning on expression of microRNAs during hypoxia-reoxygenation in H9c2 myocardial cells[J]. Chin Pharmacol Bull, 2015, 31 (11): 1552-7. |
| [13] | Lin X F, Kong J J, Wu Q T, et al. Effect of TLR4/MyD88 signaling pathway on expression of IL-1β and TNF-α in synovia fibroblasts from temporomandibular joint exposed to lipopolysaccharide[J]. Mediators Inflamm, 2015, 2015 : 329405. |
| [14] | 雷梅先, 王云开, 殷然, 等. 肝X受体通过NF-κB信号通路减轻高糖诱导的H9c2细胞凋亡[J]. 中国药理学通报, 2014, 30 (12): 1698-704. Lei M X, Wang Y K, Yin R, et al. Liver X receptors attenuate high glucose-induced apoptosis in H9c2 cells through NF-κB signaling pathway[J]. Chin Pharmacol Bull, 2014, 30 (12): 1698-704. |
| [15] | 李燕巍, 谢广茹, 李玲, 等. TLR4/MyD88/NF-κB信号通路对LPS诱导的人鼻咽癌5-8F细胞增殖及凋亡的影响[J]. 临床耳鼻咽喉头颈外科杂志, 2015, 29 (11): 1012-5. Li Y W, Xie G R, Li L, et al. The effect of TLR4/MyD88/NF-κB signaling pathway on proliferation and apoptosis in human nasopharyngeal carcinoma 5-8F cells induced by LPS[J]. J Clin Otorhinolaryngol Head Neck Surg, 2015, 29 (11): 1012-5. |

