


2. 三峡大学 仁和医院,湖北 宜昌 443002
 ,
ZHANG Chang-cheng1,
WANG Ting1,
LIU Zhen-cai1,
HAN Gui-fang1,
YUAN Ding1,2,
ZHAO Hai-xia1
,
ZHANG Chang-cheng1,
WANG Ting1,
LIU Zhen-cai1,
HAN Gui-fang1,
YUAN Ding1,2,
ZHAO Hai-xia1

2. Renhe Hospital of China Three Gorges University, Yichang Hubei 443002, China
随着人类寿命不断延长,我国社会老龄化程度加剧,脑衰老及相关认知功能障碍性疾病如阿尔茨海默病、帕金森病等患者的数量不断增加[1]。研究显示,随着年龄的增长,中枢的炎症稳态会逐步失调而产生中枢炎症反应[2],且中枢促炎因子会增加脑衰老相关退行性疾病的易感性[3]。因此,抑制中枢炎症反应,延缓脑衰老,是防治中枢神经退行性疾病的重要措施之一。
淫羊藿为我国传统的补益中药,现代研究表明其对神经系统具有调节作用,并具有明显的抗炎、抗衰老的作用,而淫羊藿总黄酮(total flavonoids of Epimedium,TFE)为其主要有效成分[4-5],但其延缓自然衰老大鼠脑衰老的作用机制却少见研究。MAPK/NF-κB通路是炎症反应中重要的信号通路[6]。有研究显示,激活的MAPK可通过活化NF-κB,使其转移入核,从而调控其下游多种炎症因子,如IL-1β、TNF-α、COX-2等的表达,产生炎症反应[7-8]。故本实验通过研究TFE对自然衰老大鼠脑组织MAPK/NF-κB信号通路的调节作用,从而探讨其延缓脑衰老的可能作用机制,并为进一步开发和应用该药提供一定的实验基础和理论依据。
1 材料 1.1 动物SPF级SD ♂大鼠18月龄30只,体质量(705±20)g;3月龄10只,体质量(220±10)g;购于北京维通利华实验动物技术有限公司,动物生产许可证号:SCXK(京)2012-0001,批号:11400700003309。
1.2 药物与试剂TFE,购自成都仁诚生物科技有限公司,HPLC测定其含量为80%,临用前将其用质量分数为1%的羧甲基纤维素钠(CMC-Na)溶液进行超声溶解,后配成相应浓度的溶液。Tris-base、SDS、甘氨酸、PMSF、磷酸蛋白酶抑制剂,武汉谷歌生物有限公司;Western blot marker、RIPA裂解液、BCA蛋白浓度定量试剂盒,北京普利莱基因技术有限公司;细胞核蛋白与细胞质蛋白抽提试剂盒、ECL显影液,上海碧云天生物技术研究所;β-actin抗体(货号:66009-1-lg),美国Proteintech公司;p21抗体(货号:ab109199),美国Abcam公司;LaminA(货号:sc-20680)、ERK1/2(货号:sc-94)、p-ERK1/2(货号:sc-7383)、TNF-α(货号:sc-1351)、IL-1β(货号:sc-7884)、Bax(货号:sc-7480)抗体,美国Santa Cruz公司;NF-κB p65(货号:#6956)、JNK(货号:#9252)、p-JNK(货号:#9251)、p38 MAPK(货号:#9212)、p-p38 MAPK(货号:#4631)、COX-2(货号:#12282)、Bcl-2(货号:#2876)抗体,美国Cell Signaling公司;辣根过氧化酶标记的山羊抗兔、山羊抗小鼠及兔抗山羊二抗,武汉科瑞有限公司。
1.3 仪器PowerPacTM Basic电泳仪,美国Bio-Rad;BioshineChemiQ 4800化学发光凝胶成像自动显影仪,中国上海欧翔科学仪器有限公司;IX53显微镜,日本Olympus;LEICA EG 1150H石蜡包埋机、LEICA TP 1020自动脱水机、LEICA EG 1150C超薄切片机,德国Leica。
2 方法 2.1 实验分组及给药30只18月龄大鼠随机分为3组,每组10只,即自然衰老组、TFE低剂量组(10 mg·kg-1)、TFE高剂量组(20 mg·kg-1)。10只3月龄大鼠为青年对照组。TFE各剂量组分别同时灌胃给予相应浓度的TFE,青年对照组和自然衰老组大鼠均灌胃给予质量分数为1%的CMC-Na溶液。各组每天灌胃1次,每周灌胃6 d后停药1 d,共给药6个月。
2.2 HE染色观察大鼠海马区神经元形态的变化大鼠腹腔注射质量分数为7%水合氯醛5 mL·kg-1麻醉后,进行心脏灌注,快速取出整个脑组织,经质量分数为4%的多聚甲醛固定24 h后,梯度乙醇脱水,石蜡包埋,制作石蜡切片,切片厚度为4 μm,HE染色,光镜下观察海马区神经元形态的变化。
2.3 Western blot检测大鼠海马组织蛋白的表达称取约50 mg的海马组织,尽可能将组织剪成细小碎片,加入600 μL裂解液(按RIPA裂解液 ∶PMSF ∶磷酸蛋白酶抑制剂=100 ∶1 ∶1的比例配制)提取总蛋白;按照细胞核蛋白与细胞质蛋白抽提试剂盒操作步骤提取核蛋白。BCA法对蛋白进行定量,加入Loading buffer后煮沸变性5~10 min,再进行电泳和转膜,5%脱脂牛奶封闭1 h,然后一抗4 ℃孵育过夜和二抗室温孵育1 h,用ECL化学发光显影液,于化学发光凝胶成像系统中显影成像,Image-proplus 6.0软件对结果进行灰度扫描分析,总蛋白以β-actin为内参,核蛋白以LaminA为内参,计算各蛋白条带与内参照的灰度比值。每组实验各重复3次。
2.4 统计学处理采用SPSS 18.0软件进行统计学处理,Western blot结果采用Image-proplus 6.0软件进行分析,数据以x±s表示,用单因素方差分析检验组间差异的显著性。
3 结果 3.1 TFE对自然衰老大鼠行为、体质量方面的影响给药前,各组大鼠均饮食正常,毛色有光泽,且活动性较好,除青年对照组(3月龄)和自然衰老组大鼠(18月龄)的体质量比较有明显差异外,自然衰老组与TFE用药组比较均无明显差异;随着年龄增加,自然衰老组(24月龄)与青年对照组(9月龄)比较,其饮食量明显减少,毛色暗淡,逐渐出现掉毛现象,且大鼠的活动和反应逐渐迟缓,随用药时间的延长,其大鼠饮食情况、毛色光泽度、精神状态、活动情况均有明显地改善,除自然衰老组与青年对照组的体质量比较差异具有显著性外,自然衰老组(24月龄)与TFE用药组(24月龄)组比较,其体质量无明显变化,见Tab 1。
| Group | Body weight | |
| Before experiment/g | After experiment/g | |
| Adult | 220±10 | 490±12 |
| Aging | 705±20## | 698±25## |
| TFE 10 mg·kg-1 | 710±16 | 709±22 |
| TFE 20 mg·kg-1 | 708±16 | 704±18 |
| ##P<0.01 vs adult | ||
HE结果显示,青年对照组大鼠海马CA1、CA3、DG区神经细胞排列整齐紧密,形状规则,结构清晰,自然衰老模型组中海马神经细胞排列疏松散乱,且细胞出现大量变性,变性的神经细胞的细胞核固缩深染呈不规则形状;而TFE可明显改善和恢复海马神经细胞的形态,变性的神经细胞数明显减少,见Fig 1。
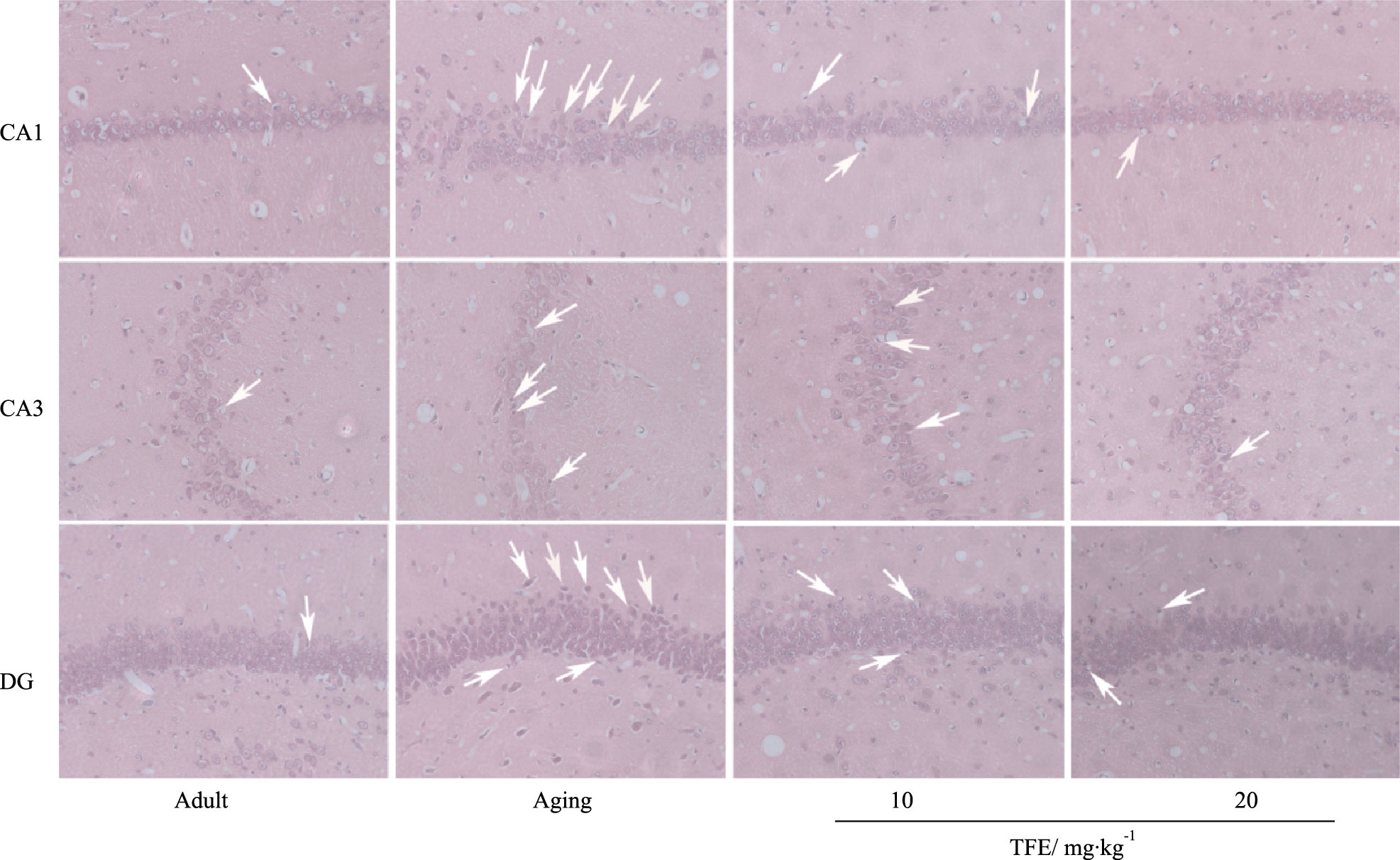
|
| Fig 1 Morphology of hippocampal neurons in rats (HE×200) Arrows indicate the denatured neurons |
与青年对照组相比,自然衰老组大鼠海马组织中p21蛋白表达水平上调(P<0.01);与自然衰老组比较,TFE可下调p21的蛋白表达水平(P<0.01),见Fig 2。
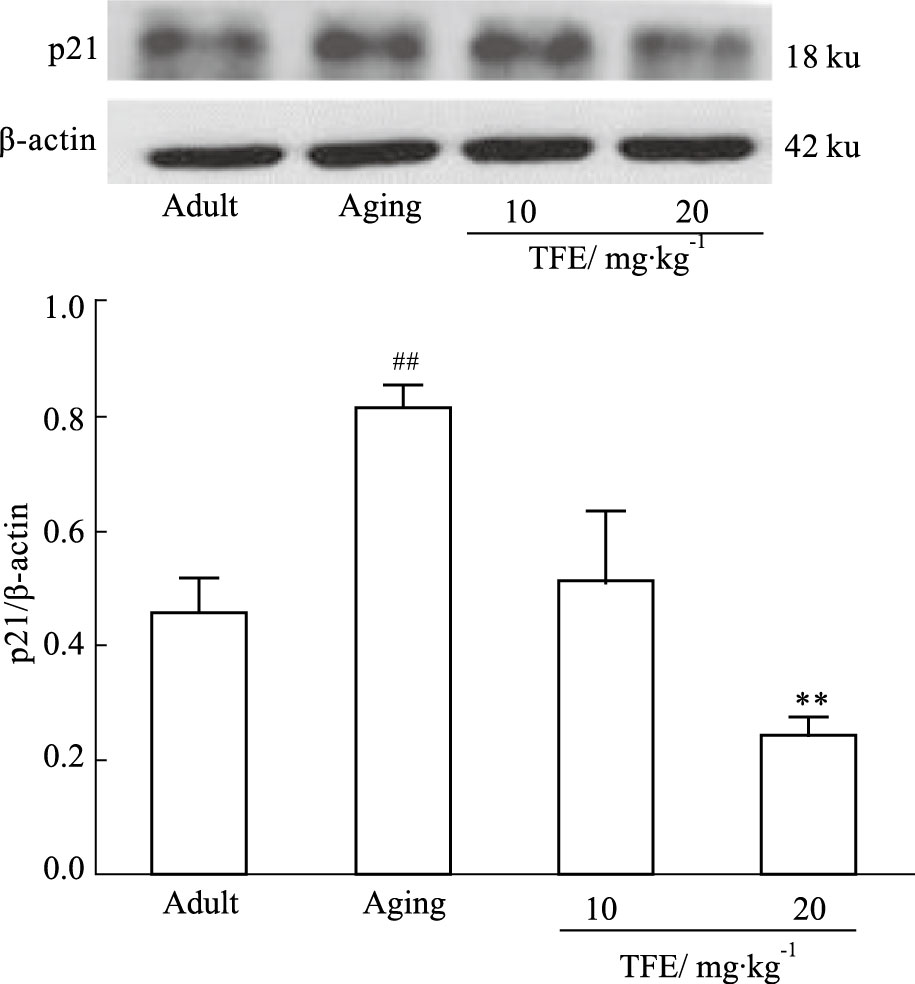
|
| Fig 2 The protein expression levels of p21 in hippocampus of rats ##P<0.01 vs Adult;**P<0.01 vs Aging |
与青年对照组相比,自然衰老组大鼠海马组织中Bax蛋白的表达明显增加,Bcl-2蛋白的表达和Bcl-2/Bax比值明显降低,且差异均具有显著性(P<0.01);而给予TFE后,Bax蛋白的表达降低(P<0.01),Bcl-2蛋白的表达和Bcl-2/Bax的比值均升高(P<0.01),差异有统计学意义,见Fig 3。
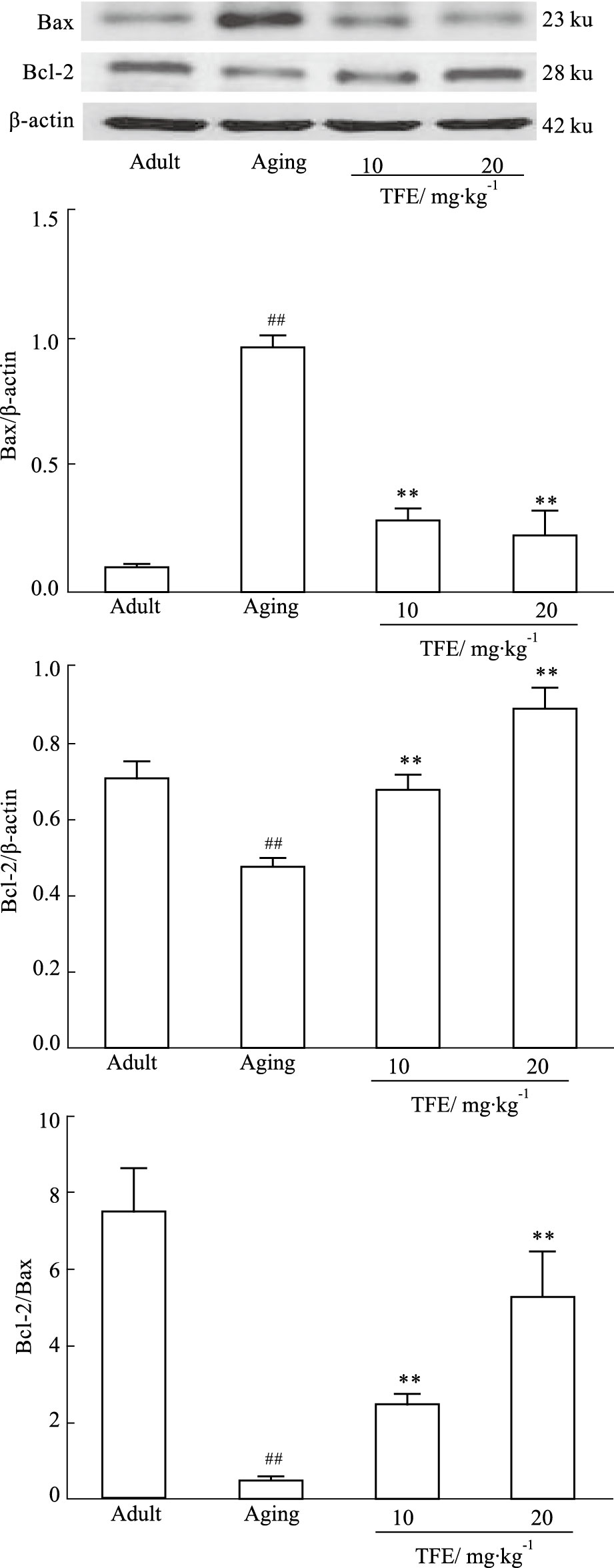
|
| Fig 3 The protein expression levels of Bax and Bcl-2 in hippocampus of rats ##P<0.01 vs Adult;**P<0.01 vs Aging |
与青年对照组比较,自然衰老组海马组织中COX-2、TNF-α、IL-1β蛋白的表达均上调(P<0.05或P<0.01);而TFE低、高剂量组均可下调COX-2、TNF-α、IL-1β的蛋白水平(P<0.05或P<0.01),见Fig 4。
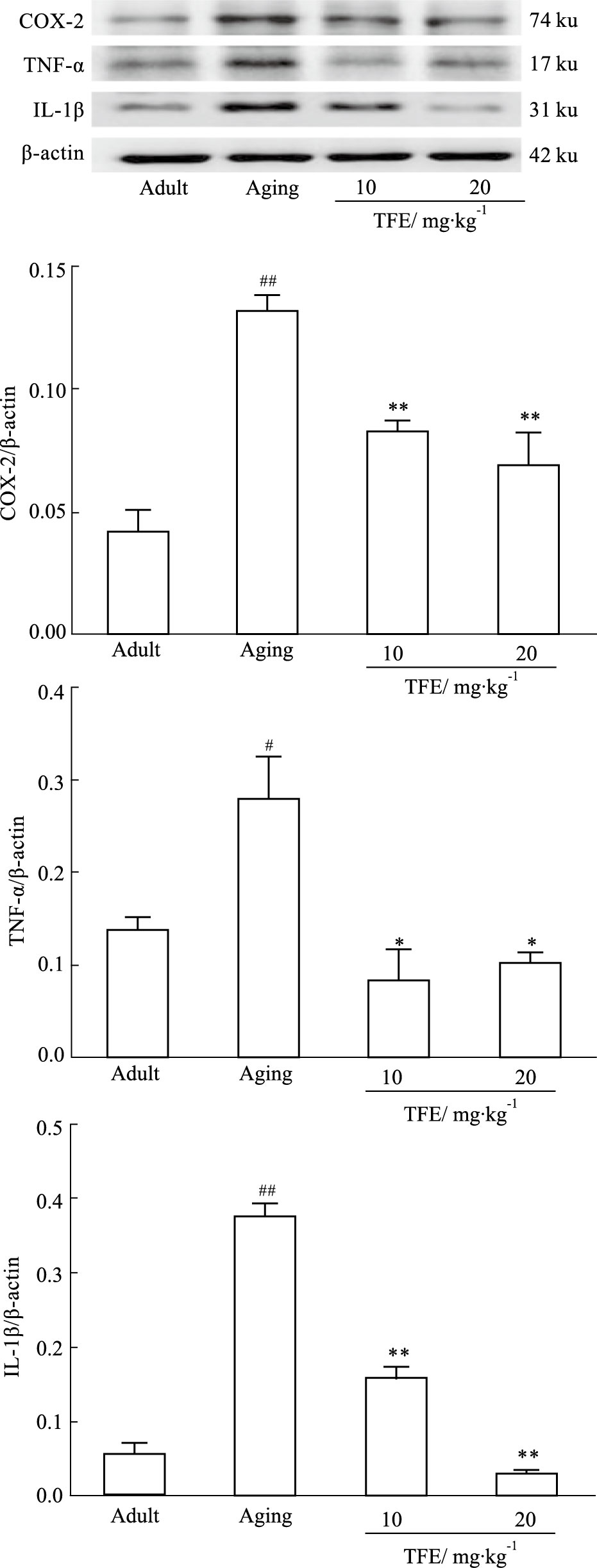
|
| Fig 4 The protein expression levels of inflammatory factorsCOX-2,TNF-α and IL-1β in hippocampus of rats #P<0.05,##P<0.01 vs Adult;*P<0.05,**P<0.01 vs Aging |
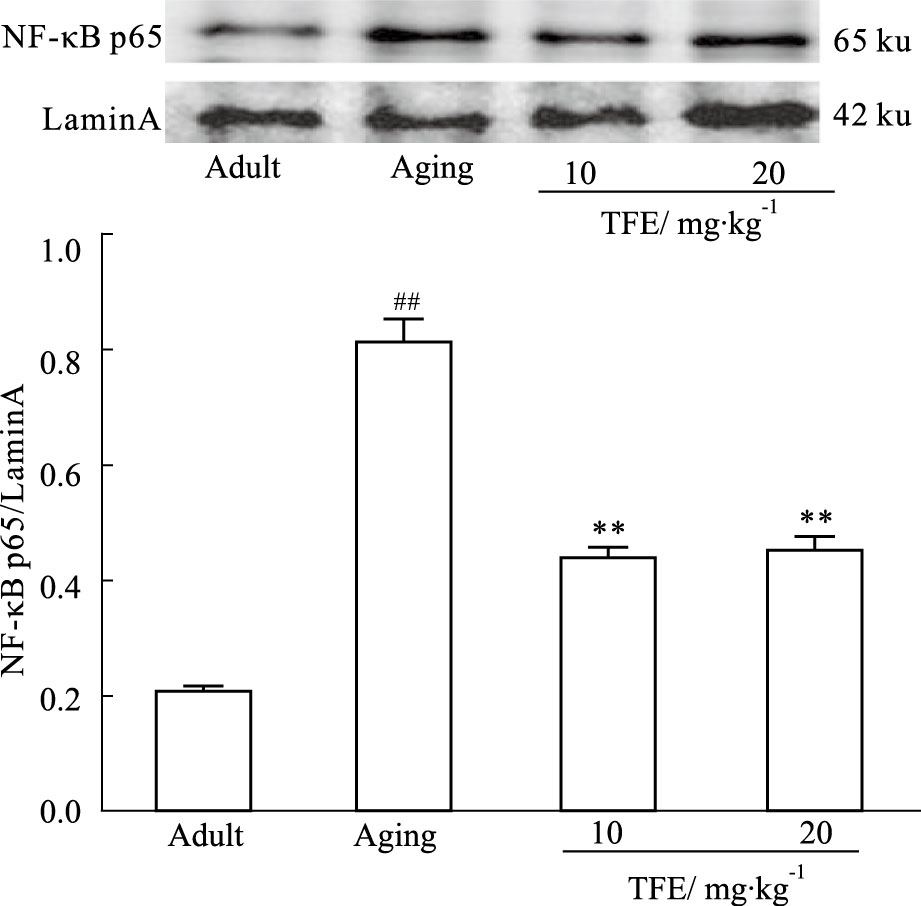
p65表达水平的影响 如Fig 5所示,自然衰老组中核蛋白NF-κB p65的表达水平较青年对照组明显上调(P<0.01);而TFE用药后,核蛋白NF-κB p65的蛋白表达水平明显下调(P<0.01)。
|
| Fig 5 The protein expression levels of nuclear protein NF-κB p65 in hippocampus of rats ##P<0.01 vs Adult;**P<0.01 vs Aging |
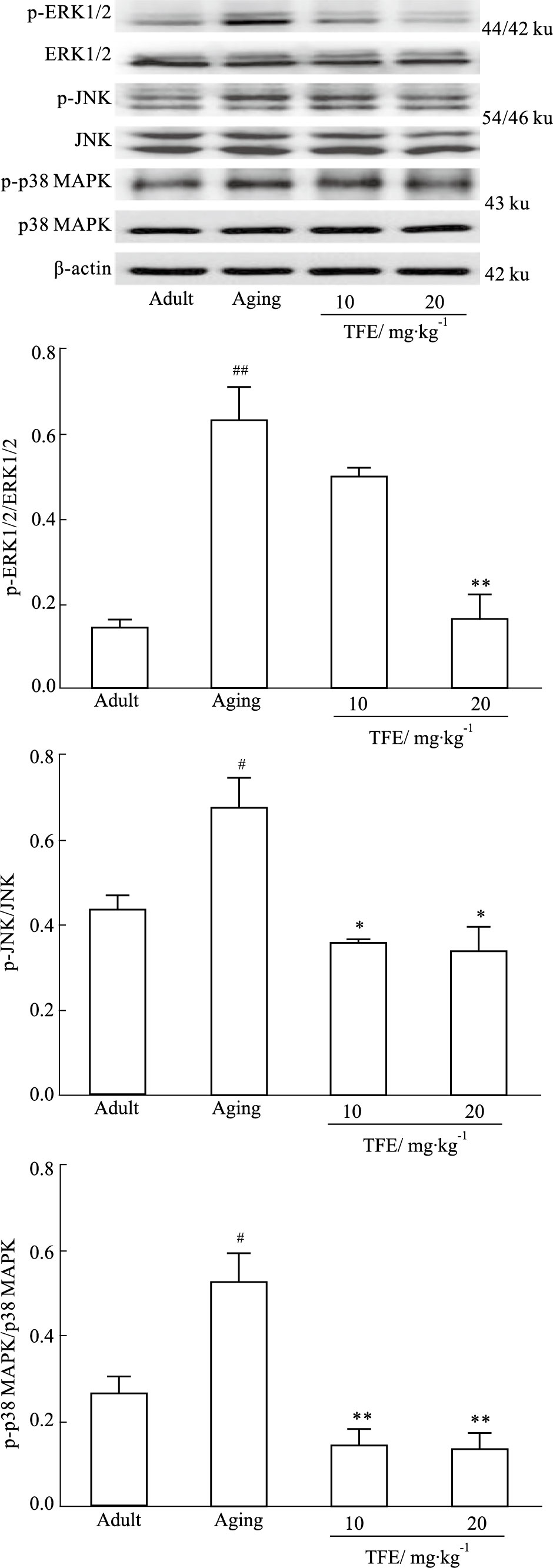
与青年对照组比较,自然衰老组中p-ERK1/2、p-p38 MAPK、p-JNK蛋白表达水平均增加(P<0.05或P<0.01),而总蛋白表达水平无明显变化。给予TFE干预后,p-ERK1/2、p-JNK、p-p38 MAPK的蛋白表达水平降低(P<0.05或P<0.01),见Fig 6。
|
| Fig 6 The protein expression levels of MAPK signal in hippocampus of rats #P<0.05,##P<0.01 vs Adult;*P<0.05,**P<0.01 vs Aging |
随着年龄的增加,机体在形态结构和生理功能方面会出现一系列的退行性变化。神经系统是生命机能的重要调节系统,也是受衰老影响最大的系统[9]。本实验以自然衰老大鼠为模型,通过观察各组大鼠行为和体质量等方面的变化,发现TFE可明显改善自然衰老大鼠的饮食情况、毛色光泽度、精神状态、活动情况,但对其体质量无明显的影响。提示,TFE可改善自然衰老大鼠的衰老状态。通过组织形态学观察,结果发现TFE对自然衰老组大鼠海马神经细胞排列散乱、疏松的形态结构具有明显改善作用,且核固缩深染呈不规则形状的变性神经元明显减少,提示TFE对自然衰老大鼠海马神经细胞形态结构具有明显保护作用。
p21基因是细胞周期蛋白依赖性激酶抑制因子,研究表明,p21是衰老的标志物,其表达水平与细胞衰老联系紧密,在衰老过程中,p21表达会明显增加[9-11]。本实验结果显示,自然衰老组海马组织中p21蛋白表达水平明显升高,而TFE用药组可明显降低p21蛋白表达。凋亡是机体发生衰老退化的关键基础。有研究发现,在利用高糖诱导的内皮细胞衰老模型中,内皮细胞凋亡明显增加[12]。在调控细胞凋亡的过程中,抑凋亡蛋白Bcl-2和促凋亡蛋白Bax具有十分重要的作用,Bcl-2和Bax的比值决定着细胞存亡[13]。本研究发现,自然衰老组海马组织中Bcl-2/Bax的比例降低,而TFE可明显升高Bcl-2/Bax的比例。以上结果表明,TFE具有延缓脑衰老的作用。基于此,本实验进一步深入研究TFE延缓脑衰老的作用机制。
中枢神经炎症反应在脑衰老相关认知功能障碍性疾病的发展中起着很大的促进作用。TNF-α、IL-1β和COX-2均是参与炎症反应的重要介质,是早期炎症的标志物。NF-κB是早期核转录因子,NF-κB p65为NF-κB转录因子家族的重要成员,在炎性反应中起中心调控作用。正常生理状态下,NF-κB以无活性的形式存在于胞质中,当受到其他外部抗原刺激后,可被活化并转移至细胞核中,调控下游多种炎症相关因子表达,如TNF-α、IL-1β和COX-2等,进而参与各种炎症反应。MAPK信号通路在调节炎症介质中发挥着重要作用,其主要包括由JNK、ERK1/2、p38 MAPK介导的3条途径,该通路的激活可促进炎症细胞因子的生成而加剧炎症反应[14]。此外,另有研究显示,激活的p38 MAPK、ERK1/2、JNK均可活化NF-κB,使其发生核移位,从而介导炎症反应[7-8]。本研究结果显示,TFE可下调自然衰老组MAPK的磷酸化水平,并降低胞核NF-κB p65蛋白及其下游炎症相关因子TNF-α、IL-1β和COX-2的表达。
综上所述,TFE对自然衰老大鼠炎症反应具有较好的保护作用,其机制可能是通过抑制MAPK的磷酸化,从而抑制NF-κB的核易位,下调其下游相关炎症因子的表达水平。故推测,TFE延缓脑衰老的作用机制可能与调控MAPK/NF-κB信号通路有关。
( 致谢: 本实验主要在三峡大学医学院国家中医药管理局中药药理科研三级实验室和三峡大学肿瘤微环境与免疫治疗湖北省重点实验室完成。在此,感谢实验室老师、本课题组的全体老师及同学对我的指导和帮助。 )
| [1] | Qiu J. Ticking time bomb faced by China's ageing population[J]. Lancet Neurol, 2007, 6 (7): 582-3. doi:10.1016/S1474-4422(07)70162-X |
| [2] | Akintola A A, van Heemst D. Insulin, aging, and the brain: mechanisms and implications[J]. Front Endocrinol (Lausanne), 2015, 6 : 13. |
| [3] | Salvioli S, Capri M, Valensin S, et al. Inflamm-aging, cytokinesand aging:state of the art, new hypotheses on the role of mitochondria and new perspectives from systems biology[J]. Curr Pharm Des, 2006, 12 (24): 3161-71. doi:10.2174/138161206777947470 |
| [4] | 叶丽卡, 陈济民. 淫羊藿的药理研究进展[J]. 中国中药杂志, 2001, 26 (5) : 293-5. Ye L K, Chen J M. The research progress of total flavonoids from Epimedium[J]. Chin J Chin Mat Med, 2001, 26 (5): 293-5. |
| [5] | 王梅玲, 李润今, 甄瑾. 淫羊藿保护脑神经和提高免疫作用的研究进展[J]. 内蒙古医学院学报, 2008 (S1) : 668-71. Wang M L, Li R J, Zhen J. Process of protection nervicerebrales andimproving immune function of Epimedium[J]. ActaAcadMedNeiMongol, 2008 (S1): 668-71. |
| [6] | 王金磊, 李承德, 孙宏伟, 等. 黄芪多糖抑制NF-κB/MAPK信号通路和改善哮喘大鼠气道炎症的作用[J]. 中国药理学通报, 2016, 32 (4) : 489-93. Wang J L, Li C D, Sun H W, et al. Astragalus polysaccharide regulates NF-κB/MAPK signaling pathway and attenuates airway inflammation in OVA-induced asthmatic rats[J]. Chin Pharmacol Bull, 2016, 32 (4): 489-93. |
| [7] | Karunakaran S, Ravindranath V. Activation of p38 MAPK in the substantia nigra leads to nuclear translocation of NF-kappaB in MPTP-treated mice: implication in Parkinson's disease[J]. J Neurochem, 2009, 109 (6): 1791-9. doi:10.1111/jnc.2009.109.issue-6 |
| [8] | Lee S M, Kim E J, Suk K, Lee W H. Stimulation of Fas (CD95) induces production of pro-inflammatory mediators through ERK/JNK-dependent activation of NF-κB in THP-1 cells[J]. Cell Immunol, 2011, 271 (1): 157-62. doi:10.1016/j.cellimm.2011.06.019 |
| [9] | 崔德华. 脑衰老与认知障碍的研究进展[J]. 实用老年医学, 2010, 24 (1) : 19-23. Cui D H. Research progress of brain aging and cognitive impairment[J]. Pract Geriatr, 2010, 24 (1): 19-23. |
| [10] | Hua Y, Robinson T J, Cao Y, et al. Cathepsin K knockout alleviates aging-induced cardiac dysfunction[J]. Aging Cell, 2015, 14 (3): 345-51. doi:10.1111/acel.2015.14.issue-3 |
| [11] | 高志清, 海春旭, 张晓迪, 席庆祥. D-半乳糖诱导的衰老模型中RAGE和P21的表达和意义[J]. 中国老年学杂志, 2007, 27 (17) : 1661-3. Gao Z Q, Hai C X, Zhang X D, Xi Q X. Expression and significance of RAGE and P21 in the D-galactose induced aging model[J]. Chin J Gerontol, 2007, 27 (17): 1661-3. |
| [12] | 刘小莺, 吴莉, 陈洲, 刘礼斌. PTEN抑制剂对高糖诱导的内皮细胞衰老的影响[J]. 中国药理学通报, 2016, 32 (4) : 514-9. Liu X Y, Wu L, Chen Z, Liu L B. PTEN inhibitors attenuates high glucose induced endothelial cell senescence[J]. Chin Pharmacol Bull, 2016, 32 (4): 514-9. |
| [13] | Cory S, Adams J M. The Bcl-2 family: regulators of the cellular life-or-death switch[J]. Nat Rev Cancer, 2002, 2 (9): 647-56. doi:10.1038/nrc883 |
| [14] | Wang S, Hibberd M L, Pettersson S, Lee Y K. Enterococcus faecalis from healthy infants modulates inflammation through MAPK signaling pathways[J]. PLoS One, 2014, 9 (5): e97523. doi:10.1371/journal.pone.0097523 |